当归补血汤治疗化疗相关性骨髓抑制作用机制的分析
2021-06-15罗伊扬江婷丁诗意王彬彬
罗伊扬 江婷 丁诗意 王彬彬*
化疗相关性骨髓抑制是化疗的常见不良反应之一,可以表现为中性粒细胞减少、淋巴细胞减少、贫血和血小板减少,且可以导致感染、出血等并发症,从而增加发病率和死亡率[1]。现代药理学研究表明,当归多糖和黄芪多糖能够激活PI3K/AKT信号转导通路[2],当归补血汤的载药血清能促进骨髓基质细胞增殖和GMCSF、IL-3的分泌,增加骨髓有核细胞抗凋亡基因Bcl-2和促细胞增殖基因cmyc mRNA表达[3]。网络药理学是英国药理学家Hopkins于2007年提出的概念,是一门新兴的药理学分支学科,其在构建“药物-成分-靶点-疾病”多层次结构网络基础上多分子药物协同治疗疾病的作用机制,与中医的整体观念相吻合。本文借助网络药理学,研究当归补血汤的主要活性成分、治疗化疗相关性骨髓抑制的潜在靶点以及可能作用机制。
1 材料与方法
1.1 当归补血汤活性成分及靶基因的收集与筛选 中药系统药理学数据库与分析平台(TCMSP,http://tcmspw.com/tcmsp.php)是一个建立在中草药系统药理学基础上的数据库及分析平台。本实验通过TCMSP平台,以“黄芪”“当归”作为关键词检索,选择“Ingredients”,再通过设置口服生物利用度(OB)>30%,类药性(DL)>0.18作为筛选条件,得到当归补血汤的关键活性成分。再选择“Related Targets”,筛选后获得当归补血汤关键活性成分所相对应的靶基因,并通过uniprot数据库(https://www.uniprot.org/)进行基因标准化。
1.2 疾病靶基因的查找 GeneCards (https://www.genecards.org/)是一个关于人类基因注释性信息的全面、权威的汇编。OMIM (https://omim.org/)是根据已出版的生物医学文献每天更新的一个人类基因和表型的知识库。本实验通过GeneCards及OMIM疾病数据库检索化疗相关性骨髓抑制的相关靶基因。
1.3 当归补血汤治疗化疗相关性骨髓抑制靶基因预测 将当归补血汤活性成分相对应靶基因与化疗相关性骨髓抑制靶基因进行成分映射,得到药物-疾病共同靶基因,这些靶基因可能是当归补血汤治疗化疗相关性骨髓抑制的关键靶基因,并记录共同靶基因所对应的当归补血汤关键活性成分。
1.4 “药物-成分-靶点-疾病”网络的构建 将当归补血汤的活性成分,当归补血汤与化疗相关性骨髓抑制的关键靶基因以及属性关系导入到Cytoscape3.7.2中,构建“药物-成分-靶点-疾病”网络,实现可视化处理。在网络图中,节点(node)表示关键活性成分以及关键靶基因,边(edge)表示各个节点之间的相互作用关系。
1.5 蛋白质-蛋白质相互作用(PPI)网络的构建 登录STRING (Version 11.0,https://string-db.org/),选择“multiple proteins”,输入当归补血汤与化疗相关性骨髓抑制的共同靶基因,选择研究物种为“Homo sapiens”进行检索,选择中等置信度(0.400),得到PPI网络,并筛选出排名前30的PPI网络核心基因。
1.6 GO富集分析以及KEGG通路富集分析 通过Bioconductor数据库将药物-疾病共同靶基因转换成entrezID。在R软件(Version 3.6.2)安装Bioconductor相关安装包,设置pvalue<0.05,qvalue<0.05进行药物-疾病共同靶基因的GO富集分析以及KEGG通路富集分析,输出结果并绘制柱状图和气泡图。
2 结果
2.1 当归补血汤活性成分和靶基因 TCMSP数据库检索到当归补血汤共有212个活性成分,其中黄芪活性成分87个,当归活性成分125个,经OB>30%及DL>0.18筛选后,分别剩余20个黄芪和2个当归活性成分,见表1。再选择“Related Targets”,筛选后获得当归补血汤关键活性成分所相对应的靶基因。其中,黄芪中共得到360个靶基因,当归中得到52个靶基因,删除重复项后,剩余141个靶基因,其中有33个靶基因为黄芪和当归所共有。
2.2 药物-疾病靶基因预测 共得到46个共同靶基因,视为当归补血汤治疗化疗相关性骨髓抑制的可能的关键靶基因。同时,记录共同靶基因所对应的当归补血汤关键活性成分,最终得到关键活性成分8个,分别为Jaranol(熊竹素),hederagenin(常春藤皂苷元),isorhamnetin(异鼠李素),3,9-Di-O-methylnissolin,Bifendate(联苯双酯),formononetin(芒柄花黄素),kaempferol(山奈酚),Quercetin(槲皮素)。见图1。

表1 当归补血汤活性成分及其OB与DL值
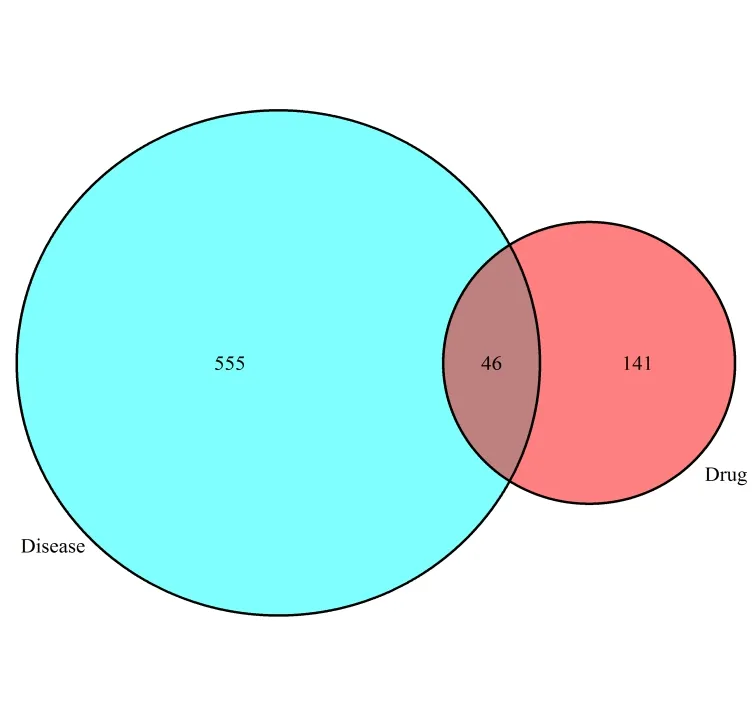
图1 当归补血汤活性成分靶基因与化疗相关性骨髓抑制靶基因取交集后的韦恩图
2.3 “药物-成分-靶点-疾病”网络 此网络共包含56个节点,100条边。通过网络图观察到多种成分作用于同一个靶点或一种成分作用于多个靶点,表明当归补血汤治疗化疗相关性骨髓抑制具有多成分、多靶点以及多作用途径的特点。使用CentiScape2.2计算活性成分的度中心性(DC),DC是网络分析中的一个重要指标,一个节点的DC越大,表明该节点在此网络中的重要性越大。Quercetin(槲皮素)为28,kaempferol(山奈酚)为11,isorhamnetin(异鼠李素)为4,位于前3位。见图2。
2.4 PPI网络分析 将关键靶基因导入到STRING平台,选择研究物种为“Homo sapiens”,选择中等置信度(0.400),得到PPI网络,见图3。该网络包含46个节点,411条边。通过R语言计算每个基因的连接节点的数目,从而得到前30个核心基因,见图4。其中,AKT1、IL-6、VEGFA、CXCL8以及IL1B位于前5位。

图2 “药物-成分-靶点-疾病”网络(红色-化疗相关性骨髓抑制,黄色-当归补血汤,紫色-当归补血汤活性成分,绿色-关键靶基因)

图3 PPI网络
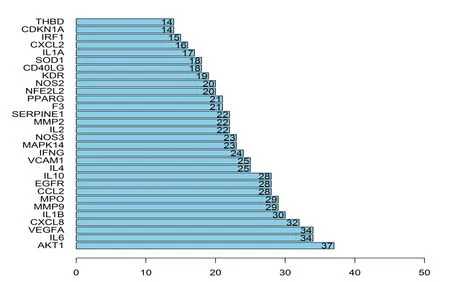
图4 PPI核心基因
2.5 GO功能富集分析 当归补血汤主要参与细胞因子活性,细胞因子受体结合,受体配体活性,生长因子受体结合,蛋白磷酸酶结合,作用于NAD(P)H、以血红蛋白为受体的氧化还原酶活性,磷酸酶结合,血红素结合,四吡咯结合,生长因子活性,抗氧化活性,单加氧酶活性,作用于成对供体、掺入或合并氧分子、以NAD(P)H为一个供体并掺入一个氧原子的氧化还原酶活性,核受体活性,直接配体调节的序列特异性DNA结合的转录因子活性等。见图5。
2.6 KEGG通路富集分析 当归补血汤治疗化疗相关性骨髓抑制的信号通路主要包括流体剪切应力与动脉粥样硬化通路,糖尿病并发症中的AGE-RAGE信号通路,恰加斯病通路,HIF-1信号通路,人巨细胞病毒感染通路,IL-17信号通路,TNF信号通路,JAK-STAT信号通路,铂类药物耐药通路,EGFR酪氨酸激酶抑制剂耐药通路等。见图6。

图5 关键靶基因GO功能富集

图6 关键靶基因KEGG通路富集
3 讨论
传统中医并无“骨髓抑制”这一病名,通过患者乏力纳差、心悸短气、头晕目眩、倦怠自汗等症状推断出化疗相关性骨髓抑制的主要病机是气血不足[8]。而化疗药物性情刚猛,为有毒之物,易损伤脏腑。中医学气血生化理论认为,肾为先天之本,藏精之处,主骨生髓;脾为后天之本,气血生化之源,故脾肾两脏与气血生化密切相关,治疗化疗相关性骨髓抑制时多从这两脏入手。
本研究最终得到22个当归补血汤的活性成分,预测出槲皮素,山奈酚,异鼠李素可能是当归补血汤治疗化疗相关性骨髓抑制的关键成分。已有研究表明,槲皮素无论在体内还是体外都可以显著降低依托泊苷对DNA的氧化损伤,同时也能显著减少由依托泊苷引起的骨髓前体细胞和红系有核细胞的减少[4],另外,闵珺[5]发现槲皮素可以通过调控PI3K/Akt/FoxO1/NF-kB信号通路并抑制自由氧释放来抵抗TNF-α诱导的骨髓间充质干细胞(BMSCs)凋亡,而BMSCs与造血干细胞关系密切,不仅对其有机械支持作用还能分泌IL-6,IL-11等生长因子促进造血。山奈酚对小型猪肝微粒体系统中的羟基自由基具有显著保护作用,从而可以减轻阿霉素导致的骨髓抑制[6]。山奈酚也可以通过下调ROS/Fox O信号通路抑制氧化反应导致的BMSCs凋亡现象[7]。异鼠李素可以抑制RANKL诱导的骨髓巨噬细胞中的MAPK、NF-κB和AKT信号通路的活化[8]。
通过关键靶基因的PPI蛋白互作分析,得到PPI网络的核心基因,其中AKT1、IL-6、VEGFA、CXCL8以及IL1B位于核心位置。AKT1基因对多种细胞功能至关重要,在PI3K/Akt1信号通路中占据重要地位,是维持长期造血干细胞功能的调节因子[9]。IL-6具有显著造血调控作用,其具有促进造血干细胞从G0期进入G1期,促进髓系前体细胞增殖分化以及促进晚期红系造血等功能[10],已有研究表明IL-6可以显著提高化疗后小鼠外周血中血小板及中性粒细胞的数量[11]。VEGFA是VEGF家族中最主要的因子,其信号转导对内皮和造血干细胞的表达至关重要[12],而VEGF可通过自分泌环控制造血干细胞的存活和再增殖而调节造血功能[13]。CXCL8对中性粒细胞、T淋巴细胞具有趋化作用,并能促进骨髓前体细胞以及多能造血干细胞进入外周血[14]。IL1B在稳态造血和紧急造血中发挥重要作用,其可以通过诱导IL-17的产生和分泌,继而诱导粒细胞集落刺激因子的产生和分泌促进造血干细胞和髓细胞的增殖[15],其次,也可以通过驱动产生IL-6来进行造血调控。
当归补血汤治疗化疗相关性骨髓抑制关键靶基因的生物学过程富集分析表明,靶基因关联的生物学过程主要涉及细胞因子活性,细胞因子受体结合,受体配体活性,生长因子受体结合,蛋白磷酸酶结合等。这些生物学过程都在关键靶基因和具体通路过程中得到体现。骨髓是一个天然的低氧腔室,HIF-1信号通路介导造血干细胞对低氧的反应,可以通过调控Notch受体、VEGFA以及CXCR4保障造血干细胞的存活、调控造血干细胞的更新和分化[16]。IL-17信号通路与炎症反应、免疫调节以及肿瘤密切相关。研究发现,大部分肿瘤患者血清中的IL-17表达水平高于正常人[17],化疗会诱导IL-17快速而显著侵袭[18],而IL-17过高表达则会抑制造血功能,故当归补血汤可能通过作用于此信号通路,降低外周血中IL-17等炎性因子的表达,减少造血干细胞的破坏及骨髓微环境的失衡,从而发挥治疗作用的。此外,当归补血汤还通过细胞凋亡通路、MAPK信号通路等多个与造血功能相关的通路以及免疫相关信号通路发挥作用。
综上所述,当归补血汤治疗化疗相关性骨髓抑制体现中药复方多成分、多靶点以及多作用途径的特点,为后续进一步探究提供一定参考。
