聚乙二醇多柔比星脂质体与表柔比星在乳腺癌新辅助化疗中的疗效比较
2021-06-11薛梦圆刘柳荫谷元廷
薛梦圆,刘柳荫,谷元廷
(郑州大学第一附属医院 乳腺外科,河南 郑州 450000)
乳腺癌是女性最常见的恶性肿瘤之一[1]。化疗作为乳腺癌治疗手段的重要组成部分,明显改善了乳腺癌患者的预后[2]。新辅助化疗(neoadjuvant chemotherapy,NAC)即在手术切除肿瘤前进行全身化疗,已经成为局部晚期乳腺癌患者首选的初始疗法组成部分,NAC可以提高实施保乳手术的机会,并使不可手术的肿瘤被切除[3-4]。NAC提供了研究肿瘤早期系统治疗、评估治疗效果以及化疗生物学效应的机会[5]。术前的全身化疗也为根除肿瘤细胞远处的微转移提供了可能性,从而提高整体治疗效果[6]。以蒽环类和紫杉类药物为基础的NAC是局部晚期乳腺癌的推荐治疗方法,传统蒽环类药物在给患者带来显著临床效果的同时也带来药物相关的毒性反应[7]。聚乙二醇多柔比星脂质体(pegylated liposomal doxorubicin,PLD)已被证明与常规多柔比星疗效相似,同时呕吐、骨髓抑制、心脏毒性等发生率较低[8]。表柔比星(epirubicin,EPI)也是乳腺癌化疗常用的蒽环类药物之一。然而,关于PLD与EPI疗效对比的临床数据不足,国内外报道较少。本研究回顾性对比PLD与EPI在乳腺癌NAC中的疗效。
1 资料与方法
1.1 一般资料选取郑州大学第一附属医院乳腺外二科2016年1月至2020年5月收治的接受NAC的121例乳腺癌患者作为研究对象,年龄22~69岁。本研究获得郑州大学第一附属医院医学伦理委员会批准。
1.2 选取标准(1)纳入标准。①根据2020年版中国临床肿瘤学会(Chinese Society of Clinical Oncology,CSCO)乳腺癌诊疗指南所示,满足以下条件之一者可选择术前NAC治疗:a.肿块较大(>5 cm);b.腋窝淋巴结转移;c.HER-2阳性;d.三阴型;e.有保乳意愿,但肿瘤大小与乳房体积比值高,难以保乳。②女性。③美国东部肿瘤协作组性能状况≤2。④预期寿命在6个月以上。⑤无明显心脏疾病临床症状(美国纽约心脏病协会心功能分级≤Ⅱ级)。⑥器官功能:a.左室射血分数>50%;b.肌酐值为44~133 μmol·L-1;c.胆红素<1倍正常上限值;d.谷丙转氨酶和谷草转氨酶<1倍正常上限值(肝转移患者谷丙转氨酶或谷草转氨酶<65倍正常上限值);e.碱性磷酸酶<1倍正常上限值。⑦骨髓功能:a.血小板≥100×109L-1;b.中性粒细胞绝对值≥2×109L-1;c.白细胞≥4.0×109L-1;d.血红蛋白>90 g·L-1。(2)排除标准:①曾接受过任何乳腺癌相关治疗;②对化疗药物或类似化疗药物成分过敏;③有任何其他严重或不受控制的全身疾病;④脾切除;⑤心理、家庭、社会或地理条件可能影响治疗依从性;⑥妊娠或者哺乳期。
1.3 治疗方法根据治疗方法将患者分为PLD组和EPI组。PLD组:第1天接受600 mg·m-2注射用环磷酰胺(Baxter Oncology GmbH,批准文号H20160467)和45 mg·m-2PLD(石药集团欧意药业有限公司,国药准字H20113320)静滴,治疗4个周期。EPI组:第1天接受600 mg·m-2注射用环磷酰胺和100 mg·m-2EPI[辉瑞制药(无锡)有限公司,国药准字H20000496]静滴,治疗4个周期。每个周期间隔14 d,然后接受4个周期的紫杉烷类药物治疗。两组中Her-2基因扩增的患者联合注射用曲妥珠单抗[Roche Pharma(Schweiz)Ltd.,批准文号J20170037]治疗,首次剂量为8 mg·kg-1,以后每次6 mg·kg-1,每21 d静脉注射1次,持续17个周期。当患者出现3级或4级白细胞减少、血小板减少、贫血、胆红素水平升高、口腔炎、手足综合征等毒副反应时,可减少PLD的剂量。EPI剂量调整也适用于白细胞减少或其他3级或4级的毒副反应。若毒副反应造成的影响持续进展,则停止治疗。若使用对症支持治疗,如镇痛药、止吐药、抗生素、骨髓生长因子以及输血和血液制品等,均被记录在病例报告表上。另根据中国乳腺癌新辅助治疗专家共识(2019年版)内容,每2个治疗周期后需要对疗效进行评估,当疗效为疾病稳定(stable disease,SD)或疾病进展(progressive disease,PD)时,则更换化疗药物。当患者完成NAC后,根据最佳的实践标准和患者意愿为患者制定后续的治疗方案,后续的治疗策略参考2020年版CSCO乳腺癌诊疗指南进行,例如完成根治术或保乳术、靶向治疗、保乳和腋窝淋巴结转移患者术后接受放疗以及激素受体阳性患者接受内分泌治疗等。
1.4 观察指标(1)在首次化疗前检查内容如下。①肿瘤相关评估:a.病理诊断和肿瘤临床分期;b.肿瘤病理类型、组织学分级、分子特征(HER-2、ER、PR、Ki-67);c.肿瘤瘤床定位。②自身状况评估:a.既往史(尤其需关注与治疗相关的重要病史);b.体格检查;c.一般血液学检查;d.主要器官功能(包括肝、肾、心脏);e.心理评估及疏导;f.育龄期女性必要时进行生育咨询。另外,化疗期间每次化疗前需对患者进行体格检查及实验室评估,化疗第8天复查血常规,对于白细胞或中性粒细胞计数较低患者给予短效粒细胞集落刺激因子注射液,每2个周期复查乳腺彩超、淋巴结彩超、心脏超声和磁共振成像,对于心脏彩超显示异常的患者加做心电图。(2)参考《实体肿瘤疗效评价标准1.1》评价PLD和EPI的化疗效果。对于靶病灶:所有靶病灶消失,全部病理淋巴结(包括靶结节和非靶结节)短直径必须减少至<10 mm为完全缓解(complete response,CR);靶病灶直径之和比基线水平减少至少30%为部分缓解(partial response,PR);靶病灶减小的程度未达到PR,增加的程度也未达到PD水平,介于两者之间为SD;以整个研究过程中所有测量的靶病灶直径之和的最小值为参照,直径和相对增加至少20%(如果基线测量值最小就以基线值为参照),除此之外,必须满足直径和的绝对值增加至少 5 mm为PD,出现1个或多个新病灶也视为PD。对于非靶病灶:所有非靶病灶消失,且肿瘤标志物恢复至正常水平,所有淋巴结非病理尺寸短径<10 mm为CR;存在1个或多个非靶病灶或持续存在肿瘤标志物水平超出正常水平为SD;已存在的非靶病灶出现明确进展为PD,出现1个或多个新病灶也被视为PD。总体有效(overall effective,OR)率为CR例数与PR例数之和除以总例数,总体无效(overall invalid,OI)率为SD例数与PD例数之和除以总例数。(3)参考美国国立癌症研究所常见毒性反应标准第5版对毒副反应进行分级。
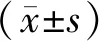
2 结果
2.1 基本情况PLD组年龄为(47.32±7.94)岁,EPI组年龄为(47.06±10.13)岁,两组患者年龄比较,差异无统计学意义(t=0.140,P=0.889)。两组患者临床分期、病理类型、组织学分级、分子分型比较,差异无统计学意义(P>0.05)。见表1。
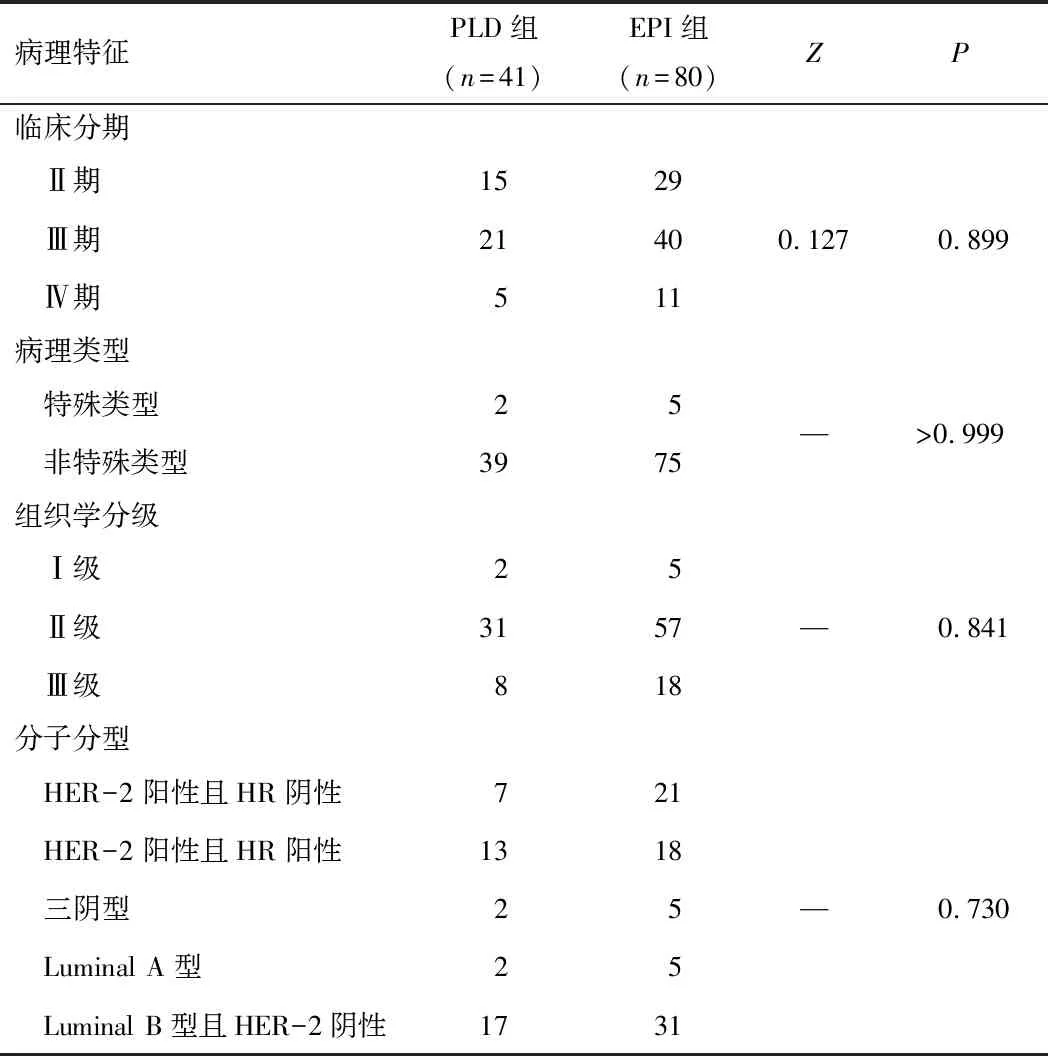
表1 PLD组和EPI组患者病理特征比较
2.2 疗效
2.2.1总体疗效 两组OR率比较,差异无统计学意义(P>0.05)。见表2。
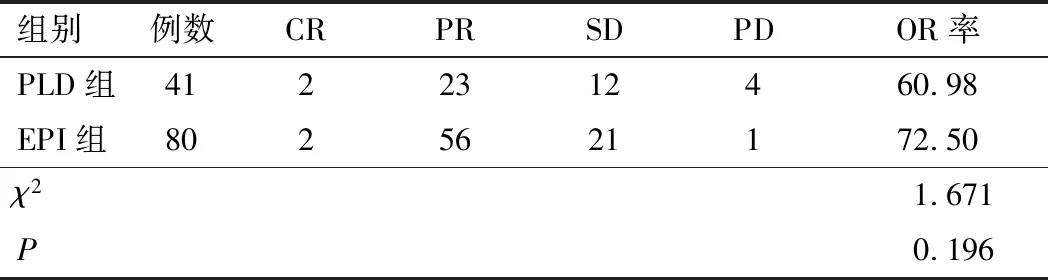
表2 PLD组和EPI组疗效比较(n,%)
2.2.2不同分子分型疗效 PLD组和EPI组各分子分型疗效比较,差异无统计学意义(P>0.05)。见表3。

表3 PLD组和EPI组各分子分型疗效比较[n(%)]
2.3 毒副反应PLD组白细胞减少、呕吐、脱发发生率均低于EPI组,口腔炎、手足综合征发生率均高于EPI组(P<0.05)。大多数不良事件是轻微的、短暂的或可管理的。见表4。
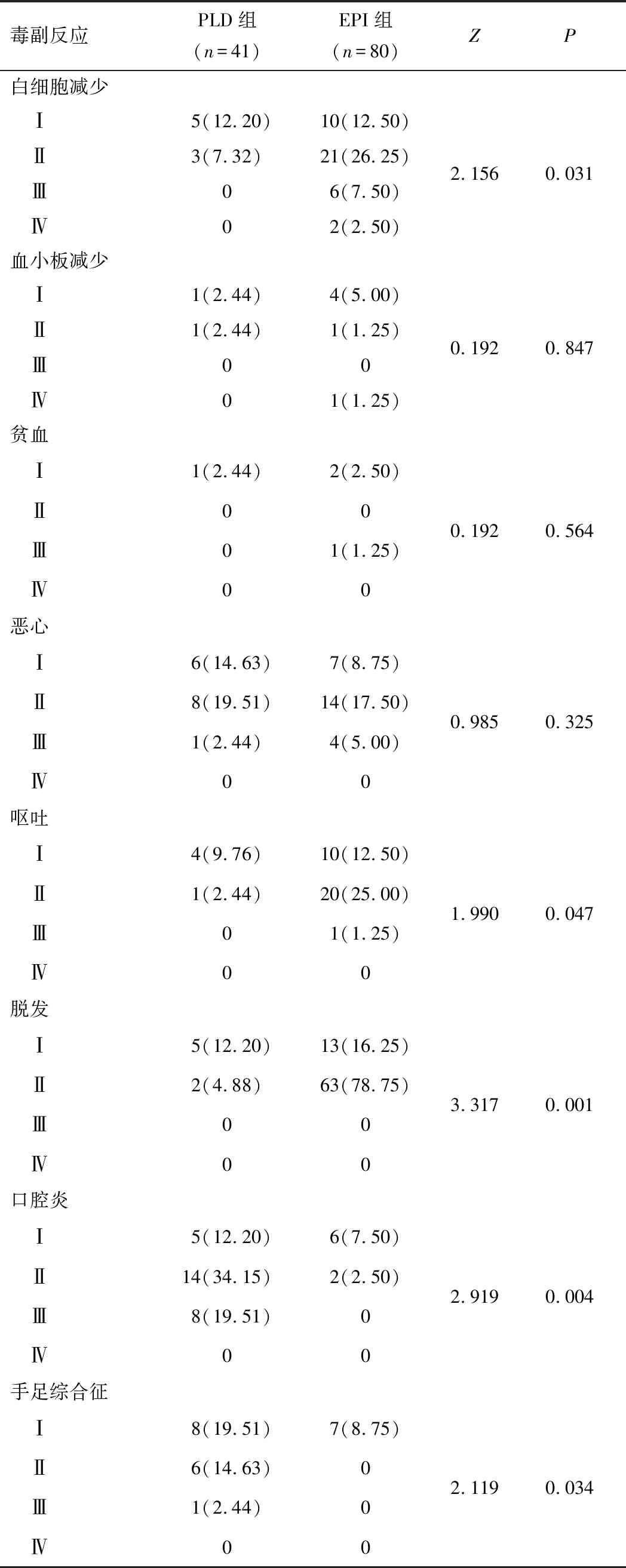
表4 PLD组与EPI组毒副反应比较[n(%)]
3 讨论
蒽环类化疗药物是一种经典的抗肿瘤药物,对乳腺癌患者具有良好的临床疗效,然而它的临床效果却受到治疗相关毒性的限制。本研究中PLD和EPI都是阿霉素的优良变构体,在乳腺癌化疗中作为基础药物被广泛应用[9]。
PLD是一种聚乙二醇包覆的多柔比星脂质体,具有较长的循环时间和不同的毒性特征[10-11]。其外部的磷脂分子为双亲分子,有利于提高溶解度,在血液循环中几乎100%以脂质体形式存在,脂质体被生物降解后,药物缓慢释放,体内半衰期为55~70 h,明显长于常规阿霉素的半衰期(10 min)。此外,脂质体不能通过正常组织的血管间隙,却可以通过肿瘤组织的血管间隙,有利于肿瘤组织对药物的最大摄取,这种脂质体结构可以降低经典蒽环类药物的毒性,并保持其有效性。
本研究中PLD组与EPI组患者病理特征对比无差异,具有可比性。本研究结果显示:PLD与EPI总体临床疗效相当,且各分子分型疗效比较无差异,而PLD骨髓抑制较弱,且呕吐、脱发发生率均低于EPI。虽然PLD的皮肤毒性(口腔炎、手足综合征)发生率较高,但与骨髓抑制不同,这种副作用不会危及生命。对于化疗引起的手足综合征,虽然目前还无明确的治疗方法,但通过适当的支持性护理措施是可逆、可管理的。穿宽松的衣服、避免暴露在高温环境中以及避免剧烈运动等措施可能会使手足综合征的发生率降低。PLD清除率的改变具有临床意义,因为PLD较长的半衰期已被发现会引起更高的皮肤毒性风险。而紫杉烷类等能延缓PLD清除速率的药物会提高皮肤毒性的发生风险和严重程度。对于蒽环类药物的研究表明其最严重的不良反应是心脏毒性,然而在本研究中因为样本量小且观察时间短,未发现表现出心脏毒性的患者。PLD在NAC中的疗效与EPI相当,且较安全,这为PLD在乳腺癌NAC中的应用提供了依据。PLD可作为具有骨髓危险因素(患有血液疾病、高龄或既往接受过蒽环类药物治疗等)患者的优选药物。而且对于女性患者来说,PLD的低脱发发生率可以满足其对美观的需求,减轻心理负担,这对于乳腺癌患者的治疗是有益的。对于需要新辅助化疗的乳腺癌患者来说,PLD是一种安全有效的NAC药物,因为绝大多数与该药物有关的毒副反应都是可以控制的。
