自制β-人绒毛膜促性腺激素、孕酮室内质控品及初步评价
2021-06-11裴蕴锋张先梅
裴蕴锋,张先梅
(江苏省徐州市中心医院检验科,江苏 徐州 221009)
血清β-人绒毛膜促性腺激素(β-HCG)、孕酮(PG)定量检测,作为妊娠过程监测的常规检查项目[1-2],临床实验室检测方法众多,但因技术平台的不同,试剂质量不一,各生产厂商仪器间检测结果缺乏可比性,在这种情况下,有稳定可靠的室内质控品显得十分重要。为保证检验质量,降低运行成本,我们尝试自制混合血清β-HCG、PG质控品,现将初步应用结果及评价报道如下。
1 材料与方法
1.1 试剂和仪器 β-HCG、PG试剂盒和定标液均购自安图生物工程有限公司。仪器使用安图生物工程有限公司AutoLumo A2000全自动化学发光免疫分析仪。
1.2 方法
1.2.1 β-HCG、PG质控血清的制备:根据中国合格评定国家认可委员会(CNAS)-GL005:2018文件要求[3],收集2020年6月徐州市中心医院产科孕妇及女性健康体检者血清,经检测乙型肝炎表面抗原、丙型肝炎病毒、人类免疫缺陷病毒等指标均为阴性,血清无溶血、黄疸、脂血。
1.2.1.1 低值、高值血清收集:β-HCG收集低值20 mIU/mL左右、高值300 mIU/mL左右的血清;PG收集低值4.0 ng/mL左右、高值35.0 ng/mL左右的血清。分别混合标本血清。
1.2.1.2 血清灭活:混合血清经56 ℃加热30 min灭活。
1.2.1.3 离心去除沉淀物:1 500 r/min,水平转子大型离心机,离心30 min,取上清备用。
1.2.1.4 防腐分装:用0.2 g/L叠氮钠防腐,取有盖离心管按0.2 mL/管,分装后按照不同的批号分别于-20 ℃冰冻保存备用。
1.2.2 自制β-HCG、PG血清质控品的性能评价:
1.2.2.1 仪器定标校正:测定前,将仪器重新定标并使用原厂校正品做好仪器校正,使仪器处于最佳测定状态,每次按需取出相应的自制β-HCG、PG质控品,经室温融化平衡30 min,轻轻混匀后测定,并做好结果记录。
1.2.2.2 不精密度测定:批内不精密度测定:在同一天内,分别对自制β-HCG、PG两水平质控品各进行20 次测定,分别计算平均值(x)、标准差(s)、变异系数(CV)。批间不精密度测定:每天分别对自制β-HCG、PG两水平浓度质控品随标本批次各测定1 次,连续测定20 d,分别计算x、s、CV。
1.2.2.3 稳定性比较:将β-HCG、PG自制质控血清放置-20℃冷冻保存,每工作日取出,测定β-HCG、PG低值和高值各1 次,连续测定6 个月,分别统计每个月的x、s,观察自制混合血清质控品的稳定性。
1.2.2.4 均匀性评估:随机抽取已分装在-20 ℃冰箱中的两浓度水平的β-HCG、PG质控品各10 支,共计40 支。经室温融化后混匀,测定3 次并计算其x、s、CV值,以观察瓶间均匀性是否良好[4]。
1.3 统计学分析 采用SPSS 13.0统计软件包进行分析。所有数据均以均数±标准差(±s)表示;多组比较采用单因素方差分析,P<0.05为差异有统计学意义。
2 结果
2.1 自制β-HCG、PG质控血清批内和批间不精密度检测结果见表1、表2。
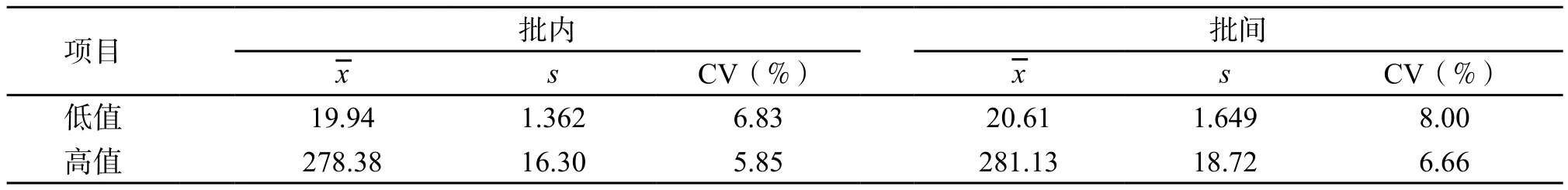
表1 自制β-HCG质控血清批内和批间不精密度
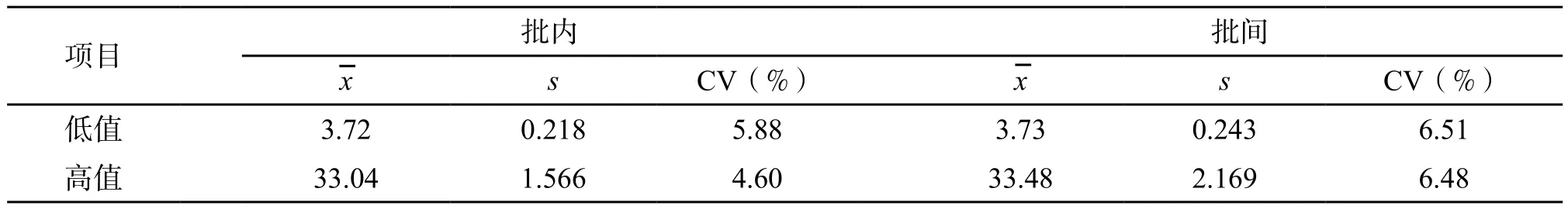
表2 自制PG质控血清批内和批间不精密度
2.2 自制β-HCG、PG质控血清稳定性比较 结果见表3。经单因素方差分析,自制β-HCG、PG低值和高值质控品每个月结果间的差异无统计学意义(P值均>0.05)。2.3 自制β-HCG、PG质控品瓶间均匀性评估 β-HCG质控血清低值为(19.78±0.669)mIU/mL,CV 3.38%;高值(280.10±7.818)mIU/mL,CV 2.79%。PG质控血清低值为(3.72±0.229)ng/mL,CV 6.15%;高值(33.16±0.766)ng/mL,CV 2.31%。均满足<1/3 TEA的室内质控要求[5],提示瓶间均匀性良好。
表3 自制β-HCG、PG质控品稳定性(±s)

表3 自制β-HCG、PG质控品稳定性(±s)
时间 β-HCG(mIU/mL) PG(ng/mL)低值 高值 低值 高值2020年7月 20.61±1.649 281.13±18.72 3.73±0.24 33.48±2.17 2020年8月 20.24±1.655 280.04±19.46 3.76±0.18 34.01±2.49 2020年9月 19.70±1.613 278.36±21.64 3.72±0.21 34.33±2.35 2020年10月 19.50±1.453 281.33±19.89 3.73±0.18 34.02±1.98 2020年11月 20.06±1.621 281.03±20.68 3.73±0.20 33.85±2.58 2020年12月 19.94±1.656 281.28±19.90 3.75±0.20 33.44±2.49 F 1.155 0.064 0.088 0.435 P 0.336 0.997 0.994 0.824
3 讨论
β-HCG主要由胎盘滋养层细胞分泌,在妊娠后的开始几周分泌成倍增加,起到维持卵巢黄体分泌功能,满足早期胚胎发育需要的重要作用,在怀孕后8~12 周β-HCG达到峰值。早孕阶段,如β-HCG水平不随孕龄增长呈倍增态势或有回落,则提示可能有宫内孕囊发育不良、早孕流产迹象[6-7]。PG同样在妊娠过程中十分重要,足量PG可保证子宫内膜功能正常,促进胚胎生长发育,避免母体发生胚胎排异反应。PG能降低肌纤维兴奋性,进而降低孕妇子宫对缩宫素敏感性,为妊娠顺利进行提供保证。正常情况下,早孕孕妇PG水平随孕龄增加而稳步增长。PG水平下降,则提示孕妇可能不能维持正常妊娠[8-9],因此,血清PG可以作为判断早孕先兆流产的有效指标之一。目前,国内医疗单位使用的β-HCG、PG检测方法学不同,实验室间结果相差较大,使得β-HCG、PG临床应用受到影响,尤其是一些基层医疗单位,因质控品价格昂贵的影响,甚至室内质控不能正常开展。据于此,我们尝试制备相对简单、成本低廉、质量满足实验室需求的室内质控品,在指导基层卫生院质量保证上做出努力。应用血清标本的好处之一就是基质同临床检测标本完全一致,不添加任何物质[10]。其次,考虑到正常及妊娠情况下的β-HCG、PG血清浓度范围,质控品设计了2个不同水平。在血清标本的选择上,除了有浓度范围的要求外,同时也对传染性指标进行检测,保证自制质控品的生物安全性。性能评价,主要考量稳定性及瓶间均一性。
通过评价β-HCG、PG低值和高值两个水平自制混合血清质控品的不精密度、6 个月稳定性及瓶间均匀性,所有观察指标均能满足实验室要求。批内、批间不精密度,符合美国临床生物化学学会(NACB)检验要求,-20 ℃保存6个月稳定(P>0.05);结果显示瓶间变异系数较小,均匀性良好。
初步评估结果显示,自制β-HCG、PG混合血清质控品符合化学发光免疫法室内质控品要求,制作简单、结果稳定,尤其为基层临床实验室β-HCG、PG检测的室内质控提供了有效解决方案。同样,这个自制质控血清也可作为使用POCT方法质控品,对β-HCG、PG急诊检验质量提高具有一定意义。
