氮化碳纳米片的合成、结构表征和光催化性能测试
——基于科教融合的化学综合实验
2021-06-08张明文陈仪魏小莲陈益宾
张明文,陈仪,魏小莲,陈益宾
(福建技术师范学院材料与环境科学学院,福建福清 350300)
科教融合将科研与教学在形式和内容上互相渗透,是培养应用和创新兼备型人才的有效途径[1].针对化学专业本科生的人才培养,应在现有的基础上,积极通过科教深度融合的教学模式进行人才培养:一方面,教师的创新研究应因地制宜转变为教学内容,让学生有机会接触到最新、最前沿的化学相关学科知识;另一方面,科学研究应作为本科培养的一种有效方式,鼓励学生参与创新研究,培养学生的实践能力[2].
化学综合实验是在教育部《关于进一步加强高等学校本科教学工作的若干意见》中“增加综合性与创新性实验,引导大学生了解多种学术观点并开展讨论,追踪本学科领域最新进展,提高自主学习和独立研究的能力”的号召下,在无机、分析、物化、有机等基础化学实验的基础上,开设的综合性实验课程,旨在强化化学相关知识和实验方法的综合应用,最终达到解决化学相关方面综合问题的目的[3].在“科教融合”大背景下的化学综合实验,不仅要能够突出应用型高校的办学特色和专业特点,还要利用学校在教学和科研方面的资源,让学生能够有意识地聚焦科技前沿,抓住关键科学问题,设计合理的实验方案,通过一系列的实验手段,借助相关基础化学理论知识进行分析讨论,从而解决相关科学问题[4].本文结合了化学综合实验教学目的和自身科研成果,引导学生关注当今社会能源短缺和环境污染的现实问题,以光催化新兴技术为切入点,将探寻兼具量子效率、可见光利用率、稳定性和经济性的光催化剂为目标,设计了题为“氮化碳纳米片光催化剂的合成、结构表征和性能测试”的综合化学实验.本实验新颖、成熟、安全、低耗,将前沿科学研究理念与启发式教学相结合,不仅提升了学生对前沿科技的洞察力,而且强化了学生基础化学实验操作和理论知识综合运用,有助于学生创新能力的提高.
1 教学设计的背景及意义
现代工业化的迅猛发展,大量消耗不可再生的化石燃料,同时排放出有毒污染物,引发严峻的能源危机和环境恶化等问题[5].以罗丹明B为例[6],它是一种典型的碱性三苯甲烷类染料,稳定性强、难以降解,进入到环境后容易造成环境污染,有一定的致癌性.若以罗丹明B为对象进行降解研究,能够给三苯甲烷染料废水治理带来一定的参考价值.
半导体光催化技术是一个多学科交叉的新兴研究领域[7].该技术可将低密度的太阳能转化为高密度的化学能(如氢气、甲烷等),亦或以太阳光作为驱动力来降解、矿化有机污染物,有望解决能源短缺和环境污染等问题.现市面上已出现相关以光催化技术为核心的环境污染控制技术[8].该技术领域的核心课题是研制太阳能利用率高、稳定性强、廉价易得的光催化剂.传统的半导体光催化剂主要为含过渡金属的化合物[5].然而它们之中尚无法同时满足上述要求,且主要组分大都包含昂贵的稀有金属元素,难以实现大规模实际应用.氮化碳(g-CN)具有类似石墨的层状结构,层层之间通过范德华力连接,而层内多以七嗪为基本单元通过N原子桥连起来,结构模型如图1.基本单元中的C和N原子都发生sp2杂化,而未杂化的pz轨道可以形成大的芳环π键,构成一个高度离域的共轭体系.这样的共轭体系使其具有半导体的能带结构,能吸收波长小于460 nm的光,并激发出有一定还原性的电子和一定氧化性的空穴,参与各类匹配的还原氧化反应.g-CN可由多种富含N的有机小分子通过热聚合的方式合成;g-CN不溶于酸、碱或有机溶剂,是一种非常稳定的材料;其聚合物的本质有利于从分子层面上通过表面化学工程手段来调控g-CN的化学性质.因此g-CN作为一种不含金属组分的可见光光催化剂,具有廉价、稳定、易于改性等特点,广泛用于光催化水的分解、有机物的绿色合成、有机污染物的降解矿化等,至今仍是前沿科研的热点材料[10].然而,较高的光生电子和空穴的复合率,较低的可见光响应(无法吸收大于460 nm波长的光)和表面传质效率等,限制了g-CN的实际应用.针对这些科学难题,科研人员开展了大量的改性研究工作来优化g-CN的光催化活性,包括制备方法优化与纳米结构设计、元素掺杂、共聚合改性、异质结构筑等.
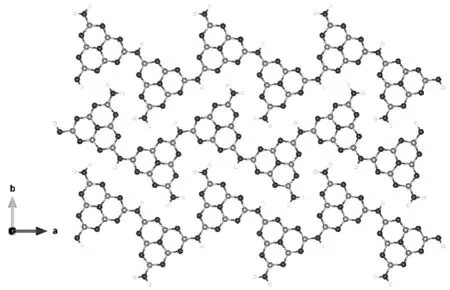
图1 最常见的g-CN单层结构模型[9]
本文所涉及的科教融合化学综合实验教学设计,应在学生掌握化学学科理论知识和实验的基础上,引导学生关注环境治理的迫切需求,以氮化碳光催化剂这一热点材料为例,让学生在纳米材料的可控合成、结构表征和光降解罗丹明B性能研究等方面开展实验.学生可以通过文献调研与学习,参与综合创新实验的相关具体设计与实验,培养学生自主参与科学研究的兴趣,掌握开展科学研究应具备的能力,提高其创新能力和综合应用能力[11].
2 实验设计
2.1 实验目的
1)了解半导体光催化技术的原理;
2)了解g-CN的结构特点,掌握合成g-CN纳米片的方法;
3)掌握常见的结构、形貌表征手段的基本原理和操作流程;
4)掌握光催化染料降解测试流程,综合分析“构—效”关系.
2.2 实验原理
2.2.1 半导体光催化
半导体光催化技术是一个多学科交叉的新兴研究领域[7].光催化过程主要以半导体的能带结构理论为主:能带分为价带(能量低,充满电子)和导带(能量高,电子未充满),价带、导带间的宽度称为禁带宽度(Eg);当入射光的能量大于半导体的禁带宽度(hv≥ Eg)时,价带上的电子将会被激发到导带上,价带则因少一个电子而产生一个带正电的空穴;光生电子和空穴分别具有较强的失电子和得电子的能力,蕴含一定的化学势;它们若顺利迁移到材料表面接触到反应物,且符合反应热力学要求,即可参与相关反应,显示出还原性和氧化性.
2.2.2 氮化碳光催化剂
聚合物氮化碳(g-CN)是通过富含N的有机物(如氰胺、二聚氰胺、三聚氰胺等)通过高温热聚合的方式获得,所得产物以七嗪碳氮杂环(C6N7)为单元通过桥连的N原子相连形成准二维的平面结构.该平面中,C和N原子部分轨道发生sp2杂化形成C-N键,而未杂化的pz轨道则共轭成类似石墨烯的高度离域的结构.因此g-CN稳定性较强,有一定的半导体性能.然而常规热聚合方法只能合成出无规则块体的微观形貌,其在实际应用中受限较多,如光生电荷复合率高等.g-CN纳米片具有各向异性的结构特点:暴露出较大的微观接触面,有利于太阳光的捕获和反应物的传质作用;其较小的片层厚度,缩短了光生电荷从材料内部到表面的迁移距离.因此g-CN纳米片在光催化领域的应用具有较大的优势[12].本实验引入三种操作简便的方法来制备g-CN纳米片,并对其进行结构和性能的对比:以二聚氰胺为原料、氯化铵为助剂的软模板法;在体相g-CN的基础上通过二次热处理的热剥离法;以尿素为原料的自模板法.实验过程中,可对学生进行分组,让学生自行选择其中一种方法来合成氮化碳纳米片.实验结束后,可将所有学生的数据进行合理共用,以此探究不同纳米片合成方法对结构和光催化降解罗丹明B性能的影响.
2.2.3 粉末X射线衍射仪
粉末X射线衍射仪常用于分析多晶粉末样品.基本原理是通过一束单波长的X射线照射到随机取向分布的粉末固体上,根据采集器上采集的反射X射线谱线特征,借助Jade软件进行进一步的拟合分析,即可获得样品的晶型属性、结晶度高低和晶面间距变化等晶体结构特征[13].
2.2.4 傅里叶红外光谱仪
当不同红外波长的光通过不同的化学基团时,其光波吸收情况不同,产生特征吸收峰;不同化合物中相同基团的特征吸收峰大致相同.因此通过红外光谱可以分析化合物中存在的官能团和微观化学结构.本实验涉及的氮化碳材料属于由C、N、H非金属元素组成的共轭共价材料,其表面含有丰富的官能团,如-NH2,C-N等,具有极其丰富的红外光谱信息,因此可用傅里叶红外光谱仪来表征样品的化学结构.
2.2.5 扫描电子显微镜
扫描电子显微镜是一种微观形貌的分析工具,其分辨率高于光学显微镜.它主要利用聚焦的高能电子束以光栅状扫描的方式逐点轰击到样品表面,激发出的不同深度的二次电子信号被样品上方多种信号接收器接收,再通过放大器同步传送到电脑显示屏,将样品微观特征形成实时立体图像显示出来[14].2.2.6 紫外-可见分光光度计
波长在紫外-可见范围内的光通过物质时,会被选择性的吸收,进而引发物质分子振动能级跃迁和电子能级跃迁[15].多数有机染料分子中具有较多的共轭键和发色团,在200~800 nm波长间有一个特定的吸收峰.利用紫外-可见分光光度计测定有机染料溶液中的特征吸收峰相对强度值,可定性、定量分析该染料分子在溶液中的浓度,从而研究光降解反应速率.
2.3 实验试剂和仪器
2.3.1 试剂
二聚氰胺,氯化铵,尿素,罗丹明B,去离子水.
2.3.2 仪器
分析天平,研钵,带盖坩埚,高温马弗炉,粉末X射线衍射仪(XRD),傅里叶红外光谱仪(FT-IR),扫描电子显微镜(SEM),鼓风干燥箱,超声机,光催化染料降解装置,离心机,离心管,容量瓶,量筒,滴管,紫外-可见分光光度计.
2.4 实验内容
2.4.1 体相g-CN和g-CN纳米片的合成
将学生进行分组,每组同学选择1~2种氮化碳纳米片的合成方法,并将所合成样品与CN-B进行结构和性能等方面的对比.
体相g-CN:5.0 g二聚氰胺置于带盖坩埚,放入高温马弗炉进行煅烧(程序:以2.3℃/min的速率从室温升温至550 ℃,保温240 min).所得黄色块状物置于研钵中研磨30 min.记为CN-B.
g-CN纳米片-软模板法:1.0 g二聚氰胺和适量的氯化铵(氯化铵的质量可让学生在一定范围内自行选择,如:3 g,5 g,7 g),置于研钵中充分研磨,移入带盖坩埚,放入高温马弗炉进行煅烧(程序:以2.3 ℃/min的速率从室温升温至550℃,保温240 min).所得淡黄色絮状物置于研钵中研磨5 min.记为CNA(1:X).
g-CN纳米片—热剥离法:1.0 g CN-B样品,置于带盖坩埚,放入高温马弗炉进行二次煅烧(以5.0 ℃/min的速率从室温升温至550℃,具体的保温时间可让学生在一定范围内自行选择,如:2 h,4 h,6 h).所得淡黄色絮状物用药勺刮出,并置于研钵中研磨5 min.记为CN-H.
g-CN纳米片—自模板法:称取15.0 g尿素置于带盖坩埚,放入高温马弗炉进行煅烧(程序:以5.0 ℃/min的速率从室温升温至550℃,保温时间可让学生在一定范围内自行选择,如:2 h,3 h,4 h).所得淡黄色絮状物置于研钵中研磨5 min.记为CN-U.
2.4.2 氮化碳的化学结构、晶体结构、微观形貌表征
采用Nicolet 380型傅里叶变换红外光谱仪来测定样品的化学结构:在干燥的环境下(在红外灯的持续照射下),将样品与KBr固体以1∶100的质量比进行均匀研磨,用磨具压制成薄而透明的圆片.测试条件:扫描范围为4 000~400 cm-1,循环扫描次数为32次.
采用日本岛津Ultima IV型粉末X射线衍射仪来测定样品的晶型:采用的X射线为Cu靶射线(波长为0.154 nm),工作电压为40 kV,工作电流为40 mA,扫描范围设定为2θ= 5°~ 60°,扫描步长为0.02 o/s.将样品预先用研磨至粉状,移取少量至带有粗糙凹面的载玻片上,并用另一干净的载玻片压实压平,水平移入该仪器的载物台上.
采用Thermo Scientific Q250扫描电子显微镜来观察样品的微观形貌:1)称取10 mg至1 mL水中,超声分散10 min;2)取少量导电胶黏在载物台上,滴入10 μL上述悬浮液至导电胶上,60 ℃烘箱中烘干(预先放在带盖的表面皿中,避免导电胶污染);3)将载物台进行喷金(喷金电流10 mA,时间为60 s),以增强氮化碳样品的导电性;4)放入电镜样品台,调节到不同尺度,拍摄有代表性的微观块体或纳米片状形貌的图像.
2.4.3 光催化降解罗丹明B的性能测试实验
1)罗丹明B母液的配置:采用万分之一天平准确称取干燥的罗丹明B 0.040 0 g,用去离子水进行溶解定容到500 mL容量瓶中,最终得到质量浓度为80 mg/L的标准溶液.
2)样品的光催化染料降解实验
A.打开循环冷凝水,设置循环冷凝水温度为20℃,以恒定保温夹套中的温度.
B.打开紫外-分光光度计,待稳定后设置相关参数.
C.准确量取5.0 mL的罗丹明B母液倒入反应器(扁平瓶),并加入75 mL去离子水,配制成质量浓度为10 mg/L的罗丹明B待降解溶液.取2 mL待测,此浓度记为c0.
D.称取20 mg光催化剂(氮化碳)加入上述溶液中,超声分散1 min.将反应器置于恒温夹套中,并在夹套中加入适量水.往反应瓶中加入磁力子,将装置放在搅拌器上搅拌.
E.反应器用锡箔纸盖住,进行暗吸附实验,半小时后取样(2 mL反应液)到离心管中,待测.暗吸附后,样品将达到吸附平衡.
F.打开LED灯(50 W,420 nm),灯源紧靠保温夹套外延.不同催化剂的降解速率快慢有所区别,按实际情况每隔2~30 min取样一次,每次取样2 mL,待测.待溶液无色后可停止取样.
3)紫外-可见光谱法测试罗丹明B浓度的变化
A.将待降解罗丹明B溶液移入比色皿中,测其紫外-可见吸收光谱图,确定其最强吸光度所对应的波长数值.
B.将上述暗吸附过程和光照过程中所取的悬浊液通过离心机(转数n=10 000 n/min)离心10 min,按顺序依次移取上清液到比色皿中,并在最大吸光波长处测定其吸光值,确定光催化在吸附、光降解过程中罗丹明B的浓度变化率c/c0.由于吸光度A和浓度c成正比,两者关系符合比尔朗伯定律,且同一系列待测溶液中的其它参数为固定数值,因此c/c0= A/A0.
2.5 数据处理和结果讨论
2.5.1 化学结构
将数据导出成“.CSV”的格式,并用origin软件进行作图.根据FT-IR的谱图特征,结合所学的《波谱学》课程内容,可对测试样品的化学结构做出深入地分析.如图2所示,所有氮化碳材料的FT-IR谱图有以下三组特征的红外吸收峰[16],分别位于3 500~3 000 cm-1、1 600~1 200 cm-1和 810 cm-1.其中3 500~3 000 cm-1范围内的吸收峰范围较大较宽,主要是N-H键和O-H键的伸缩振动,归属于氮化碳表面未完全聚合的氨基和材料吸附的水分子.在1 600~1 200 cm-1内的吸收峰是C=N键和C-N键的伸缩振动引起的,在810 cm-1处出现的尖峰是七嗪环的呼吸振动,这说明所合成的氮化碳具有七嗪环的分子结构.由于氮化碳纳米片的微观形貌结构开放,表面末端氨基增多,吸附水的能力较强,因此FT-IR谱图特征与体相氮化碳CN-B有一定区别,特别在3 500~3 000 cm-1范围内的红外吸收较强,亦有一定的峰的偏移,应仔细对比分析.
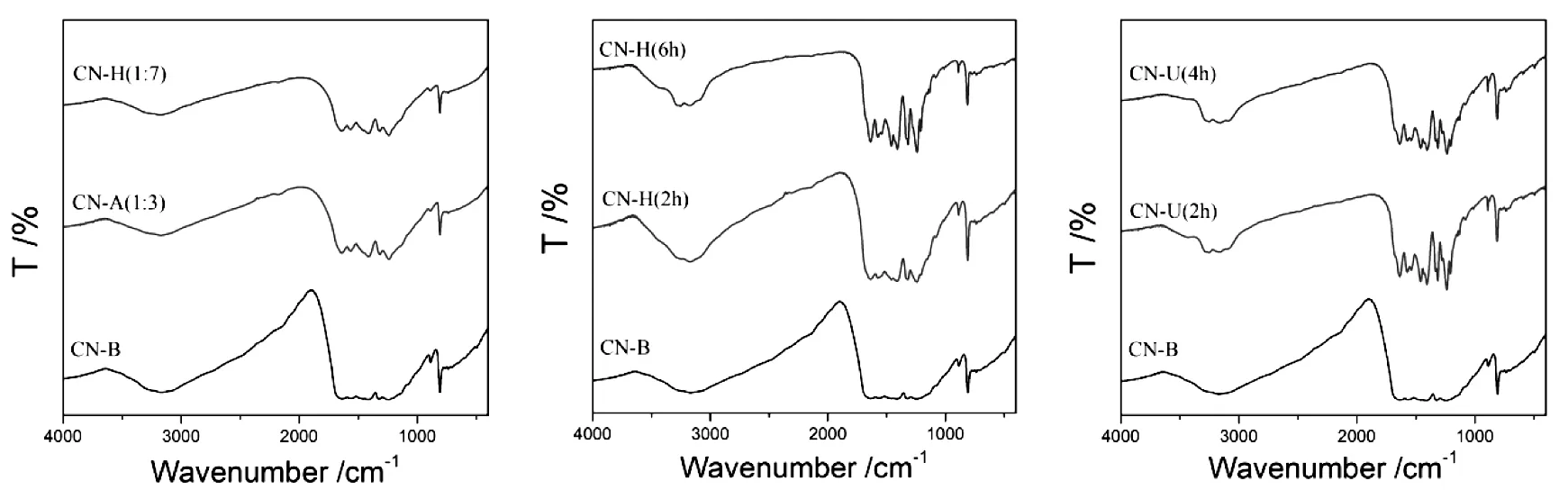
图2 体相氮化碳CN-B与不同氮化碳纳米片CN-A、CN-H、CN-U的FT-IR对比图
2.5.2 晶体结构
将数据导出成“.txt”的格式,并用origin软件进行作图.根据XRD的谱图峰的2θ值和强弱情况,对测试样品的晶体结构做出分析,如图3.体相氮化碳CN-B的XRD谱图特征有以下两个特征峰,分别位于27.4°和13.0°.其中2θ值为27.4°的主特征峰,是层间堆叠的(002)晶面衍射.2θ值为13.0°的特征峰表示氮化碳七嗪结构重复单元的(100)晶面衍射.相比于CN-B,氮化碳纳米片的XRD图相特征基本不会改变.但是由于纳米片中层间堆叠方向上的尺寸减少,因此(002)晶面衍射将会变矮变宽,即氮化碳晶型有一定程度的破坏.此外,CN-A和CN-U两种纳米片的合成方法是依靠热聚合过程中产生大量气体使氮化碳层与层的剥离,因此其层间堆叠的间距发生变化,显示出(002)峰会向高角度偏移[17].
2.5.3 微观形貌
通过SEM照片,可以将氮化碳的微观形貌进行放大,如图4.借助照片上的标尺,我们也可以测量出样品的尺寸大小.典型的体相氮化碳CN-B的SEM图是形状不规则、表面致密的板块结构.三种氮化碳纳米片的SEM照片显示出明显的片状形貌.其中,CN-H和CN-U两种纳米片由于张力的作用发生卷曲[17].从图中还能比较出,CN-U的纳米片形貌最好,且孔洞较多,这将有利于光催化性能的提升.

图3 体相氮化碳CN-B与不同氮化碳纳米片CN-A、CN-H、CN-U的XRD对比图

图4 体相氮化碳CN-B与不同氮化碳纳米片CN-A、CN-H、CN-U的SEM对比图
2.5.4 光催化染料降解
由罗丹明B的紫外-可见吸收光谱图中标出其最大吸收峰的波长位置(λ=554 nm)[6].以时间为横坐标、c/c0为纵坐标,做出罗丹明B暗吸附和光催化降解曲线图.从图5可以看出,在暗吸附过程,氮化碳纳米片显示出较大的吸附容量,这与纳米片开放的微观结构有关.不同方法合成的纳米片相比于体相氮化碳CN-B,其光催化染料降解速率都有明显的提升,其中CN-U的活性相对较高.
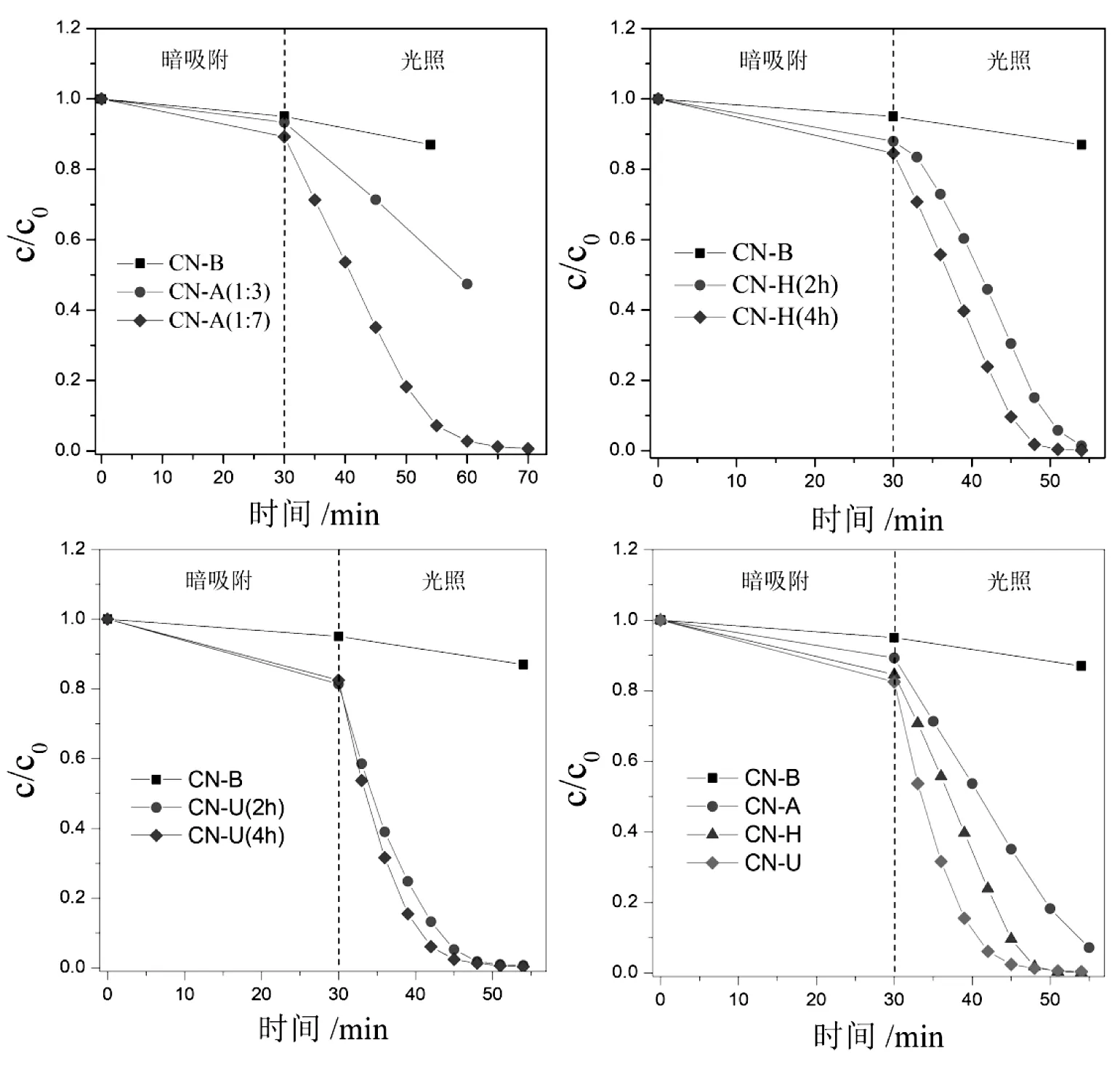
图5 体相氮化碳CN-B与不同氮化碳纳米片CN-A、CN-H、CN-U的光催化降解罗丹明B速率对比图
2.5.5 构—效关系的讨论
把所有分组的实验数据进行整合分析,讨论光催化剂的结构与效率之间的关系.引导学生从取得的实验结果和已解决的部分科学问题出发,分析讨论还存在的问题以及可能解决问题的方案.
3 教学设计
3.1 授课对象及课前准备
本实验是一门面向化学、材料相关专业的本科综合实验.本实验适用的学生层次是已掌握四大基础化学和仪器分析相关理论知识及其实验技能的大三至大四本科生.此外,学生应在实验开展前,自主进行相关项目的预习准备:查阅文献或本实验课件,了解光催化、光催化剂等相关概念及原理;了解g-CN在光催化领域的应用及常见合成、改性方法;复习XRD、FT-IR、SEM、紫外-可见分光光度计的基本工作原理和数据处理方法.
3.2 学时安排
本实验计划设置16学时,具体安排如下:
1~4学时:进行背景知识的讲解,以及样品光催化剂的合成(为节约时间,体相g-CN的制备可由老师提前合成准备;样品的合成可能需要持续等待较多时间,因此可在开始热处理1天后进行第二阶段的实验);
5~10学时:样品的结构、形貌表征测试.XRD、FT-IR、SEM三个测试操作单元各2个学时.可对学生进行分组,交替进行;
11~16学时:进行样品的光降解染料性能实验,并通过紫外-可见分光光度计测试罗丹明B浓度的变化规律.
3.3 实验过程实施
本实验依据“以问题为导向——寻求解决策略——实验探索——分析讨论——总结”的思路进行实施,引导学生互相探讨实验设计及结果,促进学生创新能力的培养.教师向学生讲解光催化技术背景和原理,介绍g-CN光催化剂的特点,让学生理解研究的意义;提出g-CN光催化剂目前存在的问题,并让学生查阅资料,确定合成g-CN纳米片的合成策略及相关工艺参数;进行分组(分成四大组:一组主要研究软模板法,二组主要研究热剥离法,三组主要研究自模板法,四组综合研究三组方法的异同;每个大组进行若干单因素变量的实验),引导学生在本实验框架下互相探讨,并进行材料制备、结构表征和性能测试实验;分析单因素变量对材料结构的影响,进而讨论对光降解性能的影响;总结“构—效”关系,并指导高效光催化剂的合成.
3.4 思考题
为了让学生更加深入地思考和学习这个实验,可以设置如下思考题供学生思考、讨论.
1)三种方法(软模板法、热剥离法和自模板法)合成g-CN纳米片的原理是什么?从体相g-CN到g-CN纳米片的过程中,最需要破坏的化学键是什么?
2)相对于体相g-CN,g-CN纳米片中的XRD图有何显著的变化趋势?为什么?
3)本实验中,如何根据溶液的吸光度值的变化初步判断光降解活性的优劣?影响光催化降解效率的因素有哪些?
4)请提出一些可行的改性策略,以实现g-CN的实际应用.
3.5 实验完成评价
实验结束后,各组同学整理相关数据结果,用origin或excel数据处理软件进行作图,并共享所有数据.通过模拟学术报告交流会的方式,对实验条件及相关实验数据进行分析讨论,并要求学生能够按照科技论文的格式完成相应实验报告的撰写.
教师应从多个方面综合评定学生的实验成绩:实验操作,能按实验步骤进行,重点考察溶液配制、移取、稀释等基础实验操作和学生实验安全意识;数据处理,合理运用相关数据处理软件,作出直观、美观的数据图,方便进行数据分析讨论;汇报讨论,对相关科研背景知识、科学原理有一定的了解,能以实际应用为导向,根据材料的特点进行针对性地改进优化,结合相关表征手段的实验数据,适当讨论材料的“构—效”关系;科技论文格式的完整性.
4 结语
本文设计了题为“氮化碳纳米片光催化剂的合成、结构表征和性能测试”的实验教学项目.首先以半导体光催化新技术为切入点,让学生聚焦科学前沿,了解氮化碳的发展现状和亟待解决的问题;其次掌握氮化碳的结构特点和合成方法,引导学生运用多种纳米材料的改性策略,制备氮化碳纳米片光催化剂;再次掌握基本的化学结构、晶体结构和微观结构表征手段,通过实验方案的合理设计,借助相关化学基础知识,分析所制备的氮化碳纳米片的结构;最后利用光催化降解罗丹明B的实验,让学生探索对比不同改性策略的特点.在该实验教学过程中,通过“引导——设计——探索”的模式,可以让学生对化学基础知识和实验操作的得到全面的巩固和提升,掌握部分大型仪器的测试方法和原理,具备前沿科学研究的洞察力,有利于创新思维和综合素质的培养.
