北京协和医院经皮心内膜心肌活检临床操作规范
2021-06-02徐希奇荆志成张抒扬
徐希奇,田 庄,方 全,荆志成,张抒扬
1中国医学科学院 北京协和医学院 北京协和医院心内科,北京 100730 2 疑难重症及罕见病国家重点实验室,北京 100730
经皮心内膜心肌活检是利用导管式活检钳,经周围血管到达右心室或左心室夹取心内膜心肌组织的技术。心内膜心肌活检及心肌病理学诊断是心肌炎、疑难心肌病精准诊断、治疗指导及疗效评价的重要手段。为规范经皮心内膜心肌活检的临床应用,提高其操作安全性,提升我国心肌炎、心肌病的诊治水平,结合北京协和医院近年来的临床实践撰写本操作规范。
1 心内膜心肌活检发展史
1958年美国Rush-Presbyterian-St. Luke’s医学中心Weinberg等[1]采用局麻、小切口开胸手术行心包和心肌活检,以明确心肌炎或心包炎的诊断。1960年美国西北大学医学院Sutton等[2]报道了经胸穿刺心肌活检方法,但临床实践中发现创伤较大,且并发症发生率高。1962年日本东京女子医学院附属医院Sakakibara等[3]采用心导管式活检钳对450余例患者进行了心内膜心肌活检,无严重并发症。1973年美国斯坦福大学医学院Caves等[4]研发出可反复使用的Stanford Caves-Shultz活检钳。目前临床应用的一次性可弯曲活检钳即是在Stanford Caves-Schultz活检钳基础上改进而来,钳瓣更小,并发症发生率更低。
20世纪80年代初,我国开始尝试经皮心内膜心肌活检。1981年11月,西安医学院第二附属医院孙济川等[5]在国内率先发表使用自制活检钳进行经皮心内膜心肌活检操作的研究结果。随后哈尔滨医科大学附属第二医院王璞等[6]和重庆医学院附属医院饶邦复等[7]先后发表使用改良的支气管或十二指肠活检器进行经皮心内膜心肌活检的论文,在一定程度上推动了我国心肌病理学工作的进步。2004年5月,中国医学科学院阜外医院杨跃进、荆志成采用心肌活检钳(美国Cordis公司)为一例心脏移植术后患者完成了经皮心内膜心肌活检,开启了心脏移植术后移植排异反应监测的临床工作。2014年中国医学科学院阜外医院心内科荆志成、徐希奇等与病理科阮英茆、赵红等合作,采用Argon心肌活检钳(美国Argon Medical Devices)对临床疑诊心肌炎、心肌病患者进行经皮心内膜心肌活检和心肌病理学诊断工作,截至2019年底共完成270余例。20世纪80年代,中国医学科学院北京协和医院的焦溥蕙在美国自费购买了一把心肌活检钳;1987年焦溥蕙、方圻等完成了13例次犬经皮心内膜心肌活检操作及病理诊断[8];2007年方全等开展了经皮心内膜心肌活检的临床工作,目前已完成260余例,积累了丰富的操作经验。本规范在系统总结500余例患者经皮心内膜心肌活检操作经验的基础上撰写而成。
2 心内膜心肌活检诊断价值:从受到质疑到成为金标准
早在1978年,美国国家心肺血液研究所的Ferrans等[9]就以“心内膜心肌活检:究竟是一种诊断手段还是研究工具?”为题,在AmJCardiol发表述评,认为心内膜心肌活检对心肌炎的诊断价值有限,主要原因是当时心肌炎病理诊断采用的是Dallas标准,即HE染色发现炎症细胞浸润和心肌细胞坏死。且当时心内膜心肌活检的并发症发生率较高,因而临床使用受限。
20世纪90年代以来,免疫组织化学诊断已成为心肌炎病理学诊断的重要指标,定性或定量PCR和逆转录 PCR可检测DNA和RNA病毒的基因序列,通过电镜观察浸润性心肌病患者心肌细胞内外的超微结构进行诊断,以及心脏移植术后需不定期进行排异反应监测等,均离不开心内膜心肌活检和心肌病理学专家的参与[10]。随着手术器械的改善以及术者经验的提升,右心室和左心室心内膜心肌活检的安全性均明显提高(严重并发症发生率低于1%)[11]。现今经皮心内膜心肌活检和心肌病理学诊断受到高度重视,已成为一项安全的检查手段,且操作者经验越丰富并发症发生率越低。更重要的是,无创检查手段如心脏MRI无法替代心内膜心肌活检,心内膜心肌活检仍是确诊心肌炎、炎症性心肌病、浸润性心脏病等的金标准[12]。因此,我国心内科医师应高度重视并积极开展经皮心内膜心肌活检工作,充分发挥其在疑难心脏病诊断及鉴别诊断中的价值。
3 心内膜心肌活检适应证和禁忌证
3.1 适应证
结合文献报道[12- 13]及临床实践经验,北京协和医院制定经皮心内膜心肌活检的适应证如下:(1)心脏移植术后排异反应监测;(2)临床疑诊心肌炎(如感染性心肌炎、自身免疫性心肌炎、嗜酸粒细胞心肌炎、巨细胞心肌炎等);(3)疑诊浸润性心肌病(如限制性心肌病、心肌淀粉样变、糖原贮积病、含铁血黄素沉着症等);(4)系统性疾病或化疗药物、毒物等可能累及心肌;(5)2周及以内新发心力衰竭,无论心脏大小是否正常;(6)新发心力衰竭超过2周,仍合并左心室扩大及新发室性心律失常、二或三度房室传导阻滞,或常规治疗1~2周无法完全恢复正常者;(7)心脏肿瘤;(8)无法解释的肥厚型心肌病或疑诊致心律失常性右心室发育不良/右心室心肌病等。
3.2 禁忌证
结合文献报道[12- 13]及临床实践经验,北京协和医院制定经皮心内膜心肌活检的禁忌证如下:(1)出血性疾病、严重血小板减少症及正在接受抗凝治疗者;(2)急性心肌梗死、左心室内附壁血栓形成或室壁瘤形成者禁忌左心室活检;(3)心脏明显扩大伴严重左心功能不全者;(4)近期有感染者;(5)不能很好配合的患者;(6)分流缺损是相对禁忌证,应避免左心室活检,以免引起矛盾性体循环栓塞。
4 心内膜心肌活检操作径路及要点
4.1 径路选择和引导方式
当前研究表明,绝大多数心内膜心肌活检在室间隔右心室面取材即可,只有病变主要累及左心室或存在左心室肿瘤时才需行左心室活检[14]。经皮心内膜心肌活检既可在X线引导下进行,也可经超声心动图引导,或二者结合使用,尤其是右心房或右心室肿瘤活检时。北京协和医院常规采用经右侧颈内静脉径路,后前位投照体位,必要时加左前斜45°体位验证,或床旁超声心动图协助定位,进行右心室室间隔心内膜心肌活检。少数情况下可采用股静脉径路。不建议采用左侧颈内静脉、锁骨下静脉、前臂静脉径路,引导方法以导管室X线+超声心动图引导为主,可明显减少并发症的发生。
4.2 术前准备
术前需完善常规实验室检查、心电图、超声心动图和心脏MRI检查。由于经皮心内膜心肌活检取材部位的限制,易造成漏诊,超声心动图及心脏MRI有助于确定心肌病变部位而减少漏诊的发生。临床医师应综合临床及心脏MRI检查结果作出初步诊断、发出经皮心内膜心肌活检申请单。
需注意,由于冠状动脉粥样硬化性心脏病(简称“冠心病”)是导致心肌病变及心力衰竭最常见的原因,因此在心内膜心肌活检前务必先排除冠心病。所有患者心内膜心肌活检前均不应进行抗凝或抗血小板治疗,服用华法林者需停药,国际标准化比值(international normalized ratio,INR)≤1.5时方可进行检查;应用肝素或低分子量肝素治疗的患者,检查前应停药至少16 h,检查结束12 h后且无并发症时方可恢复抗凝治疗。
4.3 操作要点
4.3.1 器材准备
四腔或六腔漂浮导管、Argon心肌活检钳(Jawz 2.2 mm Forceps, Maxi-Curved,50 cm)、床旁超声心动图机。
4.3.2 人员配备
术者(负责右心导管检查及心肌活检操作),助手(协助血流动力学测量、术中采集血气标本及移动检查床),导管室护士(器材准备及血流动力学数据记录),超声科医师(穿刺引导、必要时在活检过程中协助定位)。
4.3.3 右心导管检查
患者进入导管室后去枕仰卧位,头部左偏约30°,取右侧颈部胸锁乳突肌三角顶点为穿刺点,常规消毒铺巾,1%利多卡因局麻,穿刺右侧颈内静脉成功后,置入7 F或以上血管鞘。穿刺右侧颈内静脉可在超声引导下进行,以提高穿刺成功率、减少穿刺并发症。
首先进行右心导管检查,测量上腔静脉压、右心房压、右心室压、肺动脉压、肺小动脉楔压及心输出量等血流动力学参数,并在上述不同部位抽血进行血气分析。根据血流动力学检查结果进行肺高血压诊断分类(表1)[15],以指导制定治疗策略。
4.3.4 右心室心内膜心肌活检操作
完成右心导管检查后按以下步骤进行心内膜心肌活检:第一步,检查Argon心肌活检钳钳瓣工作是否正常,并用肝素盐水冲洗其表面。第二步,在后前位X线透视下将活检钳送至右心房中下约1/3处,此时右手逆时针旋转活检钳手柄使其头端指向三尖瓣,跨过三尖瓣后在X线透视下逆时针调整方向并继续推送,如推送不顺利可退回右心房重新进入,接触室间隔右心室面后可感觉到心脏跳动;心电监护可见室性早搏;后前位X线透视可见活检钳头端位于脊柱左缘4~7 cm处。需注意,推送过程中不应张开钳瓣,以免心脏穿孔。第三步,当确认活检钳位置抵住室间隔后,回撤1~2 cm,透视下张开钳瓣,如张开的钳瓣与推送杆组成典型的“Y”形提示位置正确,否则可能指向右心室游离壁,应重新调整方向。确认方向正确后继续向前推送至遇到阻力且心电图出现室性早搏,右手拇指用力按压手柄关闭钳瓣,轻拽活检钳使其脱离室间隔,如轻拽2~3次仍不能使之脱离,则可能是钳咬的组织块过大或为腱索,应松开钳柄,撤出活检钳,冲洗钳瓣后重新操作。若回撤活检钳时有明显离断感,则说明已钳取到心肌组织,保持钳瓣处于关闭状态,将其撤回至右心房后撤出,将活检钳头置于盛有生理盐水的器皿中,轻柔取下心肌组织,避免二次损伤。第四步,肝素盐水中冲洗活检钳,继续进行心内膜心肌活检。术后,询问患者有无胸闷、憋气、胸痛等不适,即刻行床旁超声心动图检查,观察是否有心包积液征象。如一切正常,拔鞘包扎穿刺部位,患者回病房行常规监测。

表 1 肺高血压的血流动力学分类
4.3.5 术后监测
心内膜心肌活检术后第2天,应常规检查穿刺部位有无血肿;复查心电图有无新出现的传导阻滞;复查胸片有无气胸或血胸;复查超声心动图观察有无心包积液或原有心包积液有无增多等。
注意事项:活检钳推送过程应全程在X线透视下进行,如遇到阻力应旋转手柄通过,不可强行推送。在后前位投射体位时,钳尖位置应离开胸骨左缘至少4 cm,否则活检钳可能未完全进入右心室或指向右心室游离壁(图1)。避免活检钳进入冠状静脉窦(操作过程中活检钳似乎进入右心室但无室性早搏时,应考虑活检钳误入冠状静脉窦可能,可在左前斜45°~60°下验证,一旦确定进入冠状静脉窦应立即将活检钳退至右心房,调整方向重新操作)。操作过程中可联合超声心动图引导。一旦钳夹应保持钳瓣处于闭合状态,撤至体外后方可再次打开。术后应询问患者有无明显胸闷、胸痛等症状。术后第2天常规进行心电图检查观察有无传导阻滞,拍胸片观察有无气胸、血胸等穿刺并发症,行超声心动图检查观察有无心包积液或原有心包积液增多等征象。
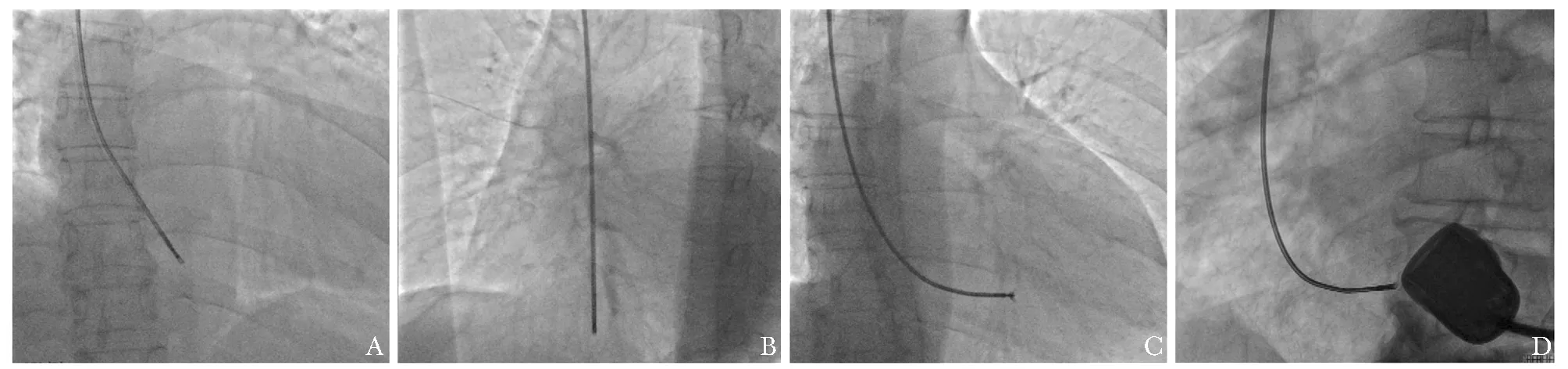
图 1 右心室心内膜心肌活检X线引导图像
5 心内膜心肌活检术后标本处理
标本取出后小心操作,可用细针或在生理盐水中转动钳瓣取下组织,避免因再次损伤而影响病理诊断。心肌组织通常为粉红色,大小1~3 mm3为佳,常规取3~6块。如所取组织为灰白色或漂浮水面,通常为脂肪或三尖瓣瓣叶等组织。操作结束后应尽快处理心肌组织:至少将2块心肌组织放置于室温的4%甲醛溶液中固定,冰盐水可导致心肌收缩带形成;将1块心肌组织放置于室温下2.5%戊二醛溶液中,然后转移至4 ℃冰箱保存;至少将1块心肌组织用无菌棉吸附水分,放入干燥冻存管中,转移至-80 ℃冰箱保存以备质谱分析或病毒PCR检测。每个冻存管外均贴上患者基本信息(图2),并将患者基本信息以及取材数目和病理类型记录至电子表格内。根据心肌活检取样数量不同,分别记录于表2,并整理病理切片及冷冻标本,组建生物样本库。

编号: ***姓名性别住院号光镜/电镜/液氮时间

表 2 活检组织记录表
所有心内膜心肌活检标本均应常规行HE染色和Masson染色;疑诊心肌炎或HE染色后发现淋巴细胞增多时,增加CD3、CD4、CD8、CD19、CD20、CD68等免疫组织化学染色;疑诊淀粉样变加行刚果红染色,必要时可加行抗λ、抗κ、抗TTR抗体免疫组织化学染色;临床疑诊糖原贮积病、溶酶体病或病毒性心肌炎时可加行透射电镜检查。-80 ℃冰箱保存的样本可用于免疫组织化学或分子病理学研究,如PCR或逆转录PCR进行病毒基因组分析。
6 心内膜心肌活检术后并发症
文献报道经皮心内膜心肌活检并发症的发生率为0~3.3%,考虑到研究时间的影响,估计近年来的发生率不超过1%[11,14]。常见并发症包括血管迷走性晕厥、心脏穿孔、心包填塞、心源性休克、室上性和室性心律失常、罕见心房穿孔、气胸、血管损伤、神经损伤、肺栓塞、冠状动脉心腔瘘、出血、三尖瓣损伤等。心脏穿孔是少见但严重的并发症,一旦怀疑心脏穿孔不应拔除静脉穿刺鞘(可作为液体通路进行补液及输注血管活性药物,病情稳定后再拔除鞘管),立即行超声心动图检查以评估心包积液量,一旦出现心包填塞或血流动力学不稳定应立即行心包穿刺引流,通常不会导致严重后果。另一严重并发症是不可逆的完全性房室传导阻滞,需植入永久起搏器治疗。绝大多数并发症无需特殊处理,只需严密观察即可。
为提高心内膜心肌活检的安全性,国内外医学中心均制定了严格的准入制度,要求操作者必须具有扎实的介入工作基础,且需在有经验术者的指导下完成至少50例心内膜心肌活检后方可独立操作[11,16]。
总之,经皮心内膜心肌活检不仅是心脏移植术后排异反应的重要监测手段,还是心肌炎、疑难心肌病及心脏肿瘤确诊的重要方法。国内外研究报道,有经验的临床中心心内膜心肌活检的并发症发生率低于1%,严重并发症发生率则更低,是一种安全性较高的检查手段[11,16]。目前北京协和医院能够独立进行经皮心内膜心肌活检的医师超过5人,且仍有医师正在接受培训。由于心肌病变往往分布不均匀,经皮心内膜心肌活检具有漏检可能,需要与超声心动图、心脏MRI及心血管病理等方面专业医师密切配合,以减少漏诊、误诊。随着心肌病特异性治疗药物的陆续出现,基于心内膜心肌活检的病理诊断越来越受到关注,建议全国三级医院心内科积极开展此项检查,以提高我国心肌炎、心肌病的精准诊断能力。
利益冲突:无