改性桃核壳对水中刚果红的吸附研究
2021-05-26温俊峰刘玲娜
刘 侠,温俊峰,薛 帆,刘玲娜
(1.榆林学院化学与化工学院,陕西 榆林719000;2.陕西省低变质煤洁净利用重点实验室,陕西 榆林 719000)
印染废水中含有的大多数染料都有较高毒性,且难以生物降解。大量印染废水排放到自然水体中,不仅会降低水体透明度,还会阻碍水生生物和微生物生长,致使水质恶化[1]。目前印染废水的处理方法主要有:絮凝法[2]、氧化法[3]、膜分离法[4]、活性炭吸附法[5-6]、生物降解法[7]等,但这些技术大多效率低、成本高。生物吸附法由于具有简单、高效、经济的优势备受人们重视。近年来,以农林废弃物作为生物吸附剂处理印染废水已成为研究热点[8-9]。
我国是产桃大国,陕北榆林地区种植了大量桃树,桃产量可观[10]。废弃桃核壳、仁除了用作工艺饰品、中药材之外,丢弃居多。鉴于此,作者以废弃桃核壳为原料,经环氧氯丙烷、乙二胺改性后用于处理刚果红溶液(模拟刚果红废水),拟为染料废水处理提供一条经济可行的途径。
1 实验
1.1 材料、试剂与仪器
桃核壳:废弃桃核产自榆林地区,洗净晾干,破碎、去仁,再经洗涤、80 ℃烘干、粉碎、过筛后装袋,备用。
刚果红,西陇化工股份有限公司;环氧氯丙烷、盐酸,济宁百川化工有限公司;氯化钠、无水碳酸钠,西安化学试剂厂;乙二胺、氢氧化钠,济宁宏明化学试剂有限公司;所用试剂均为分析纯,未经预处理。
Fw80型高速万能粉碎机,天津鑫博仪器有限公司;SHA-B型水浴恒温振荡器,金坛精达仪器制造有限公司;DF-101S型集热式恒温磁力搅拌器,巩义科瑞仪器有限公司;L-600型台式低速离心机,长沙湘仪离心仪器有限公司;722s型可见分光光度计,上海菁华科技仪器有限公司;Vario EL Ⅲ型有机元素分析仪,德国Elmentar公司;IRPrestige-21型傅立叶变换红外光谱仪,日本岛津公司。
1.2 方法
1.2.1 改性桃核壳的制备[11-12]
(1)称取预处理后的桃核壳2.0 g置于250 mL圆底烧瓶中,加入45 mL 1.25 mol·L-1的氢氧化钠溶液和25 mL环氧氯丙烷,在恒温水浴锅中于40 ℃下搅拌反应30 min,过滤,滤渣用蒸馏水洗至滤液为中性,于65 ℃下烘干至恒重,即得环氧氯丙烷改性桃核壳。
(2)称取10.0 g环氧氯丙烷改性桃核壳置于250 mL圆底烧瓶中,加入10 mL乙二胺、100 mL蒸馏水和1.0 g无水碳酸钠,于65 ℃下反应2 h后,过滤,滤渣用蒸馏水洗至滤液为中性,于70 ℃下烘干至恒重,即得改性桃核壳。
1.2.2 改性桃核壳的表征
1.2.2.1 等电点(pHzpc)测定
在锥形瓶中加入10 mL 0.01 mol·L-1的氯化钠溶液,调节溶液pH值在2.00~11.00范围内,分别加入改性桃核壳0.02 g,在25 ℃下振荡7 h,取出,再次测定溶液的pH值,以ΔpH值对pH值作图,得到改性桃核壳的等电点[13]。
1.2.2.2 元素含量测定
分别称取一定量的未改性及改性桃核壳,在有机元素分析仪上测定其N、C、H元素含量。测定条件为:以氩气作为载气,将未改性及改性桃核壳分别加热至950 ℃,测定各元素的含量。
1.2.2.3 FTIR图谱测定
分别称取未改性及改性桃核壳各5 mg置于玛瑙研钵中,加入一定量的高纯KBr,研磨后,压成透明薄片,测定红外光谱。测定条件为:分辨率2 cm-1,扫描次数60次,扫描范围400~4 000 cm-1。
1.2.3 改性桃核壳对刚果红的吸附性能
称取改性桃核壳置于锥形瓶中,加入刚果红溶液,用一定浓度的氢氧化钠溶液和盐酸溶液调节溶液的pH值,然后置于恒温水浴振荡器中,振荡一定时间后,离心过滤,用分光光度计在波长为498 nm处测定上清液中刚果红溶液的浓度。改性桃核壳对刚果红的吸附率、吸附量分别按下式进行计算:


式中:c0为吸附前刚果红溶液的浓度,mg·L-1;c1为吸附后刚果红溶液的浓度,mg·L-1;V为刚果红溶液体积,L;W为改性桃核壳的质量,g。
2 结果与讨论
2.1 改性桃核壳的表征
2.1.1 等电点分析(图1)
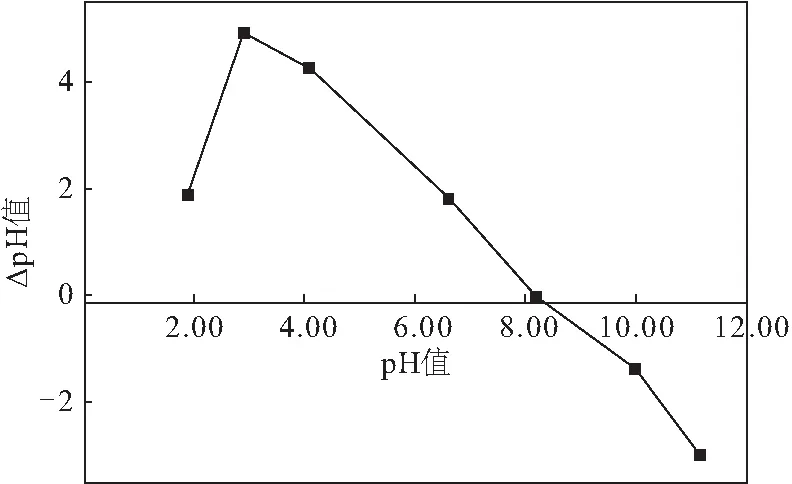
图1 改性桃核壳的等电点Fig.1 pHzpc of modified peach shell
由图1可知,改性桃核壳的pHzpc为8.16。当溶液pH=8.16时,改性桃核壳的静电荷为零;当溶液pH
2.1.2 元素含量分析(表1)

表1 未改性及改性桃核壳的元素含量/%
由表 1 可知,桃核壳改性后 C、H元素的含量略有增加,而 N元素含量明显增加。这是因为,在桃核壳的改性过程中,引入了氨基基团。
2.1.3 FTIR图谱分析(图2)

图2 未改性及改性桃核壳的FTIR图谱Fig.2 FTIR spectra of unmodified and modified peach shell
由图2可知,未改性桃核壳在3 442 cm-1处的波峰是O-H的伸缩振动吸收峰,1 734 cm-1处的波峰是C=O的吸收峰,1 044 cm-1处的波峰则归属于纤维素和半纤维素中C-O的伸缩振动吸收峰;改性桃核壳在1 044 cm-1和1 734 cm-1处的吸收峰明显减弱,说明桃核壳表面的C-O、C=O 与乙二胺中的氨基发生了反应。
2.2 改性桃核壳对刚果红的吸附性能研究
2.2.1 改性桃核壳投加量对吸附性能的影响
分别称取0.2 g、0.4 g、0.6 g、0.8 g、1.0 g、1.2 g、1.4 g、1.6 g、2.0 g改性桃核壳,置于9个100 mL锥形瓶中,分别加入50 mL 100 mg·L-1的刚果红溶液,于25 ℃下恒温振荡4 h后取出,离心,取上清液测定吸光度,并计算吸附率和吸附量,结果如图3所示。

图3 改性桃核壳投加量对刚果红吸附性能的影响Fig.3 Effect of modified peach shell dosage on adsorption performance to Congo Red
由图3可知,随着改性桃核壳投加量的增加,吸附率逐渐升高,当投加量超过1.6 g(32 g·L-1)后,吸附率升幅逐渐趋缓;当投加量从0.2 g(4 g·L-1)增加到2.0 g(40 g·L-1)时,吸附率从39.33%升高到98.21%。但吸附量却随投加量的增加而减少。这是由于,增加吸附剂投加量,吸附活性位点增多,吸附率不断升高;但在刚果红溶液浓度一定的情况下,染料分子总量不变,因此,增加吸附剂投加量,使得单位质量吸附剂上吸附刚果红的质量减少,即吸附量减少。综合考虑,选择最佳投加量为0.6 g,即12 g·L-1。
2.2.2 溶液pH值对吸附性能的影响
将7份50 mL 100 mg·L-1刚果红溶液的pH值分别调至2.00~10.00,分别加入12 g·L-1改性桃核壳,于25 ℃下恒温振荡4 h后取出,离心,取上清液测定吸光度,并计算吸附率,结果如图4所示。

图4 pH值对刚果红吸附性能的影响Fig.4 Effect of pH value on adsorption performance to Congo Red
由图4可知,增大溶液pH值,吸附率逐渐降低。这可能是由于,在pH值较大时,溶液中大量的OH-和刚果红在吸附剂表面竞争吸附,OH-占据了较多的吸附活性位点,影响刚果红与吸附活性位点的接触,使得吸附率较低;随着溶液pH值的减小, H+浓度增加,吸附剂表面的正电荷增加,有利于刚果红在吸附活性位点的吸附,故吸附率逐渐升高。
2.2.3 吸附动力学
采用准一级动力学和准二级动力学方程[14],探讨改性桃核壳对刚果红的吸附机理,得到的动力学有关参数如表2所示。

表2 改性桃核壳吸附刚果红的动力学有关参数
由表2可知,改性桃核壳对刚果红的吸附更符合准二级动力学方程,说明该吸附包含表面吸附、颗粒内部扩散和外部液膜扩散等吸附过程[15]。
2.2.4 等温吸附模型
分别在25 ℃、35 ℃和 45 ℃下测定改性桃核壳对刚果红的平衡吸附量,将实验数据分别用Langmuir和Freundlich等温吸附模型进行拟合[16-17],结果如表3所示。

表3 改性桃核壳吸附刚果红的Langmuir和Freundlich等温吸附模型有关参数
由表3可知,改性桃核壳对刚果红的吸附更符合Langmuir等温吸附模型。随着温度的升高,改性桃核壳对刚果红的平衡吸附量逐渐增加,表明改性桃核壳对刚果红的吸附是一个吸热过程。
3 结论
废弃桃核壳经环氧氯丙烷、乙二胺改性后,对水中刚果红具有较好的吸附效果。改性桃核壳投加量、溶液pH值、吸附时间及温度等影响其吸附性能,吸附过程满足准二级动力学方程和 Langmuir等温吸附模型,在温度为45 ℃时,改性桃核壳对刚果红的最大吸附量可达到20.408 2 mg·g-1。桃核壳是一种来源丰富的农业副产物,其作为新型染料废水处理用生物吸附剂具有良好的开发应用前景。
