联合动脉血气、hs-CRP、NT-proBNP及超声心动图评估慢性肺源性心脏病的病情严重程度
2021-05-26吕欣芳潘晨亮
吕欣芳 潘晨亮 吴 雪
1.甘肃中医药大学附属医院老年医学科,甘肃兰州 730020;2.兰州大学第一医院心脏中心,甘肃兰州 730000;3.兰州大学第二医院心血管中心,甘肃兰州 730030
慢性肺源性心脏病(pulmonary heart disease,PHD)在我国是常见病,主要继发于慢性阻塞性肺疾病,其发病关键是肺血管阻力增加和肺动脉高压[1]。随着病情反复发作,患者的肺功能不断下降,病情逐渐加重。该病预后差,严重影响患者的生活质量,给家庭及社会造成了较重的负担。若能早期判别病情的严重程度,予以积极的预防和治疗措施,将会延缓病情的发展。目前运用于肺心病诊断中的辅助检查主要包括:X线胸片,心电图,超声心动图,磁共振成像等。本研究旨在通过从临床使用的简便、易得的检查中发现与慢性肺心病病情严重程度相关的指标,为疾病的早期预防和治疗提供依据。现报道如下。
1 资料与方法
1.1 一般资料
选取2016年1月至2019年1月甘肃中医药大学附属医院老年医学科的96例慢性肺源性心脏病住院患者,根据诊断标准及是否出现并发症分为代偿期组(36例)及失代偿期组(60例)。代偿期组男25例,女11例;年龄55~94岁,平均(75.1±9.7)岁;病程6~20年,平均(12.92±2.35)年。失代偿期组男35例,女25例;年龄59~97岁,平均(78.7±8.1)岁;病程8~20年,平均(13.41±3.05)年。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究对象均已知情同意并签署知情同意书,本研究经甘肃中医药大学附属医院医学伦理委员会批准。
纳入标准:①符合慢性肺源性心脏病基层诊疗指南(2018年)[1];②心力衰竭者符合中国心力衰竭诊断和治疗指南2018[2]诊断标准;③急性发作病程在1周以内(包括1周)的年龄54~80岁患者。排除标准:①合并其他肺部疾病者;②肺部影像学检查见气胸、胸腔积液、肺栓塞者;③严重精神障碍患者。根据纳入标准,共纳入PHD患者96例,分为两组:①肺心病代偿组:符合上述诊断标准。②肺心病失代偿组:符合上述诊断标准,且已出现并发症,如呼吸衰竭、心力衰竭、肺性脑病、酸碱平衡失调、水电解质紊乱、消化道出血、肾脏损害、肝脏损害及休克等。
1.2 方法
观察两组间pH值、二氧化碳分压(PCO2)、氧分压(PO2)、超敏C反应蛋白(C reactive proteins,hs-CRP)、N末 端B型 钠 尿 肽 前 体(N terminal B natriuretic peptide precursor,NT-proBNP)及右心房长径、右心房横径、右心室前后径、右心室长径、右心室横径、右心室流出道内径、肺动脉内径、肺动脉收缩压等指标差异。
1.3 观察指标
1.3.1 动脉血气分析 入院后立即使用动脉采血针采集动脉血2 ml,使用美国GEM3500血气分析仪检测pH值、PCO2、PO2等指标。
1.3.2 hs-CRP及NT-proBNP 入院当天采集静脉血2 ml,使用基蛋生物科技股份有限公司生产的Getein 1600全自动荧光免疫定量分析仪检测其水平。
1.3.3 超声心动图 入院后第二天使用德国西门子ACUSONSC2000超声检测仪进行心脏彩超检查,检测右心房长径、右心房横径、右心室前后径、右心室长径、右心室横径、右心室流出道内径、肺动脉内径、肺动脉收缩压等指标。
1.3.4Logistic回归分析 采用Logistic回归分析与慢性肺源性心脏病病情严重程度相关的因素。
1.4 统计学方法
采用SPSS 22.0统计学软件进行分析,计数资料以[n(%)]表示,比较采用χ2检验。计量资料符合正态分布以()表示,采用t检验;不符合正态分布以四分位数法表示,采用秩和检验。独立相关变量进行Logistic回归分析。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者动脉血气分析比较
两组患者pH值、PCO2、PO2比较,差异无统计学意义(P>0.05),见表1。

表1 两组患者动脉血气分析比较[M(Q1,Q3)]
2.2 两组患者hs-CRP及NT-proBNP比较
失代偿期组hs-CRP及NT-proBNP高于代偿期组,差异有统计学意义(P<0.05),见表2。
2.3 两组患者超声心动图比较
失代偿期组患者右心房长径、右心房横径、右心室前后径、右心室长径、右心室横径、右心室流出道内径、肺动脉内径值高于代偿期组,差异有统计学意义(P<0.05);两组患者肺动脉收缩压比较,差异无统计学意义(P>0.05),见表3。
2.4 慢性肺源性心脏病病情严重程度相关因素Logistic回归分析
Logistic回归分析结果提示与慢性肺源性心脏病病情严重程度相关的因素有以下几个:年龄(OR=1.396,95%CI:1.134~1.717,P=0.002)、NT-proBNP(OR=1.002,95%CI:1.001~1.004,P=0.0 0 5)、h s-C R P(O R=1.2 2 5,9 5%C I:1.031~1.454,P=0.021)。见表4。
3 讨论
在我国,慢性阻塞性肺疾病(COPD)是PHD的主要病因。支气管、肺、胸廓或肺血管的慢性病变导致肺血管阻力增高,肺毛细血管床减损,血液黏稠度与血容量增加,导致肺动脉高压[3]。肺循环阻力增高导致右心室代偿性肥厚,但代偿发生于肺动脉高压早期,此时舒张末期压可维持正常。随着病情逐渐加重,尤其是到了急性加重期,持续升高的肺动脉压超过了右心室的代偿能力,失代偿发生,右心排血量下降,右心增多的收缩末期残留血量及增高的舒张末期压力促使右心壁增厚、右心腔扩张,最终导致右心衰竭[4]。本研究发现年龄、hs-CRP及NTproBNP水平是PHD病情严重程度的独立危险因素。这与既往研究结果[5-7]相一致。
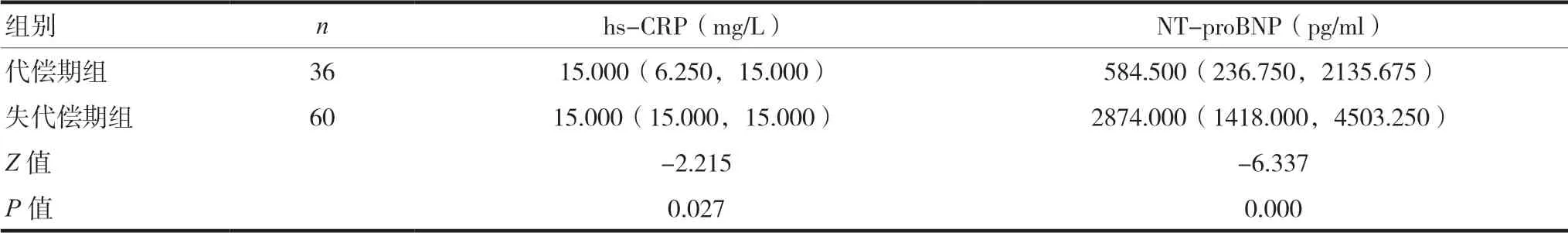
表2 两组患者hs-CRP及NT-proBNP比较[M(Q1,Q3)]

表3 两组患者超声心动图参数比较[M(Q1,Q3)]

表4 慢性肺源性心脏病病情严重程度相关因素
本研究结果提示,年龄越大,PHD的病情越严重,与文献报道相一致[8-9]。究其原因,可能是随着年龄增加,老年人生理功能减退更为显著,且原发病长期慢性损耗,导致病情逐渐加重。增多的Tr细胞和明显减少的TU细胞使老年人依赖T细胞抗原的免疫反应下降,增加了老年人对微生物的易感性[10]。感染后肺部通气及换气功能严重障碍,导致机体供氧减少或二氧化碳潴留,最终发生呼吸衰竭。这时痉挛的肺小动脉增高了肺动脉的压力,加重了右心负荷导致右心衰竭,心肌收缩力因缺氧、酸中毒减弱,进而使左心功能减退,易发生心律失常甚至心肌变性坏死,右心衰竭增加了肺内分流,加重了左心负荷,最后导致全心衰竭[11]。
hs-CRP是由肝脏合成的一种非特异性标志物,全身性急性炎症反应时血清中含量增多,识别并清除宿主体内的病原体和凋亡、坏死的细胞,并通过募集补体系统和吞噬细胞来保护宿主抵抗病原体是其主要生物学功能[12]。有学者[12-13]发现,肺心病的发生、发展与hs-CRP的水平升高密切相关,可据此判断PHD的病情和预后。正常人血清中的C反应蛋白(CRP)含量很低,在炎症等因素作用下,CRP含量会明显升高,加重气道阻塞及气道炎症,使呼吸功能减弱[14];而且在心肌细胞中,CRP可作用于补体系统,使炎症反应进一步增强,心肌细胞凋亡加速,进一步加重心肌损伤[15],故心功能分级与hs-CRP含量成正比,心功能Ⅰ~Ⅳ级患者血清hs-CRP含量逐渐升高[16]。因此,hs-CRP的变化是判断肺心病患者病情严重程度、预后及疗效的有效指标。
受刺激的心肌细胞首先产生B型利钠肽原前体(pre-proBNP),随后形成B型钠尿肽前体(proBNP),前者含134个氨基酸,后者含108个氨基酸。由于内切酶的作用,proBNP可裂解为NT-proBNP和B型钠尿肽(BNP),前者含有76个氨基酸、无生物活性,后者含有31个氨基酸、有生物活性。在心力衰竭患者中NT-proBNP较BNP浓度高,对心力衰竭的诊断更加有利[17]。近年研究[18-19]发现,脑钠肽水平不仅在影响左心室的病理条件下会显著升高,在导致急性或慢性右心室负荷过重的临床条件下也会升高。NT-proBNP水平与肺动脉高压患者右心形态及功能障碍有关,其水平升高可提供右心衰竭患者的病情严重程度和预后信息。这与本研究的结果一致。PHD导致NTproBNP升高的具体机制尚不明确,可能为长期严重缺氧增加心、肺NT-proBNP分泌量,且通过刺激促红细胞生成素分泌增加使红细胞代偿性增多,增加血容量,增大血黏度,加重右心室负荷,从而增加NT-proBNP的分泌量;此外,引起慢性肺心病急性加重至失代偿期的常见原因是呼吸系统感染,感染可导致心肌耗氧量增加,加重心室负荷从而增加NT-proBNP的分泌量;最后,肾脏是清除NT-proBNP的唯一途径,肾血管在缺氧状态下收缩,降低了肾小球滤过率,使其清除NT-proBNP的能力下降,增加了血浆NT-proBNP浓度[20]。
综上所述,随着年龄增加,肺心病患者病情逐渐加重,为反映病情严重程度及判断预后可联合检测hs-CRP及NT-proBNP水平。
