槐杞黄颗粒治疗慢性湿疹的疗效及对干扰素-γ、白细胞介素-4水平的影响
2021-05-26郝思雨
何 谐 郝思雨 张 宇 党 林
1.哈尔滨医科大学附属第二医院皮肤科,黑龙江哈尔滨 150081;2.深圳市人民医院皮肤科,广东深圳 518020
湿疹是一种常见的炎症性皮肤病,发病机制尚不明确,可能与免疫异常、皮肤屏障功能障碍及微生物相关[1]。其免疫学机制主要是Th1/Th2失衡引起的细胞因子分泌紊乱,其中Th2细胞过度应答导致细胞因子白细胞介素(IL)-4、IL-13等升高,而Th1型细胞因子干扰素(IFN)-γ、IL-2等则降低[2]。湿疹分为急性、亚急性及慢性湿疹,慢性湿疹常由前两者迁延而成,易反复发作,严重降低患者的生活质量。因此,寻求有效且复发率低的治疗方案仍是当前的研究重点。本研究将槐杞黄颗粒与糠酸莫米松乳膏联合应用治疗慢性湿疹,评估其疗效及安全性,并通过观察治疗前后细胞因子IFN-γ、IL-4的变化,探讨可能的作用机制,现报道如下。
1 资料与方法
1.1 一般资料
选取2020年1—6月于哈尔滨医科大学附属第二医院(我院)皮肤科门诊就诊的60例慢性湿疹患者,按就诊顺序编号,应用随机数字表法随机分为治疗组和对照组。治疗组30例,男13例,女17例,年龄19~55岁,平均(36.87±10.19)岁,病程6个月至5年,平均(2.51±1.03)年,湿疹面积及严重度指数(EASI)评分(8.00±1.99)分,瘙痒程度评分(2.40±0.67)分;对照组30例,男16例,女14例,年龄20~56岁,平均(35.40±8.89)岁,病程6个月至4.5年,平均(2.83±0.96)年,EASI评分(8.30±1.76)分,瘙痒程度评分(2.43±0.73)分。两组患者的性别、年龄、病程及疾病严重程度比较,差异均无统计学意义(P>0.05),具有可比性。本研究获得医院医学伦理委员会批准,患者及家属对实验内容知情同意,并签署知情同意书。
1.2 纳入与排除标准
纳入标准:①符合《中国临床皮肤病学》[3]中慢性湿疹诊断标准的患者,即患处皮肤肥厚,皮损呈棕红色或灰色,伴苔藓样变、鳞屑及色素改变,自觉瘙痒,反复发作;②符合中医湿疹阴虚血燥证的诊断标准[4],主症为皮损粗糙肥厚,苔藓样变,伴严重瘙痒;次症为口干或手足心热,舌红,苔少,脉细;③年龄18~60岁,性别不限;④皮损相对局限,1%体表面积≤皮损面积≤10%体表面积;⑤同意作为此次临床研究的对象,签署知情同意书者。
排除标准:①对本研究中的药物过敏者;②1个月内使用过抗组胺药物、糖皮质激素、免疫抑制剂治疗者;③伴有严重心脏、肝脏、肾脏功能障碍及其他免疫系统疾病者;④妊娠期和哺乳期妇女;⑤合并其他皮肤疾病者;⑥合并细菌、病毒、真菌感染者;⑦合并其他过敏性疾病者;⑧糖尿病患者。
1.3 方法
治疗方法:对照组给予糠酸莫米松乳膏(商品名:艾洛松,含0.1%糠酸莫米松,上海先灵葆雅制药有限公司,5 g/支,国药准字H19991418)外用治疗,每日一次。治疗组在外用糠酸莫米松乳膏的基础上,另口服槐杞黄颗粒(商品名:还尔金,启东盖天力药业有限公司,10 g/袋,国药准字B20020074),每日2次,一次10 g。两组疗程均为4周,治疗期间不使用其他药物。
细胞因子检测方法:于治疗前后抽取两组患者空腹静脉血3 ml,肝素抗凝,离心分离血清,采用酶联免疫吸附法(ELISA)检测血清IFN-γ及IL-4水平,试剂盒产自上海晶抗生物工程有限公司,严格遵照试剂盒说明进行操作。
1.4 观察指标
①治疗前后评估患者湿疹面积和严重程度,计算EASI评分,观察治疗后EASI评分改善情况;②治疗前后评估患者的瘙痒程度,观察治疗后瘙痒程度评分改善情况;③治疗前后测定患者血清IFN-γ及IL-4水平,观察治疗后两者的变化情况;④治疗前后检查两组患者血常规及肝肾功能,观察治疗后的变化情况,并记录治疗过程中出现的不良反应;⑤在治疗后第3个月进行随访,观察患者的复发情况。
1.5 评价标准
1.5.1 疗效评估 采用赵辨教授改良的EASI评分标准,按照皮损面积和严重程度进行评分[5]。①皮损面积评分将体表分为头/颈部(H)、上肢(UL)、躯干(T)及下肢(LL)四部分,各占体表面积的10%、20%、30%、40%,四个部位分别评价皮损面积,无皮 损 计0分,皮损<10%计1分,10%~19%计2分,20%~49%计3分,50%~69%计4分,70%~89%计5分,≥90%计6分;②皮损严重程度评分需观察红斑(E)、水肿/丘疹(I)、表皮剥脱(Ex)、苔藓化(L)及渗出/结痂(Ei)五项表现,并按严重程度计分,无皮损计0分、轻度计1分、中度计2分、重度计3分。各部位EASI评分=(E+I+Ex+L+Ei)×皮损面积评分×该部位占体表面积比例,各部位分值相加即为EASI总分值。疗效指数=(治疗前EASI评分−治疗后EASI评分)/治疗前EASI评分×100%。临床疗效分为四级[6]:痊愈为疗效指数>90%;显效为疗效指数60%~90%;好转为疗效指数20%~59%;无效为疗效指数<20%。总有效率=(痊愈例数+显效例数)/总例数×100%。
1.5.2 瘙痒评估 根据瘙痒程度及对生活质量的影响进行评分[7]:0分为无瘙痒;1分为轻度瘙痒,不影响日常生活和睡眠;2分为中度瘙痒,影响日常生活和睡眠,尚能耐受;3分为重度瘙痒,严重影响日常生活和睡眠。
1.6 复发判定
治疗后第3个月对痊愈及显效患者进行随访,计算EASI评分。复发指数=(治疗前EASI评分−随访时EASI评分)/治疗前EASI评分×100%。复发指数<60%判定为复发,复发率=复发例数/(痊愈例数+显效例数)×100%。
1.7 统计学方法
采用SPSS 22.0软件。计量资料以()表示,组间比较采用独立样本t检验,组内比较采用配对样本t检验。计数资料以百分数(%)表示,组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组治疗前后EASI评分及瘙痒程度评分比较
治疗前,两组EASI评分及瘙痒程度评分相比,差异无统计学意义(P>0.05)。治疗后,两组EASI评分及瘙痒程度评分均较治疗前降低,差异有统计学意义(P<0.05);治疗后,治疗组EASI评分及瘙痒程度评分均低于对照组,两组比较差异有统计学意义(P<0.05)。见表1。
表1 治疗前后两组EASI评分及瘙痒程度评分比较(±s,分)
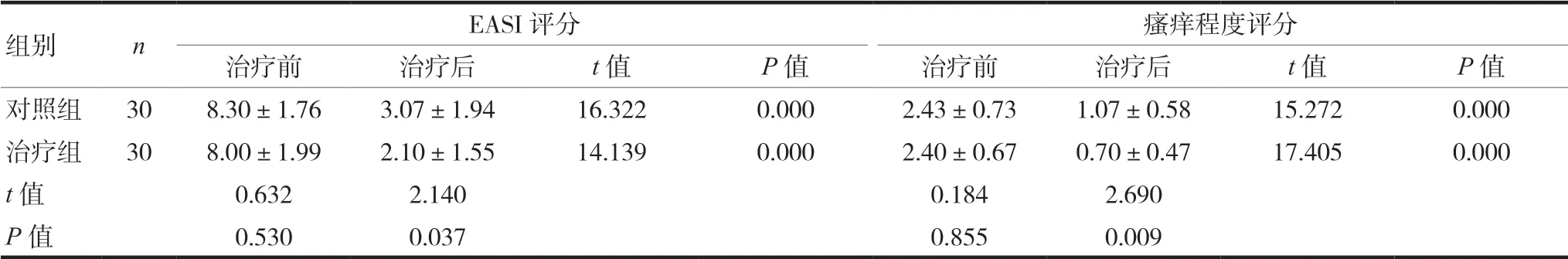
表1 治疗前后两组EASI评分及瘙痒程度评分比较(±s,分)
组别 n EASI评分 瘙痒程度评分治疗前 治疗后 t值 P值 治疗前 治疗后 t值 P值对照组 30 8.30±1.76 3.07±1.94 16.322 0.000 2.43±0.73 1.07±0.58 15.272 0.000治疗组 30 8.00±1.99 2.10±1.55 14.139 0.000 2.40±0.67 0.70±0.47 17.405 0.000 t值 0.632 2.140 0.184 2.690 P值 0.530 0.037 0.855 0.009
2.2 两组治疗后疗效比较
治疗后,两组痊愈率、显效率、好转率及无效率比较,差异无统计学意义(P>0.05)。治疗后,治疗组总有效率为86.67%(26/30),对照组总有效率为63.33%(19/30),治疗组总有效率高于对照组,差异有统计学意义(P<0.05)。见表2。

表2 治疗后两组的疗效比较[n(%)]
2.3 两组治疗后3个月复发情况比较
两组痊愈和显效的患者治疗后第3个月随访,治疗组2例患者复发,复发率为7.69%(2/26),对照组7例患者复发,复发率为36.84%(7/19),治疗组复发率低于对照组,差异有统计学意义(P<0.05)。见表3。

表3 治疗后3个月两组的复发情况比较[n(%)]
2.4 两组患者不良反应发生情况比较
治疗4周后复查两组患者的血常规及肝肾功能,与治疗前比较,差异无统计学意义(P>0.05),两组患者均未出现严重不良反应。治疗期间,治疗组有2例患者出现腹部不适及轻微腹泻,1例患者出现局部瘙痒、刺痛及灼热感,均未行特殊处理,症状自行缓解,未影响治疗。对照组1例患者出现局部干燥、瘙痒及脱屑,给予保湿剂外用后症状缓解,并继续治疗。治疗组和对照组的不良反应率分别为10.00%(3/30)和3.33%(1/30),两组比较差异无统计学意义(χ2=0.268,P=0.605>0.05)。
2.5 两组治疗前后血清IFN-γ、IL-4水平比较
治疗前,两组患者血清IFN-γ、IL-4水平比较,差异无统计学意义(P>0.05)。治疗后,治疗组血清IFN-γ水平较治疗前升高,IL-4水平较治疗前降低,差异均有统计学意义(P<0.05);治疗后,对照组血清IL-4水平较治疗前降低,差异有统计学意义(P<0.05),IFN-γ水平与治疗前相比,差异无统计学意义(P>0.05);治疗后,治疗组IL-4水平低于对照组,IFN-γ水平高于对照组,差异均有统计学意义(P<0.05)。见表4。
表4 治疗前后两组血清IFN-γ、IL-4水平比较(±s,ng/L)

表4 治疗前后两组血清IFN-γ、IL-4水平比较(±s,ng/L)
组别 n IL-4 IFN-γ治疗前 治疗后 t值 P值 治疗前 治疗后 t值 P值对照组 30 76.46±18.76 49.16±20.21 5.421 0.000 31.66±12.90 34.93±12.09 1.011 0.316治疗组 30 73.85±21.58 36.03±13.93 8.063 0.000 36.29±13.91 43.22±11.19 2.125 0.038 t值 0.499 2.928 1.335 2.755 P值 0.620 0.005 0.187 0.008
3 讨论
湿疹是一种常见的炎症性皮肤病,其发病的内在因素包括遗传易感性、免疫功能异常及皮肤屏障功能障碍,外在因素包括环境或食物刺激、微生物、心理因素等[1]。湿疹的免疫学机制与Th2优势应答有关,Th2细胞分泌的IL-4、IL-5、IL-13及IL-31等细胞因子诱导嗜酸性粒细胞增多和免疫球蛋白E(IgE)产生,参与过敏性炎症的发生,并介导瘙痒的产生[8]。慢性湿疹发病率高,病程迁延,易反复发作,严重影响患者的生活质量。目前治疗上主要以外用糖皮质激素、钙调磷酸酶抑制剂及口服抗组胺药物为主,虽然能够在一定程度上缓解病情,但停药后容易复发,有一定局限性,因此寻求新的用药方案非常重要。有研究表明一些中药如复方甘草酸苷、苦参碱等具有调节Th1/Th2平衡的作用,对湿疹具有理想的治疗效果[9-10]。因此,从调节免疫功能的角度出发,纠正Th1/Th2失衡,也许是湿疹的新治疗方法。
中医学认为湿疹是在禀赋不耐的基础上,由饮食不节、素体虚弱或湿热蕴久等因素引起,主要分为风热蕴肤证、湿热浸淫证、脾虚湿蕴证及阴虚血燥证四种证型[4]。阴虚血燥证常见于慢性湿疹,治疗上应滋阴养血,润燥止痒。槐杞黄颗粒是一种中药复方制剂,具有益气养阴的功效,适用于儿童或成人体质虚弱的治疗,目前广泛应用于免疫相关性疾病如肾病综合征、支气管哮喘等的辅助治疗[11]。糠酸莫米松乳膏是一种中效糖皮质激素,具有抗炎、抗过敏及免疫抑制作用,是慢性湿疹的一线外用药物。本研究将槐杞黄颗粒与糠酸莫米松乳膏联合应用治疗慢性湿疹,观察临床疗效及治疗后血清细胞因子IFN-γ、IL-4水平的变化,从而探讨槐杞黄颗粒治疗慢性湿疹的可能机制。
槐杞黄颗粒由槐耳菌质、枸杞子及黄精组成,三种成分均具有免疫调节作用。槐耳可通过调控巨噬细胞和T细胞功能,调节细胞因子水平并抑制NLRP3炎性小体的活化,进而发挥重要的免疫调节作用[12]。此外,槐耳还具有抑制细胞增殖及抗血管生成的作用[13]。Su等[14]研究证实槐杞黄颗粒可通过抑制细胞周期G1期,有效抑制皮肤角质形成细胞增殖。枸杞子含有枸杞多糖、甜菜碱、氨基酸、矿物质和维生素等多种成分。现代药理学研究表明,枸杞多糖对于免疫系统具有重要调节作用,不仅促进T细胞、B细胞的增殖,还可作用于固有免疫细胞,增强树突状细胞的抗原提呈能力及巨噬细胞的吞噬活性[15]。黄精可通过促进T细胞、B细胞的增殖及巨噬细胞的吞噬作用而增强免疫功能,还具有抗炎、抗氧化的作用[16]。
本研究结果显示,槐杞黄颗粒联合糠酸莫米松乳膏治疗4周后,患者EASI评分、瘙痒程度评分均较治疗前及对照组明显降低,总有效率明显高于对照组,表明槐杞黄颗粒联合糠酸莫米松乳膏治疗慢性湿疹疗效较好,优于单用糠酸莫米松乳膏。治疗后3个月治疗组复发率明显低于对照组,表明外用糖皮质激素基础上加用槐杞黄颗粒能够降低慢性湿疹的复发率。治疗期间两组未出现严重不良反应,治疗前后血常规及肝肾功能无明显变化,两组不良反应发生率相比差异无统计学意义,表明槐杞黄颗粒联合糠酸莫米松乳膏治疗慢性湿疹不良反应少,安全性较好。治疗后,治疗组血清 IFN-γ水平较治疗前明显升高,血清IL-4水平明显降低,与对照组相比差异有统计学意义,表明槐杞黄颗粒治疗慢性湿疹的作用机制可能与降低血清IL-4水平,升高IFN-γ水平,调节Th1/Th2平衡有关。机体内Th1与Th2处于动态平衡,Th1细胞产生IFN-γ、IL-2、TNF-α等细胞因子,介导细胞免疫应答;Th2细胞产生IL-4、IL-13、IL-31等细胞因子,辅助体液免疫应答,两者分泌的细胞因子可相互拮抗。IFN-γ能够以自分泌方式促进Th1细胞的增殖分化,同时抑制Th2细胞的分化。IL-4可参与IgE类别转换,促进组胺及酶类物质的释放,从而参与湿疹的过敏性炎症反应[8]。IL-4还能够抑制表皮中紧密连接的形成[17],下调皮肤屏障相关蛋白及抗菌肽的水平[18],与湿疹患者皮肤屏障功能的破坏密切相关。有研究表明槐杞黄颗粒具有调节Th1/Th2及Th17/Treg平衡的作用[19],具体机制尚不明确,可能与其对JAK-STAT和MAPK等信号通路的调控相关[20]。本研究的结果也显示槐杞黄颗粒可调节慢性湿疹患者的Th1/Th2平衡,其治疗湿疹的作用可能与直接下调IL-4水平、抑制Th2过敏性炎症有关,而复发率的降低可能与其上调IFN-γ水平、进一步拮抗IL-4作用而间接修复皮肤屏障有关,具体机制有待进一步研究。
综上所述,本研究结果表明,槐杞黄颗粒联合糠酸莫米松乳膏治疗慢性湿疹具有较好的疗效及安全性,可降低复发率,其作用机制可能与降低血清IL-4水平,升高IFN-γ水平,从而调节Th1/Th2平衡有关。但本研究具有一定的局限性,疗程较短,纳入病例较少,结果需要进一步临床试验证实。总之,槐杞黄颗粒与糠酸莫米松乳膏联用治疗慢性湿疹疗效较好,有利于降低复发率,值得临床推广。
