单宁酸-鱼明胶共价、非共价相互作用 复合物抗氧化活性比较研究
2021-05-20郭扬凯白春清
◎ 郭扬凯,赵 利,白春清
(1.江西科技师范大学生命科学学院,江西 南昌 330013;2.江西科技师范大学有机功能分子研究所,江西 南昌 330013)
明胶是一种极其重要的结构蛋白,可由胶原蛋白水解得到,广泛存在于动物的软骨、韧带、肌膜、皮肤中[1],其提取制品因具有良好的保湿性、乳化性及成膜性已广泛应用于医药、保健、食品加工、化妆品等领域[2]。由于鱼鳞中含有大量的胶原蛋白,且近些年来疯牛病、口蹄疫等传染性疾病的发生和盛行,人们对来源于牲口的明胶的安全性产生了怀疑[3],所以研究和开发鱼鳞等水产品加工废弃物中鱼明胶逐渐受到人们的重视。但以鱼为原料提取得到的鱼明胶制品普遍存在溶解度低、抗氧化活性及乳化性不理想等问题,限制了其在食品工业中的进一步应用。科学研究表明,多酚可以进入蛋白质分子的内部,且可以与肽链以非共价键或共价键链接[4],改变蛋白质的结构,进而影响其功能特性。大量实验证明多酚与蛋白质共价键链接可以提高蛋白质的抗氧化活性、热稳定性以及乳化活性[5]。单宁酸是公认的安全食品添加剂,可广泛用于烘焙食品、饮料,乳制品及糖果中,因含有足够的羟基和羧基,可以与蛋白质作用形成复杂的聚合物[6]。当前,关于单宁酸与其他来源蛋白质相互作用的研究较多,而其与淡水鱼明胶间的相互作用报道较少。因此,本研究拟以抗氧化活性为指标,评价不同形式明胶-单宁酸结合方式对明胶功能特性的改善效果,为鱼明胶的改性研究提供参考。
1 材料与方法
1.1 材料与试剂
鱼明胶、95%乙醇溶液、3-乙基苯并噻唑啉-6磺酸(ABTS)、1,1-二苯基-2-三硝基苯肼试剂(DPPH),上海国药集团化学试剂有限公司生产;单宁酸(95%)、过硫酸钾、8-苯胺-1-萘磺酸,湖北信康医药化工有限公司生产;啡啰嗪,长春汇力生物技术有限公司生产。
1.2 仪器与设备
UV-1800紫外-可见分光光度计,上海美谱达仪器有限公司生产;BSA224S-CW型电子天平,德国赛多利斯公司生产;HH-600型恒温水浴锅,青岛聚创世纪环保科技有限公司生产。
1.3 氧化单宁酸-明胶共价结合物(OTA-G)的制备
称取一定量的明胶,溶于水制备浓度为1.2%的蛋白溶液,用1 mol·L-1NaOH调整体系pH至9.0。向单宁酸溶液中加入蒸馏水溶解至浓度为2%,然后用 1 mol·L-1NaOH调pH至9.0,40 ℃吹氧气1 h将单宁酸(TA)氧化为氧化单宁酸(OTA)。75 mL明胶溶液与2.25 mL OTA溶液进行混合,并加水至蛋白浓度为1%。将此混合物室温磁力搅拌12 h后透析除去游离的OTA和明胶。
1.4 单宁酸-明胶非共价结合物(TA-G)
按照类似1.3的步骤制备单宁-明胶价非共价结合物,区别为体系pH为7.0,且TA无需加氧反应。
1.5 抗氧化活性测定
以明胶为对照,分别采用以下几种方法测定单宁酸-明胶结合物的抗氧化活性。
1.5.1 DPPH自由基清除实验
取样品1.5 mL与0.10 mmol·L-11,1-二苯基-2-三 硝基苯肼(DPPH)的95%乙醇溶液1.5 mL超声 5 min,充分摇晃,在暗处静置0.5 h。同样方法做空白样品,在517 nm处测定样品吸光度。
1.5.2 ABTS自由基清除率测定
7.4 mmol·L-12,2’-叠氮杂环(3-乙基苯并噻唑 啉-6磺酸)(ABTS)[7]与过硫酸钾(2.6 mmol·L-1)按体积比1∶1(v/v)混合,室温放置12 h制备ABTS工作液。将ABTS工作液与甲醇进行混合稀释,直至吸光度在734 nm处吸光度为1.1±0.02,即可得ABTS工作液。取150 μL样品与2850 μL ABTS工作液进行混合、涡旋,在暗处放置2 h后,在734 nm处测量样品对ABTS的猝灭效果。其活性以μmol-TE/g蛋白表达。
1.5.3 铁还原力测定(FRAP)
用0.3 mol·L-1pH3.6的醋酸缓冲液、10 mmol·L-1三吡啶基三嗪(TPTZ)[8]溶液与20 mmol·L-1FeCl3溶液以10∶1∶1的比例混合可得FRAP溶液。取新制备的2.85 mL FRAP溶液在37 ℃条件下预热30 min,然后与150 mL样品混合,混合物在室温下暗处反应0.5 h后,测定样品在593 nm处的吸光度。同时用蒸馏水代替样品溶液进行反应作为样品空白。FRAP表达为μmol-TE/g蛋白。
1.5.4 Fe2+螯合率的测定
取样品(4.7 mL)于试管中加入0.1 mL 2 mmol·L-1FeCl2和0.2 mL 5mmol·L-1啡啰嗪[9],混匀后,黑暗处静置20 min。然后同时用蒸馏水代替样品溶液进行反应作为样品空白。在562 nm处测定样品吸光度。
1.6 数据分析
所有实验在操作时进行5个平行实验,以防误差,结果以平均值±ds表示。
2 结果与分析
2.1 DPPH自由基清除实验
单宁酸作为抗氧化剂,因含有大量的羟基,而具有有着较强的DPPH自由基清除能力。从图1可发现,鱼明胶与氧化单宁酸共价相互作用后ORAC值为80.59 μmol-TE/g,非共价相互作用后ORAC值为85.32 μmol-TE/g,分别约为抗氧化剂单宁酸抗氧化能力的65.51%和61.88%,且都显著高于鱼明胶的测定值。上述结果,一方面说明单宁酸与鱼明胶间的相互作用可以改善鱼明胶的自由基清除能力,从而提高鱼明胶的还原性;另一方面,说明被改性的鱼明胶抗氧化能力的高低很大程度上取决于与单宁酸的结合形式。TA-G通过非共价相互作用完成单宁酸对明胶的改性,因此,单宁酸的结合率较高,同等条件下明胶分子中可引入更多的单宁酸,而单宁酸的羟基可向明胶提供大量的氢原子,以提高明胶的抗氧化活性,致使TA-G自由基清除率高于OTA-G。
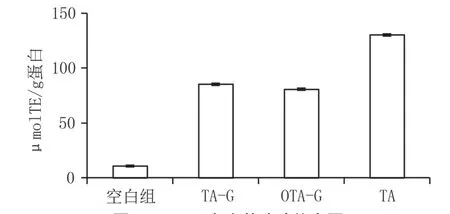
图1 DPPH自由基清除能力图
2.2 ABTS自由基清除率测定
TA和OTA改性明胶对ABTS自由基清除活性如图2所示。整体来说,样品的ABTS自由基清除活性与其对DPPH自由基清除活性基本一致。改性明胶对ABTS自由基的清除率高于明胶对照组,但其活性却低于游离单宁酸。单宁酸具有较强的抗氧化活性,在其对明胶进行改性的过程中,可有效清除体系自由基,形成更稳定的结合产物,而终止了自由基连锁反应[7-8]。然而,在结合过程中,单宁酸的羟基有所减少,导致其抗氧化活性低于游离单宁酸。与TA改性明胶相比,OTA改性明胶的ABTS自由基清除活性较低,可能是因为OTA为氧化型,其与明胶结合后,失去了抑制自由基的能力。

图2 ABTS自由基清除能力图
2.3 多酚-鱼明胶相互作用对铁还原力的影响
在酸性条件下Fe3+可以被多酚还原为Fe2+,与TPTZ络合形成蓝紫色溶液。测定在593 nm波长处的荧光强度,即可作为样本总抗氧化能力的指标。对铁的还原力越大说明抗氧化性越强。从图3中可以看出,单宁酸对铁的还原能力最强,展现了其较强的还原能力;明胶经单宁酸共价修饰和非共价修饰明胶后对铁的还原能力都显著高于对照组,说明单宁酸与鱼明胶的结合可提高明胶的抗氧化活性。虽然,非共价修饰明胶对铁离子的还原能力显著高于共价修饰明胶,且低于游离单宁酸,但整体来说与DPPH、ABTS自由基清除率结果一致。
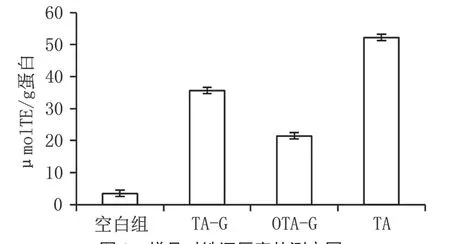
图3 样品对铁还原率的测定图
2.4 多酚-鱼明胶相互作用对Fe2+螯合率的影响
亚铁离子(Fe2+)是作为重要的金属离子促氧化剂之一,通过催化活性氧、羟基自由基(OH·)的生产,引发脂质氧化链式反应[9]。相同条件下,Fe2+螯合率越大说明抗氧化剂的抗氧化性越强。由图4可知,鱼明胶与单宁酸自身都可以与Fe2+螯合,明胶改性后对Fe2+螯合率有所提高,且高于游离单宁酸的测定值。可能明胶分子中带负电的羧基与Fe2+间的静电相互作用提高了结合物的螯合能力。
3 结论
单宁酸与鱼明胶结合会提高鱼明胶的抗氧化活性,且单宁酸-鱼明胶以非共价键结合时抗氧化能力更为强烈。因此在以后的食品加工过程中,可以用单宁酸对鱼明胶进行改性,以便更合理的利用鱼明胶的特性。本研究将填补单宁酸对鱼明胶相互作用研究的理论空白。
