茶碱血药浓度室内质量控制方法的建立Δ
2021-05-20苗仁华庄星星
苗仁华,庄星星,张 鹏
(安徽医科大学附属巢湖医院药剂科,安徽 巢湖 238000)
茶碱的临床治疗安全窗较窄,相同剂量个体血药浓度差异大[1-2];其体内药动学过程个体差异大,血药浓度超过临床推荐治疗范围时极易出现中毒症状[3-4]。因此,在使用茶碱类药物时对其进行血药浓度监测显得尤为重要,血清茶碱浓度监测逐渐被临床医师和患者所接受,血药浓度监测被认为是保证茶碱类药物合理使用的最重要手段[5]。
室内质量控制(internal quality control,IQC)作为全面质量管理体系的重要环节,是检测实验室测定结果准确性、及时发现检测方法实验误差的管理体系[6-7]。现阶段,治疗药物监测工作实现IQC的一般方法是由实验室工作人员采取特定的方法和程序,连续一段时间内评价本实验室检测结果的可靠性,以判断实验结果的真实性[8-10]。治疗药物监测室实行IQC旨在对实验室检测数据的真实性进行评价,以判断实验室检验工作的可靠性。 IQC结果对实验室检测结果的有效性和准确性有着参考价值。
因此,本研究采用自制不同浓度的茶碱质控血清,连续20 d不间断监测质控血清,绘制质控图,结合 Westgard多规则[6,11]质量控制评价体系评价本实验室IQC情况,建立、完善茶碱血药浓度监测IQC体系[12],提高血药浓度监测的准确性。
1 材料
1.1 仪器
Viva-E型全自动生化分析仪(德国SIEMENS公司);Sartorius型电子天平(赛多利斯科学仪器(北京)有限公司);TGL-16E型高速离心机(长沙英泰仪器有限公司);海尔DW-4OL188型医用低温保存箱(青岛海尔特种电器有限公司)。
1.2 药品与试剂
Emit法茶碱检测试剂(德国SIEMENS公司,批号为4P01946963);茶碱对照品(中国食品药品检定研究院,规格为100 mg/支,批号为100121-201805);Emit法茶碱定标液(0、2.5、5.0、10.0、20.0及40.0 μg/ml,德国SIEMENS公司,批号为4P10938092);空白血清(上海斯信生物科技有限公司,批号为MR16118)
2 方法与结果
2.1 质控样品的制备
精密称定茶碱对照品10.0 mg置于10.0 ml容量瓶中,定容,制备1.0 mg/ml的茶碱对照品溶液,备用。
分别精密移取1.0 mg/ml的茶碱对照品溶液50.0、100.0及200.0 μl置于10.0 ml容量瓶中,分别用9 950.0、9 900.0及9 800.0 μl空白血清定容,制备成质量浓度为5.0、10.0及20.0 μg/ml的质控样品。
2.2 IQC规则

2.2.2 Westgard多规则质控规则:将低、中及高3个浓度水平的质控测定值转换成Z分数形式,绘制Z-分数质控图。 根据Westgard多规则控制方法,当Z>2或者Z<-2时,即违反12 s规则的警告;当Z>3或者Z<-3时,即违反13 s规则,为失控[13]。
2.3 标准曲线的建立
每次测定前,取出在2~8 ℃保存的茶碱定标液放置室温(25 ℃),分别取0、2.5、5.0、10.0、20.0及40.0 μg/ml定标液1.0 ml上机检测,仪器自动绘制标准曲线。
2.4 精密度
取5.0、10.0及20.0 μg/ml的质控样品。连续测量3次,计算日内精密度;连续测量3 d,计算日间精密度,结果见表1。精密度试验结果符合《中华人民共和国药典:四部》(2015年版)通则9012[14]的要求。

表1 茶碱血药浓度IQC精密度和回收率试验结果Tab 1 Precision and recovery test results of IQC of blood concentration of theophylline
2.5 回收率
日内平均回收率=精密度试验中日内差测得值/质控样本标示浓度×100%;日间平均回收率=精密度试验中日间差测得值/质控样本标示浓度×100%,见表1。回收率试验结果符合《中华人民共和国药典:四部》(2015年版)通则 9012的要求。
2.6 稳定性
取5.0、10.0及20.0 μg/ml的质控样品。将质控样品即时进样后,放置于冷冻条件(-80 ℃)下分别冷冻储藏12、24和48 h后取出,复融测量,计算RSD,考察质控样本在冷冻条件(-80 ℃)下反复冻融3次的稳定性,见表2。稳定性试验结果符合《中华人民共和国药典:四部》(2015年版)通则 9012的要求。

表2 样品稳定性试验结果(n=5)Tab 2 Results of stability test (n=5)
2.7 回顾性质量控制
2.7.1 Levey-Jennings质控方法:(1)低浓度质控样品连续20 d测定结果显示,靶值(平均值)为5.36 μg/ml,标准差为0.20;10个测定值高于靶值,10个测定值低于靶值;2个测定值低于控制线(-1 s),3个测定值高于控制线(+1 s);第15个点超过警戒线(+2 s),提示警告1次。见图1。(2)中浓度质控样品连续20 d测定结果显示,靶值(平均值)为10.81 μg/ml,标准差为0.39;10个测定值高于靶值,10个测定值低于靶值;4个测定值低于控制线(-1 s),3个测定值高于控制线(+1 s);第11个点超过警戒线(+2 s),提示警告1次,见图2。(3)高浓度质控样品连续20 d测定结果显示,靶值(平均值)为20.33 μg/ml,标准差为0.89;10个测定值高于靶值,10个测定值低于靶值;2个测定值低于控制线(-1 s),4个测定值高于控制线(+1 s);第12个点超过警戒线(+2 s),提示警告1次,见图3。
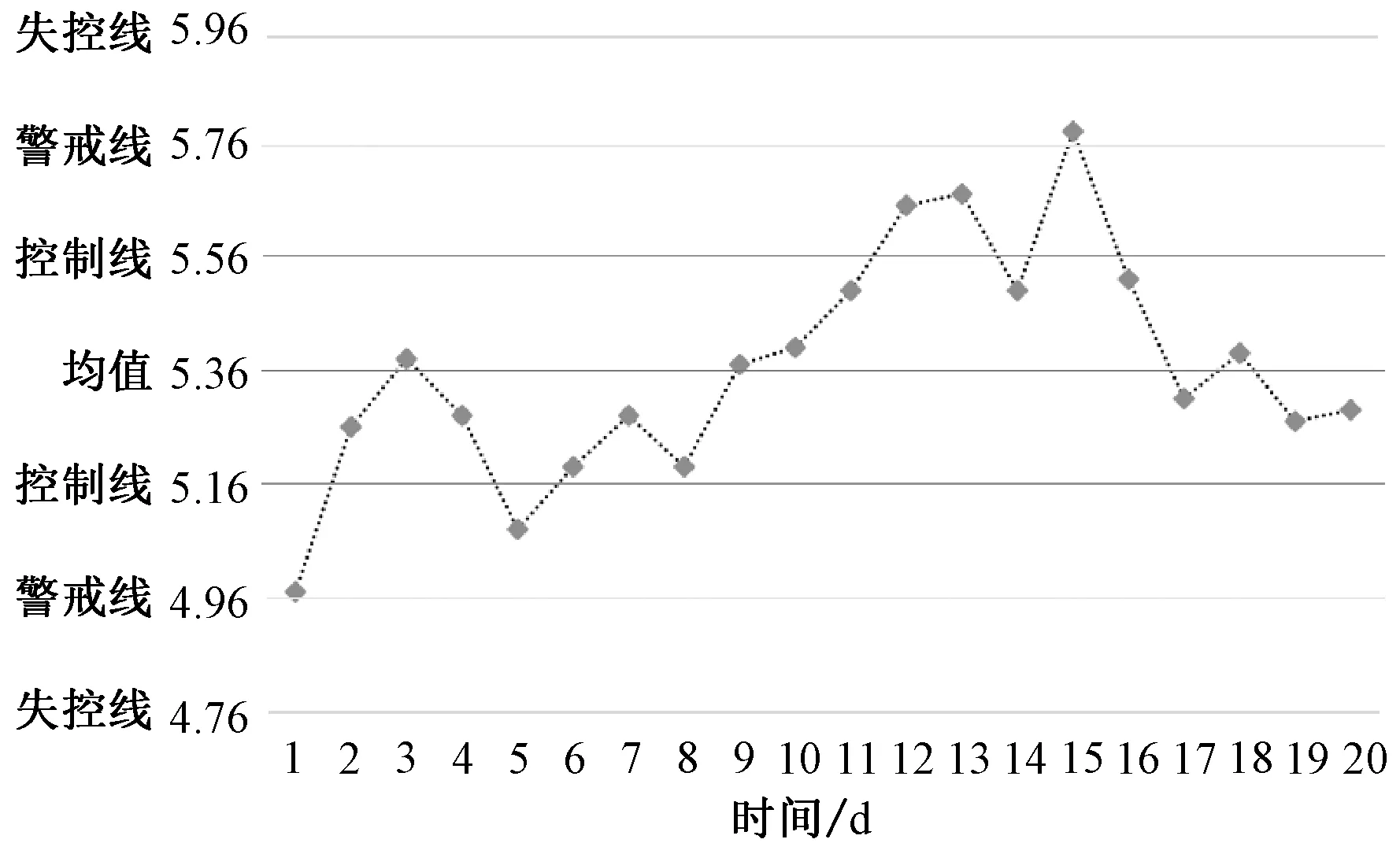
图1 低浓度茶碱质控数据分布图趋势Fig 1 Trend of quality control data distribution of low concentration theophylline

图2 中浓度茶碱质控数据分布图趋势Fig 2 Trend of quality control data distribution of medium concentration theophylline

图3 高浓度茶碱质控数据分布图趋势Fig 3 Trend of quality control data distribution of high concentration theophylline
2.7.2 Westgard多规则控制方法:将低、中及高3个浓度水平的质控测定值转换成Z分数形式,绘制Z-分数质控图,见图4。由图4可知,低浓度第15个测量值Z分数>2,即违反12 s规则的警告;高浓度第12个测量值Z分数>2,即违反12 s规则的警告。

图4 茶碱Z-分数质控图Fig 4 Z-score quality control chart of theophylline
3 讨论
随着药学服务转型的需要,药学实验室检测工作越来越得到临床的接受和认可,而数据的准确性显得日益重要,受临床关注程度得到提升。做好室间质控和IQC日益受到药学专业人员的重视[15]。因此,本研究结合日常工作实际,依据《中华人民共和国药典:四部》(2015年版)通则中相关要求,对所建立的血药浓度监测方法进行验证,参照临床医学实验室质量专用要求建立IQC体系,在样本的采集、保存和测定等方面提高样本稳定性的控制方法,建立血药浓度监测的质量控制方法,规范工作流程,保证所得结果及时可靠[16]。
目前,实验室外部质量控制的权威性无疑是高于IQC的,但实验室外部质量控制的成本高、对实验室样本数量要求比较高,因此实验室外部质量控制的可操作性一般。此外,实验室外部质量控制也是建立在IQC能够切实有效实施的基础上,由此可见,IQC是实验室全部质量控制工作的基础。IQC开展的目的就是把检测结果的误差控制在允许范围内,保证检测过程精密、准确和可重复,使实验结果误差处于规定的置信区间内[17]。IQC主要措施就是对同一样本重复多次进行测定,然后使用对照样品比较测定结果,对测得结果的精密度和准确度进行评价和控制[18]。本研究选用日内差、日间差2个指标考核精密度试验,结果符合《中华人民共和国药典》对生物样品检测误差的要求。
