污水前置分离混凝剂及其应用研究
2021-05-19张翔刘海龙
张翔,刘海龙
(山西大学 环境与资源学院,山西 太原 030006)
城镇污水中的有机物质通常包括蛋白质、糖类、脂类及其他有机物(例如表面活性剂、核酸等)[1-3]。除溶解态有机物外,从粒径分布的角度看,城镇污水的有机物分为颗粒态和胶体态,占污水中有机物的35% ~ 91%[1-3],在生化处理中属于较难降解有机物形态,是影响生物处理效率的重要问题[1-5]。“前置混凝分离+生物处理”污水处理系统通过前置混凝较大比例地去除上述颗粒态、胶体态等污染物,优化后续生物处理的水质条件,可以在保证出水质量的前提下,有效地缩短停留时间,节约投资和运行成本、提升出水稳定性[2,4]。
混凝在水质净化和污水处理过程中被广泛应用,发挥着极为重要的作用[4-8],主要体现在对颗粒态及胶体态等污染物的分离去除。混凝沉淀后产生的絮体可能包括微生物及其残体、颗粒态和胶体态污染物、混凝剂与其水解产物以及吸附在上述沉淀物表面的部分溶解性污染物等[4-7]。底泥(沉积在池底的絮体)不仅成分复杂,多种物质聚集,其中还可能发生复杂的物理作用和生化反应,比如溶解-沉淀平衡、吸附-解吸附、微生物对污染物的降解和转化等,让底泥的成分随着时间的变化显得更为复杂。同时,对于发生一定反应或作用后的底泥,其中的一些污染物质的分散性能可能发生变化,比如溶解性增强等。在排泥间隔时间内,底泥中的污染物可能释放到水中[8-10]。以河流底泥对上覆水体的影响为例,其中,COD的含量比自然背景值高2~11倍,TP和TN的峰值含量比自然背景值高1~2倍,很大程度上影响了水质[10]。因此,研究底泥中污染物的释放规律并对其有效控制,可以进一步提升水处理效率和出水水质;研发一种能有效分离污染物且能抑制底泥污染物释放的混凝剂,将进一步强化“前置混凝分离+生物处理”系统,提升处理效率和出水水质。由此,本文目的在于研究前置混凝剂对混凝效率、底泥释放等的影响,以期望找出合适的混凝剂适配“前置混凝分离+生物处理”系统。
铜离子与铁和铝有相似的特性,即相对较高的正电荷,在pH为中性(6~8)水解形成的氢氧化物溶解性较低,具有成为混凝剂的潜力。铜作为一种生物活性金属,连同其合金,已成为重要的抗菌物质。事实证明[11-13],大约355种铜合金能够在2 h内杀死99.9%的致病细菌;美国环境保护署(EPA)已经批准将这些铜合金注册为“有助于公共健康的抗菌材料”;医院使用铜制门把手来减少疾病的传播;而水暖系统中铜管可抑制军团病的发生;在英国、爱尔兰、日本、韩国、法国、丹麦和巴西等国家的医疗机构中都安装了具有抗菌效果的铜合金产品;2011年-2014年,智利圣地亚哥的地铁运输系统中,站台安装上了铜锌合金扶手以防止接触感染;铜还被用作水坝或水库的消毒剂[13]。此外,铜是所有真核生物的有氧呼吸中必不可少的一种元素,比如线粒体中细胞色素c氧化酶就是氧化磷酸化作用中的一种含铜蛋白质[13]。混凝剂中复合铜的成分可能起到抑菌效果,在一定程度上抑制底泥污染物的释放。
本研究以传统聚合硫酸铁(PFS-polyferric sulfate)混凝剂为基础,通过聚合加入硫酸铜对PFS进行化学改性,制备出新型混凝剂——聚合硫酸铜铁(PFCS-polyferric copper sulfate);研究聚合硫酸铜铁混凝剂的混凝效果和底泥中污染物的释放规律,分析底泥释放对沉后水和后续生物处理产生的影响以及PFCS对其控制的有效性。
1 材料与方法
1.1 实验用水
实验中所有配置试剂用水为超纯水。
实验中所用污水样来自太原市某污水处理厂,在实验前24 h采集,保存于4℃的恒温暗箱中待用。使用前1 h,恢复到室温(16℃)。主要的水质指标见表1。

表1 水样水质指标Table 1 Key parameters of the sample water
1.2 实验方法
仪器:六联搅拌仪(深圳中润)、光电式浊度仪(美国哈希)、紫外可见分光光度计(日本岛津)、原子吸收光度计(日本岛津)、pH计(上海雷磁)、恒温水浴锅,高压灭菌锅。
测定方法[14]:浊度,光电式浊度仪测定法;TN,过硫酸钾氧化-分光光度法;NO3-N,紫外分光光度法;NH3-N,纳氏试剂分光光度法;COD,重铬酸钾法;Cu2+,火焰原子吸收法。
1.3 混凝剂制备
将硫酸铁和硫酸铜溶液按照铜铁摩尔比为1∶30、1∶40和 1∶50进行混合,运用 Chang等的合成方法[15],制成碱化度为 0.3的 PFCS 和 PFS。在冷干机中干燥48 h得固态混凝剂。
1.4 混凝实验
分别取1 000 mL废水,分批次按照一定剂量梯度投加不同的混凝剂在250 r·min-1下搅拌2 min,再调节转速至60 r·min-1搅拌15 min,搅拌结束后将水样静置20 min,取液面下2 cm处的上清液,测定浊度、TN、COD及总铜浓度。
1.5 底泥释放实验
使用50 mg·L-1不同种类的混凝剂进行混凝实验,结束后用蠕动泵去除约600 mL沉后水,将剩余的沉后水和底泥的混合物离心,分离出沉后水,保留底泥(所有的底泥约10 g),分别称取5 g底泥用消毒过的标准盐溶液(质量分数为0.9%)定容至100 mL,放入敞口棕色瓶中。棕色瓶放入恒温暗箱内,温度为25℃,静置培养,定期取样测定上覆水中COD,氨氮和硝态氮。
1.6 底泥灭菌实验
将离心后的底泥放入敞口棕色瓶,用棉花塞住瓶口,用布包裹瓶口后高压蒸汽灭菌,相关参数为压力1.05 kg·cm-2,温度130 ℃,灭菌时间60 min。
1.7 微生物的取样与培养
将离心后的底泥样品放置在50 mL标准盐溶液(质量分数为0.9%)中搅拌均匀制成悬液,然后稀释至10-2和10-3,用涂布法在牛肉膏琼脂固体培养基上培养,在35℃环境下恒温培养24 h~48 h,统计微生物数目。
2 结果与讨论
2.1 前置混凝对出水浊度、TN和COD去除率的影响
取一定量的水样,分别加入PFS和3种PFCS(铜铁比为 1∶30、1∶40 和 1∶50,分别记作 PFCS(1∶30)、PFCS(1∶40)和 PFCS(1∶50))混凝剂进行混凝实验,混凝剂的投加量分别为 10、20、30、40、50、60、70和 80 mg·L-1(以投加的铁离子浓度为标准,下同),分别测量沉后水中的浊度和TN的去除率。部分实验结果见图1。

图1 不同混凝剂投加量下剩余浊度和TN的去除率Fig.1 Residual turbidity and TN removal rate under different coagulant dosages
从残余浊度看(图1),随着剂量的增加,4种混凝剂混凝效果呈现类似的趋势。投加量为<50 mg·L-1时,浊度随着投量增加而快速降低。在50 mg·L-1~80 mg·L-1间,浊度下降趋缓,在4 ~ 6 NTU之间,部分混凝剂作用的沉后水(PFCS(1∶30)和 PFS)中剩余浊度略有上升,这可能是出现复稳现象。因而后续实验如未特别说明,混凝剂剂量均采用50mg·L-1。整体上看,4种混凝剂都可以有效控制污水浊度,且PFCS的浊度去除率较PFS稍好,随着铜铁比的增大,去除率增大。
混凝对TN有一定程度的去除,去除率约为27%~34%,且随着混凝剂投量的增加,去除率增大。PFCS对TN去除效果普遍高于PFS,且随着铜铁比的增大,TN去除率增大。相同剂量下,混凝对 TN 的去除效果大小顺序为:PFCS(1∶30)>PFCS(1∶40)>PFCS(1∶50)>PFS。 污 水 TN中包括颗粒态、胶体态和溶解态含氮物质[4,6,11],其中颗粒态和胶体态可以被混凝沉淀有效分离去除,而溶解态如氨氮、硝氮等,混凝分离效果较差[4,6]。PFCS 去除TN和浊度效果较好的原因,可能是PFCS能更好地和含氮颗粒物或胶体结合,形成沉淀,有效分离;此外,可能是由于混凝剂的投加量是以铁离子的投加量所计算,混凝剂中有混凝效果的金属离子为铁和铜,因此相同剂量下的金属阳离子含量顺序为:PFCS(1∶30)>PFCS(1∶40)>PFCS(1∶50)>PFS,金属阳离子含量高的混凝剂,混凝效果更好。
混凝剂投量为50 mg·L-1时,PFCS的浊度去除率达到97%以上;其对COD的去除效果见表2。
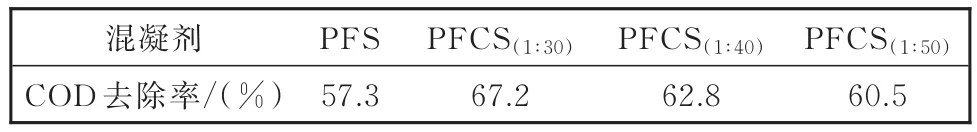
表2 不同混凝剂对COD的去除率Table 2 Removal rates of COD by different coagulants
4种混凝剂对COD都有显著的去除效果;PFCS的去除率明显高于PFS,且随着铜铁比的增大,COD 去除率依次增大;PFCS(1∶30)的 COD 去除率达67.2%。结合浊度、TN和COD的数据,前置混凝可以有效去除水中的颗粒物和胶体态物质,同时TN和COD都有一定程度的去除。PFCS类混凝剂与PFS相比在上述三项指标的去除率方面均有更好的表现,且随着铜铁比的上升,去除率升高。
生活污水和常见的工业废水中胶体、悬浮态有机物(包括含氮和含磷物质)在生化处理中属于较难降解有机物形态,在相应的污染物中占比大、反应时间长,且与溶解态有机物存在动态转化关系[1-3],是影响生物处理效率的主要问题。充分发挥前置混凝对水中颗粒物、胶体态物质(包括有机物、TN等)的去除效果,与后续生物处理相配合的设计可以大幅降低污水在生物反应池的停留时间,减少处理占地面积,节约建设成本,提升处理效果及出水稳定性[2,4]。从上述 PFCS(1∶30)的前置混凝效果看,COD、TN去除率分别达67.2%和33.7%,有望大幅缩短沉后水在曝气池的停留时间,提升其硝化效率。污水中的污染物在前置混凝分离过程中大比例地进入沉淀,其稳定性和释放能力可能对后续处理过程和出水水质发生一定程度的影响。
2.2 底泥的释放
上述混凝过程把污水中大量颗粒物和胶体态物质(其中包括有机物、有机氮等)沉降为底泥,实现前置分离以减轻后续处理如曝气、脱氮等环节的负荷。有效发挥前置分离效果一方面取决于沉降分离效率,另一方面取决于底泥中污染物质的释放率。底泥中污染物的释放可能对后续的处理过程和出水水质造成影响。但这方面的研究报道较少[17-22],未见到混凝形成底泥释放规律的报道;有些研究仅报道了湖泊、水库、河流等底泥的释放[16-19]。其中借鉴意义较强的是朱辉发现单位污泥的氮磷释放量分别为2.53 mg NH4+-N·g-1MLSS和0.54 mg PO43--P·g-1MLSS;厌氧水解污泥能大大加快污泥的水解速率,在12 h内能使污泥水解出大量的溶解性COD(50 mg·L-1~60 mg·L-1)[17]。Chen等研究认为底泥藻毒素释放对后续的水质恢复可能产生重要影响,PAC混凝可以有效分离微囊藻,但对底泥微囊藻毒素的释放影响不大[22]。
污水中原有的颗粒物及胶体态污染物沉降性能差,不易收集。但通过本研究组前期研究[2]表明,经前置混凝分离—生物接触氧化池工艺处理,与同一原水样单独生物接触氧化处理相比,COD的去除率和脱氮效果均明显好于后者。当水力停留时间为2.5 h时前置混凝沉后水的COD的生物接触氧化去除率已达89%,而只经生物接触氧化处理在6 h后COD的去除率为85%;相应地,NH3-N去除率由45%提升到91%,TN去除率由59%提高到72%。这从一定程度上表明,污水颗粒物及胶体态污染物(可认为是原污水沉淀物的最重要的构成部分)的存在,造成污染物的释放导致处理效率下降,可见底泥释放对水质可能造成相当程度的影响。
设置了底泥未灭菌组PFS、PFCS(1∶30)、PFCS(1∶40)、PFCS(1∶50)和灭菌对照组(PFS 灭菌底泥)进行释放实验,对COD、硝态氮和氨氮进行检测(图2-图4)。随着时间的增加,底泥释放对于沉后水的污染程度逐步增加。所有底泥COD的释放速率最快的时段都是在前8 h内;8 h以后,释放速率放慢。在整个研究时间范围内,PFS底泥释放量均为最高,灭菌对照组最低,PFCS组介于上述二者之间。在32 h时PFS底泥COD平均释放量为40.3 mg·L-1,而灭菌对照组的平均释放量仅为9.2 mg·L-1;PFCS 组 PFCS(1∶50)、PFCS(1∶40)、PFCS(1∶30)32 h的释放量分别为 20、17 mg·L-1和 18 mg·L-1。

图2 底泥COD释放量变化Fig.2 Dynamics of COD release from sediment
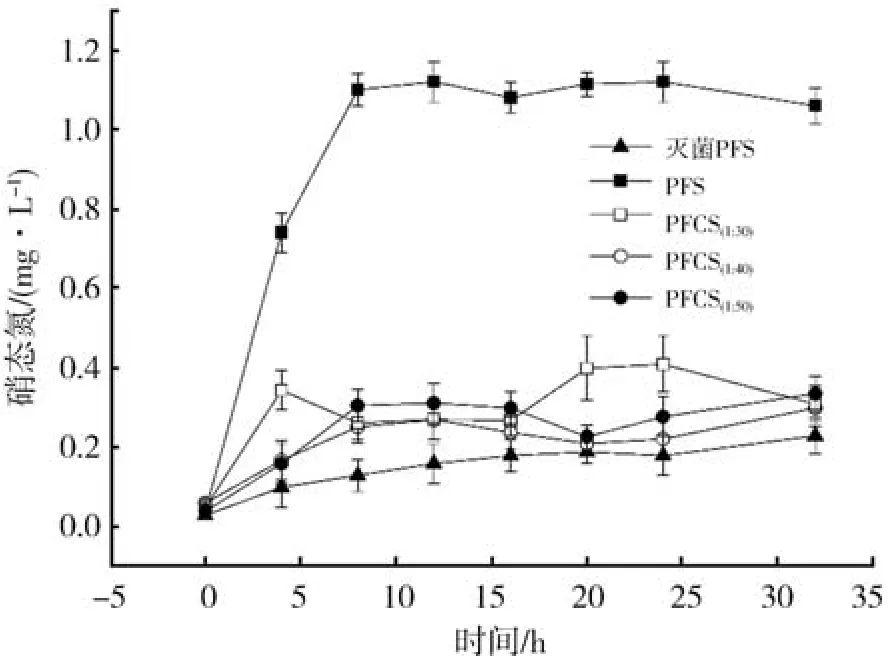
图3 底泥硝态氮释放量变化Fig.3 Dynamics of nitrate release from sediment
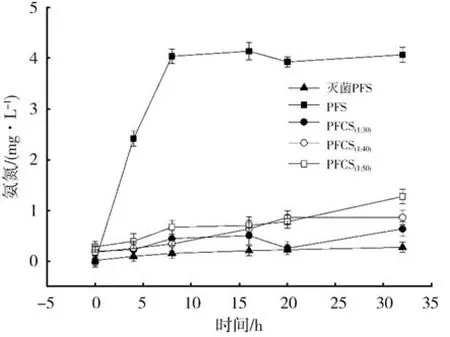
图4 底泥氨氮释放量变化Fig.4 Dynamics of ammonia release from sediment
硝氮和氨氮的释放如图3-图4所示。与COD释放趋势类似,在整个研究时间范围内,PFS底泥硝氮和氨氮释放量均为最高,灭菌对照组最低;PFCS组介于上述二者之间,但与PFS差距较大。PFS底泥硝氮释放量于8h内达到最高,之后窄幅波动,但表观释放量始终在1.2 mg·L-1以下;其余组包括灭菌对照组底泥的硝氮释放量只是在前期有少许增加,之后便窄幅波动,表观释放量始终在0.5 mg·L-1以下。对于氨氮,除灭菌对照组外,几乎所有底泥的释放量均大于同期硝氮释放量。PFS底泥氨氮表观释放量于8 h时达到最高,约为4 mg·L-1左右,是原水氨氮(均值 26.4 mg·L-1)的15%左右,是国家城镇污水处理厂污染物排放标准《GB19819-2002》一级标准 5 mg·L-1的 80%。可见,底泥释放对后续污水处理过程及出水水质有重要的影响,尤其是对COD和氨氮。
未经前置混凝分离的原污水中颗粒态、胶体态污染物(包括含氮有机物)的随流而下逐步被释放和分解对后续水处理过程和出水水质会产生明显的影响。前置混凝分离大幅降低COD,同时去除了部分总氮,改善了好氧池微生物硝化作用,有利于除氨脱氮[2]。混凝形成的底泥中污染物释放得到一定程度的抑制,减少了停留时间,改善了出水水质[2]。对比上述4种混凝剂形成底泥的污染物释放抑制能力,PFCS组均好于PFS。
2.3 底泥中的微生物数目
已有研究[23-26]指出,影响底泥释放的因素主要包括:水力扰动、微生物活动以及化学反应。在流动反应系统中,水力扰动对底泥泛起和释放会产生较大的作用。但在本研究中,水力扰动和化学反应条件类似,其造成的影响应该差异较小,这样微生物就可能是影响底泥释放的主要因素。作为验证,我们对比了4种混凝剂沉淀底泥经历培养后微生物的数量差异。
图5中的混凝剂投加量按铁含量计算均为50 mg·L-1,与之对应的不同混凝剂PFS、PFCS(1∶50)、PFCS(1∶40)和 PFCS(1∶30)的铜投加量分别为 0、1、1.25和1.67 mg·L-1。培养后,4种混凝剂底泥微生物菌落数出现显著差异(图5),其中PFS组菌落数最高。在两种稀释度下,随着铜离子含量的升高,PFCS培养基中的微生物数目依次减少,PFCS(1∶30)<PFCS(1∶40)<PFCS(1∶50),都远低于 PFS 组。显然,微生物数量的下降与铜铁比高低有关。混凝剂中大部分铜会沉淀于底泥中,铜铁比越高,混凝剂对于底泥的抑菌性越好。培养24 h后,PFS底泥中的菌落数大约是 PFCS(1∶50)菌落数的 2.5 倍,是PFCS(1∶30)的50倍。尽管研究中合成、使用的PFCS除了铜铁比不同外,合成工艺和混凝参数等均相同,研究出现上述规律的原因,仍有必要进一步系统分析其结构特征和混凝、抑菌机制,但本研究着重于“前置混凝分离-生化处理”系统的适配混凝剂性能的研究,同时限于研究条件,有待后续深入研究。至少从表观上,可以得出结论,铜的参与对混凝剂的混凝效率有促进,对底泥污染物释放有一定的抑制作用。

图5 不同混凝剂产生的底泥经培养24小时后的微生物菌落数Fig.5 Microbial colony number of sludge produced by different coagulants after 24 hours of culture
结合图2-图4,当混凝剂投量均为50 mg·L-1、底泥培养8 h时,PFS非灭菌组对于氨氮、COD和硝氮的释放量是灭菌组的13.2倍、4倍和10倍。可见微生物活动对于底泥中污染物的释放影响显著,造成的污染物释放速度较快;通过抑制微生物的数目和活性可以有效减少底泥中污染物的释放。
污染物的释放主要发生在底泥形成后的前期,8 h内污染物快速释放,之后减缓,其原因或许是达到动态相对平衡。底泥中微生物、污染物、有机颗粒污染物、混凝剂水解成分等富集,微生物降解其中有机质或污染物,可逐渐影响底泥的结构和物质组成,在一定时间表现为底泥有机质释放,因而COD增长;有机氮被微生物氨化作用脱氨,形成氨氮的释放;微生物在残存的溶解氧、硝化菌的作用下,可能发生硝化作用,形成硝氮的释放。4种混凝剂形成底泥中硝氮释放量较小的原因可能是底泥中溶解氧缺乏,硝化微生物数量少或被抑制,因而硝化作用弱;另一种可能是存在反硝化作用(PFS组),消耗了部分硝氮。大多数污水处理厂混凝沉淀池底泥停留时间为12 h~24 h,期间底泥污染物释放到沉后水中进入后续水处理流程,将削弱混凝沉淀的作用;而过于频繁的排泥,会导致污泥浓缩的时间不够,泥水分离效果不好,浓缩周期后的含水率过高(98.5%),严重影响后续污泥处理[24-26]。因而如果混凝剂通过其成分抑制底泥释放,对于减轻沉后水的后续污染具有重要的意义[27]。3种PFCS混凝形成的底泥释放量介于PFS和灭菌PFS组之间,抑制作用明显,且抑制作用随着混凝剂中铜铁比的升高而增强。已有研究[28-31]表明,铜离子容易通过静电吸引被吸收到细胞中,导致蛋白质凝聚和细胞合成酶活性的破坏等,发挥抑菌作用,0.5 mg·L-1以上的铜离子具有微生物抑制效果。本文实际投量下混凝剂中的铜离子量都较小(1.0 mg·L-1~ 1.67 mg·L-1),但大多数沉淀在底泥中浓缩成了较高浓度的铜离子,因而抑菌性得以明显发挥。尽管PFCS和PFS成分略有差异,但其生成的底泥中的化学反应条件非常近似。由此推测,由于化学反应及溶解-沉淀、吸附-解吸附等导致的污染物释放量近似。因此,综合上述分析,底泥释放量之间的差异主要归因于铜对底泥微生物的抑制作用,其中 PFCS(1∶30)对底泥的抑菌作用最强,有效抑制了底泥中污染物的释放,可以有效降低后续生物处理的负荷、提高出水水质。
2.4 铜离子残余
尽管铜离子具备类似铁、铝所具有较好的絮凝性能,但极少作为混凝剂成分的原因就是出于对铜离子毒性的担忧[31]。中国国家《城镇污水处理厂污染物排放标准》[25]规定,总铜的最高允许排放浓度为0.5 mg·L-1。为了验证PFCS的安全性,对沉后水中铜离子浓度进行检测,4种混凝剂投量均为10 mg·L-1~80 mg·L-1,混凝效果见图6。
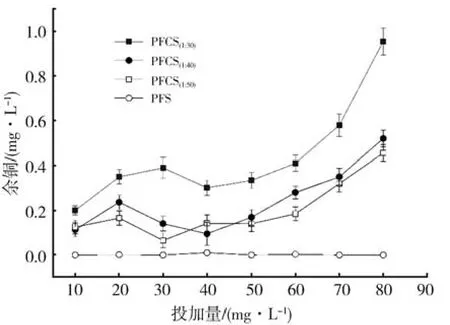
图6 不同混凝剂对余铜浓度的影响Fig.6 Influence of different coagulants dosage on residue copper concentration
3种不同铜铁比的PFCS的余铜趋势相似:随着混凝剂投量的增加,余铜的浓度先小幅度增加,到混凝剂投量达到 30 mg·L-1~ 40 mg·L-1后,略有下降;混凝剂投量超过60 mg·L-1后,余铜的浓度明显上升。当混凝剂(PFCS)投入水中,铜会立即水解并形成多核铜物质和氢氧化铜,然后和污染物形成絮体沉降分离。混凝剂投量不足或过高时,絮体沉降性能差,分离不充分,造成残留铜的升高。Fe3+与Cu2+(Ksp=3×10-38,Ksp=2.2×10-20)相比,同等pH条件下,Cu2+溶解能力较强,因而铜离子残留相对铁离子高。各铜铁比PFCS之间混凝沉后水余铜量的差别主要来自于其本身铜含量的不同,铜铁比高的余铜量较大。相同混凝剂投量下 PFCS(1∶30)沉后水中铜残留率相对较高,如混凝剂投量为50 mg·L-1时,余铜 0.38 mg·L-1,明显高于另外两种比例PFCS(1∶40)和 PFCS(1∶50)。PFCS 在适当的投药量(30 mg·L-1~ 60 mg·L-1)下能很好去除浊度和颗粒态及胶体态污染物且余铜离子不超标,因而可以很好地发挥前置分离和抑制底泥释放的作用。鉴于残余铜的问题,不同来源的污水可能呈现不同的规律和效果,PFCS的应用必须经预先试验确定并及时监控余铜量。
已有研究表明[31-33],铜离子对活性污泥中的硝化菌的活性表现出明显的“低促高抑”的现象,低浓度的铜离子对生物反应是有积极影响的。裴立影等[31]研究认为,低浓度(0.5 mg·L-1)的铜会促进生物脱氮。张肖静等[32]研究指出,低浓度的Cu2+(≤10 mg·L-1)对亚硝化有促进作用,并且在 3 mg·L-1~10 mg·L-1范围内影响规律相似;高浓度(20 mg·L-1)对 AOB(氨氧化菌)有抑制作用,抑制作用可以在一定条件下得以减弱或消除。张兰河等[33]对城市污水处理厂进行分析,发现当Cu2+浓度较低时(<2 mg·L-1),Cu2+对活性污泥的沉降性能、SOUR和Zeta电位影响较小。这也是本文在混凝剂中引入铜的原因之一,含有少量铜(<0.5 mg·L-1)的前置混凝的出水进入生化池,或对后续生物处理有促进作用,至少不至于对生物反应造成负面影响。综上所述,PFCS的使用不仅可以强化混凝单元,还可能在一定程度上促进后续生物反应速率,实现了一次投药,多级强化的结果,这是对整个“前置混凝分离+生物反应”系统的深度强化。
3 结论
(1)合成了新型铜铁混凝剂PFCS,并用不同铜铁比的PFCS与PFS进行对比实验,结果表明,PFCS具有良好的混凝效果,其在颗粒态和胶体态污染物的去除上更有优势(浊度去除率>97%),以较大比例去除了颗粒态和胶体态COD和有机氮等污染物,减少了后续生物反应的负荷。
(2)PFCS在其形成的底泥中有效抑制污染物质(氨氮、硝态氮和COD)的释放,减少对沉后水水质的影响。在实际运用中,PFCS抑制释放可以在一定程度上减轻后续工艺污染负荷,提升出水水质,提升强化混凝的效果,弱化了排泥间隔时间长对于水质的影响。其效果随混凝剂铜铁比增大而提高,PFCS(1∶30)> PFCS(1∶40)>PFCS(1∶50)>PFS。
(3)PFCS的合理使用不会导致沉后水中余铜超标,在有效去除浊度和颗粒态及胶体态污染物的同时,沉后水铜离子浓度低于0.5 mg·L-1。
