恩替卡韦对rtA181V/T突变的慢性乙型肝炎患者的抗病毒效果观察
2021-05-17李淑芹马晓燕汪莉萍
李淑芹,周 静,高 远,马晓燕,汪莉萍
徐州医科大学附属医院 感染性疾病科,江苏 徐州 221002
慢性乙型肝炎(CHB)是全球性的公共健康问题,可引起严重的肝脏疾病,包括肝衰竭、肝硬化及原发性肝癌。据世界卫生组织估计,全球约有2.5亿人感染HBV[1]。在CHB患者中,高水平的HBV DNA复制增加肝硬化及肝癌的发生风险。因此,通过抗病毒治疗将HBV DNA载量降至非常低或无法检测的水平,可以延缓和减少疾病进展以及降低死亡率[2-4]。目前,包括拉米夫定(LAM)、替比夫定(LdT)、阿德福韦酯(ADV)、恩替卡韦(ETV)、替诺福韦(TDF)、丙酚替诺福韦(TAF)在内的核苷(酸)类似物(NAs)被批准用于抗HBV来预防肝脏疾病的进展。但由于cccDNA的半衰期较长,CHB患者需长期口服NAs来抑制病毒的复制,而长时间NAs治疗会导致HBV逆转录酶(reverse transcription,RT)区发生耐药突变的风险增加,最终影响抗病毒治疗效果。
目前主要的耐药模式(通路)有L型核苷耐药模式(LAM、LdT)、无环磷酸盐耐药模式(ADV、TDF)、共享耐药模式(ETV)、双重耐药模式及ETV初治耐药模式5种[5-6]。而HBV RT181位点发生的氨基酸改变属于多药耐药,会同时影响L型核苷耐药模式和无环磷酸盐耐药模式,从而对LAM、ADV、LdT、TDF的药物敏感性呈不同程度的下降[6]。此外,体外研究[7]显示,rtA181V/T变异会影响病毒的复制,使HBsAg的分泌减少,具有潜在的致癌性[8]。研究[9]还发现181位点变异联合其他变异后的耐药性较其单独变异的耐药性增加。欧洲肝病学会指南[10]指出,ETV可作为rtA181V/T的挽救治疗。对此,本研究通过回顾性分析研究ETV对rtA181V/T突变的CHB患者的抗病毒治疗效果。
1 资料与方法
1.1 研究对象 选择2012年1月—2017年1月就诊于本院门诊及住院部,进行HBV基因耐药变异检测,并排除存在对ETV耐药变异的CHB患者(rtTl84A/G/I/S、rtS202G/I、rtM2041/V/S、rtM250V/L、rtL180M、rtM250V/L、rtV173L)。纳入标准:(1)年龄18岁以上,HBsAg持续阳性≥6个月;(2)所有病例诊断均参照《慢性乙型肝炎防治指南(2019年版)》[11]。排除标准:(1)其他嗜肝病毒感染、自身免疫性肝病、酒精性肝病、非酒精性脂肪肝、药物性肝损伤及遗传代谢性肝病等;(2)既往使用PEG-IFN治疗的患者;(3)不符合《慢性乙型肝炎防治指南(2019年版)》[11]及资料不全的患者。
1.2 治疗方法 所有患者均予以ETV(正大天晴药业集团股份有限公司,国药准字H20100019)口服,0.5 mg,1次/d。
1.3 观察指标及判定标准
1.3.1 检测仪器与设备 (1)血清HBV DNA检测:采用美国ABI公司生产的 ABI7500实时荧光定量PCR仪检测,检测下限为500 IU/ml。(2)血清HBeAg及HBsAg检测:采用美国Abbott I2000全自动微粒子化学发光免疫分析仪定量检测。HBsAg检测范围为0.05~250 IU/ml,>250 IU/ml时采用1∶500自动稀释检测,HBeAg检测下限为0.50 PEIU/ml,<0.50 PEIU/ml定义为 HBeAg阴性。(3)采用Beckman Coulter AU5800全自动生化分析仪检测ALT、AST、TBil。(4)HBV基因耐药检测:采用ABI基因测序仪3130对HBV DNA>1.0×103拷贝/ml的标本进行检测,定量检测HBV的P基因区有关于LAM、LdT、ADV、ETV、TDF的耐药位点。上述所有指标均在本院感染科实验室完成。
1.3.2 疗效评估指标 依据《慢性乙型肝炎防治指南(2015年更新版)》[12],病毒学应答是指治疗过程中血清HBV DNA低于检测下限。应答不佳或部分病毒学应答是指NAs抗病毒治疗中依从性良好的患者,治疗24周时HBV DNA较基线下降幅度<2 log10IU/ml,但仍然可以被检测到。病毒学突破是指NAs抗病毒治疗中依从性良好的患者,在未更改治疗的情况下,HBV DNA水平比治疗中最低点上升1个log值或一度阴转后又转为阳性,并在1个月后以相同试剂重复检测加以确定,可有或无ALT升高。病毒学无应答是指NAs治疗依从性良好的患者,治疗12周时HBV DNA较基线下降幅度<1 log10IU/ml或治疗24周时HBV DNA较基线下降幅度<2 log10IU/ml。
1.4 伦理学审查 本研究已通过徐州医科大学附属医院伦理委员会批准,批号:XYFY2020-KL214-01。

2 结果
2.1 一般资料 共纳入符合入组条件的CHB患者155例,按照耐药变异类型将患者分为3组,A组:无耐药变异72例(均为初治的CHB患者);B组:rtA181V/T变异45例;C组:rtA181V/T+rtN236T变异38例。其中,A组男47例,女25例;年龄30~66岁,平均(47.53±9.80)岁。B组男28例,女17例;年龄32~63岁,平均(46.27±9.57)岁。C组男20例,女18例;年龄30~64岁,平均(47.42±9.54)岁。3组比较,年龄、性别以及ALT、AST、TBil水平差异均无统计学意义(P值均>0.05)(表1)。
2.2 患者既往用药情况及耐药变异模式 本研究共随访了102例发生包含rtA181V/T单一或多位点突变的经治CHB患者,其中发生rtA181V/T突变者45例,包含rtA181V/T在内的多位点突变者57例。同时对于已纳入的多耐药位点患者,需排除已出现ETV耐药位点的病例(表2),最后符合条件的共38例,均为rtA181V/T+rtN236T变异。根据患者既往临床NAs用药史可知,有76例曾服用两种及以上NAs抗病毒治疗,其中47例出现多位点耐药(61.84%),既往单药NAs抗病毒治疗的26例患者中,10例出现多位点耐药(38.5%),2组患者多位点耐药人数经χ2检验结果显示,差异有统计学意义(χ2=4.295,P=0.038),表明用药模式影响耐药位点的发生,既往服用多种NAs的患者,更容易出现多位点突变和多重耐药的可能。

表2 102例慢性HBV感染者既往用药情况及耐药变异模式
2.3 基线特征 对于B、C 2组患者来说,其初始服用NAs治疗时基线HBV DNA水平[(7.08±1.59)、(6.94±1.61)log10IU/ml]比发生181位点突变时的HBV DNA基线水平[(6.22±1.48)、(5.94±1.45)log10IU/ml]较高(t=3.098,P=0.002;t=2.850,P=0.004)。当经治CHB患者出现rtA181V/T相关耐药时,平均HBV DNA水平超过4 log10IU/ml。3组患者HBV DNA、HBsAg、HBeAg比较差异均无统计学意义(P值均>0.05)(表1)。

表1 ETV挽救治疗时3组患者相关基线特征
2.4 3组病毒学应答、生化学反应的比较 随访至48周,ETV挽救治疗无1例患者出现病毒学无应答的情况,提示ETV对于发生rtA181位点耐药变异挽救治疗具有良好的效果。在ETV挽救治疗24周时,A、B、C 3组分别有50、31和28例达到病毒学完全应答水平,但HBV DNA阴转率差异无统计学意义(P>0.05)。24周时3组HBeAg阴转情况分别为3例(4.2%)、1例(2.2%)、2例(5.3%),差异无统计学意义(P>0.05)。治疗48周3组HBV DNA阴转率、HBeAg阴转率比较,差异均无统计学意义(P值均>0.05)。ETV挽救治疗24周及48周后3组患者的ALT、AST及TBil均下降,但3组相比差异均无统计学意义(P值均>0.05)(表3)。
2.5 影响ETV挽救治疗效果的单因素及多因素分析 根据是否出现HBV DNA低于检测下限为准,将治疗48周后的患者分为有效和无效组进行logistic回归分析。单因素分析显示,HBV DNA水平和HBeAg滴度对治疗后病毒学应答有影响(P值均<0.05)(表4)。多因素分析则提示HBV DNA水平是影响治疗效果的危险因素(OR=1.655,95%CI:1.128~2.428,P=0.01)。
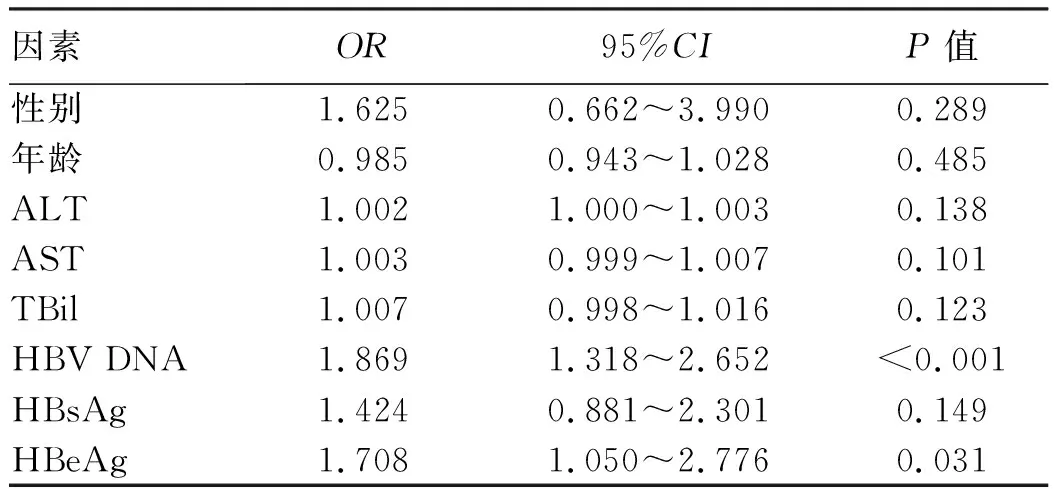
表4 ETV挽救治疗期间病毒学反应预测的单因素分析
3 讨论
由于初期我国经济条件不足,低效、高耐药的NAs如LAM、ADV等被广泛用于临床中,加之医务人员对耐药问题认识不足,导致耐药现已成为NAs抗病毒治疗中越来越严峻的问题。HBV对NAs的耐药变异往往发生在HBV RT区,而不同位点突变的情况则是由所服用的NAs所决定、所诱导。181位点变异最早是Yeh等[13]在研究LAM耐药中发现的,而根据HBV耐药模式通路[6]可知,181位点变异是交叉核苷和核苷酸两大类抗病毒药物的共同耐药位点,会影响大部分的NAs抗病毒治疗效果,包括LAM、ADV、LdT、TDF。Villet等[14]的体外研究结果显示,rtA181V/T突变降低了对LAM(10倍)、ADV(2~8倍)和TDF(2~3倍)的敏感性。本研究共纳入102例发生rtA181位点突变的经治CHB患者,结果显示既往曾服用多种NAs抗病毒治疗的患者更容易出现多位点耐药变异。据报道[15]在欧美韩日等发达地区,有80%~90%的初治CHB患者选用高效、低耐药的NAs治疗,而我国高达81%的初治CHB患者因经济等原因而选用了低效、高耐药的NAs。并且随着人们对耐药的认识,发现了部分患者即使未使用任何NAs抗病毒治疗,也会出现相关耐药位点的预存耐药现象[16]。因此对于CHB患者而言,初始抗病毒治疗宜选用高耐药基因屏障的一线药物,如ETV、TDF或者TAF。对于已经选用二线抗病毒药物的患者,在没有发生耐药变异前建议尽早换用一线抗病毒药物;已经发生病毒学突破或应答不佳的情况,建议予以基因耐药检测,根据检测结果选择敏感的一线药物,或者联合用药,以减少耐药变异的发生。
rtA181位点突变是近年来耐药变异研究的重点。该位点突变主要与LAM、ADV有关,但在目前几乎所有的NAs治疗中都可以检测到rtA181V/T突变位点,包括具有高耐药屏障的TDF,甚至部分发生预存耐药的患者也能检测出rtA181V/T突变。另外由于HBV基因组中S区完全重叠于RT区,当RT区某些碱基发生突变时,S区的改变也就相应而生。其中发生rtA181T突变,会引起S区第172位氨基酸突变成终止密码子,从而生成了截断的S蛋白,记作rtA181T/sW172*,而研究[13,17]表明,该截断蛋白会影响病毒的复制、HBsAg的分泌及具有潜在的致癌性。因此,本回顾性研究追踪了发生耐药变异的患者初始服用NAs治疗的基线水平,结果与姬粉芝等[18]的论文结果一致:发生rtA181V/T突变位点的患者其HBV DNA基线水平较服用NAs治疗基线时HBV DNA基线水平有所下降。
ETV属于一线抗HBV药物,能快速抑制病毒复制、改善肝纤维化,并且具有很低的耐药率[19]。欧洲肝病学会指南[10]建议ETV可作为发生rtA181V/T变异的CHB患者的挽救治疗。中国学者姬粉芝等[18]在一项回顾性研究中发现对于发生rtA181位点变异的经治CHB患者,ETV单药的效果要明显优于LdT。韩登高等[20]研究显示,ETV单用与联合ADV治疗rtA181V/T突变的患者在病毒学及生化学指标上均无显著差异,而本研究选用ETV挽救治疗后,3组患者治疗后的HBV DNA水平明显下降,截止至随访结束,大部分患者都达到了病毒学完全应答,且3组之间HBV DNA阴转率、HBeAg阴转率比较无显著统计学差异,ALT、AST、TBil复常率之间也无统计学差异,且未出现病毒学突破或病毒无应答现象,说明ETV对rtA181位点突变有很好的挽救治疗效果。但是作者观察到无耐药变异组24、48周HBV DNA阴转率与Luo等[21]研究结果(69.4% vs 85.0%、83.3% vs 89.4%)存在差异。考虑到以下方面的原因:第一,多项研究结果表明HBV DNA高载量、HBeAg阳性、ALT低水平等影响ETV治疗初治CHB患者的病毒学应答[21-22],本文中无耐药变异组所纳入的CHB患者HBeAg均为阳性,相较于Luo等研究中的HBeAg阳性率(113/230)较高。其次,尽管在ETV治疗之前已对无耐药变异组进行基因耐药变异检测,但由于检测技术有限而有可能出现漏检情况。因此,对于初治CHB患者,服用ETV治疗1年后仍有持续低病毒血症,临床上要如何处理?Luo等[21]的研究中对于这类患者继续给予ETV单药治疗,结果显示在144、192周HBV DNA阴转率均为100%。因此,在临床中对于治疗1年仍表现持续低病毒血症的初治CHB患者可以暂时不予以调整抗病毒药物,但需要动态观察HBV DNA水平,如果有持续下降之势,则可以继续应用;如果HBV DNA在继续ETV抗病毒治疗过程中处于平台期,则需及时调整抗病毒方案,可以换用TDF或TAF,也可以选择联合用药。
若患者服用ETV后再次出现应答不佳或耐药,该如何治疗?Lim等[23]经过96周的随访观察发现TDF单药组与ETV联合TDF组在病毒学、生化学及血清学应答上无显著差异。其他的研究[22,24]也表明TDF单药治疗对LAM、ADV及ETV耐药的患者是有效的。但国外的一项队列研究[25]显示,与初治的CHB患者相比,TDF单药治疗对ADV耐药患者的疗效较低,尤其是对LAM、ADV均耐药的患者。且2019年版更新的《慢性乙型肝炎防治指南》[11]也建议:对于出现LAM、ADV及ETV的多重耐药,建议ETV联合TDF/TAF治疗。因此,对于多重耐药CHB患者,建议选择联合抗病毒治疗。
Li等[26]研究报道,HBV DNA水平可以预测ETV挽救治疗的治疗效果。本研究单因素分析发现HBV DNA水平及HBeAg滴度影响ETV抗病毒疗效,但多因素分析提示初始治疗时HBV DNA水平是ETV抗病毒治疗48周效果的独立预测因子。
综上,本研究探讨ETV挽救治疗rtA181V/T变异及rtA181V/T+rtN236T变异患者的疗效,结果表明ETV挽救治疗效果较好,而基线HBV DNA水平是治疗48周时抗病毒效果的唯一预测因子。但本研究仍存在一定的局限性。首先,该设计是回顾性的,为了克服由此产生的选择偏差,本研究采用严格的纳入和排除标准,并试图延长观察期。其次,1年的调查可能不足以观察抗病毒药物的长期疗效。第三,纳入患者数量相对不足(n=155),随访时间较短,因此需要更长时间的随访来评估ETV挽救治疗rtA181V/T突变患者的长期疗效,以及观察该位点耐药变异后疾病进展情况和肿瘤发生情况等。
利益冲突声明:本研究不存在研究者、伦理委员会成员、受试者监护人以及与公开研究成果有关的利益冲突。
作者贡献声明:李淑芹负责课题设计,资料分析,撰写论文;周静、高远、马晓燕参与收集数据,修改论文;汪莉萍负责拟定写作思路,指导撰写文章并最后定稿。
