苯扎贝特缓释片的制备及体外释放研究
2021-05-12刘竹冯煜马久太肖功胜魏荣石辉吴云生邢涛
刘竹,冯煜,马久太,肖功胜,魏荣,石辉,吴云生,邢涛*
(1.陕西步长制药有限公司,陕西咸阳 712000;2.杨凌步长制药有限公司,陕西咸阳 712100;3.陕西省食品药品检验研究院,陕西西安 710065)
高血脂症的患病原因主要与不良生活习惯有关。随着生活水平的提高,人们的食物主要以蛋、油炸食品等高热量、高胆固醇食物为主,同时现代人的生活节奏加快、工作压力大,户外运动逐渐减少等不良生活习惯直接导致高血脂人群数量的增加[1],并且呈现年轻化的趋势,甚至在儿童群体也很常见[2]。
苯扎贝特为氯贝丁酸衍生物类(贝特类)血脂调节药,能有效地降低血浆胆固醇[3-4],同时升高HDL-C(高密度脂蛋白胆固醇)水平[5]。苯扎贝特口服吸收快,半衰期短,因此国外研制生产了苯扎贝特缓释片,只需每日服用一次即可,既方便使用,又能平稳降低血浆胆固醇,降低毒副作用。
在临床效果方面,苯扎贝特缓释片更有利于稳定血脂水平。在国外,苯扎贝特缓释片已应用了很长时间,积累了大量的临床经验,缓释片剂是苯扎贝特的首选剂型,国内已有研究机构或企业在研制苯扎贝特缓释制剂,但目前均没有获得生产批件。苯扎贝特缓释片的研制成功将为患者提供疗效更好的缓释制剂,降低服药成本,提高产品疗效,而且本品上市后将借助剂型的优势,进一步扩大市场份额,提高产品竞争力。
1 材料与方法
1.1 仪器
SHK-6型湿法混合制粒机,西安润天制药机械有限公司;DP30A型单冲压片机,北京国药龙立科技有限公司;JGB-5D高效糖衣薄膜包衣机,浙江小伦制药机械有限公司;CT-C0型热风循环烘箱,常州倍成干燥设备公司;RZQ-8D型溶出取样系统、RCZ-8M型溶出试验仪,天津天大天发;UV-2600紫外分光度计,日本岛津;S400-uMix型pH计,德国梅特勒。
1.2 试药与试剂
市售苯扎贝特缓释片(批号04308),德国STADA;苯扎贝特,牡丹江恒远药业有限公司;羟丙甲纤维素(Hydroxypropyl Methyl Cellulose,HPMC)E5LV、E50LV,美国DOW;淀粉,山东聊城阿华制药有限公司;羧甲基淀粉钠、硬脂酸镁,安徽山河药用辅料股份有限公司;药用级乙醇,梅河口市阜康酒精有限责任公司。
1.3 试验方法
1.3.1 苯扎贝特缓释片的制备
称取适量的苯扎贝特、HPMC E5LV、HPMC E50LV、淀粉于湿法混合制粒机中,开启搅拌桨和切刀进行混合,喷雾加入70%乙醇制粒,将湿颗粒整粒后在热风循环烘箱中于50 ℃干燥,干颗粒经整粒后,加入适量的羧甲基淀粉钠及硬脂酸镁混合均匀,压片,包衣,即得,每片含主药为0.4 g。
1.3.2 制备工艺优化
1.3.2.1 缓释材料比例
保持缓释材料总用量为7.5%不变,分别考察羟丙甲纤维素E5LV与羟丙甲纤维素E50LV的比例为3∶1、2∶1、1∶1和1∶2时的释放度。按照《普通口服固体制剂溶出度试验技术指导原则》中非模型依赖相似因子(f2)方法,对自制样品和参比制剂(市售苯扎贝特缓释片)的释放度进行对比研究。
1.3.2.2 羧甲基淀粉钠用量
分别考察羧甲基淀粉钠用量为2%、4%和6%时对释放度的影响。羧甲基淀粉钠采用外加法,并通过调整稀释剂用量使片重保持不变。对自制样品和参比制剂的释放度进行对比研究。
1.3.3 不同介质下体外释放行为对比
按照释放度测定法,以氯化钠盐酸溶液(pH 1.2)、醋酸盐缓冲液(pH 4.0)、磷酸盐缓冲液(pH 6.8)及水均为900 mL为释放介质,转速为50 r/min,分别依法对自制样品和市售样品进行操作,30 min、60 min、90 min、120 min、180 min、240 min 时,分别取溶液10 mL,滤过,并同时在操作容器中补充相同温度、相同体积的释放介质,滤过,精密量取续滤液适量,用释放介质稀释制成10 μg/mL的溶液,摇匀,作为供试品溶液进行释放度测定。对自制样品和参比制剂的释放度进行对比研究。
1.3.4 苯扎贝特缓释片释放度测定方法
按照《中国药典》(2015年版四部)溶出度与释放度测定法第二法,以磷酸盐缓冲液pH 6.8(取氢氧化钠0.896 g、磷酸二氢钾6.805 g,加水溶解稀释至1 000 mL,用磷酸或氢氧化钠调节pH值为6.8)900 mL为释放介质,转速为50 r/min。依法操作,经30 min、90 min和180 min时,分别取溶液10 mL,滤过,并同时在操作容器中补充相同温度、相同体积的释放介质,精密量取续滤液适量,用释放介质稀释制成10 μg/mL左右的溶液,摇匀,作为供试品溶液,采用紫外分光光度计在228 nm的波长处分别测定吸光度。
1.3.5 苯扎贝特标准曲线绘制
取苯扎贝特对照品适量,精密称定,加释放介质稀释制成100 μg/mL左右的苯扎贝特溶液,作为对照品溶液贮备液。分别精密量取对照品贮备液到一定容积的量瓶中,用释放介质稀释至刻度,摇匀,分别配制成约相当于完全释放度浓度的20%、40%、80%、120%、160%的线性试验供试品溶液。照拟定的释放度测定方法,测定吸光度,绘制苯扎贝特吸光度-浓度曲线。
2 结果与讨论
2.1 苯扎贝特标准曲线
苯扎贝特缓释片在2.026~16.210 μg/mL范围内线性方程为Y=0.052 0X+0.007 9,其中r=0.999 5。
2.2 缓释材料对缓释片体外释放的影响
图1结果表明,当处方中缓释材料总量不变时,缓释片释药速率随着HPMC E5LV用量增加而加快,这是因为HPMC E5LV较HPMC E50LV粘度低。通过与参比制剂体外释放度相似性比较,确定二者的比例为2∶1。

图1 缓释材料间比例(E5LV∶E50LV)对释放度的影响
羟丙甲纤维素是缓控释制剂中应用较多的一种亲水凝胶骨架材料,此类骨架片口服后在体内发生水化作用生成凝胶,药物可通过扩散、溶蚀以及扩散与溶蚀相结合方式释放药物,其特点是羟丙甲纤维素凝胶骨架能够完全溶解,药物可以完全释放,生物利用度高[8]。本试验筛选处方时固定缓释材料总量,调节羟丙甲纤维素E5LV和E50LV的比例,其二者比例不同所形成的凝胶强度也会有差异。羟丙甲纤维素E5LV粘度低,羟丙甲纤维素E50LV粘度较E5LV高,缓释作用羟丙甲纤维素E50LV较E5LV强,故制剂释放度随着羟丙甲纤维素E50LV比例的增大而降低。当一种羟丙甲纤维素的粘度和缓释作用无法满足要求时,可以考虑用两种羟丙甲纤维素调节成一定比例以达到制剂释放度要求。
2.3 崩解剂对缓释片体外释放的影响
图2结果表明,羧甲基淀粉钠用量为2%~4%时,药物的释放速率随用量增加而加快;羧甲基淀粉钠用量为4%~6%时,随着用量增加,药物的释放速率没有显著变化。根据与参比制剂释放度相似性比较,确定崩解剂的用量为4%。
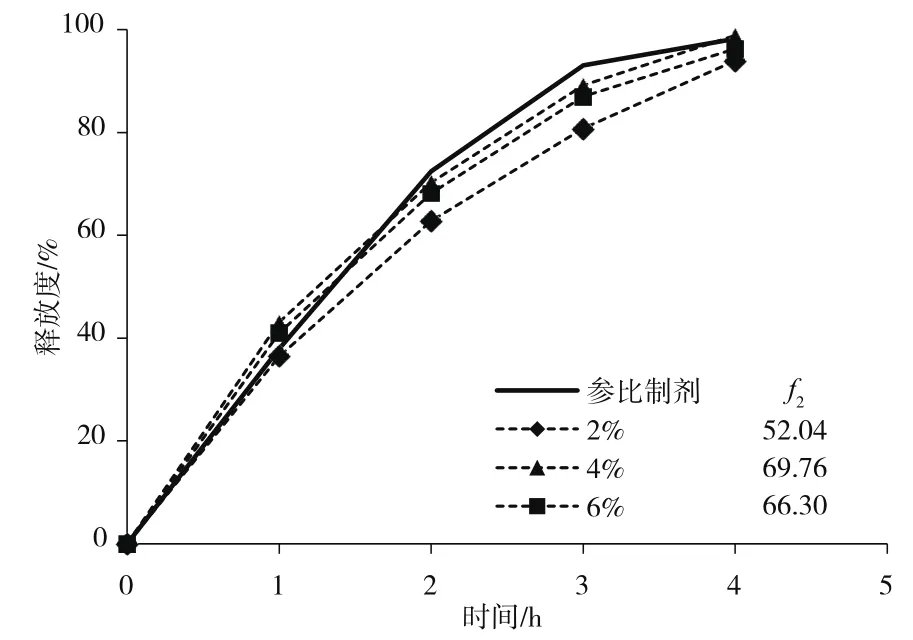
图2 羧甲基淀粉钠用量对释放度的影响
2.4 自制样品与参比制剂体外释放行为对比
如图3所示,自制苯扎贝特缓释片在4种介质中与参比制剂的相似因子均大于50,且没有出现“突释”现象[9],达到药物缓慢释放的目的。根据《普通口服固体制剂溶出度试验技术指导原则》,非模型依赖相似因子f2值高于50时,可认为两条曲线具有相似性,受试样品与参比样品具有等效性。

图3 4种释放介质下苯扎贝特缓释片的释放度测定结果
研究缓控释制剂药物释放机制时,通常采用数学模型对药物释放曲线进行拟合,然后根据拟合结果对释药机制进行推断[6]。一般可用零级方程、一级方程及Higuchi方程等拟合[7],拟合方法、拟合方程及相关系数见表1。拟合时以相关系数r最大者为最佳拟合结果。由结果可知,一级方程的相关系数r最大,故自制苯扎贝特缓释片在释放介质中的释放机制接近一级释药模型。Higuchi方程拟合相关性较差,说明制剂释药方式不是单纯的扩散机制,自制苯扎贝特缓释片可能为扩散与骨架溶蚀相协同的释药机制。

表1 释药模型及相关系数
3 结论
苯扎贝特缓释片最佳制备工艺为羟丙甲纤维素E5LV和E50LV的比例为2∶1、羧甲基淀粉钠用量为4%;制剂在氯化钠盐酸溶液、醋酸盐缓冲液、磷酸盐缓冲液及水4种介质中的相似因子f2均大于50,体外释药符合一级动力学方程,与参比制剂体外溶出行为相似。
