阿帕替尼治疗进展期胃癌对患者血清正常上皮细胞特异性-1及免疫功能的影响
2021-05-12赵建红李鸿彬程相超
赵建红,李鸿彬,程相超
河南省直第三人民医院1消化内科,2消化病诊疗中心,郑州 450000
胃癌属于常见消化道肿瘤,早期多因无特殊临床症状而导致错失最佳治疗时机,被确诊时多已处于进展期甚至晚期,严重影响了患者的治疗效果及预后。进展期胃癌患者因肿瘤细胞转移和患者身体原因一线治疗主要采用化疗药物,但部分患者由于治疗出现严重不良反应及对化疗药物较低的敏感性而治疗效果较差[1]。因此,探寻化疗耐药后的治疗方法已成为临床肿瘤治疗研究的重要方向。靶向治疗的出现为化疗耐药的肿瘤患者带来了新的治疗方式,相关研究提示,多种肿瘤应用表皮生长因子受体-酪氨酸激酶抑制剂取得了满意的效果[2-3]。阿帕替尼、吉非替尼等作为重要的表皮生长因子受体-酪氨酸激酶抑制剂已逐渐在临床使用,但关于阿帕替尼治疗进展期胃癌的疗效研究资料较少。故而,本研究探讨阿帕替尼治疗进展期胃癌的临床疗效及对患者血清正常上皮细胞特异性-1(normal epithelial cell specificity-1,NES1)表达及免疫功能的影响,现报道如下。
1 资料与方法
1.1 一般资料
收集2017年1月至2019年12月在河南省直第三人民医院治疗的进展期胃癌患者的病历资料。纳入标准:①经病理学检查确诊为胃癌;②经一线治疗后失败;③具有可客观测量的病灶;④卡氏功能状态(Karnofsky performance status,KPS)评分>70分;⑤前1个月内未进行放化疗;⑥临床资料保存完整。排除标准:①合并其他系统恶性肿瘤;②有心、肝、肾等其他脏器疾病、免疫系统疾病、血液系统疾病等。根据纳入、排除标准,共纳入118例进展期胃癌患者,按治疗方案不同分为观察组(n=68)和对照组(n=50),两组患者各临床特征比较,差异均无统计学意义(P>0.05)(表1),具有可比性。
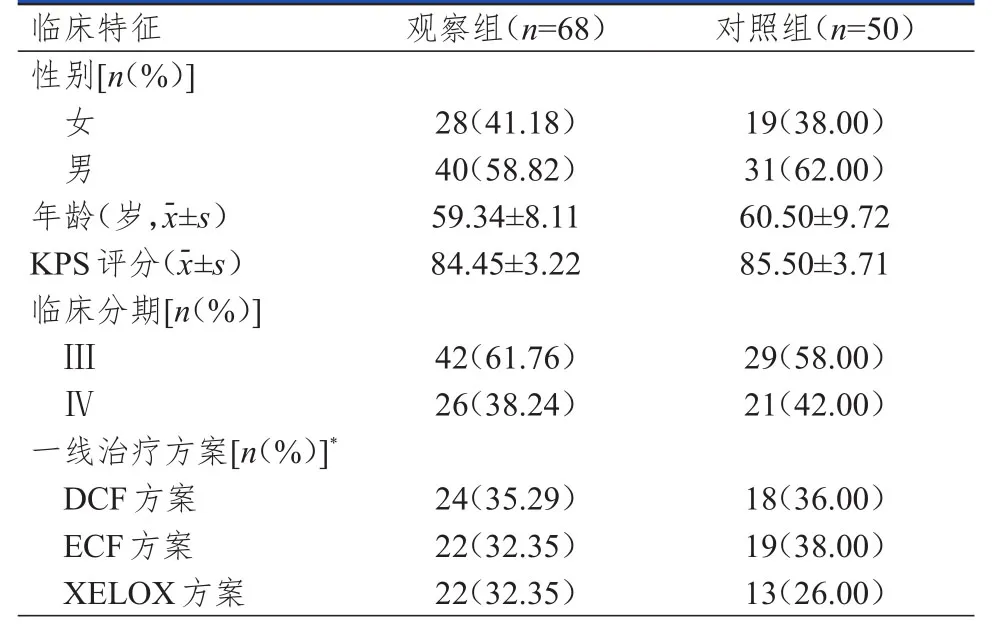
表1 两组患者的临床特征
1.2 治疗方法
所有患者均给予抑酸、保肝、保肾及止吐的基础治疗。对照组给予替吉奥治疗(体表面积<1.25 m2,早晚每次各40 mg;体表面积1.25~1.50 m2,每次早上40 mg,晚上60 mg;体表面积>1.50 m2,早晚每次各60 mg),于早饭后和晚饭后各服1次,连服28天,之后停药14天,至少接受2个周期的治疗并进行疗效评价。观察组给予阿帕替尼+替吉奥治疗:替吉奥给药方法同对照组,阿帕替尼每日口服1次,每次500 mg,21天为1个周期,至少接受2个周期的治疗并进行疗效评价。
1.3 观察指标
观察两组患者疗效及总生存时间。所有患者抽血前均应禁食8 h以上,于入院24 h内及治疗后2个周期晨起空腹肘静脉抽血3 ml,置于EDTA抗凝真空采血管中,静置30 min后,3000 r/min离心10 min,分离血清,将血清转移至EP管中,保存于-80℃的冰箱中24 h内进行检测。采用酶联免疫法检测血清NES1,酶标仪(购自美国BD公司)检测450 nm波长读数;采用流式细胞仪(购自美国贝克曼公司)检测治疗前后两组患者CD3+、CD4+、CD8+T淋巴细胞比例。
1.4 疗效评价[4]
完全缓解(CR)为病灶消失,且维持≥4周;部分缓解(PR)为病灶较治疗前缩小≥50%,且维持≥4周;疾病稳定(SD)为病灶较治疗前缩小<50%或增大<25%;疾病进展(PD)为病灶较治疗前增大≥25%。疾病控制率(disease control rate,DCR)=(CR+PR+SD)例数/总例数×100%。
1.5 统计学方法
采用SPSS 22.0统计学软件进行数据分析,计量资料以均数±标准差(±s)表示,组间比较采用t检验;计数资料以例数及率(%)表示,组间比较采用χ2检验;等级资料的比较采用秩和检验;采用Kaplan-Meier法绘制生存曲线,生存情况的比较采用Log-rank检验;以P<0.05为差异有统计学意义。
2 结果
2.1 疗效的比较
观察组患者疗效优于对照组,差异有统计学意义(Z=-2.267,P=0.023),观察 组 患者 DCR 为79.41%(54/68)。(表2)
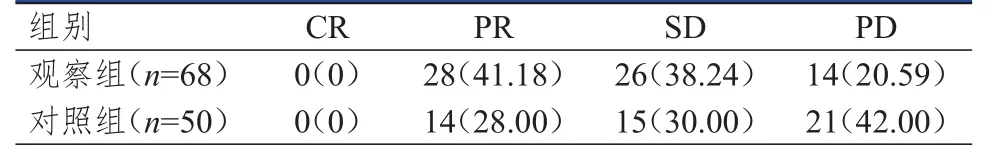
表2 两组患者的疗效[n(%)]*
2.2 治疗前后免疫功能指标的比较
治疗前,两组患者CD3+、CD4+、CD8+T淋巴细胞比例比较,差异均无统计学意义(P>0.05);治疗后,观察组患者CD4+T淋巴细胞比例明显高于对照组,CD8+T淋巴细胞比例明显低于对照组,差异均有统计学意义(P<0.01)。(表3)
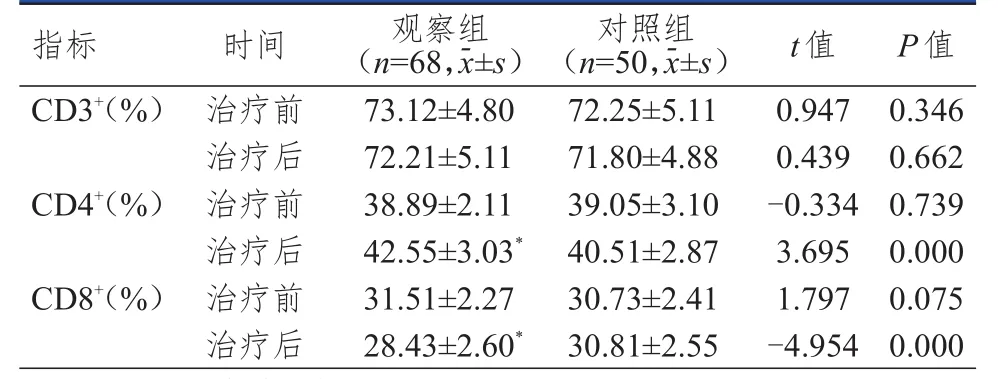
表3 治疗前后两组患者免疫功能指标的比较
2.3 治疗前后血清NES 1水平的比较
治疗前,两组患者血清NES1水平比较,差异无统计学意义(P>0.05);治疗后,两组患者血清NES1水平均升高(P<0.05),且观察组血清NES1水平明显高于对照组(P<0.01)。(表4)
表4 治疗前后两组患者血清NES 1水平的比较(±s)
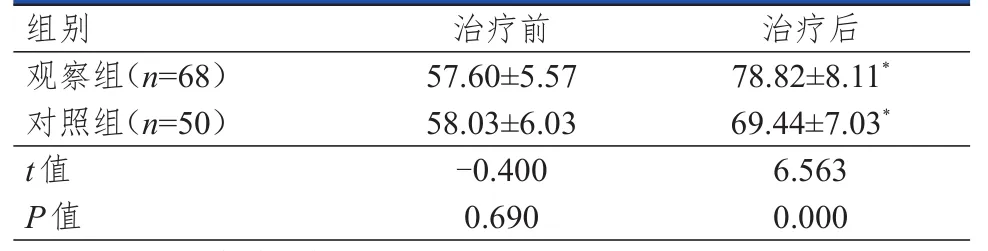
表4 治疗前后两组患者血清NES 1水平的比较(±s)
注:*与本组治疗前比较,P<0.05
images/BZ_79_1289_788_2246_1023.png
2.4 生存情况的比较
观察组患者中位生存时间为9个月(95%CI:8.64~9.36),明显长于对照组的 5个月(95%CI:4.51~5.49),差异有统计学意义(χ2=27.291,P<0.01)(图1)。Ⅲ期和Ⅳ期观察组患者中位生存时间分别为 10个月(95%CI:9.10~11.43)和 8个月(95%CI:7.67~9.88),差异无统计学意义(χ2=4.022,P>0.05)。
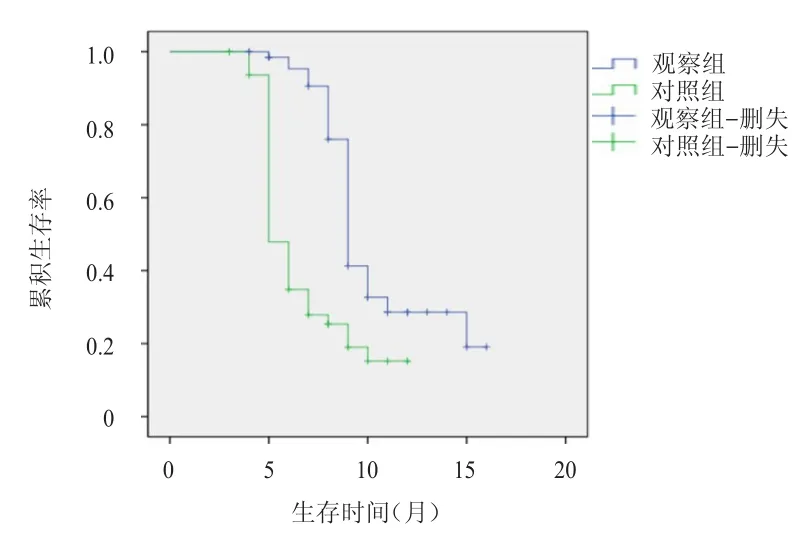
图1 观察组(n=68)与对照组(n=50)胃癌患者的生存曲线
3 讨论
中国胃癌发生率尽管低于韩国和日本,但由于人口较多,患病总人数居亚洲第一,每年新确诊胃癌患者可达67.9万并具有较高病死率,2015年相关数据提示中国约49.8万人因胃癌死亡[5-7]。国内外研究均发现已处于多发转移的进展期或晚期胃癌患者,单纯的手术治疗已无法取得显著效果而需要长期的化疗维持,但临床实践证实长期化疗后患者后期极易出现化疗耐药而降低治疗效果,而且化疗的药物毒性较强,对机体的损伤也较大[8-10]。
基础研究证实,血管生成是胃癌转移、浸润的重要因素,而血管内皮生长因子及酪氨酸激酶受体是使胃癌细胞转移、浸润能力最强和特异度最高的因子[11-12]。阿帕替尼作为小分子酪氨酸激酶抑制剂,可通过抑制血管内皮生长因子结合其受体的信号转导而抑制肿瘤细胞血管内皮细胞异常增殖,抗肿瘤效果良好并已在肺癌及卵巢的临床治疗中取得疗效[12-14]。本研究结果显示观察组患者疗效优于对照组,DCR可达79.41%。上述结果提示阿帕替尼较替吉奥具有更好的疗效。阿帕替尼是属于典型的表皮生长因子受体-酪氨酸激酶抑制剂,能够通过抑制表皮生长因子受体-酪氨酸激酶阻碍肿瘤细胞的增殖、转移及肿瘤血管生成等,促进肿瘤细胞凋亡,与化疗联合应用后发挥协同作用,更有助于促进肿瘤细胞的凋亡,抑制肿瘤细胞的增殖、发展,提高治疗效果。
NES1是新型抑癌基因,对防治胃癌具有指导性意义。本研究结果提示,治疗后观察组患者血清NES1水平明显高于对照组。免疫系统受多种因子调控,免疫应答或激活免疫耐受均可能损伤机体组织。本研究发现,观察组患者CD4+T淋巴细胞比例明显高于对照组,CD8+T淋巴细胞比例明显低于对照组。上述结果提示阿帕替尼治疗进展期胃癌具有改善免疫功能提升血清NES1水平的作用。国外研究发现,机体处于免疫抑制状态时部分肿瘤细胞可能逃出免疫清除而出现免疫逃逸现象,加速了进展期胃癌患者的病情,靶向治疗作用于细胞分子水平并针对性地选择致癌位点使肿瘤细胞出现特异性死亡,对肿瘤组织周围细胞几乎不产生任何影响,属于进展期胃癌的有效手段;另外,阿帕替尼联合基础化疗可将产生耐药的靶向药物细胞亚群较彻底清除,改善机体免疫功能并提高抑癌基因NES1水平[15]。
生存分析研究结果提示,观察组患者中位生存时间明显长于对照组。该结果提示替吉奥联合阿帕替尼更有助于延长患者的总生存时间。阿帕替尼属于高效血管内皮生长因子抑制剂,口服经肠道吸收后可高度聚集于肿瘤血管内皮,选择性竞争结合细胞内的血管内皮生长因子受体2(vascular endothelial growth factor receptor 2,VEGFR2)ATP结合位点,阻断下游信号而抑制肿瘤新血管生成,还能够减小肿瘤血管的直径,改善血管曲折度和通透性,改善患者的远期预后。
综上所述,阿帕替尼治疗进展期胃癌有较好的临床疗效,改善免疫功能,升高血清NES1水平。这为临床进展期胃癌的治疗提供了数据参考和新的思路,具有一定的临床意义,但本研究未分析替吉奥联合阿帕替尼安全性的不足,还有待进一步分析探讨。先前的临床研究提示阿帕替尼单药治疗的主要不良反应包括高血压、纳差、皮疹或蛋白尿等,经过对症治疗均可逆转,安全性总体可控[16-18],但关于联合化疗的不良反应还有待进一步研究分析。
