肝豆状核变性并发红斑狼疮4例及文献复习
2021-05-11施文黄晓明冯云路费允云焦洋
施文,黄晓明,冯云路,费允云,焦洋
作者单位: 100730 北京,中国医学科学院 北京协和医学院 北京协和医院消化内科(施文、冯云路),全科医学科(普通内科)(黄晓明、焦洋),风湿免疫科,风湿免疫病学教育部重点实验室,疑难重症及罕见病国家重点实验室,国家皮肤与免疫疾病临床医学研究中心(费允云)
肝豆状核变性(Wilson’s disease, WD)是一种常染色体隐性遗传性疾病。患者由于ATP7B基因突变引起铜排泄障碍,导致铜在肝脏、中枢神经系统等多种脏器内蓄积[1]。WD患者病程可较隐匿,临床表现中肝脏病变最为常见,此外神经系统、血液系统、肾脏、骨骼、关节以及内分泌系统均可受累[2]。近年来,有研究报道WD可并发系统性红斑狼疮(systematic lupus erythema-tosus,SLE)等自身免疫性疾病[3-4]。然而WD与SLE均可表现为多系统受累,且其临床表现多有重叠,因此误诊和漏诊并不少见[5-7]。另一方面,青霉胺作为治疗WD的一线药物,亦有引起药物性红斑狼疮的报道(drug induced lupus erythematosus,DILE)[8]。现将本院2013年至2020年收治的4例WD并发红斑狼疮病例报告如下,总结其病例特点,并复习国内外文献报道病例,以提高对本病的认识。
1 对象与方法
1.1 研究对象
2013年1月至2020年1月在北京协和医院住院WD患者中,选出并发SLE或DILE的患者。其中WD诊断依赖临床特征及基因检测结果。SLE及DILE的诊断按照2009年SLICC修改的ACR系统性红斑狼疮分类标准[9],且DILE诊断需要既往无SLE病史,存在青霉胺的应用史,停用药物后好转。
1.2 资料收集及分析
收集临床资料,包括一般情况、临床表现、体格检查、实验室检查、炎症指标、自身抗体、治疗方案、疾病转归。
2 结果
2.1 一般情况
2013年1月至2020年1月在北京协和医院住院的WD患者共69例,并发红斑狼疮共4例,占5.8%。其中仅1例为男性,中位就诊年龄18(13,20)岁。应用青霉胺后出现DILE者2例,非药物诱导SLE 2例(表1)。
2.2 临床表现
2例DILE患者分别在开始青霉胺治疗WD后5年和2年出现红斑狼疮表现,在另2例患者WD和SLE同时被发现并诊断。WD的临床表现:3例患者存在肝酶升高,1例患者则表现为肢体震颤、不自主运动等锥体外系症状。4例患者均存在眼科检查证实的K-F环(Kayser-Fleischer rings)。红斑狼疮的临床表现:1例青霉胺相关DILE患者表现为乏力、贫血、镜下血尿、蛋白尿、血肌酐升高,肾脏穿刺活检提示系膜增生性肾小球肾炎,符合狼疮性肾炎表现。另1例青霉胺相关DILE患者表现为发热、关节炎、多浆膜腔积液。1例WD并发SLE患者表现为白细胞下降、镜下血尿、蛋白尿、颅内压升高、脑脊液蛋白升高、口干、眼干;另1例并发SLE患者表现为皮疹、血小板减少。
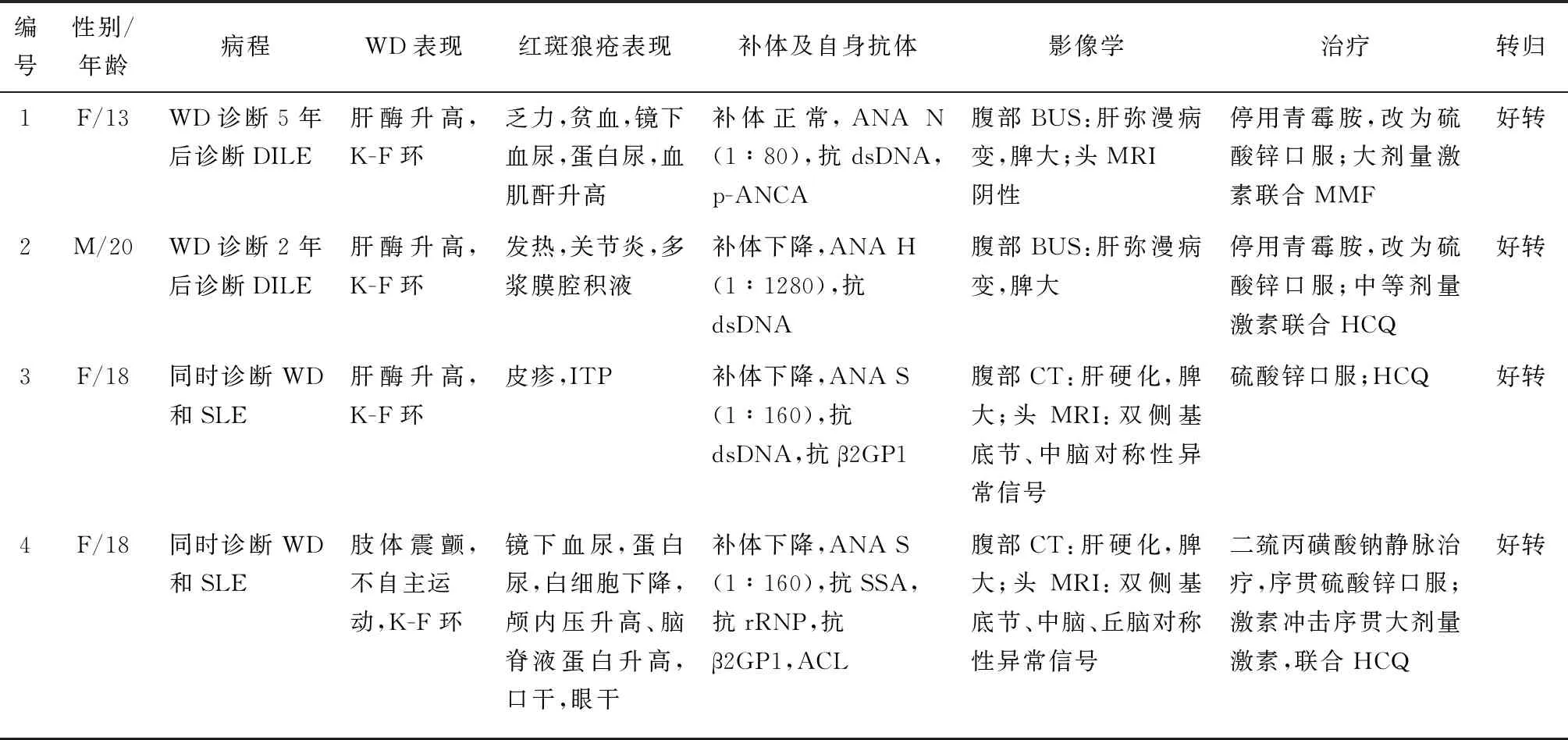
表1 4例WD并发红斑狼疮患者临床表现及治疗随访
2.3 实验室检查及影像学检查
除1例DILE患者外,余3例患者均存在补体下降。自身抗体方面,2例DILE患者均存在抗核抗体(anti-nuclear antibody,ANA)、抗双链DNA(dsDNA)抗体,其中1例DILE患者还存在抗中性粒细胞胞浆抗体(ANCA)。2例SLE患者均存在ANA、抗磷脂抗体谱(antiphospholipid antibody, APLA)。其中1例SLE患者存在抗dsDNA抗体,另1例SLE患者则存在抗SSA抗体、抗核糖体核糖核蛋白(rRNP)抗体。
3例患者腹部超声提示肝弥漫性病变、脾大,其中2例患者腹部电子计算机断层扫描(CT)提示肝硬化。2例患者头核磁共振成像(MRI)提示双侧基底节区、中脑对称性异常信号。
2.4 治疗及结局
2例DILE患者均停用青霉胺,改为口服硫酸锌治疗WD,患者症状可以部分好转但DILE不能完全缓解,遂加用了激素治疗。其中1例加用大剂量激素[泼尼松1 mg/(kg·d)]并逐渐减量,联合霉酚酸酯(MMF),总疗程12个月,随访2年WD病情控制稳定,DILE缓解。另1例加用中等剂量激素[泼尼松0.5 mg/(kg·d)]并逐渐减量,联合羟氯喹,3个月时随访患者病情稳定,此后因家庭因素失访。1例WD并发SLE患者因存在WD中枢神经系统受累,选择二巯丙磺酸钠静脉初始治疗,序贯为硫酸锌口服,并加用甲强龙静脉冲击(1 g/d)序贯大剂量激素[泼尼松1 mg/(kg·d)]联合羟氯喹治疗,患者病情好转,随访6个月时SLE病情复发,表现为血尿、蛋白尿再发,遂将泼尼松由2.5 mg/d加量至20 mg/d,患者病情缓解,随访1年病情稳定。另1例WD并发SLE患者加用口服硫酸锌治疗WD,并加用羟氯喹控制SLE,随访1年病情稳定。
3 讨论
本文总结本院收治的WD并发红斑狼疮病例,包括SLE和DILE。此外,在PubMed数据库中对WD并发SLE或DILE进行了文献检索。其中,共收集7例WD并发SLE报道病例(包括本院2例)。SLE是一种多系统受累的自身免疫性疾病,而WD亦可累及肝、中枢神经系统、血液系统等多个系统和脏器。WD并发SLE较为罕见,近年来国内外陆续有相关的个案报道。有学者发现,WD患者较对照人群IgG和IgM水平升高,而T细胞百分比降低,不除外是游离铜对淋巴细胞的作用,引起WD患者的免疫异常,从而使其更易出现自身免疫性疾病[10]。但相关证据仍较少,WD和SLE之间是否存在相关性尚不能明确。然而,当这两种多系统受累疾病并发时,临床表现可有较多重叠,可能引起误诊、漏诊。而当WD并发SLE时,不推荐应用青霉胺作为WD的初始治疗。因此,对WD并发SLE临床特点进行分析有助于及时、正确而完整地进行诊断,对后续治疗方案的选择意义重大。
对已有文献复习并结合本院2例WD并发SLE病例,发现WD可在SLE之前、之后或同时被诊断。WD肝脏受累可表现为肝酶升高、肝硬化甚至爆发性肝功能衰竭。据文献报道,约50%的SLE患者亦可出现肝损[11],因此,当SLE和WD同时出现时,肝酶升高对诊断与鉴别诊断价值有限。在文献复习中,1例已确诊SLE患者在原发病控制稳定的情况下,新发肝脏损害,最终诊断并发WD[12]。另1例患者尽管SLE控制稳定,但在随访期间转氨酶仍持续高于正常上限2~3倍[13]。因此,当控制稳定的SLE患者出现无法解释的肝损伤时,临床医生需要将其他肝病(如WD)纳入鉴别诊断。神经系统方面,与SLE不同,WD神经系统最常见表现为锥体外系症状(如构音障碍、震颤、肌张力障碍、步态异常和帕金森样症状等)[14-15],核磁共振成像(MRI)在T2加权图像和FLAIR图像上可见双侧基底节区对称性高信号[16]。在本文复习的7例病例中,有2例以锥体外系症状为突出表现(包括构音障碍、震颤和步态异常),MRI均在T2加权图像和FLAIR图像上发现双侧基底节区的高信号[13]。正是这些难以用经典神经精神狼疮解释的临床表现和影像学特征,成为了这2例患者诊断WD的最初线索,而进一步的检验检查证实了WD的诊断。Kayser-Fleischer环(K-F环)是WD患者最常见的眼科表现,其在神经系统受累的WD患者中几乎100%存在,此外,40~50%的肝损患者和20%~30%无症状患者中亦会出现K-F环[17]。在本文复习的7例患者中,2例患者在体格检查时发现K-F环,成为WD诊断的最初线索[4],另2例患者因为不明原因的肝酶异常并发K-F环发现WD[12,18],提示眼科检查对于存在神经系统或肝脏异常的患者具有重要意义。治疗方面,由于青霉胺本身可以诱发药物性红斑狼疮,7例患者中大多数选择非青霉胺作为初始治疗(如硫酸锌、二巯丙磺酸钠)。2例患者最初接受了青霉胺治疗,但由于症状加重改为硫酸锌口服[3,18]。WD并发SLE患者结局总体尚可,仅1例因爆发性肝衰死亡[12]。有研究表明,血浆置换可以快速降低WD患者血清中游离铜的水平,早期应用可为爆发性肝衰患者争取等待肝脏移植的机会[19],进一步提示早期诊断和治疗对于WD患者的重要意义。该例患者明确诊断WD时已进展至肝性脑病阶段,虽然积极加用了血浆置换治疗,仍没有机会完成肝脏移植,最终死亡。
作为治疗WD历史最为悠久的药物,青霉胺目前仍是WD的一线初始治疗药物之一[20]。早在20世纪70年代就有学者发现青霉胺可诱发自身免疫性疾病[21]。具体机制尚不明确,但有研究提示可能与青霉胺引起巨噬细胞和淋巴细胞过度激活相关[22-23]。其中,青霉胺诱导的DILE是一种少见的与剂量无关的药物不良反应,发生率约为1%~3%,用药后2周到20年之间均可能出现[24]。DILE的临床表现多样,轻重不一。与SLE相比,DILE患者皮肤、关节、浆膜腔受累以及乏力等系统性症状更为多见,而肾脏、中枢神经系统、血液系统表现相对少见[8],本院2例DILE均以系统性症状起病,1例存在肾脏受累,另1例则表现为关节炎和浆膜腔积液。自身抗体方面,DILE常见ANA、抗ds-DNA抗体阳性[25],与本院报道2例亦相符。治疗方面,DILE患者在停用青霉胺的同时常需要联用中到大剂量糖皮质激素[泼尼松0.5~1 mg/(kg·d)],也有少数患者单独停用青霉胺后即可出现临床缓解,整体结局尚可[8,25-26]。本院2例DILE均在停用青霉胺后加用糖皮质激素,最终病情得到控制。值得一提的是,有研究提示WD患者开始治疗前ANA(+)者可能更容易出现DILE,且应用青霉胺患者如监测发现ANA滴度较基线升高可能更易出现DILE[24],但后续研究结论并不完全一致[26]。遗憾的是,本院2例患者加用青霉胺治疗前的ANA基线水平已不可考,ANA对于发生DILE的预测价值还需要后续研究进一步证实。因此,对于WD患者在开始治疗前应筛查自身抗体,对加用青霉胺的患者应在治疗过程中监测自身抗体及症状变化,警惕DILE的发生,及早调整治疗。
总之,WD可并发SLE或DILE,临床上较为罕见,对该病的认识相对不足,易误诊、漏诊。当WD并发SLE时,WD可在SLE之前、之后或同时被诊断,控制稳定的SLE患者出现无法解释的肝损伤、锥体外系症状突出、MRI提示T2加权图像和FLAIR图像上双侧基底节区高信号以及体格检查发现K-F环是WD诊断最重要的线索;治疗上应尽量选择非青霉胺类药物,因青霉胺可能会诱发临床症状恶化。青霉胺诱导的DILE可在用药后2周到20年之间出现,与SLE相比,DILE患者皮肤、关节、浆膜腔受累以及乏力等系统性症状更为多见,而肾脏、中枢神经系统、血液系统表现相对少见,多有ANA、抗ds-DNA等自身抗体阳性,治疗上应停用青霉胺,常需要联用糖皮质激素,预后总体较好,而ANA对于发生DILE的预测价值还需要后续研究进一步证实。
