局部外用噻吗洛尔与口服普萘洛尔治疗表浅型婴幼儿血管瘤效果对比的Meta 分析
2021-05-09李兴红李晨曦龚忠诚
李兴红, 李晨曦,2, 凌 彬, 龚忠诚
[1. 新疆医科大学第一附属医院(附属口腔医院)颌面肿瘤外科,新疆维吾尔自治区口腔医学研究所,新疆维吾尔自治区 乌鲁木齐 830054;2. 汉堡大学艾本德附属医院头部及神经中心口腔颌面外科,口腔颌面部肿瘤遗传学及再生医学实验室,德国 汉堡 20246]
婴幼儿血管瘤(infantile hemangiomas,IHs)在新生儿及儿童中的发病率约为4%~5%[1],其致病原因多是由于毛细血管内皮细胞及周围组织增生而引起,好发于头面部、躯干,四肢次之[2]。 根据瘤体累及深度可分为表浅型、深部型及混合型。 婴幼儿血管瘤早期可表现为皮肤充血、血管扩张,呈斑片样;进入增殖期后,血管瘤体积增大,突出于皮肤,呈草莓样瘤体,随后增殖渐缓,部分患儿的血管瘤可在数年后消失[3]。 据不少文献报道,自行消退的血管瘤仍会遗留瘢痕、色素、红斑、纤维增生等,重者可能会损害呼吸功能及影响视力[4]。 因此,对于有临床意义的婴幼儿血管瘤,建议根据其部位、大小、稳定程度给予积极治疗而不是观察。
治疗婴幼儿血管瘤的方法有很多种,主要包括药物及手术治疗,药物中以糖皮质激素及β 受体阻滞剂为主,目前口服普萘洛尔应用最广泛,是公认的一线用药。 口服普萘洛尔能快速减小血管瘤的体积,且具有良好的耐受性,能明显缩短婴幼儿血管瘤的病程,但该药生物利用度不高,半衰期短,易受其他药物影响,而且会引起很多副作用,如心率减慢、血压降低、支气管哮喘、失眠、食欲降低、梦魇、手脚发凉等[5]。 很多研究者在局部应用马来酸噻吗洛尔治疗表浅型婴幼儿血管瘤,也取得了很好的疗效,局部外用药物能减少全身性不良反应。 但此类研究的样本量较小,可信度不高。 本文对关于口服普萘洛尔与局部涂抹噻吗洛尔治疗表浅型婴幼儿血管瘤的研究进行系统综述,并通过Meta 分析,明确局部涂抹噻吗洛尔是否能够取代口服普萘洛尔成为婴幼儿血管瘤治疗的一线药物。
1 资料和方法
1.1 文献检索
在多个中英文主流数据库如:PubMed、Web of Science、Cochrane、Embase、中国知网、万方、维普等,搜索相关文献。 本篇文章的主题词为propranolol,timolol, infantile hemangioma,关键词为β-bloker, infantile hemangioma,propranolol,timolol,treatment。 搜索的文献无语种限制。 中文检索以普萘洛尔、噻吗洛尔、心得安及婴幼儿血管瘤等为主题搜索词。 最后检索日期为2020 年6 月。
1.2 数据提取
①纳入标准:确诊为婴幼儿血管瘤的患者(依据ISSA 诊断标准)。②排除标准:有服用普萘洛尔/噻吗洛尔禁忌证、临床实验进行期间,患儿服用β 受体激动剂、 患儿接受β 受体阻滞剂以外的治疗方法。 ③干预与对照:实验组干预措施为局部应用马来酸噻吗洛尔,对照组为口服普萘洛尔。 ④疗效评估:根据Achauer 标准,评价疗效分为Ⅰ~Ⅳ级。本篇Meta 分析中将Ⅲ级和Ⅳ级定义为有效,Ⅰ级和Ⅱ级为无效。 ⑤全身不良反应:包括心率、血压明显下降,呕吐腹泻、过敏、低血糖等。 ⑥研究类型:选取随机对照试验(randomized controlled trial,RCT)、非随机对照试验、临床观察性研究。 ⑦研究数据必须齐全,缺乏对照组或缺少结局事件或重要数据等的文献均会被排除。 同时满足上述标准的研究方可纳入本次Meta 分析。
1.3 文献筛选
由2 位研究者单独完成文献检索过程,并利用文献管理软件整理文献,逐步进行文献筛选,剔除重复发表研究,并对文献进行一般描述,并提取相关研究数据。 当两位研究者有意见分歧,并不能达成一致时,请第三位研究者判定。
1.4 文献质量评估
RCT 研究使用改良的Jadad 量表进行质量评估。 主要评估随机化、盲法、退出、隐藏等多个方面。 总分共7 分,其中得分小于3 分的文章质量较差。 队列研究采用NOS 评价标准进行质量评估。 主要从选择人群、暴露、可比性、结局等方面进行评价,总分为9 分。 文献质量评鉴过程由3 名研究者采用标准化表格背靠背独立完成。
1.5 数据分析
本研究应用RevMan 5.3 软件进行Meta 分析,评估局部涂抹马来酸噻吗洛尔及口服普萘洛尔用于治疗表浅型婴幼儿血管瘤的有效性及安全性。 效应量选取相对危险度值(risk ratio,RR 值)和95%置信区间。 根据I2及P值进行异质性检验,根据检验结果选取不同的效应模型进行Meta 分析。 发表偏倚的评估通过漏斗图直观进行。
2 结果
共计检索出280 篇相关文献,其中英文83 篇,中文197 篇。 阅读文献的题目及摘要, 初步排除237 篇,仔细阅读全文,最终有8 篇文献[6-13]纳入本次Meta 分析。 检索流程见图1。
2.1 纳入文献的基本特征及文献质量评分结果
所有的研究中,实验组均为局部应用0.5%马来酸噻吗洛尔滴眼液,对照组均为口服普萘洛尔,其中随机对照试验 (RCT)3 项, 临床对照研究(clinical controlled trial,CCT)5 项,共纳入1 860 例患者,其中实验组942 例,对照组741 例,共177 例退出实验。 大多数研究应用马来酸噻吗洛尔滴眼液2 次/d, 应用普萘洛尔1 mg/kg。 最长用药时长48 周,最短时长9 周。 各个研究的基本特征见表1。通读本文所纳入的文献, 对RCT 及CCT 研究进行质量评价(表2、3)。
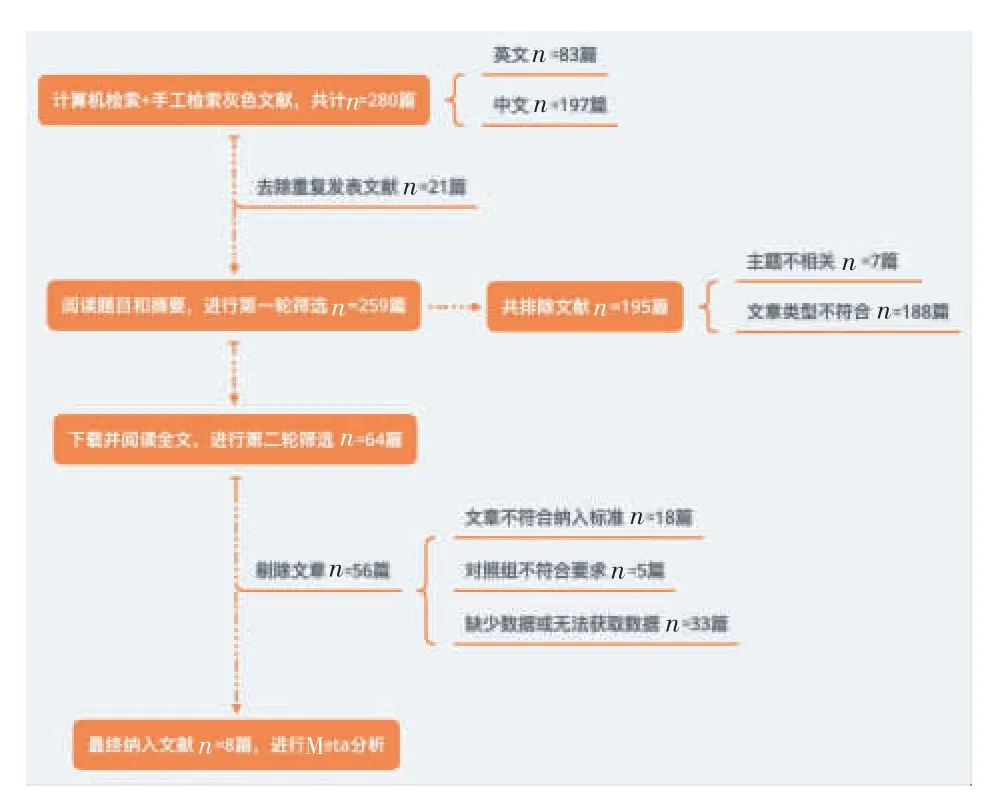
图1 文献筛选流程图Figure 1 The flowchart of literatures screened through the review process

表1 纳入研究的基线特征Table 1 Characteristics of included studies

表2 RCT 研究的改良Jadad 质量评价得分表Table 2 Quality evaluation score table of modified Jadad in RCT studies

表3 CCT 研究的NOS 质量评价表Table 3 NOS quality evaluation form of CCT study
根据RevMan 5.3 软件自带ROB 量表对每篇文章进行风险评估,并对其分出等级(图2、3)。

图2 纳入研究偏倚风险评估Figure 2 Quality assessment and risk of bias in included studies
2.2 Meta 分析结果
2.2.1外用噻吗洛尔与口服普萘洛尔疗效对比 纳入的8 篇研究均提供了相关疗效数据,局部外用噻吗洛尔组共942 例,口服普萘洛尔组741 例。 异质性检验显示8 篇研究之间有轻度异质性 (χ2=16.71,I2=58%,P=0.02), 遂采用随机效应模型对两组对象进行Meta 分析。结果显示,局部外用噻吗洛尔治疗婴幼儿血管瘤疗效优于口服普萘洛尔者[RR=1.15,95%CI(1.01,1.30),P=0.04],差异有统计学意义(图4)。
局部外用噻吗洛尔与口服普萘洛尔疗效对比的漏斗图呈倒漏斗状,表明所纳入的文献无明显发表偏倚(图5)。
根据研究类型对所纳入的研究进行亚组分析,分为RCT 组(3 项研究)和CCT 组(5 项研究)。 在RCT 组中,局部涂抹与口服用药相比,疗效无明显差异[RR=1.16, 95%CI(0.94,1.40),P=0.14];CCT 研究中,局部应用噻吗洛尔治疗婴幼儿血管瘤与口服普萘洛尔效果比较,差异无统计学意义[RR=1.14,95%CI(0.96,1.35),P=0.13](图6)。
2.2.2外用组与口服组全身不良反应的对比 共4 项研究比较了两种方法治疗后的全身不良反应。 异质性检验显示χ2=1.42,I2=0%,P=0.49, 各研究之间无明显异质性,故应用固定效应模型对两组数据进行统计合并。结果提示局部应用0.5%马来酸噻吗洛尔治疗婴幼儿血管瘤时,全身不良反应发生率比口服普萘洛尔组明显降低[RR=0.26,95%CI(0.17,0.40),P<0.000 01],差异有统计学意义(图7)。
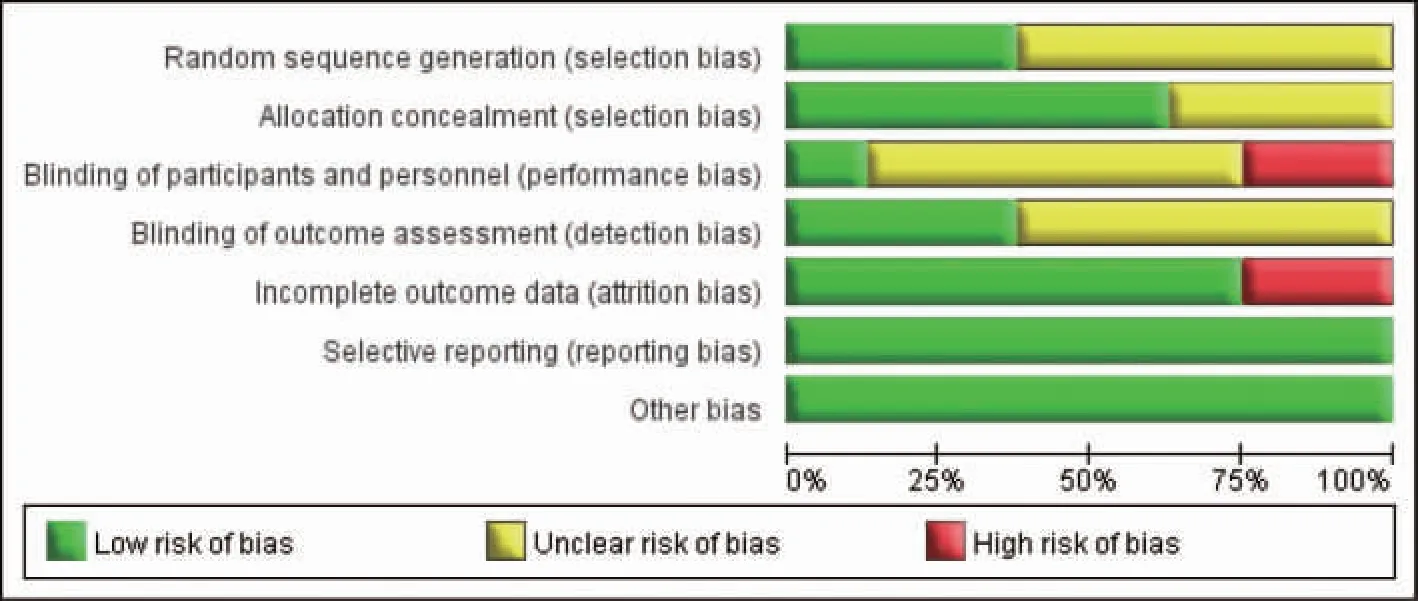
图3 纳入研究产生偏倚风险项目所占百分比Figure 3 The proportion of risk of bias in included studies
3 讨论
本文通过对相关研究进行系统综述及Meta 分析发现,外用0.5%马来酸噻吗洛尔滴眼液治疗表浅型婴幼儿血管瘤的疗效比口服普萘洛尔更好,且全身不良反应更小。
研究显示婴幼儿血管瘤中的血管增生有新生及新发2 种,其起源不同[14]。 Yu 等通过生化技术证实了在血管瘤增生的过程中, 内皮前体细胞(endothelial progenitor cells,EPCS)参与其中。 目前多项研究已证实血管内皮生长因子(vascular endothelialgrowth factor,VEGF)转导通路在血管瘤发展过程中起了重要的作用。 在血管瘤的内皮细胞中,整合蛋白β1 活性下降, 血管内皮生长因子受体(vascular endothelial growth factor receptor,VEGFR)减少,VEGF升高,促进信号转导,加速内皮细胞增殖[15]。此外,婴幼儿血管瘤的发生还与多种遗传因素有关。 正如文献报道所述,在血管瘤组织中发现了编码VEGF 的基因突变、 编码VEGFR2、TEM8 基因错义、Sq 染色体变异等,进一步佐证了这一假说[16-18]。 Hunjan 等[19]对血管瘤婴幼儿进行了一项对照研究发现,胎儿在缺氧的环境中更容易发生血管瘤。 实验室研究中发现,雌激素和缺氧的协同作用能加速血管瘤内皮细胞增殖。
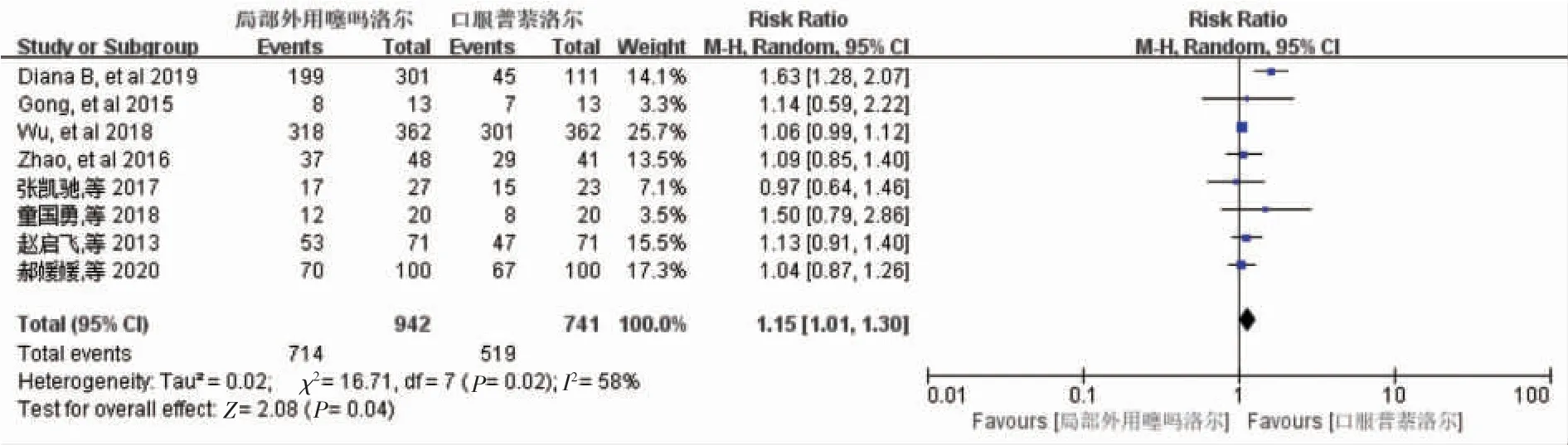
图4 局部外用噻吗洛尔与口服普萘洛尔治疗婴幼儿血管瘤的疗效对比Figure 4 Comparison of the efficacy of topical use of timolol and oral propranolol in the treatment of hemangioma in infants
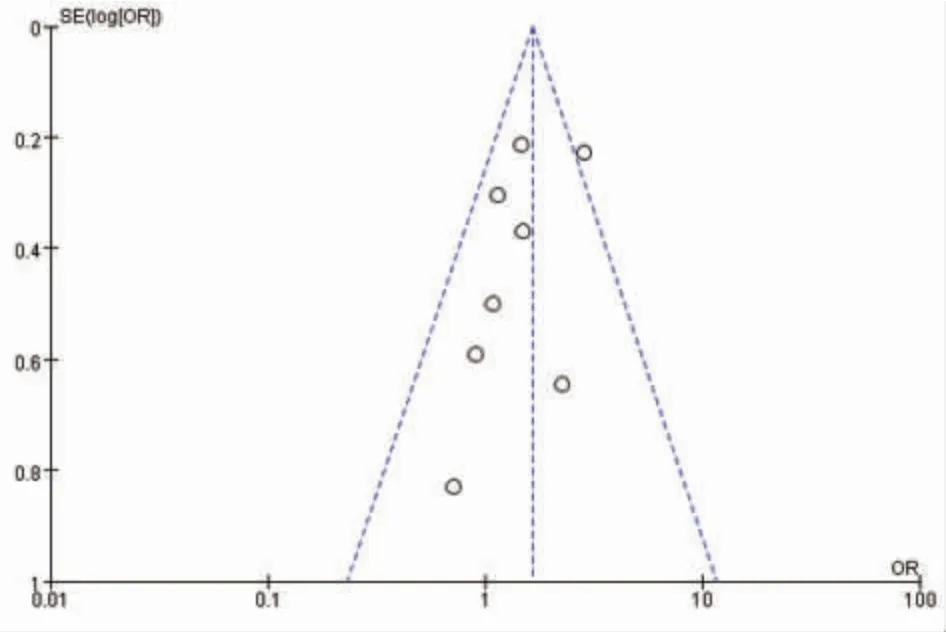
图5 纳入文献的漏斗图Figure 5 Funnel plot of included literatures
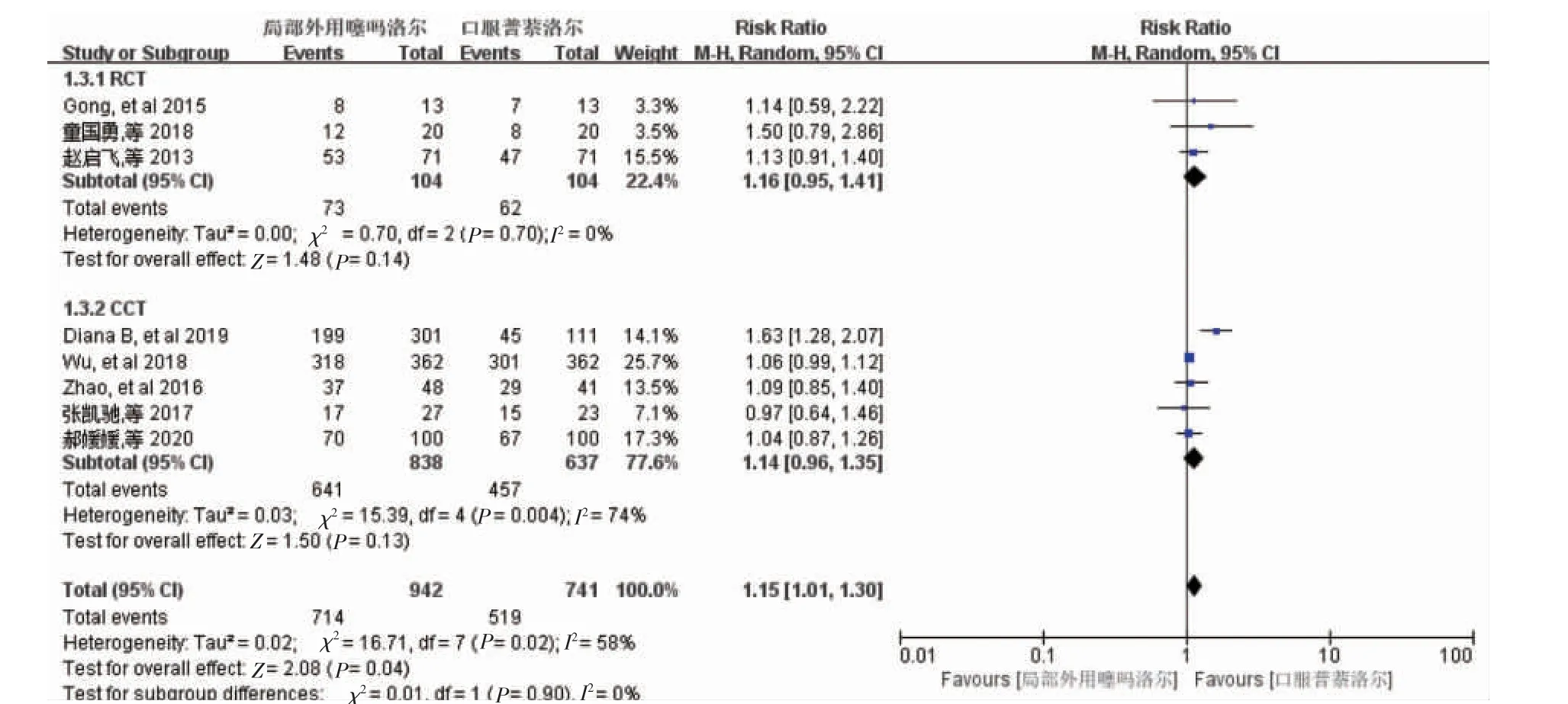
图6 以临床研究类型为分组依据的亚组分析Figure 6 Subgroup analysis based on clinical research type
婴幼儿血管瘤的治疗包括手术治疗、口服药物治疗及局部药物治疗。 对于消退期的婴幼儿血管瘤可采用外科手术切除多余的纤维组织,恢复正常外观。 但病灶的部位、大小及形态不同,手术的时机也有所不同。 且对于增生期血管瘤是否采取手术切除治疗,学术界仍有争议[20]。
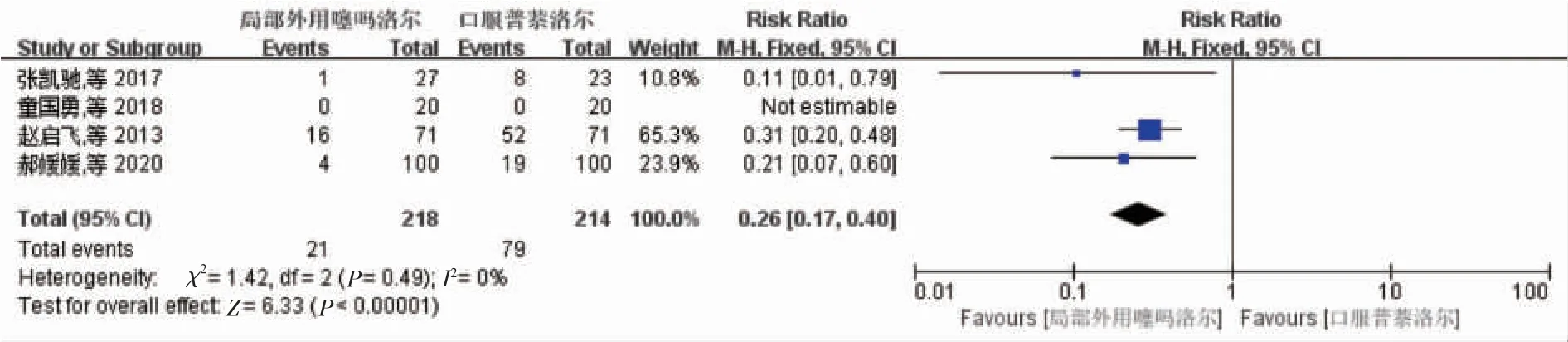
图7 局部应用噻吗洛尔与口服普萘洛尔全身不良反应对比Figure 7 Meta-analysis for the side effects between topical use of timolol and oral propranolol
口服药物包括两大类:β 受体阻滞剂及激素。Meta 分析显示,与口服泼尼松相比,普萘洛尔治疗婴幼儿血管瘤有效率明显较高,且不良反应明显减少[21]。 目前绝大多数口服糖皮质激素已经被口服β受体阻滞剂所取代。 但对于有普萘洛尔禁忌证的患儿,糖皮质激素仍然有一定价值。 鉴于激素的副作用,如Cushing 综合征、影响生长发育、高血压等,其用量、疗程的制订,我们都应对患儿进行个体化治疗[22-24]。 因此,在血管瘤形成的多个时期,多个部位,口服普萘洛尔都有效,这也奠定了其一线药物的基础。 但口服普萘洛尔可能引起患儿四肢发冷、失眠多梦、腹泻等不适,影响生长发育[25]。
局部用药同样包括2 大类:β 受体阻滞剂及糖皮质激素。 多项随机对照研究均发现,局部应用马来酸噻吗洛尔不仅能有效抑制血管瘤增生,还很少引起上述副作用,该药物安全有效[26-27]。 特别在表浅而局限的小血管瘤中,局部外用噻吗洛尔有非常好的效果[28]。 目前,血管瘤局部注射糖皮质激素的治疗方法,在临床中应用得越来越少,已基本被前者替代。
传统的治疗方法如手术, 口服糖皮质激素等,因治疗后遗留瘢痕或药物不良反应等副作用,其临床应用受到很大限制。 婴幼儿口服普萘洛尔可能出现低血压、心率减慢等严重的不良后果,特别是对于面积较小,位置表浅的婴幼儿血管瘤,不适合口服普萘洛尔,传统观点多主张等待,任其自然消退。但对于头面部及敏感部位的表浅型血管瘤,需要进行早期治疗。 多个研究表明,局部应用噻吗洛尔治疗表浅型血管瘤的疗效及安全性比普萘洛尔更好。本篇Meta 分析也支持该观点。
目前关于β 受体阻滞剂治疗婴幼儿血管瘤的Meta 分析,多集中在应用普萘洛尔的治疗,包括口服普萘洛尔和局部应用普萘洛尔,而关于局部外用噻吗洛尔与口服普萘洛尔相比的Meta 分析, 国内外尚未发表相关系统综述及Meta 分析文献。
本篇研究的局限性在于,纳入的RCT 研究较少且大部分研究都来自中国, 可能存在一定的偏倚。还需要更多更高质量的多中心随机对照研究深入探索该领域。
综上所述,本篇Meta 分析显示,局部外用噻吗洛尔治疗浅表型婴幼儿血管瘤,其总体有效率明显高于口服普萘洛尔组,且全身不良反应的发生率明显低于后者。
