早老素-1 p.Met139Ile突变对SH-SY5Y细胞模型相关蛋白与miR-34a表达影响
2021-05-08孙雪纯杨绍楠王源张雅梦潘旭东马爱军
孙雪纯 杨绍楠 王源 张雅梦 潘旭东 马爱军
[摘要]目的探讨早老素-1(PSEN-1)p.Met139Ile突变对早发性阿尔茨海默病(EOAD)人神经母细胞瘤细胞(SH-SY5Y细胞)模型中相关蛋白及microRNA-34a(miR-34a)表达的影响。方法分别将携带有阴性对照空载体的慢病毒(NC组)、野生型PSEN-1的慢病毒(WT组)以及突变型PSEN-1 p.Met139Ile(c.417G>C)的慢病毒(MT组)转染至SH-SY5Y细胞,以未感染慢病毒细胞作为正常组(N组)。ELISA方法检测各组细胞β-淀粉样蛋白表达(Aβ42/Aβ40值),Western blot方法检测各组PSEN-1、淀粉样蛋白前体(APP)、NOTCH-1蛋白的表达,qRT-PCR方法检测各组miR-34a的表达。结果与N组、NC组、WT组比较,MT组Aβ42/Aβ40值、PSEN-1蛋白、APP蛋白及miR-34a表达升高,而NOTCH-1蛋白表达下调,差异有显著性(F=28.540~425.600,q=7.349~30.180,P<0.05),N组、NC组、WT组各指标比较差异无显著性(P>0.05)。结论PSEN-1 p.Met139Ile为致病性突变位点,可引起SH-SY5Y细胞模型中相关蛋白及miR-34a的异常表达。
[关键词]早老素-1;阿尔茨海默病;淀粉样β肽类;微RNAs
[中图分类号]R745.7[文献标志码]A[文章编号]2096-5532(2021)01-0087-04
[ABSTRACT]ObjectiveTo investigate the influence of presenilin-1 (PSEN-1) p.Met139Ile mutation on the expression of related proteins and microRNA-34a (miR-34a) in a model of human neuroblastoma SH-SY5Y cells in early-onset Alzheimers di-sease. MethodsSH-SY5Y cells were transfected with the lentivirus carrying negative control (NC group), the lentivirus carrying wild-type PSEN-1 (WT group), and the lentivirus carrying mutant-type PSEN-1 p.Met139Ile (c.417G>C) (MT group), and the cells not transfected with lentivirus were established as normal group (N group). ELISA was used to measure the expression of amyloid β-proteins (Aβ42/Aβ40 ratio); Western blot was used to measure the protein expression of PSEN-1, amyloid precursor protein (APP), and NOTCH-1; qRT-PCR was used to measure the expression of miR-34a. ResultsCompared with the N, NC, and WT groups, the MT group had significant increases in Aβ42/Aβ40 ratio and expression of PSEN-1, APP, and miR-34a and a significant reduction in the expression of NOTCH-1 (F=28.540-425.600,q=7.349-30.180,P<0.05), while there were no significant differences in these indices between the N, NC, and WT groups (P>0.05). ConclusionPSEN-1 p.Met139Ile is a pathogenic mutation site and can cause abnormal expression of related proteins and miR-34a in the model of SH-SY5Y cells.
[KEY WORDS]presenilin-1; Alzheimer disease; amyloid beta-peptides; microRNAs
早發性阿尔茨海默病(EOAD)常由早老素-1(PSEN-1)、PSEN-2和淀粉样蛋白前体(APP)等基因的突变导致[1],其中PSEN-1突变占70%~80%[2]。PSEN-1作为γ-分泌酶的重要组成部分,其突变会影响APP、NOTCH-1以及β-淀粉样蛋白(Aβ)的表达[1,3]。微小RNA(miRNA)是一类长度约22个核苷酸的内源性非编码小RNA,通过识别靶基因mRNA的3′端非编码区(3′UTR),并与之结合以抑制靶基因的表达[4]。最近研究结果表明,多种miRNA参与调控阿尔茨海默病(AD)的病理过程,miR-101、miR-106靶向APP可促进Aβ产生[5]。 既往我们在一家族性EOAD家系中发现存在PSEN-1 p.Met139Ile(c.417G>C)突变,本研究在体外建立PSEN-1 p.Met139Ile(c.417G>C) 突变人神经母细胞瘤细胞(SH-SY5Y细胞)模型,分别检测其Aβ42/Aβ40、PSEN-1、APP、NOTCH-1及microRNA-34a(miR-34a)的表达,以探讨PSEN-1 p.Met139Ile(c.417G>C)突变对SH-SY5Y细胞模型的影响。现将结果报告如下。
1材料和方法
1.1细胞培养
SH-SY5Y细胞购自上海中乔新舟公司,培养于含体积分数0.44的MEM、体积分数0.44的F12、体积分数0.10的胎牛血清、体积分数0.01的双抗及体积分数0.01的丙酮酸钠培养液中,在37 ℃、含体积分数0.05的CO2细胞培养箱中培养。本实验所用细胞的传代次数均控制在P10~P30之间。
1.2实验分组及处理
将处于对数生长期的SH-SY5Y细胞接种于96孔板,细胞生长汇合度在20%~30%时,随机分为N组(正常细胞组,未感染慢病毒)、NC组(阴性对照组,感染携带有阴性空载体的慢病毒)、WT组(野生型PSEN-1组,感染携带有野生型PSEN-1的慢病毒)、MT组(突变型PSEN-1组,感染携带有突变型PSEN-1 p.Met139Ile(c.417G>C)的慢病毒)。各组分别将相应的慢病毒感染至SH-SY5Y细胞中,同时更换培养液为无血清培养液,培养12 h后更换为常规培养液继续培养。慢病毒感染约96 h后,将细胞继续培养于含3 mg/L嘌呤霉素的培养液中,每3~4 d更换1次含嘌呤霉素的培养液,直至未感染病毒的N组细胞被杀光,将嘌呤霉素浓度减至维持浓度(1 mg/L),继续对感染后的细胞进行筛选和扩增。同时,收集细胞分别进行DNA测序鉴定,并将鉴定结果正常的细胞冻存保种。慢病毒购自上海吉凯基因科技有限公司。
1.3DNA提取和测序
使用细胞基因组DNA提取试剂盒(离心柱型)提取各组细胞基因组的DNA。使用分光光度计测DNA浓度。DNA扩增引物由上海生工生物工程有限公司设计并合成。上游引物:5′-ATACCGAGAC-TGTGGGCCAG-3′,下游引物:5′-ATGAGCCACG-CAGTCCATTC-3′。按照2×Taq Plus Master Mix Ⅱ(Dye Plus)说明书进行PCR扩增。扩增后的产物进行10 g/L琼脂糖凝胶电泳,将DNA扩增产物送至上海生工生物工程有限公司进行基因测序。
1.4检测指标及方法
1.4.1Aβ42/Aβ40表达应用酶联免疫吸附试验(ELISA)方法,按照ELISA试剂盒(Elabscience)说明书进行操作。用酶标仪检测450 nm波长处光密度(OD)值。以浓度为横坐标,OD值为纵坐标,在双对数坐标纸上绘制四参数逻辑函数的标准曲线,计算各组Aβ40和Aβ42的表达。
1.4.2PSEN-1、APP、NOTCH-1蛋白表达采用Western blot方法检测。应用RIPA缓冲液+蛋白酶抑制剂(体积比为100∶1)对各组细胞进行裂解。应用BCA试剂盒测定收集到的蛋白质浓度。蛋白样本与上样缓冲液混合后煮沸变性,然后在不连续的聚丙烯酰胺凝胶(分别为100 g/L的聚丙烯酰胺分离凝胶和50 g/L的聚丙烯酰胺浓缩凝胶)中进行电泳,将凝胶中的蛋白质带转移到PVDF膜上。使用50 g/L的脱脂牛奶在室温下进行封闭,将负载蛋白的PVDF膜分别用原代羊抗兔抗体PSEN-1(1∶1 000)、APP(1∶1 000)、NOTCH-1 (1∶1 000)孵育,用HRP标记的山羊抗兔二抗(1∶5 000) 室温孵育1~2 h。用蛋白凝胶成像仪检测PSEN-1、APP、NOTCH-1蛋白,应用Image J软件计算各蛋白的表达结果。
1.4.3miR-34a表达应用TRIzol方法提取各组细胞总RNA,采用分光光度计测定RNA浓度。应用microRNA专用反转录试剂盒(Mir-XTM miRNA First-Strand Synthesis and SYBRR qRT-PCR User Manual,TAKARA公司)反轉录得到microRNA的cDNA产物。按照TB Green Premix Ex TaqⅡ说明书,应用两步法进行qRT-PCR扩增。以U6基因作为内参对照。以2-ΔΔCt法计算各组miR-34a的表达。
以上所有指标检测均重复3次。
1.5统计学方法
应用SPSS Version 21.0软件进行统计学处理。符合正态分布的计量资料结果以±s表示,两组比较采用t检验;多组比较采用单因素方差分析(ANOVA),两两比较采用q检验。以P<0.05表示差异有统计学意义。
2结果
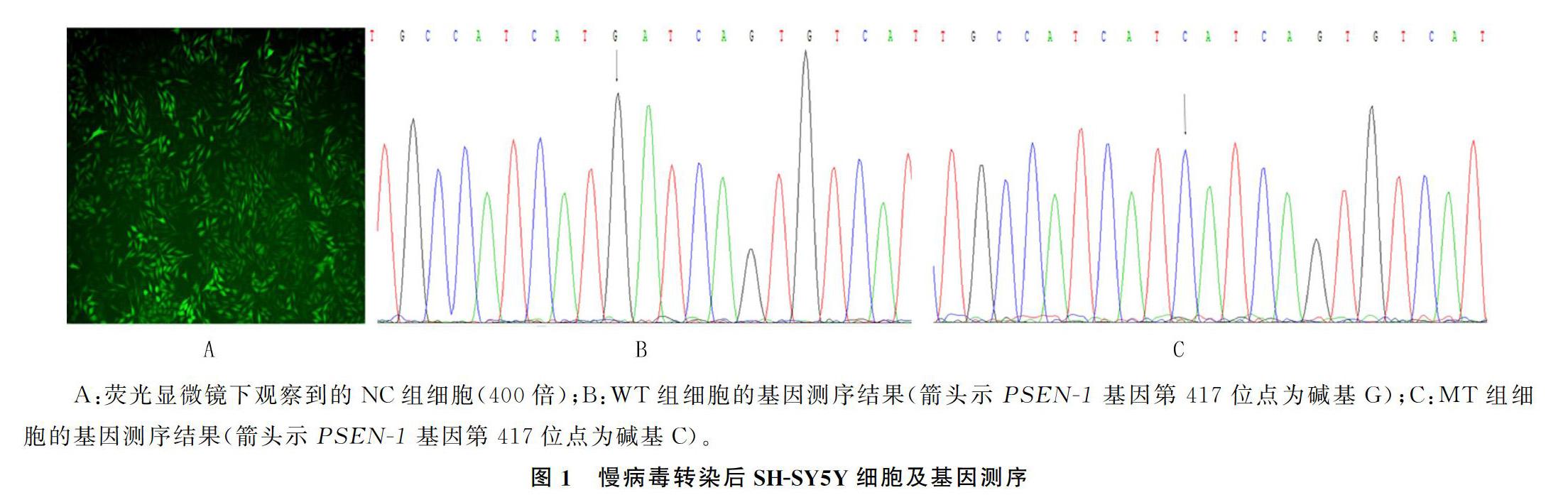
2.1慢病毒转染后SH-SY5Y细胞基因测序
荧光显微镜下观察显示,慢病毒对SH-SY5Y细胞的感染效率在80%以上(图1A)。序列分析显示,WT组细胞在PSEN-1的417位点发生G→C突变,即第5号外显子的139号密码子发生ATG→ATC错义突变(图1B、C)。
2.2各组Aβ42/Aβ40值比较
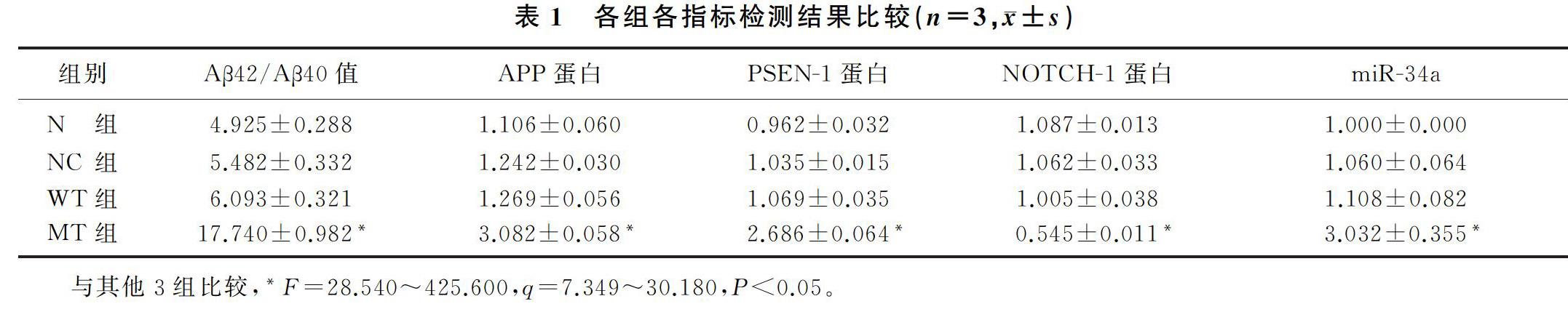
MT组Aβ42/Aβ40值明显高于N组、NC组、WT组,差异有显著意义(F=119.700,q=14.680~16.150,P<0.05)。N组、NC组、WT组Aβ42/Aβ40值比较差异均无显著性(P>0.05)。见表1。
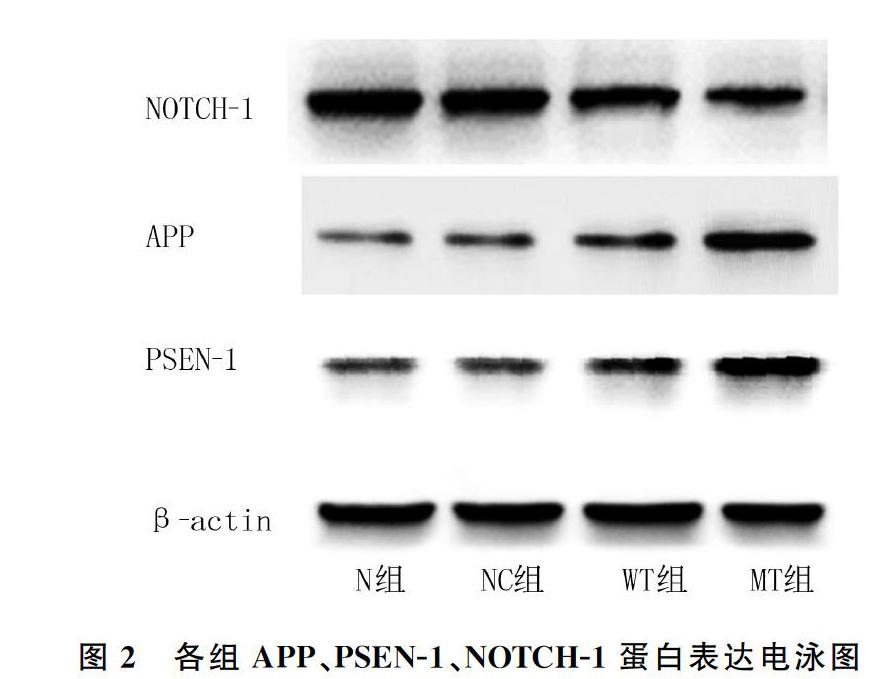
2.3各组PSEN-1、APP、NOTCH-1蛋白表达比较
与N组、NC组和WT组比较,MT组PSEN-1和APP蛋白表达升高,NOTCH-1蛋白表达水平显著降低,差异有显著性(F=90.680~425.600,q=12.120~30.180,P<0.05)。N组、NC组和WT组PSEN-1、APP、NOTCH-1蛋白表达比较差异无显著性(P>0.05)。见图2、表1。
2.4各组miR-34a表达比较
MT组miR-34a表达明显高于N组、NC组和WT组,差异有显著统计学意义(F=28.540,q=7.349~7.762,P<0.05)。N组、NC组和WT组miR-34a比较差异无显著性(P>0.05)。见表1。
目前已有超過200种PSEN-1突变对EOAD来说是致病性的[6],在致病性PSEN-1突变中,大多数为错义突变导致氨基酸的替换。本团队首次发现在PSEN-1的417位点发生G→C突变,致使第5号外显子的139号密码子发生ATG→ATC错义突变,从而导致该密码子编码的氨基酸由蛋氨酸(Met)突变为异亮氨酸(Ile)。本文进一步研究该突变位点的致病功能:首先通过慢病毒感染该突变位点至SH-SY5Y细胞,基因测序验证SH-SY5Y细胞模型构建成功;ELISA方法检测显示AD的特征性指标Aβ42/Aβ40值升高,Western blot方法检测显示APP、PSEN-1蛋白表达升高,这与AD病理变化相符合,进一步验证了体外SH-SY5Y细胞模型构建成功,也证实了PSEN-1 p.Met139Ile (c.417G>C)这一突变位点为致病性突变。
AD的重要病理特征是脑内Aβ沉积形成的老年斑,具体表现为Aβ42/Aβ40的比值增加。Aβ是由APP经γ-分泌酶剪切所产生,γ-分泌酶的主要催化亚基为PSEN-1,研究认为,突变型PSEN-1在切割APP时易形成更多的Aβ42,从而使Aβ42/Aβ40值升高。还有研究发现,γ-分泌酶也参与剪切神经信号传导通路上的重要蛋白,如NOTCH等[7-8]。Notch信号通路中,γ-分泌酶将NOTCH切割后,胞内片段(NICD)转移到核内激活基因的转录,调节神经细胞的生成、分化以及存活。研究结果显示,AD的病因之一可能是γ-分泌酶切割APP释放的APP胞内结构域(AICD)产物抑制了Notch通路[7]。作为γ-分泌酶的重要组成部分,PSEN-1突变可阻断NOTCH-1剪切及核转位,NOTCH-1蛋白减少可能使淀粉样蛋白积聚导致神经细胞易于凋亡,其机制可能与相应微环境支持及神经细胞自身端粒酶活性限制有关。也有研究认为NOTCH-1蛋白下调可能影响海马突触的可塑性,进而导致记忆障碍[8]。本文研究显示,在PSEN-1 p.Met139Ile (c.417G>C)突变的SH-SY5Y细胞模型中Aβ42/Aβ40比值、PSEN-1蛋白、APP蛋白的表达升高,NOTCH-1蛋白表达下降,推测PSEN-1 p.Met139Ile (c.417G>C)突变位点为致病性突变位点,可以造成AD的病理改变,致使Aβ42/Aβ40值增高。已有研究显示,多种miRNAs,如miR-124、miR-107、miR-29等参与AD的病理过程[9]。近期有研究发现,AD病人血浆中miR-34a升高,认为其可以作为AD的生物标志物[10]。本文结果显示miR-34a表达上调,与相关研究结果相符[9-10]。miR-34a表达升高具体机制尚不十分明确,可能是抑制神经元突触可塑性、氧化磷酸化和糖酵解等相关基因所致[11-12]。研究显示,miR-34a通过调节AD双转基因小鼠模型Bcl-2的表达而引起AD细胞凋亡[13];miR-34a通过调控NOTCH-1增加肿瘤细胞凋亡,抑制肿瘤进展[14-15]。然而,miR-34a及NOTCH-1蛋白在EOAD中作用的研究未见报道。后续我们将进一步研究miR-34a与NOTCH-1蛋白在EOAD细胞模型中的作用及其机制,为EOAD的治疗提供依据。
综上,转染PSEN-1 p.Met139Ile (c.417G>C)突变位点可在体外成功构建SH-SY5Y细胞模型,对该细胞模型研究显示Aβ42/Aβ40值、PSEN-1蛋白、APP蛋白、miR-34a表达升高,NOTCH-1蛋白表达下降。认为PSEN-1 p.Met139Ile (c.417G>C)突变位点为EOAD致病性突变位点,miR-34a可能通过与NOTCH-1蛋白作用参与调控EOAD的病理机制。
[参考文献]
[1]WINGO T S, LAH J J, LEVEY A I, et al. Autosomal recessive causes likely in early-onset Alzheimer disease[J]. Archives of Neurology, 2012,69(1):59-64.
[2]SASSI C, GUERREIRO R, GIBBS R, et al. Investigating the role of rare coding variability in Mendelian dementia genes (APP, PSEN1, PSEN2, GRN, MAPT, and PRNP) in late-onset Alzheimers disease[J]. Neurobiology of Aging, 2014,35(12):2881.e1-2881.e6.
[3]LOHMANN E, GUERREIRO R J, ERGINEL-UNALTUNA N, et al. Identification of PSEN1 and PSEN2 gene mutations and variants in Turkish dementia patients[J]. Neurobiology of Aging, 2012,33(8):1850.e17-1850.e27.
[4]PAULI A, RINN J L, SCHIER A F. Non-coding RNAs as regulators of embryogenesis[J]. Nature Reviews Genetics, 2011,12(2):136-149.
[5]SCHONROCK N, GTZ J. Decoding the non-coding RNAs in Alzheimers disease[J]. Cellular and Molecular Life Sciences: CMLS, 2012,69(21):3543-3559.
[6]LANOISELE H M, NICOLAS G, WALLON D, et al. APP, PSEN1, and PSEN2 mutations in early-onset Alzheimer disease: a genetic screening study of familial and sporadic cases[J]. PLoS Medicine, 2017,14(3):e1002270.
[7]RONCARATI R, SESTAN N, SCHEINFELD M H, et al. The Gamma-secretase-generated intracellular domain of beta-amyloid precursor protein binds Numb and inhibits Notch signaling[J]. Proceedings of the National Academy of Sciences of the United States of America, 2002,99(10):7102-7107.
[8]MARATHE S, ALBERI L. Notch in memories: points to remember[J]. Hippocampus, 2015,25(12):1481-1488.
[9]ALEXANDROV P N, DUA P, HILL J M, et al. microRNA (miRNA) speciation in Alzheimers disease (AD) cerebrospinal fluid (CSF) and extracellular fluid (ECF)[J]. International Journal of Biochemistry and Molecular Biology, 2012,3(4):365-373.
[10]JIAN C D, LU M R, ZHANG Z, et al. miR-34a knockout attenuates cognitive deficits in APP/PS1 mice through inhibition of the amyloidogenic processing of APP[J]. Life Sciences, 2017,182:104-111.
[11]COSN-TOMS M, ANTONELL A, LLAD A, et al. Plasma miR-34a-5p and miR-545-3p as early biomarkers of Alzheimers disease: potential and limitations[J]. Molecular Neurobiology, 2017,54(7):5550-5562.
[12]SARKAR S, JUN S, RELLICK S, et al. Expression of microRNA-34a in Alzheimers disease brain targets genes linked to synaptic plasticity,energy metabolism, and resting state network activity[J]. Brain Research, 2016,1646:139-151.
[13]WANG X Y, LIU P, ZHU H, et al. miR-34a, a microRNA up-regulated in a double transgenic mouse model of Alzheimers disease, inhibits bcl2 translation[J]. Brain Research Bulletin, 2009,80(4-5):268-273.
[14]GUESSOUS F, ZHANG Y, KOFMAN A, et al. microRNA-34a is tumor suppressive in brain tumors and glioma stem cells[J]. Cell Cycle (Georgetown, Tex.), 2010,9(6):1031-1036.
[15]WANG X P, ZHOU J, HAN M, et al. MicroRNA-34a regulates liver regeneration and the development of liver cancer in rats by targeting Notch signaling pathway[J]. Oncotarget, 2017,8(8):13264-13276.
(本文編辑 黄建乡)
