腹腔镜下肾盂成形术治疗小儿肾积水的临床分析
2021-05-08耿伟民郝春生刘昆强
耿伟民,郝春生,刘昆强,刘 宁
(1.北京市通州区妇幼保健院小儿外科,北京 101101;2.首都儿科研究所附属儿童医院小儿泌尿外科,北京 100000)
小儿肾积水主要是由于肾盂输尿管连接部梗阻,致使尿液潴留于肾盏、肾盂,致使肾盏、肾盂扩大、肾实质萎缩[1]。该病临床主要表现为反复腰背部疼痛、腹部包块、血尿等症状,给患儿身心健康带来极大影响[2]。目前临床针对小儿肾积水的治疗主要以手术治疗为主,传统肾盂成形术为治疗小儿肾积水的常用术式,可获得一定治疗效果。但长期的临床应用实践发现,传统肾盂成形术后创伤大,术后恢复过程易并发各类并发症,影响患者恢复进程[3]。近年来,腹腔镜技术应用于各类外科手术中取得了较大进展,腹腔镜下肾盂成形术因其术后创伤小而获得不少医师和患者的青睐。但腹腔镜下肾盂成形术操作难度较大,学习曲线长,其在小儿肾积水中的广泛应用尚需大样本量验证[4]。鉴于此,本研究通过回顾性分析笔者所在医院于2015年3月至2019年4月期间收治的经腹腔镜下肾盂成形术或者传统肾盂成形术治疗的小儿肾积水的临床资料,并对比其临床疗效,以期为小儿肾积水的最佳术式选择提供参考。
1 资料与方法
1.1 一般资料及分组
回顾性分析2015年3月至2019年4月北京市通州区妇幼保健院收治的79例肾积水患儿临床资料。纳入标准:①均符合《泌尿外科学》[5]中有关小儿肾积水的相关诊断标准,均经静脉肾盂造影、B超、彩色多普勒超声检查确诊;②均具备肾盂成形术手术指征;③所有手术操作均由同一临床医师完成;④胎儿期经超声检查诊断的肾积水,出生后连续随访检查无改善。排除标准:①既往存在心脑肺等器官严重障碍者;②既往有腹部手术史者;③肾积水再次手术者;④合并免疫缺陷、全身感染者;⑤因其他原因导致的肾积水者。根据治疗方式的不同将纳入患者分为对照组(38例)和观察组(41例)。对照组男18例,女20例,年龄0.9~4岁,平均年龄(2.56±0.34)岁;发病部位:左侧12例,右侧16例,双侧10例。观察组男20例,女21例,年龄0.7~5岁,平均年龄(2.63±0.39)岁;发病部位:左侧14例,右侧18例,双侧9例。两组患儿一般资料比较差异均无统计学意义(P均>0.05),具有可比性。
1.2 方法
两组术前均常规禁饮禁食,术前0.5 h至术后5 d均预防性应用抗生素。全麻,气管插管,麻醉结束后留置Folly气囊导尿管进入膀胱,并暂时夹闭。观察组患儿给予腹腔镜下肾盂成形术治疗:于脐环健侧作长约7 mm切口,置入Trocar(5 mm),建立气腹。随后取患侧上腹部和中下腹各作一切口,置入Trocar,暴露肾脏。依次游离输尿管上端、积水扩张的肾盂,将肾盂沿着弧形剪裁至口呈喇叭状,距离狭窄段远端0.5 cm处去除狭窄段输尿管。随后取输尿管壁近端外侧纵行剪开2 cm,常规吻合后,关闭切口。手术结束后缝合输尿管近端、肾盂,置双J管引流。对照组患儿给予传统肾盂成形术治疗:于腹膜外、腹前部入路,做上腹横切口,内侧起自腹直肌外缘,外侧至腋前线,依次切开皮肤、腹外斜肌腱膜,充分暴露肾盂输尿管连接部及输尿管上段,切断距肾门外2~3 cm处的肾盂环形,并切除狭窄及发育不良的肾盂输尿管连接部,于输尿管狭窄段远端约0.5 cm斜行切断输尿管,随后将输尿管断端纵行劈成袖口状,采用可吸收线缝合肾盂瓣,使其呈喇叭状,常规吻合后,留置腹膜后引流管,关闭切口。术后处理同观察组。
1.3 观察指标
①记录两组围术期指标情况,包括术中出血量、手术时间、住院时间及进食时间;②于术前、术后1 d采用Medison公司的AccuvixV10彩色多普勒超声断层诊断仪检测所有患者肾血流动力学指标,包括血流收缩期峰值流速(PS)、阻力指数(RI)、平均速度(TAMx)、舒张期峰值速度(ED)、最低速度(TAMn);③记录两组术后并发症发生情况;④于术前、术后1 d抽取患儿清晨空腹静脉血5 mL,以离心半径9 cm,经3600 r·min-1离心12 min,分离上清液,置于-50℃冰箱中待测。采用肌氨酸氧化酶法检测血清肌酐(Scr)含量,采用放射免疫法检测血清α1-微球蛋白(α1-MG)、β2-微球蛋白(β2-MG)水平。
1.4 统计学方法
采用SPSS 25.0统计学软件对数据进行分析。计数资料以率(%)表示,采用χ2检验。计量资料以均数±标准差(±s)表示,组间比较采用t检验,组内比较采用配对t检验。检验水准α=0.05。
2 结果
2.1 两组患者围术期指标比较
观察组手术时间、进食时间、住院时间均短于对照组(P均<0.01),术中出血量少于对照组(P<0.01),见表1。
2.2 肾血流动力学指标比较
两组术前PS、TAMx、RI、ED、TAMn比较差异均无统计学意义(P均>0.05);两组术后1 d PS、TAMx、ED、TAMn均升高,且观察组高于对照组(P均<0.05);两组术前、术后1 d以及组间RI比较差异均无统计学意义(P均>0.05),见表2。
2.3 两组相关血清学指标比较
两组术前Scr、β2-MG、α1-MG比较差异无统计学意义(P>0.05);两组术后1 dβ2-MG、α1-MG均降低,且观察组低于对照组(P<0.05);两组术前、术后1 d以及组间Scr比较差异无统计学意义(P>0.05),见表3。
2.4 术后并发症发生率比较
观察组术后发生3例尿路感染、2例吻合口尿漏、1例吻合口梗阻、1例肠梗阻,术后并发症发生率为17.07%(7/41);对照组术后发生3例吻合口尿漏、2例尿路感染、1例肠梗阻、1例吻合口梗阻,术后并发症发生率为18.42%(7/38);两组患儿术后并发症发生率比较差异无统计学意义(χ2=0.025,P=0.875)。
表1 两组患者围术期指标比较(±s)
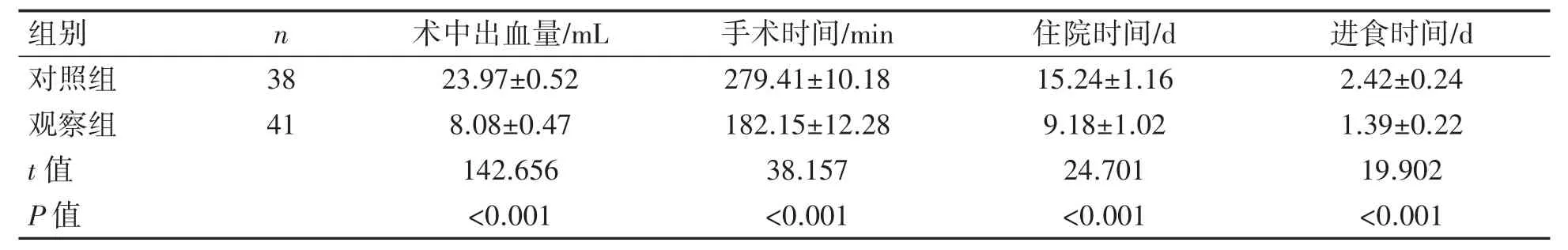
表1 两组患者围术期指标比较(±s)
?
表2 两组肾血流动力学指标比较(±s)
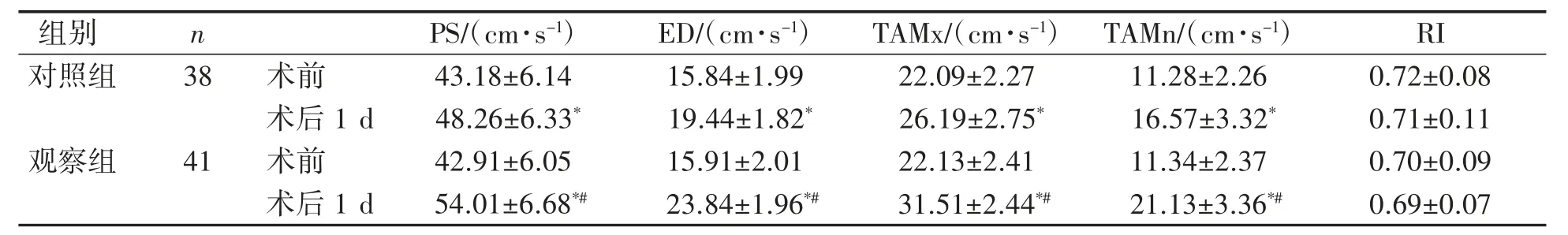
表2 两组肾血流动力学指标比较(±s)
与术前比较*P<0.05;与对照组术后1 d比较#P<0.05。
?
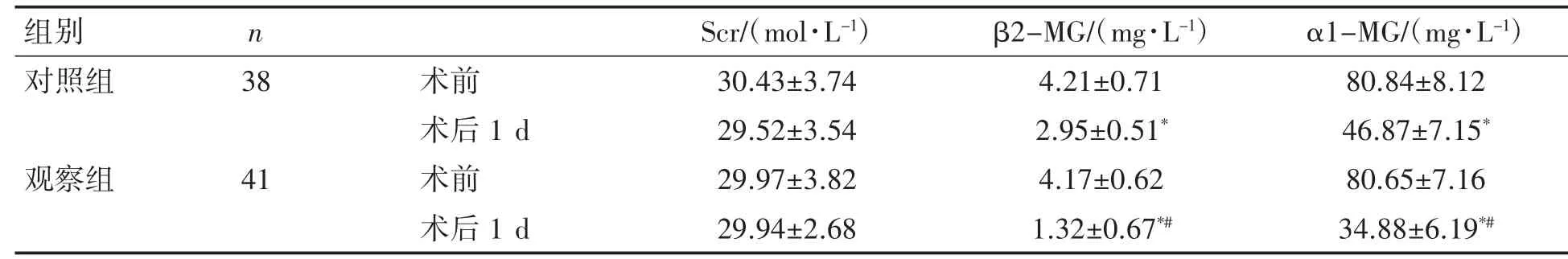
?
3 讨论
小儿肾积水是泌尿系统常见疾病,早期无特异性症状,当出现泌尿系感染、腹痛及肉眼血尿等相应的症状时,已达到严重的不可逆转的损害[6]。随着肾积水病情进展,肾功能受损严重,肾脏无法代偿,肾小管内压力升高,肾小管浓缩及重吸收功能降低,极易发生肾衰竭影响患儿健康[7]。手术是治疗小儿肾积水的主要方法,传统肾盂成形术可去除病变的肾盂输尿管连接部,实现黏膜对黏膜的吻合,缩小扩张的肾盂,疗效确切且持久,手术成功率高[8]。然而该术式创伤大,可增加切口感染等并发症发生风险。腹腔镜下肾盂成形术是对经脐单孔肾盂成形术的一种改进,随着腹腔镜技术的发展,该术式已经是小儿肾积水治疗的主要术式之一,但腹腔镜下肾盂成形术对腔镜下的缝合技术要求高,术者的学习曲线相对较长[9]。
本研究中观察组手术时间、进食时间、住院时间短于对照组,术中出血量少于对照组,可见相较于传统肾盂成形术相比,腹腔镜下肾盂成形术可获得较好的治疗效果,且不增加机体损伤,这可能与施术者技术熟练程度的提高及医疗设备的改进有关。既往研究[10]结果显示,彩色多普勒超声断层诊断仪检测的肾血流动力学指标与肾积水病情严重程度有关。正常情况下,肾脏各级血管的血流呈低阻力型频谱,但在病理情况下,肾血管阻力升高,可导致肾血流波动。Scr是反映肾功能的常用指标,但该指标在肾功能严重损害时才有所升高,肾脏早期变化并不十分明显,且极易受多种肾内外因素影响[11]。β2-MG是一类小分子球蛋白,主要由淋巴细胞、血小板、多形核白细胞产生,其在人体的合成及释放量相对稳定,99.9%可在近端肾小管处被吸收,当肾小球滤过功能受损时,可导致血清中β2-MG急剧升高[12]。α1-MG主要由淋巴细胞和肝脏合成,其在人体中主要有两种形式:一种是与免疫球蛋白A结合的形式,此类存在形式的α1-MG不易被肾小球滤过;另一种是游离型,游离型几乎可被肾小管重吸收、代谢[13]。以上三种指标均可有效反映人体肾脏功能。本研究中腹腔镜下肾盂成形术治疗者的上述指标改善情况均优于传统肾盂成形术者,可见腹腔镜下肾盂成形术可有效减轻小儿肾积水的肾脏进一步受损。这可能是因为腹腔镜下肾盂成形术经腹腔途径手术空间大,标记清晰,腹膜反光性强,视野清晰,可彻底切除病变组织,且由于腹腔镜对手术操作具有放大效果,可有效提高吻合口的缝合质量,进一步保护机体肾脏功能。两组患儿术后并发症发生率对比差异无统计学意义,可见腹腔镜下肾盂成形术安全性较好,以往研究[14]认为传统肾盂成形术创伤大,并发症也相对较高,这与本研究中结果存在一定差异。可能是样本量过小,且个体之间存在差异化所致。后续将扩大样本量、严格控制筛选标准以进行深入的研究分析。
综上所述,腹腔镜下肾盂成形术治疗小儿肾积水,可获得与传统肾盂成形术治疗相当的效果,且腹腔镜下肾盂成形术可有效改善肾血流动力学及血清β2-MG、α1-MG水平,具有一定的临床应用价值。
