高分辨率MRI 动态增强扫描在直肠癌术前TN分期及手术方式选取中的应用
2021-05-06刘金玲林吉征苏晓曲雪廷张亮
刘金玲,林吉征,苏晓,曲雪廷,张亮*
作者单位:1.青岛大学附属医院放射科,青岛266003;2.青岛市市立医院放射科,青岛266003
直肠癌是最常见的消化道恶性肿瘤之一,发生于距肛缘15 cm 以内的直肠,发病率为40/10 万,随着人们生活条件的改善,直肠癌的发病率也在逐年升高[1-4]。直肠癌患者的预后取决于诊断时疾病的分期,因此,准确的疾病分期评估是正确治疗直肠癌的必要条件[5-8]。直肠癌的手术治疗方式有很多种[9],肿瘤的位置、对周围系膜及器官的侵犯程度及淋巴结转移情况都会影响手术方式的选择,对患者预后和生存质量影响最大的就是能不能行保肛手术。高分辨率MRI动态增强扫描层厚薄,对于肿瘤范围及肠壁各层的显示更为清晰,若肿瘤穿透固有肌层,增强后呈不连续点线样强化,提示肿瘤进入T3期,进一步提高了T 分期的准确性[10]。直肠高分辨率MRI 检查对淋巴结转移的评估主要依靠淋巴结大小、形态、信号强度、强化信号来判断,然而淋巴结转移准确度仍然较低[11],笔者搜集本院经肠镜病理确诊的直肠癌患者行高分辨率MRI动态增强检查,探讨其对直肠癌术前TN分期及手术方式选取的价值。
1 材料与方法
1.1 一般资料
收集2018 年11 月至2019 年11 月经肠镜病理确诊并于本院行手术治疗的直肠癌患者154例,其中男性97 例,女性57 例,年龄43~83 岁,中位年龄为64 岁。所有患者均于术前1 周内行高分辨率MRI 增强扫描,无手术禁忌证且术前未进行任何放化疗。
1.2 磁共振检查方法
采用GE Signa HDx 3.0 T MR扫描仪,多通道相控阵线圈。患者均采取仰卧位、头先进的扫描体位。采用LAVA 多期动态增强扫描技术,先行LAVA Mask(蒙片)扫描,然后注射对比剂0.1 mmol/kg 钆喷酸葡胺,利用高压注射器经左肘正中静脉团注入体内30 s、70 s和240 s行动脉期、静脉期及平衡期扫描,采用横轴位、矢状位、冠状位三方位成像,扫描参数:FSPGR,TR 3~8 ms,TE 1~7 ms,层间距1.5 mm,层厚3 mm,矩阵256×256,FOV 26 cm×26 cm。
1.3 图像分析
由2 名具有5 年以上腹部MR 诊断经验的医师分别行影像分析,如有分歧协商达成一致。现直肠癌评估方法多用DISTANCE 评估法[12-13]。肿瘤下缘距离肛缘的距离DIS (distance from the Inferior part of the tumor to the transitional Skin):测量肿瘤下缘距离肛缘的距离,测量肿瘤上下缘的距离,根据肿瘤下缘距肛缘的距离分为高位(>10 cm)、中位(5~10 cm)和低位(<5 cm)。T 分期(T stage,T):肿瘤侵犯深度,T0:无原发肿瘤证据;T1:肿瘤侵犯黏膜下层但未侵犯肌层;T2:肿瘤侵犯肌层但未突破浆膜;T3:肿瘤突破浆膜层侵犯至直肠系膜脂肪;T4:肿瘤侵犯周围器官及结构(T4a:肿瘤侵犯腹膜反折;T4b:肿瘤侵犯其他器官及结构)。肛门复合体(and complex,A)。N 分期(N stage,N):可疑淋巴结评估标准:短径≥5 mm、形态不规整、信号不均匀,符合以上任意一条即为可疑。N0:无淋巴结转移;N1:1~3个可疑淋巴结;N2期,≥4个可疑淋巴结;环周切缘CRM(circumferential resection margin,C)。 周 围 血 管 侵 犯EMVI (extramural vascular invasion,E):可疑征象有:血管信号与肿瘤信号相似,血管局部膨大,肿瘤穿过并超出血管壁。对比高分辨率MRI 分期与术后病理分期,计算MRI 分期的诊断效能。
1.4 术前手术方式拟定
本院直肠癌主要采用的手术方式有四种:经腹会阴联合切除术(abdominoperineal resection,APR)、低位直肠前切除术(low anterior resection,LAR)、经腹直肠癌切除+近端造口+远端封闭(hartmann 术)、姑息术。外科医生根据患者MR 动态增强检查DISTANCE 评价标准术前拟定手术方式,低位直肠癌中,T3N0 期直肠癌行LAR 术式,T3N1、T3N2 期及T4 期的肿瘤行APR 术式;若肿瘤导致肠梗阻及肿瘤侵犯周围组织行Hartmann 术式;对于发生远处转移的直肠癌行姑息术。中高位直肠癌未发生转移、未侵犯直肠系膜筋膜行LAR,若侵犯系膜筋膜行临时造口后还纳。
1.5 统计学分析
采用SPSS 21.0 对数据进行统计分析。分类计数资料均采用例数(百分比)表示,拟行手术和实际手术情况比较采用配对χ2检验。采用Kappa 一致性检验对两种情况的一致性进行分析。Kappa<0.2,表示两者一致性较差;0.2≤Kappa<0.4,表示两者一致性一般;0.4≤Kappa<0.6,表示两者一致性中等;0.6≤Kappa<0.8,表示两 者一致 性 较强;0.8≤Kappa≤1,表示两者一致性很强。检验水准均为P<0.05有统计学意义。
2 结果
2.1 病理诊断
本组病例病理诊断无T1 期患者,T2 期31 例,T3 期122 例,T4 期1 例,MRI 正确诊断分期135 例,错误诊断19 例,其中将T2 期报告为T3 期14 例,T3 期报告为T4 期1 例,T3 期报告为T2 期4 例,MRI 对于T 分期的准确性为87.7%,对T2 期报告的准确性为88.3%,对T3期报告的准确性为85.7%,对T4期报告的准确性为99.4%(表1,2)。采用高分辨率MRI 动态增强扫描对患者进行T分期的敏感度、特异度、阳性预测值、阴性预测值见表1,T分期与病理结果符合率为87.7%(表2)。本组病例中,有112 例进行弹力纤维染色、免疫组化D2-40 及CD31 检测观察血管受侵及脉管瘤栓情况,术前MRI 动态增强检查有72 例与术后病理诊断相符,符合率为65.2%。
病理诊断N0期76例,N1期49例,N2期29例,MRI正确诊断分期60 例,错误诊断94 例,其中将N0 诊断为N1 期12 例,将N0 诊断为N2 期42 例,将N1 期诊断为N0 期1 例,将N1 期诊断为N2 期36 例,将N2 期诊断为N0 期1 例,将N2 期诊断为N1 期1 例,MRI 对于N 分期的准确率为38.9%,对N0 期报告的准确率为28.9%,对N1期报告的准确率为24.5%,对N2期报告的准确率为93.1%(表3,4);采用高分辨率MRI 动态增强扫描对患者进行N分期的敏感度、特异度、阳性预测值、阴性预测值见表3,N分期诊断符合率为38.9%(表4;图1,2)。

表1 MRI对直肠癌T分期的诊断效能Table 1 Diagnostic efficacy of MRI in T staging of rectal cancer
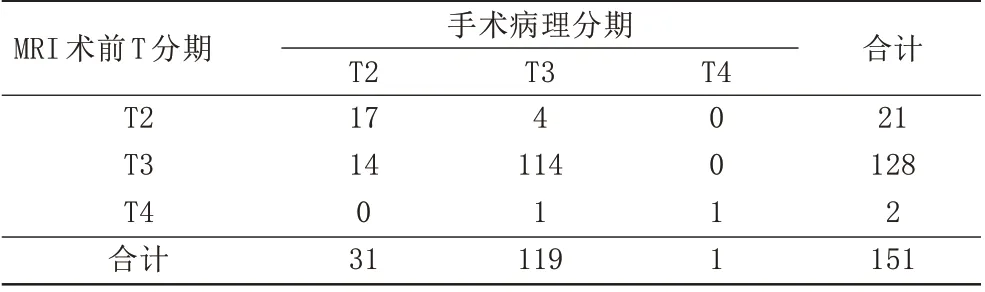
表2 MRI术前T分期与手术病理分期对比(例)Tab.2 Comparison of preoperative T staging and surgical pathological staging on MRI(n)
2.2 手术方式
154例直肠癌患者实际手术方式见表5。中高位直肠癌患者117 例,术前拟行APR 术105 例,姑息术1 例(因远处转移),拟行Hartmann 术11 例(因肿瘤侵犯周围组织并导致肠梗阻),其中2例术前拟行LAR术患者术中发现肿块距肛缘过近难以切除,术中改行APR 术。中高位直肠癌拟定手术方式与实际手术方式的符合率为98.2%(115/117),手术方式一致性检验Kappa 值为0.915,说明拟定术式与实际术式一致性很强。低位直肠癌患者37 例,术前拟行APR 术27 例,拟行LAR 术9 例,拟行Hartmann 术1 例(肿瘤侵犯周围组织并导致肠梗阻),其中3例拟行APR患者术中根据病灶与齿状线距离较近而改行LAR,2 例拟行LAR 患者术中发现肿瘤切除后肛直肠环不完整术中改行APR。低位直肠癌拟定手术方式与实际手术方式符合率为86.5%(32/37),差异无统计学意义(χ2=0.000,P=1.000)。手术方式一致性检验Kappa 值为0.643,说明拟定术式与实际术式一致性较强。154 例直肠癌患者术前拟定手术方式与实际采取术式见表6,符合率为95.5%(147/154),拟定术式与实际术式各手术方式所占比例经配对χ2检验,差异无统计学意义(χ2=0.500,P=0.480),总体手术术式一致性经Kappa 值为0.873,说明拟定术式与实际术式一致性很强。
3 讨论
直肠癌早期通常无典型临床表现,患者就诊时大多已发展至中晚期,严重威胁了患者的生命健康[14]。不同分期的直肠癌患者治疗方式和预后差别较大,手术方式也存在较大差别,严重影响患者的生存时间和生存质量,因此直肠癌的术前诊断及分期非常重要。近年来,健康查体的普及使T1 和T2 期直肠癌的检出率有所提高,早期直肠癌患者预后相对较好。早期局限于黏膜下层的肿瘤(T1 期)可以局部切除,而晚期直肠癌可以通过术前新辅助放化疗方案来实现降期。因此,准确的分期在选择患者进行新辅助治疗评估试验中至关重要,为临床制定治疗方案提供了依据,对临床治疗具有重要的指导意义。直肠癌术前分期的评估方法有很多种,以往使用指诊、肠镜等,指诊多会受检查者主观因素影响,且中高位直肠癌病灶难以触及;肠镜仅能观察肿瘤的表面情况无法窥及肿瘤对周围组织侵犯程度;超声内镜成像可以观察肿瘤对周围组织的侵犯程度,但是如果肿瘤体积过大,肠腔过窄,内镜难以通过,就会造成很大的局限性;常规MR层厚较厚,对肠壁分层分辨率不高,对病灶周围侵犯深度及程度无法准确判断。

表3 MRI对直肠癌N分期的诊断效能Tab.3 Diagnostic efficacy of MRI in N staging of rectal cancer
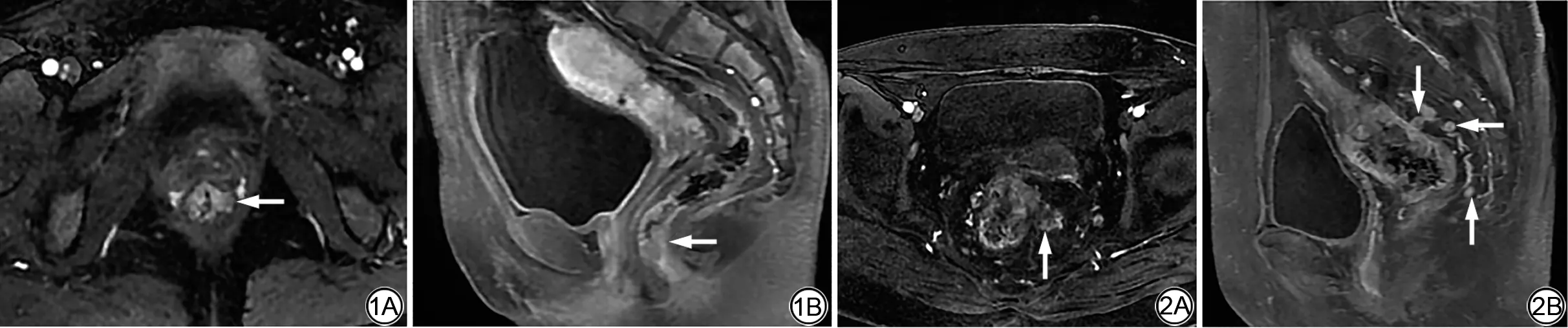
图1 女,48岁,低位直肠癌,术前MRI诊断为T3期,病理诊断为T2期。图A、B为增强扫描,显示肿瘤明显强化,部分侵犯肌层(箭),周围脂肪间隙清晰 图2 女,58岁,中位直肠癌,术前MRI及病理均诊断为T3期。图A横轴位增强扫描显示肿瘤明显不均匀强化,直肠系膜见多发血管影(箭),图B矢状位增强扫描显示系膜多发明显强化肿大淋巴结(箭)Fig.1 Female,48 years old,low rectal cancer,preoperative MRI diagnosis was T3,pathological diagnosis was T2.A and B showed that the tumor was significant‐ly enhanced, part of it invaded the muscular layer (arrow), and the fat space around it was clear. Fig.2 A 58-year-old woman with median rectal cancer was diag‐nosed as stage T3 on preoperative MRI and pathology.A contrast-enhanced scan on the horizontal axis showed obvious heterogeneous enhancement of the tumor,multiple vascular shadows were seen in the mesentery (arrow), and B sagittalcontrast-enhanced scan showed multiple significantly enhanced enlarged lymph nodes in the mesentery(arrows).

表4 MRI术前N分期与手术病理分期对比(例)Tab.4 Comparison of N staging and operative pathological staging before MRI(n)

表5 直肠癌手术方式(例)Tab.5 Surgical methods for rectal cancer(n)
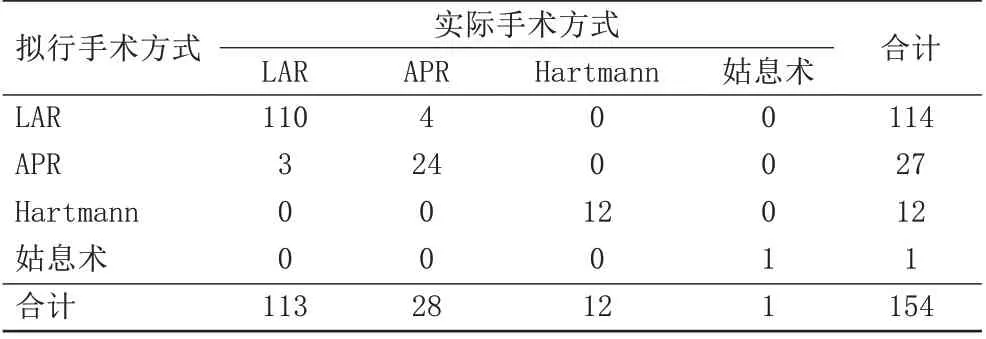
表6 直肠癌拟定术式与实际术式结果对照(例)Tab.6 Comparison of the results of the proposed operation and the actual operation for rectal cancer(n)
高场强(3.0 T)的磁共振扫描仪有较高的信号强度和较大的信噪比[3],最显著的好处是缩短了获取图像所需的时间。高分辨率MRI 检查是层厚较薄,FOV较小且适用范围广泛的一种操作方法,它具有较好的软组织分辨率,安全无损伤,具有较高的可重复性[15-16]。高场强MRI 有较高的空间和时间分辨率[17-18],直肠高分辨率MRI 扫描会提高进展期和局限于直肠壁的浅表直肠癌的诊断准确性。高分辨率MRI 平扫对肠壁各层显示清晰,提高了肿瘤术前T 分期的准确度,但是对于部分临界性的肿瘤术前T分期不好区分,由于高分辨率MRI 动态增强扫描层厚薄,对于肿瘤范围及肠壁各层的显示更为清晰,若肿瘤穿透固有肌层,增强后呈不连续点线样强化,提示肿瘤进入T3 期,进一步提高了T 分期的准确性[10]。高分辨率MRI 动态增强扫描能更准确地反映肿瘤的血流动力学改变,对评估肿瘤侵犯邻近直肠肌层、周围血管及组织器官的程度有较高的价值[19],从而提高了T 分期的准确性。本组病例T2 分期的敏感度为54.8%,特异度为96.7%,T3 分期的敏感度为93.4%,特异度为81.8%,T4分期的敏感度为100%,特异度为99.3%,由此可见,高分辨率MRI 动态增强扫描对术前T分期有很高的准确度,可以为临床治疗方案的选择起到很好的指导作用,从而改善患者的预后情况。MRI 动态增强扫描还可以评估组织微循环情况[20],判断病灶的血供情况及肌层外血管侵犯的情况[21-22],病灶血供情况是评价肿瘤恶性程度的重要指标。本组病例中,112 例直肠癌患者术后病理进行弹力纤维染色、免疫组化D2-40 及CD31 检测观察肌层外血管受侵及脉管瘤栓情况,术前MRI动态增强扫描与病理结果符合率为65.2%,肌层外血管侵犯与否对于评估患者预后有较高价值[18],直肠高分辨率MRI 动态增强扫描对评价肿瘤血供和周围血管侵犯具有较高价值。
本组病例评估淋巴结转移,主要依据淋巴结大小和强化信号是否均匀来判断,其N 分期符合率较低。本组病例对N2 期淋巴结转移诊断准确度较高,N0 期和N1 期淋巴结转移准确度较低。N0、N1 期特异度较高,敏感度较低,原因可能是忽略了部分有转移的小淋巴结;N2 期敏感度高,特异度低,原因可能是把部分正常淋巴结误诊为有转移的淋巴结。笔者考虑MRI 动态增强扫描无法分辨部分反应性增生淋巴结与转移性淋巴结,部分小的淋巴结可能为转移,部分正常大小淋巴结也可能有微小转移[11]。现多结合淋巴结大小、边缘、形态、信号强度、强化形式等多方面考虑,对提高N分期的准确率有较大的价值[15]。
根据DISTANCE评价标准得到的拟定手术方式和实际手术方式的符合率为95.5%,说明对高分辨率MRI 动态增强扫描对于手术方式的选择有很好的指导意义。患者实际住院时拟定的手术方式是综合考虑肠镜、内镜超声、全身其他影像检查评估有无转移、基础性疾病、麻醉风险等制定的,与本研究拟定的术前手术方式不完全相同,本研究旨在探讨MR 增强检查对手术方式的价值,因此,在制定术前手术方式时仅参考MR 增强检查来拟定手术方式。LAR 术式保留肛门括约肌的功能,保证了患者术后较高的生活质量;APR 术式是经典的直肠癌根治术式,由于切除范围较广,严重地影响了患者的生活质量;Hartmann 术式适用于全身情况较差不能耐受或急性肠梗阻的患者。本组病例中高位直肠癌患者,由于距离肛门较远,多采取保肛术,本组病例的拟定手术方式与实际手术方式的符合率为98.2%;对于低位直肠癌患者,本组病例拟定手术方式和实际手术方式符合率为86.5%,10 例(27.0%)低位直肠癌患者经评估后行LAR 术,自TME(直肠全系膜切除术)提出后,可以有效地降低肿瘤的局部复发率,低位直肠癌采用保肛术是具有可行性的,从而可以很大程度地提高患者以后的生存和生活质量[15]。高分辨率MRI动态增强扫描根据DISTANCE评价标准可以为直肠癌患者手术方式的选择提供依据,为患者制定更为合适的治疗方案,对患者预后有很高价值,在术前TN分期的评估、预后的判断方面具有十分重要的意义。
这项回顾性研究有一定的局限性。首先,纳入标准可能会导致选择偏倚,因为术前未做MRI检查的患者被排除在外。第二,本组患者病例数相对较少,低位直肠癌患者较少,T1期及T4期患者过少,有待于加大样本量进一步研究。第三,评估指标中环周切缘CRM 主要观察系膜筋膜是否受侵犯,但MR 增强扫描为T1脂肪抑制序列,系膜筋膜显示不佳,有待于结合MR平扫和增强进一步研究。
作者利益冲突声明:全体作者均声明无利益冲突。
