急性创伤性脑损伤发生心脏收缩功能障碍的危险因素分析
2021-04-20黄祖荣聂云辉
姚 乐,黄祖荣,聂云辉
(北海市人民医院急诊科,广西 北海 536000)
创伤性脑损伤(traumatic brain injury,TBI)在交通发达地区多发,是造成高残疾率和病死率的重要因素[1]。颅脑创伤后的继发性因素是造成脑损害进展的重要原因。最近研究表明,心脏收缩功能障碍多发生在TBI之后,是神经损伤模式后应激性心肌病的一种形式[2]。并且足够的心输出量是维持伤后脑血流量的重要因素,因此当发生心脏收缩功能障碍时会进一步加重脑损伤[3]。有研究认为TBI后的早期血压过低或过高均是TBI不良预后相关的影响因素[4]。此外,TBI后是否发生心脏收缩功能障碍,早期血流动力学参数可能会有所不同,但是这方面研究较少。研究表明,儿茶酚胺过量状态是导致其他严重神经系统疾病早期发生高血压和收缩功能障碍的主要原因[5]。了解发生心脏收缩功能障碍TBI患者的早期血流动力学特征可以提高对心脏收缩功能障碍机制的理解,进而提供一个治疗靶点来改善远期疗效。因此,笔者回顾性分析2018年7月—2019年7月北海市人民医院收治的63例急性TBI患者资料,评估早期TBI是否存在收缩功能障碍并对相关危险因素进行分析。
资料与方法
1 一般资料
纳入标准:(1)年龄18~70岁; (2)结合临床表现及病史明确诊断为TBI; (3)不伴随有其他严重危及生命的多发伤; (4)入院时间≥48h。排除标准:(1)心脏收缩功能障碍相关的重大全身性疾病(肝硬化、慢性肾功能不全2期以上、慢性阻塞性肺部疾病2期及以上、艾滋病)以及化疗史; (2)入院前发生心脏骤停; (3)既往有心脏病、高血压、肺动脉高压或脑血管病史,有恶性肿瘤或自身免疫系统疾病史; (4)伴有严重感染; (5)入院后输血量>2单位; (6)未能完成心脏超声检查; (7)住院时间<48h(自动出院或中途退出)。
根据63例患者是否发生心脏收缩功能障碍分为障碍组21例,无障碍组42例。当左室长轴缩短率(longitudinal fractional shortening,LFS)<25%时认为存在心脏收缩功能障碍[6]。障碍组男性14例,女性7例;年龄38~55岁,平均42.0岁; 无障碍组男性30例,女性12例; 年龄39~54岁,平均43.2岁。两组患者均因道路交通伤(38例)或摔伤(25例)导致颅脑损伤。患者在年龄、性别、体质量指数(BMI)方面差异无统计学意义(P<0.05),具有可比性。
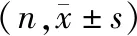
表1 患者一般临床资料
2 方法
根据美国颅脑损伤基金会指南[5],对中重度颅脑损伤患者,保持颅内压(intracranial pressure,ICP)<20mmHg,二氧化碳动脉分压35~40mmHg,血糖<180mg/dL,每小时评估1次液体平衡,根据病情使用血管加压药、甘露醇或高渗盐水、镇静镇痛药物,进行手术治疗。发热患者常规使用物理降温和退热药物。血流动力学管理方面,ICP监测仪监测下最小脑灌注压力为50mmHg;无ICP监测仪则收缩压>90mmHg。在受伤后24h内行经胸超声心动图检查。血流动力学不稳定的患者待病情平稳后进行检查。
3 心脏超声评估方法
患者入院24h内根据美国超声心动图学会指南行心脏超声检查[7](飞利浦EPIQ5),血流动力学不稳定的患者待病情平稳后进行检查。所有患者均由同1名经验丰富的超声科医师进行操作。为防止颅内压力变化,患者采用仰卧位,选择M型超声心动图评估左心室功能,收缩功能主要使用LFS评估,LFS<25%为收缩功能障碍[6]。LFS=(舒张期左心室内径-左室收缩期内径)/(舒张期左心室内径)。心脏超声在胸骨旁左心室长轴切面测量左心室舒张末期内径(left ventricular internal end diastolic diameter,LVIDd)、左心室收缩末期内径(left ventricular end systolic diameter,LVIDs),Simpson法测量左室射血分数(left ventricular ejection fraction,LVEF),在心尖四腔心切面测量二尖瓣口舒张早期及舒张晚期血流峰值速度E及A,并计算E/A值,采集并存储心尖位左心长轴切面、心尖位四腔心切面、心尖位两腔心切面各连续3个完整的心动周期图像以备分析。应用在线软件(TMQ Adv,Q Lab,Philips)将追踪点1放置于二尖瓣前瓣瓣环,追踪点2放置于二尖瓣后瓣瓣环,追踪点3放置于心尖部,自动分析得到LFS-4c和LFS-2c,取2者平均值作为患者的LFS。所记录的图像由2名有经验的超声科医师进行阅片。
4 观察指标
观察每小时收缩压(SBP)、平均动脉压(MAP)、心率(HR)等血流动力学参数,心脏超声测量LVIDd值、LVIDs值、LVEF值、E/A值等,并记录患者的住院时间和入院28d病死率。
5 统计学分析
结 果
超声心动图结果显示:在收缩功能相关参数中,障碍组的LVEF和LFS均显著低于无障碍组(P<0.001),而LVIDs明显增大(P<0.001); 其中二尖瓣环间隔组织速度是衡量纵向左心室收缩性的指标,两组差异无统计学意义(P>0.05)。在舒张功能参数方面两组之间相似,包括E与A之比,二尖瓣环间隔组织速度e’(s)(P=0.558)和E与e’(s)之比(P=0.231),均无统计学差异,仅表现为较高的E波速度(P<0.001)。见表2。
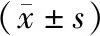
表2 创伤性脑损伤患者心脏超声检查结果
障碍组入院时格拉斯哥昏迷评分(GCS)显著低于无障碍组(P<0.001)。头颅CT诊断显示,障碍组脑室内出血比例较高(P<0.001)。见表3。
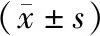
表3 TBI后发生收缩功能障碍的单因素分析
多因素分析显示GCS(OR:3.964; 95%CI:2.92~5.03,P<0.001),SBP变化程度(OR:2.115; 95%CI:1.48~2.74,P<0.001)以及MAP变化程度(OR:1.647; 95%CI:1.04~2.25,P<0.001)与TBI患者发生收缩功能障碍独立相关。见表4。
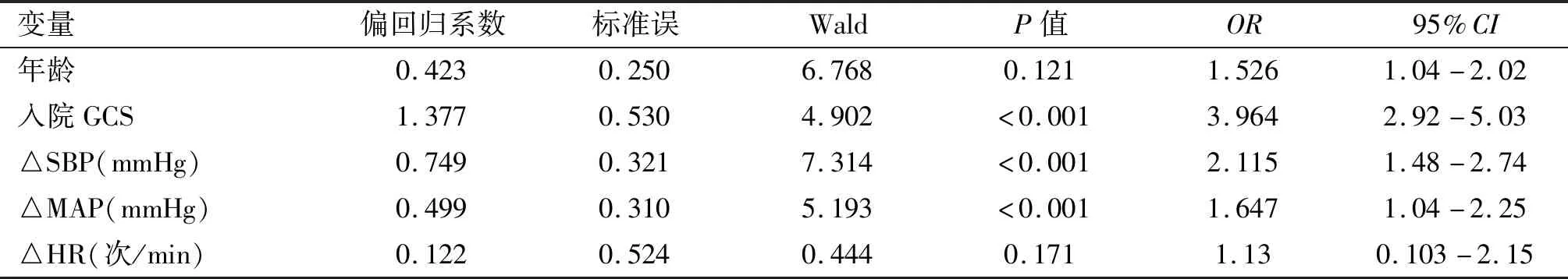
表4 TBI后发生收缩功能障碍的多因素分析
讨 论
研究表明TBI对心脏的损害主要表现为心律失常、心肌缺血、假性心肌梗死、心力衰竭甚至心脏停搏等。相应的心电图、心肌酶谱、超声心动图均可发现异常改变[3],但对TBI患者心脏功能的研究较少[8]。本研究目的在于评估早期TBI是否存在心脏收缩功能障碍,以及分析发生心脏收缩功能障碍的相关危险因素。
本研究表明心脏收缩功能障碍均发生在中重度TBI患者中,且障碍组在入院后24h内有明显的血流动力学变化,如早期高血压和心动过速,其次是入院后12h血压下降。结合既往研究结论,早期交感神经系统激活和过量的儿茶酚胺释放是引起TBI后收缩功能障碍的潜在机制之一[9],严重TBI后机体处于应激状态,颅内压升高,下丘脑和下丘脑神经内分泌通路激活后引发儿茶酚胺释放[10]。全身儿茶酚胺释放对心脏的影响极为严重,早期表现为血压升高、心律不齐、心率增加,如疾病未见好转会引起心肌缺血性损害以及退行性改变,严重者出现心肌梗死[11]。
为了预防TBI患者发生颅内压变化,经胸超声心动图检查多选用仰卧位,本研究中心脏收缩功能障碍被定义为LFS<25%。既往研究表明,高血压、冠心病、瓣膜病等患者虽然测定的左室射血分数在正常范围,但长轴功能均有不同程度受损[12]。这是因为纵行心肌纤维舒缩构成的心室长轴运动在维持正常心室功能中起到重要作用。纵行心肌主要位于左心室心内膜下、心外膜下和乳头肌内,比中层的环行心肌纤维更容易受到心肌缺血等病理因素的影响,表现为左心室长轴收缩功能受损早于短轴收缩功能。因此分析心肌长轴功能有助于早期发现心脏功能障碍。此外心脏超声结果显示,除了E波波速增加外,在障碍组中没有观察到明显的舒张功能障碍,这可能是由于舒张功能障碍多见于慢性心脏病患者,而在急性TBI后,各种神经内分泌变化引起的心肌损害导致心肌收缩力减弱,血压升高、后负荷增大可使等容收缩期延长,射血期缩短,每搏输出量减少,射血分数下降,但是对舒张功能的影响相对较小。本研究结果对中度重度TBI患者的治疗具有一定的意义,对于血流动力学特征的研究有助于阐明交感神经在脑损伤后收缩功能障碍发病机制中的作用。
本研究局限性:(1)为单中心研究,样本量较小,这可能会降低回归估计的精度,仍需进一步多中心前瞻性研究证实该结论;(2)不能完全确定患者在发生TBI前没有心脏收缩功能障碍,因此在入组标准中尽可能排除影响收缩功能的因素;(3)未能评估心脏收缩期障碍与患者预后的相关性,还需进一步深入研究。
总之,在中重度TBI患者中,很可能发生早期心脏收缩功能障碍,并且发生心脏收缩功能障碍的患者具有明显的血流动力学特征,如早期高血压和心动过速,其次是入院后12h收缩压下降。入院时GCS、SBP变化程度以及MAP变化程度与TBI后发生心脏收缩功能障碍独立相关,TBI后的患者需加强早期血压控制。