硼替佐米联合地塞米松、沙利度胺治疗多发性骨髓瘤的临床价值
2021-04-20荆雷兰学晶李玉竹
荆雷,兰学晶,李玉竹
丹东市中心医院血液科,辽宁丹东 118002
多发性骨髓瘤起源于浆细胞恶性克隆性过程中,浆细胞发生异常增生,异常分泌大量单克隆免疫球蛋白。截至目前临床所采取的最佳治疗方案为异基因造血干细胞移植。但由于该类患者年龄普遍较高,身体各项机能退化,导致移植治疗时病死率较高,且供体资源缺乏、移植后并发症多,以上各种因素均对患者生命安全构成威胁,加大了患者家庭、医院以及社会的负担[1-2]。因此积极探索辅助治疗多发性骨髓瘤的科学高效方法一直是医学界关注重点项目,旨在控制患者病症,提高其生存质量。该文选取2018 年4 月—2019 年4 月在该院接受治疗的100 例多发性骨髓瘤患者,对其临床资料进行回顾性分析,主要探讨硼替佐米联合地塞米松、沙利度胺治疗多发性骨髓瘤的临床价值,现报道如下。
1 资料与方法
1.1 一般资料
经过伦理委员会批准,选取在该院接受治疗的100 例多发性骨髓瘤患者,随机分为对照组(n=50)与观察组(n=50)。对照组 50 例,男 28 例、女 22 例,平均年龄(54.06±15.33)岁。观察组 50 例,男 21 例、女 29例,平均年龄(53.87±14.98)岁。两组一般资料差异无统计学意义(P>0.05),具有可比性。所有患者及其家属均知情并签署知情同意书。
1.2 方法
对照组为:长春新碱(国药准字 H14020811),0.5 mg/d,连续静脉滴注 4 d; 阿霉素 (国药准字H20133365),连续静脉滴注 4 d,10 mg/d; 地塞米松(国药准字 H44024185),连续静脉滴注 4 d,40 mg/d,分别于第 1~4 天、9~12 天、17~20 天时间段内使用,连续治疗28 d 为1 个疗程。观察组采用硼替佐米联合地塞米松、 沙利度胺治疗,沙利度胺 (国药准字H32026129)初始使用剂量为100 mg/d,口服,叮嘱患者于临睡前服用,之后每周递增50 mg/d,直至药剂量达 200 mg/d 不再改变; 硼替佐米 (国药准字J20120055),1.3 mg/m2,分别在第 1、4、8、11 天实施静脉滴注;地塞米松 20 mg/d,分别于治疗第 1~4 天、9~12 天实施静脉滴注,连续21 d 为1 个疗程。
以上两组均连续治疗2~4 个疗程。
1.3 观察指标
①两组患者临床疗效。严格依照国际骨髓瘤医学工会制定的标准判定: 完全缓解 (CR)、 部分缓解(PR)、疾病稳定(SD)、疾病进展(PD)、复发。②两组患者免疫因子水平。分别于治疗前后测定患者M 蛋白、β2-微球蛋白(β2-MG)水平。
1.4 统计方法
采用SPSS 20.0 统计学软件分析数据,其中计量资料以(±s)表示,组间比较采用两独立样本t 检验;计数资料以频数和百分比(%)表示,组间比较采用χ2检验或Fisher 精确概法。P<0.05 为差异有统计学意义。
2 结果
2.1 临床疗效
观察组(82.00%)、对照组(56.00%)临床疗效对比,差异有统计学意义(P<0.05),见表1。
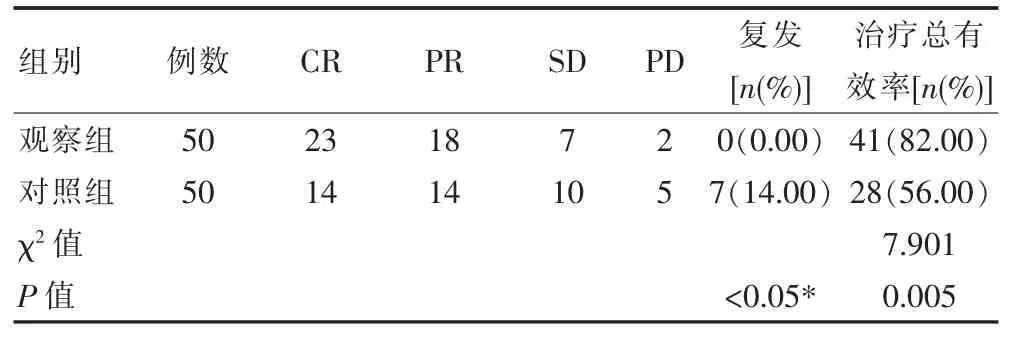
表1 两组患者的临床疗效对比
2.2 免疫因子水平
治疗前,两组患者免疫因子差异无统计学意义(P>0.05),治疗后,观察组 M 蛋白、β2-MG 水平均显著低于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组患者免疫因子水平对比(±s)
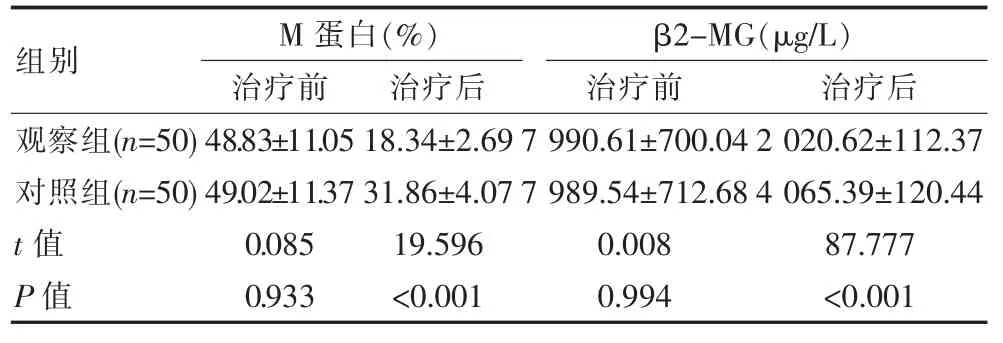
表2 两组患者免疫因子水平对比(±s)
组别M 蛋白(%)治疗前 治疗后β2-MG(μg/L)治疗前 治疗后观察组(n=50)对照组(n=50)t 值P 值48.83±11.05 49.02±11.37 0.085 0.933 18.34±2.69 31.86±4.07 19.596<0.001 7 990.61±700.04 7 989.54±712.68 0.008 0.994 2 020.62±112.37 4 065.39±120.44 87.777<0.001
3 讨论
多发性骨髓瘤属于临床上较为常见的一类血液系统恶性肿瘤,目前尚未完全明确其具体发病原因,认为化学毒物、免疫性疾病、环境辐射、病毒感染、遗传等因素均可能导致发病[3-4]。硼替佐米作为蛋白酶体抑制剂,可对肿瘤细胞增殖生长、血管生成、细胞黏附分子黏附迁移产生直接抑制作用,同时还可阻滞DNA 分子修复进程、泛素标记的蛋白质降解进程,进而克服肿瘤细胞在接受传统化疗药物以及激素的耐药性,有利于肿瘤细胞的凋亡与死亡[5-7]。此外,硼替佐米对正常的干细胞、巨核细胞产生毒性,最常见不良反应为感染、血小板减少、胃肠道反应等,但多数患者均为轻度且可逆,一般在接受对症治疗或停药后即可恢复,安全有效,已逐渐发展为临床治疗多发性骨髓瘤的新型首选药物[8]。沙利度胺治疗多发性骨髓瘤的药理机制为:①阻断细胞分裂蛋白激酶通路,抑制瘤细胞生长形成过程;②抑制血管内皮生长因子诱导以及肿瘤细胞的新生血管; ③借助DNA 氧化作用损伤肿瘤形成,促使其凋亡。且在使用沙利度胺药物治疗时不会引发骨髓抑制。该文结果显示,观察组、对照组临床疗效、不良反应均差异有统计学意义(P<0.05)。提示采用硼替佐米联合地塞米松、沙利度胺治疗多发性骨髓瘤具有良好应用价值,可明显改善患者临床症状,降低不良反应的发生。选取β2-MG 作为一种小分子球蛋白,大多数情况下其合成量以及血液中含量均处于稳定范围内,高达99.9%的β2-MG 会被肾小管吸收[9]。而对于多发性骨髓瘤患者,与肿瘤紧密联系的淋巴细胞表现出活跃性增殖,导致β2-MG 大量合成并释放,患者血清中含量增高。M 蛋白作为一种急性反应蛋白,也可参与到炎症反应过程中[10]。该文结果显示,观察组治疗总有效率为82.00%,显著高于对照组的 56.00%(P<0.05),治疗前观察组 M 蛋白(48.83±11.05)%、β2-MG 水平(7 990.61±700.04)μg/L 与对照组的 (49.02±11.37)%、(7 989.54±712.68)μg/L 相近(P>0.05),治疗后,观察组 M 蛋白 (18.34±2.69)%、β2-MG 水平(2 020.62±112.37)μg/L 均显著低于对照组的(31.86±4.07)%、(4 065.39±120.44)μg/L(P<0.05)。提示采用硼替佐米联合地塞米松、沙利度胺治疗可明显改善患者免疫水平,调整内环境恢复动态平衡状态,进一步避免该疾病产生高耐药性[10]。在顾丽丽等[11]学者文献中选取到院就诊的60 例多发性骨髓瘤患者,其中一组接受一般方案治疗,作为常规组,一组接受硼替佐米+地塞米松+沙利度胺进行治疗,作为实验组,比较两组患者的治疗效果。结果显示,实验组完全缓解15 例、部分缓解10 例,治疗总有效率为83.33%(25/30),常规组全缓解 8 例、部分缓解 8 例,治疗总有效率为 53.33%(16/30)(P<0.05); 治疗组复发率为0.0%,常规组为 6.67%(P<0.05);治疗后,实验组 M 蛋白(17.88±10.00)%、β2-MG(16.22±9.58)μg/L,优于对照 组 的 (27.52±11.20)%、(23.33±10.25)μg/L (P <0.05);上述学者文献均与该文研究结果相符,再次证明了采用硼替佐米联合沙利度胺、地塞米松方案治疗多发性骨髓瘤的应用价值。
综上所述,采用硼替佐米联合地塞米松、沙利度胺治疗多发性骨髓瘤,效果良好。
