基于心脏磁共振心功能分析定量评价未识别心肌梗塞合并心力衰竭的初步临床研究 ①
2021-04-15吕亚囡王雪梅耿文举王淑艳杨晓强郑晓群
吕亚囡,王雪梅,徐 哲,耿文举,王淑艳,杨晓强,郑晓群
(1. 大连市中心医院放射科,辽宁 大连 116000;2.陆军装备部门诊部,北京 100000)
未识别心肌梗塞(unrecognized myocardial infarction, UMI ),又称为静息心肌梗塞(silent myocardial infarction, SMI),是指无症状或症状不典型的心肌梗塞(myocardial infarction, MI),其发生率约占全部心肌梗塞的一半。虽然UMI的起病隐匿,患者没有MI自述病史和就医史,但心血管主要事件(major adverse cardiac events, MACE),包括心源性死亡、新发急性心肌梗塞、不稳定心绞痛、心衰或室性心律失常的发生率与接受过治疗的MI相似或者更高。因此早期发现并准确诊断UMI,全面精确评价心脏结构和功能对于改善病人的生存质量,降低死亡率意义重大。
心脏磁共振(cardiac magnetic resonance, CMR)是公认的、无创性评价心脏结构和功能的金标准;其卓越的空间分辨力、时间分辨力和组织分辨力是精准、可重复的心功能和结构分析的保证。同时,CMR多序列、多参数、多角度的成像,实现心肌组织特征性分析。
因此本研究基于CMR成像,同时结合磁共振心脏形态和心功能定量分析,评估UMI合并心衰的诊断,并结合心电图和实验室指标N末端B型利尿钠肽原(N-terminal pro-brain natriuretic peptide, NT-proBNP)综合评价CMR在UMI和并HF病人中的应用。
1 资料与方法
1.1 一般资料
搜集2016-01~2020-03经我院CMR确诊的21例UMI患者,男17例,女4例,平均年龄(62±16)岁的图像和心功能处理结果、心电图报告及实验室指标NT-proBNP。
UMI的诊断标准是心脏磁共振延迟增强扫描图像显示的心内膜下和/或透壁强化[1]。排除标准为:有明确MI病史、有冠脉血管再通治疗史(包括支架和搭桥手术史)、可疑或确诊心肌炎,心包疾病或有非缺血性心肌病(能引起心肌瘢痕)病史的患者。
1.2 检查方法
常规临床指标和血液学检查结果:收集入组患者的一般情况和病史,包括年龄、性别、身高、体重并计算身体质量指数(body mass index, BMI)以及高血压、糖尿病和高血脂的病史。收集心脏磁共振检查前的心电图有无病理性Q波和实验室指标NT-proBNP和的检查结果。
CMR检查扫描方案:使用GE HDXT 1.5T磁共振扫描机,心脏专用线圈,呼吸和心电门控进行扫描。选择白血电影序列、2D延迟增强扫描序列图像进行心脏结构、心功能和心肌延迟增强的处理和分析。白血电影序列扫描参数:TR 3.2ms,TE 1.3ms,NEX 1,视野为42cm×42cm,矩阵为224×224,层厚为8mm。 2D延迟增强扫描扫描方案: 团注钆喷酸
葡胺造影剂25mL后,延迟7min后开始扫描,CINE IR序列测试TI时间,延迟扫描为FGE序列,扫描参数为TR 6.7ms,TE 3.1ms,NEX 2,视野为42cm×42cm,矩阵为256×192,层厚为8mm。单次屏气单次扫描,扫描时间取决于扫描层数和每一层的扫描时间。
1.3 图像分析与后处理
由两名CMR诊断经验丰富的放射科医师分析图像,评价图像扫描质量、心脏大体形态结构、白血电影序列中左右心室壁运动状态以及心肌延迟增强扫描强化部位、方式和节段数;根据美国心脏协会(American Heart Association,AHA)标准,心肌划分为17个节段[2]。根据2018年澳大利亚心衰指南[3],本文纳入CMR功能分析LVEF<50%的患者进行研究。
左右心室容积和功能分析,应用专业心血管后处理软件(ReportCARD 4.0, GE, the United States)进行左右心室功能分析。手动勾画白血电影序列短轴位所有层面的收缩末期和舒张末期心内膜以及心外膜(腱索和乳头肌包括在左心室腔内),测定以下心功能参数:左心室/右心室射血分数(left /right ventricular ejection fraction, LVEF/RVEF),左心室/右心室舒张末期容积指数(left /right ventricular end-diastole volume index, LVEDVI/RVEDVI),左心室/右心室收缩末期容积指数(left /right ventricular end-systole volume index, LVESVI/RVESVI)。
1.4 统计学方法

2 结果
2.1 UMI合并HF患者的临床资料
21例入组患者平均年龄(62±16)岁,男17例,女4例;BMI平均值(23.5±4.6)kg/m2,所有病人的NT-pro BNP均可见增高,范围140~30000pg/mL,平均(11097±7344)pg/mL。患者的临床资料,包括病史、心电图见表1。

表1 UMI合并HF患者的临床资料(例)
应用t检验,分析心电图有无Q波病人的NT-pro BNP值的组间差异,结果具有统计学意义(P<0.05)。
2.2 UMI合并HF患者CMR分析
见表2。

表2 心脏磁共振功能测量结果
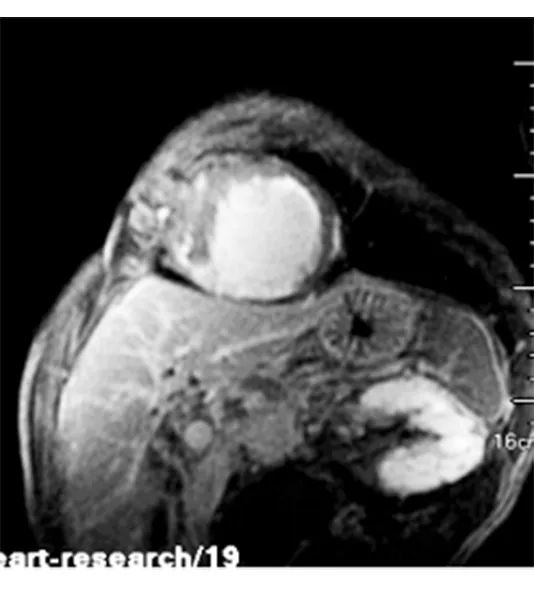
图1 心脏磁共振诊断UMI图像:短轴位,2D延迟增强显示心尖部上侧壁心内膜下强化(白色虚线箭)和下壁透壁强化(白色实箭)
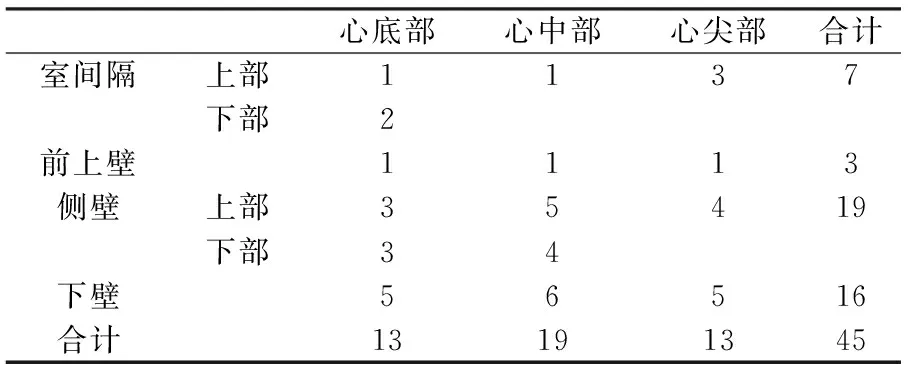
表3 UMI心肌延迟强化节段分布(例)
UMI合并HF患者CMR心肌延迟增强结果:21例患者心脏磁共振心肌延迟强化45个节段,其中心内膜下强化26(58%)个节段,透壁强化19(42%)个节段,见图1。延迟强化心肌的节段分布见表3。
2.3 相关性分析
应用Person回归法分析显示,LVEDVI、RVEDVI值以及心肌延迟强化的节段数与NT-pro BNP 有相关性(r值分别为0.268、0.309和0.307,P均<0.05)。
3 讨论
本研究结果显示,21例UMI合并心力衰竭的CMR心肌延迟强化均分布在左心室的侧壁和/或下壁,心底部、心中部和心尖部均有累及,与Charotte[4]和Min[5]等人的结论一致。5例患者(23.8%)心电图出现病理性Q波,而16例(76.2%)心电图无病理性Q波;与已报道的不合并心力衰竭的UMI比较,合并心力衰竭的UMI患者,无病理性Q波者更多,提示无病理性Q波的UMI患者更易发生心衰。心电图的病理性Q波是临床诊断UMI的主要手段和标准[6],无病理性Q波的UMI心电图无法检出,导致UMI发病率低估,而CMR明显提升了UMI的检出率。
在CMR图像后处理中,我们发现17例(81%)患者伴有不同程度或不同形式的右心功能紊乱(right ventricular dysfunction, RVD),包括RVEF值减低、RVEDVI与RVESVI增高和右心室增大。美国心脏协会的声明[7]指出,RVD与临床不良预后相关。研究UMI合并HF时的RVD发生率的文献不多,本文对RVD的分析将对全面而准确的判断患者的病情和转归提供指导作用。同时,我们还发现在LVEF值下降的同时,LVEDVI和LVESVI升高,提示左心室容量负荷加重,进一步加重心肌结构和功能受损。
本研究中,所有UMI合并HF患者的NT-pro BNP值均高于正常,数值变化从140~30000pg/mL,相关性分析发现NT-pro BNP的升高与心肌延迟增强的节段数量(与Anna报道的结果一致[8])、LVEDVI和RVEDVI相关。NT-pro BNP作为舒张末期室壁张力与容量和/或压力增高时,心肌细胞直接释放入血液的一种物质,是疾病严重程度的标志[9]。本研究的结果明确了双侧心室舒张末期容积指数升高以及瘢痕心肌多与NT-pro BNP的升高相关,为临床心力衰竭的减容治疗提供客观而有力的依据。
本研究尚存在一些局限性:首先,样本量较少。其次,纳入研究的心力衰竭病例,只选择的射血分数减低,即LVEF<50%的患者;未对射血分数保留的UMI合并心衰的患者进行研究,有待于以后进一步收集病例补充研究。
综上所述,心脏磁共振对于未识别心肌梗塞伴心力衰竭的患者,不仅能够提高检出率,而且能够多方面、精准评估心脏形态、结构的改变,是未识别心肌梗塞伴心力衰竭患者的优选影像学评价方法。
