不同材质和结构导管对肿瘤患者PICC置管后血栓形成的影响
2021-04-12张欣朱玉欣高亚伟李江花尹欣欣
张欣 朱玉欣 高亚伟 李江花 尹欣欣
经外周置入中心静脉导管(peripherally inserted central catheter,PICC)具有创伤小、安全性高等优点,广泛应用于肿瘤患者静脉治疗中,但也增加了上肢血管静脉血栓形成机率,导致血栓性静脉炎和肺栓塞等并发症,影响肿瘤患者的治疗和生活质量[1]。静脉置管对于机体来讲是一种异物,长期留置在血管内可损伤内皮细胞,诱导血小板凝聚,使肿瘤患者的机体产生血栓可能性极大提高[2]。PICC从上世纪应用临床以来,经过发展,导管材质越来越优化,但临床应用的导管材质、结构的质量以及组织相容性还是有差异,本研究通过回顾性分析我院两种不同材质、不同结构导管对肿瘤患者PICC置管后血栓形成的几率、血栓形成的时段、穿刺静脉血栓形成概率的差异性,以期为临床研究导管相关静脉血栓形成提供理论依据。
1 资料与方法
1.1 一般资料 选取2018年1月至2019年6月我院PICC置管的恶性肿瘤患者资料,根据患者的住院ID号末尾数字的单双号,选取一定比例不同材质的PICC置管病历。入组标准:年龄>18岁,诊断恶性肿瘤符合置入PICC的患者,置入有瓣膜和无瓣膜的耐高压聚亚氨酯导管的患者,住院号尾号为单号的患者;导管尖端位置在上腔静脉中下部的患者。排除标准:非恶性肿瘤患者;置入硅胶材质的患者。符合本研究条件的病历资料共110例,分为对照组和观察组。对照组58例,男33例,女25例;年龄(62.53±12.07)岁;疾病分类:肺癌9例,消化系统恶性肿瘤31例(胃癌15例、食管癌3例、结直肠10癌、肝癌2例、胆管癌1例),其他恶性肿瘤18例。观察组52例,男33例,女19例;年龄(66.15±16.15)岁;疾病分类:肺癌11例,消化系统恶性肿瘤28例(胃癌11例、食管癌6例、结直肠6癌,胰腺癌3例、肝癌2例),其他恶性肿瘤13例。2组患者的年龄、性别比、疾病类型差异无统计学意义(P>0.05),具有可比性。
1.2 PICC导管相关静脉血栓形成的因素分析 依据患者置管一般资料内容包括患者年龄、性别、诊断、住院号、置管肢体、导管材质、置管部位、置管静脉、导管尖端位置、置管日期等;患者导管使用及留置期间维护及并发症记录单,内容包括患者姓名、年龄、诊断、导管维护时间、各种并发症、血栓形成时间、血栓形成的静脉、拔管时间等。
1.3 方法 肿瘤患者PICC的置入均为2名专职护士操作,1名主任护师,1名主管护师;均取得中华护理学会PICC专科技术培训班的资质证书,PICC置管工作经历10年,年置管量500余根。置管情况:置管前首先要评估患者的病情及血管情况、治疗方案、既往史等,根据治疗方案、血管直径、患者意愿选取导管的材质及型号,导管的置入均在超声引导下MST穿刺技术下完成,置管过程中严格无菌操作,实施最大无菌化区域,置管部位均在肘横纹上>10 cm,静脉选取原则,首选贵要静脉,次选肱静脉,一针穿刺成功率为90%左右,一次送管成功率为70%左右,置管后拍胸片定位,所有入组患者导管尖端的位置均在上腔静脉中下部。
1.4 观察指标 2组肿瘤患者置管后静脉血栓形成的例数,血栓形成病历采集的依据:患者置PICC留置期间,住院期间每日观察患者穿刺点情况、测量臂围、肢体皮肤颜色改变以及患者的主诉并做记录,院外患者通过电话回访和维护导管期间观察上述内容。如果出现穿刺处渗血和渗液、肢体不适感、肩部沉重感、穿刺点压痛和红肿、肢体肿胀等症状,可疑静脉血栓形成,遵医嘱行彩色多普勒超声检查以确诊。诊断标准:(1)超声探头加压血管管腔不能完全闭合;(2)管腔内透声差,血管附壁可探及云雾状中低回声;(3)血流信号充盈缺损,血流频谱出现失期相改变,挤压肢体远端血流信号增强消失或减弱[3]。超声检查报告示静脉血栓形成,根据报告结果记录血栓形成例数和血栓形成静脉。

2 结果
2.1 2组患者一般资料比较 2组患者的性别比、年龄、疾病类型、置管肢体、置管静脉、导管留置天数方面差异无统计学意义(P>0.05);2组患者导管腔数/型号、是否化疗、是否肿瘤转移、伴有基础病等方面比较差异有统计学意义(P<0.05)。见表1。
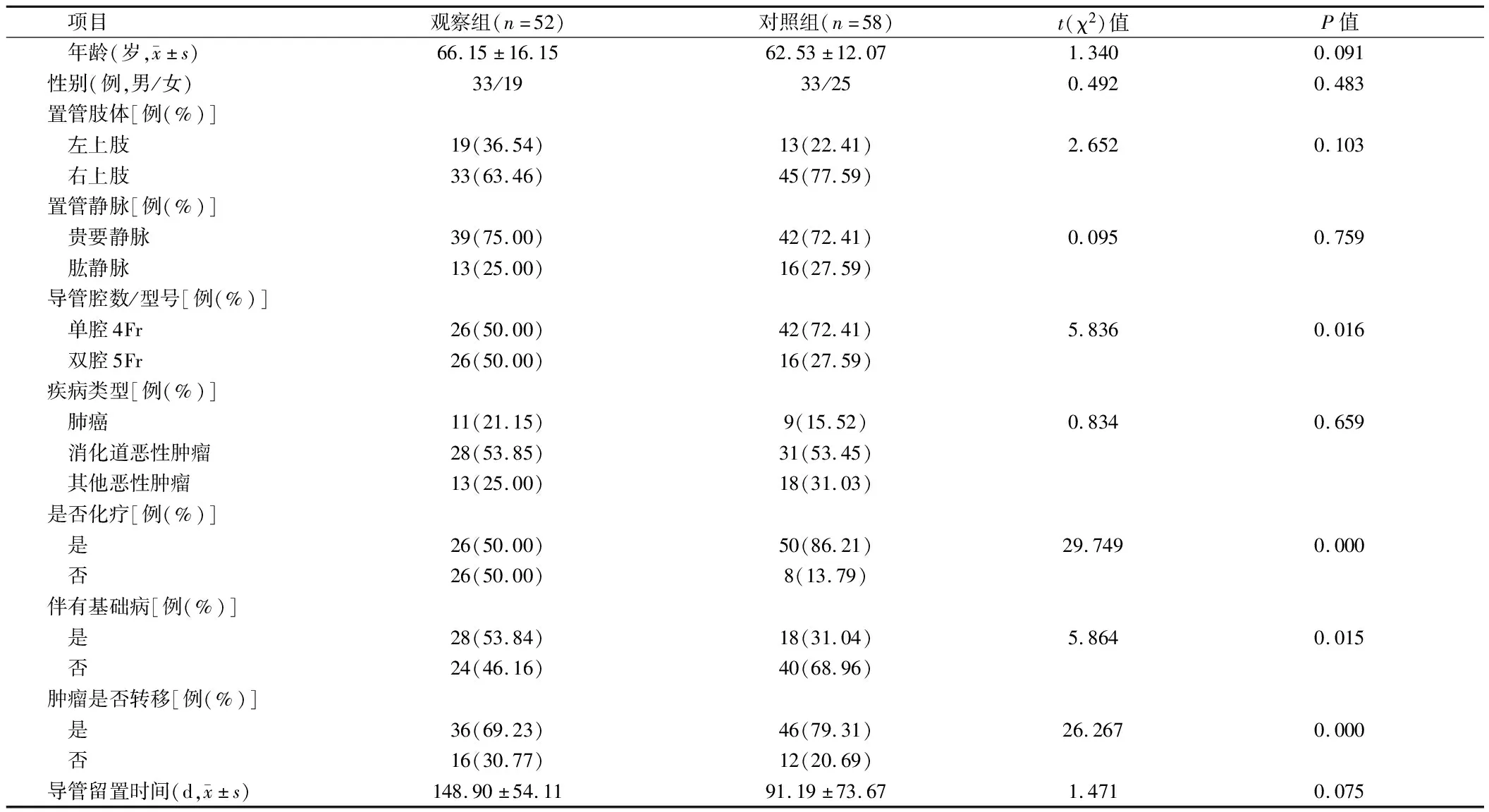
表1 2组患者一般资料比较 n=110
2.2 2组导管总的血栓形成情况比较 对照组总静脉血栓形成25例,占43.10%;观察组总静脉血栓形成11例,占21.15%;2组差异有统计学意义(χ2=6.000,P=0.028)。见表2。

表2 2组导管静脉血栓形成情况比较 n=110,例(%)
2.3 2组导管血栓形成起始静脉比较 血栓形成起始静脉为贵要或肱静脉对照组18例(43.10%),观察组4例(21.15%),血栓形成起始静脉为腋或锁骨下静脉对照组7例(78.85%),观察组7例(56.90%),2组导管在血栓形成起始静脉方面差异有统计学意义(χ2=4.082,P=0.043)。见表3。

表3 2组导管血栓形成起始静脉情况比较 例(%)
2.4 2组导管从穿刺静脉向上延伸血栓形成情况 对照组有延伸11例(61.10%),未延伸7例(38.90%),观察组有延伸3例(75.00%),未延伸1例(25.00%),2组导管在血栓形成从起始静脉向上延伸方面差异无统计学意义(χ2=0.273,P=0.601)。见表4。

表4 2组导管血栓从穿刺静脉延伸至腋、锁骨下静脉情况比较 例(%)
2.5 2组导管发生血栓时间比较 2组导管血栓形成时间差异无统计学意义(χ2=7.772,P=0.051)。见表5。
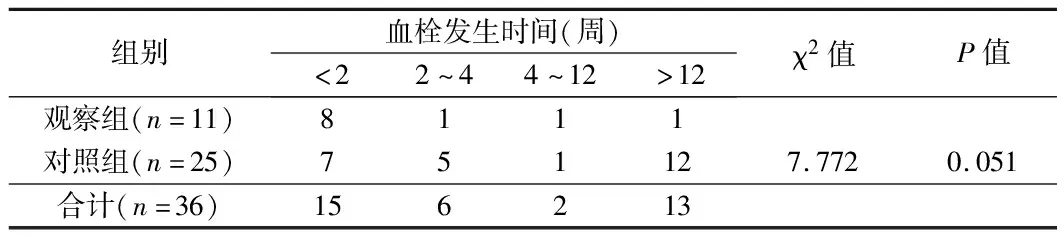
表5 2组导管发生血栓时间比较 n=36,例
3 讨论
3.1 患者一般情况对置管后血栓形成的影响 有报道肿瘤患者个体差异、疾病分期、化疗药物等多方面因素均可影响静脉血栓的形成[3]。患者的年龄、性别是否对肿瘤患者PICC相关静脉血栓形成有影响没有统一的定论。文献报道恶性肿瘤也是诱发深静脉血栓的重要风险因素,未置入PICC的肿瘤患者上臂血栓形成风险是其他患者的8倍[4]。肿瘤患者疾病血液处于高凝状态,肿瘤坏死细胞因子和白介素-Ⅰ可以是血管内膜坏死脱落,血管内壁发生有利于血栓形成的改变,增加血栓形成的风险[5]。有文献报告肿瘤细胞膜上产生一定量的凝血酶,促使血小板黏附在血管内皮上,内皮细胞、血小板和肿瘤细胞之间的复杂作用致肿瘤细胞对血管内壁的黏附,造成血栓形成前的状态[6]。说明肿瘤患者及疾病分期是PICC置管后血栓形成的危险因素。本研究对照组血栓形成明显高于观察组(χ2= 6.000,P=0.028)。有文献报道化疗药物的细胞毒性作用可损伤血管内膜致其纤维化、可逆降低蛋白S和蛋白C的水平、延迟血管内膜完整性修复等导致血栓形成危险因素增高[7,8]。本研究显示化疗患者血栓的风险高于非化疗患者(χ2=29.749P=0.000)。
3.2 PICC置管操作因素对静脉血栓形成的影响 文献报道操作因素如超声引导下置管、选择右上肢的贵要静脉、肘上置管减少肢体活动的影响等可以有效提高穿刺成功率和减少操作因素引起的上肢静脉血栓形成率[9]。本组患者的导管置入均使用超声引导下赛丁格技术穿刺、选择肘横纹上10 cm区域置管、首选贵要静脉、置管过程中辅助腔内心电图定位、置管后胸片最终定位,就是为避免因操作因素所致医源性静脉血栓形成几率增加的影响。
3.3 导管材质对静脉血栓形成的影响 除PICC置管因素的影响,PICC置入体内后,不论导管是什么材质,对于人体来说都是异物,长期留置对血管内膜会造成一定的损伤,血管内膜增厚,血管变狭窄致血流缓慢,增加血管静脉血栓形成的风险。有文献报道导管本身是导致PICC相关静脉血栓形成的主要因素之一[10]。目前临床上常用的导管有两种材质,一种是体外手感柔软的医用硅胶材质,一种是体外手感较硬的医用聚氨酯材质,医用聚氨酯耐高压导管又分为前端开口无瓣膜导管和有瓣膜导管两种,有瓣膜耐高压导管末端有一个特殊设计三项瓣膜装置,除了可防止血液返流入导管降低导管内血栓形成外,因其为热敏聚氨酯材质,进入机体内后因机体内温度增高而变软,在血管内可能处于漂浮状态,对血管壁的影响相对较小,组织相容性更好。本研究也认为导管材质可能是PICC置管静脉血栓形成的影响因素,收集置入不同材质肿瘤患者的临床资料,发现观察组11例静脉血栓形成占21.15%,对照组25例静脉血栓形成占43.10%,不同材质导管总的血栓形成情况对比存在显著性差异(χ2=6.000,P=0.028)。原因可能是无瓣膜聚氨酯导管的材质较硬,对血管内膜摩擦致其损伤有关。通过对拔出导管的外形观察,发现无瓣膜耐高压导管会因体内静脉血管走向而形成一定的弯曲形状,其更容易贴在血管壁上,长期留置对血管内膜的影响较大,也更易促使静脉血栓形成的危险性增加。而有瓣膜聚氨酯导管在体内相对变软处于漂浮状态,对血管内膜影响较小,故血栓形成的几率相对较低。
3.4 导管结构对静脉血栓形成的影响 除导管材质对血管影响外,其特殊的导管末端的倒锥形设计也是静脉血栓形成影响因素之一。有倒锥形设计的导管在接近末端大约5 cm左右其外径开始增粗,导管增粗部分的直径大于微插管鞘的直径。PICC置管因扣皮、微插管鞘直径大于导管的外径,往往置管后穿刺处创口相对较大,导管随肢体活动而移动,导致穿刺口不易愈合和皮肤细菌沿创口向隧道内移可能。导管倒锥形设计的初衷使导管增粗的部分封闭穿刺口,减少穿刺点感染和渗血渗液。但PICC置管穿刺静脉为远心端浅静脉,直径相对较细,临床观察在人体自然状态下一般贵要静脉血管的直径大多为4 mm左右,其静脉血管的直径还易受患者情绪、温度、进食等因素的影响,置管时和置管后血管直径可能发生一定的改变。我国输液导管相关静脉血栓形成中国专家共识临床实践和美国2016版输液治疗实践标准均推荐:应根据拟置管血管条件选择合适的导管型号,建议导管外径与置管静脉内径比值≤45%,临床成人置入的PICC导管多选择4Fr-5Fr型号,其外径为1.4~1.7 mm,其倒锥结构部分外径大约与6Fr-7Fr导管相当,所以增加了其导管占位效应,影响血管内的血流速度、与血管内壁接触的几率,变相增加血栓形成的风险。有文献报道导管的直径与深静脉血栓形成具有密切关系,且置管静脉与导管的直径比是影响PICC相关静脉血栓形成的关键因素[11,12]。本研究收集的2组导管均为倒锥形设计的聚氨酯导管,静脉血栓形成的比率为21.15%~43.10%,与文献报道的静脉血栓形成率为6.7%~26.7%[11]比较,本研究血栓形成比率较高,可能与拔管前超声筛查无症状静脉血栓形成有关。通过观察血栓形成的起始静脉情况,发现血栓形成的36例患者中,发生在穿刺静脉22例,2组导管血栓形成起始静脉对比:血栓形成起始静脉为贵要或肱静脉对照组18例,观察组4例,血栓形成起始静脉为腋和或锁骨下静脉对照组7例,观察组7例,2组导管相比在血栓形成起始静脉有显著性差异(χ2=4.082,P=0.043),说明静脉血管血栓形成除了导管倒锥形结构外,与导管倒锥形结构处材质软硬程度关系更密切。
3.5 静脉血栓的干预措施对血栓形成延伸的影响 静脉血栓形成后早发现、早干预对其进展和预后较好,本研究观察2组导管从穿刺静脉向上延伸至腋静脉、锁骨下静脉处情况,2组导管无显著性差异(χ2=0.273,P=0.601);可能与临床早期发现血栓形成积极抗凝干预有关。临床上我们更重视患者主诉,如果患者肢体有沉重感、穿刺点偶有疼痛不适,即给予超声筛查,一旦血栓形成即进入抗凝干预,大部分患者血栓形成在1~2周,而且不影响患者使用导管治疗。通过观察置管后血栓形成的时段,我们认为早期采取干预措施如加强松握拳、多饮水增加循环血流等对预防血栓形成非常重要,对照组导管25例血栓形成,7例发生在2周以内,观察组导管11例血栓形成,8例发生在2周以内。因在置管初期,可能与改变血管的血流、导管占位效应、置管损伤血管内膜等因素有关,文献报道置入PICC位于血管中心轴的位置,影响静脉回心血流中心轴流的血流速度,对静脉壁两侧边流血流速度影响较小[13]。置管后期发生血栓可能与导管材质的硬度、长期放置机械性刺激血管内膜有关[14,15],但总的看来2组导管发生血栓的时段无显著性差异。
肿瘤患者PICC置管后因疾病本身、化疗、年龄等因素易致静脉血栓形成、堵管等并发症[16],除上述不可规避的静脉血栓形成因素外,本研究发现导管材质、导管倒锥形结构可能也是静脉血栓形成的因素之一,提醒置管者置管前应关注导管材质和结构,评估导管的特殊结构对置管静脉的影响,优化操作流程,如倒锥形结构的PICC修剪合适长度、超声引导置管选择直径更大静脉以减少导管与静脉比的影响、根据导管的材质考虑留置的时间,为减少导管相关静脉血栓形成提供理论依据。
