从铜阳极泥分铜渣碱浸液中回收碲
2021-04-08廖春发邹建柏
廖春发,邹 耕,彭 珊,邹建柏,周 迅
(江西理工大学 材料冶金化学学部,江西 赣州 341000)
自然界中,碲的独立矿床较少,主要伴生于其他金属矿[1-2]中。工业上主要从冶金副产物[3-4]中回收碲,其中铜阳极泥是回收碲的主要原料,所生产的碲占总产量的90%左右[5]。目前,从含碲溶液中分离提取碲的方法有置换法[6]、SO2还原法[7]或Na2SO3还原法[8]、沉淀分离法[9]等。置换法采用铜粉还原溶液中的碲,碲以Cu2Te形式回收[10-11],此法环境友好,碲回收率高,但对铜粉需求大,成本较高。采用SO2或Na2SO3还原溶液中碲,碲以单质形式沉淀。相较而言,以Na2SO3作还原剂,对环境污染小,碲沉淀时间短[8]。中和沉淀分离法是通过调节溶液pH,使碲以TeO2形式沉淀析出,但此法所得中和渣含较多杂质,需除杂[12-13]。
试验针对铜阳极泥分铜渣超声强化氧化碱浸含碲溶液[14],用Na2SO3将溶液中+6价碲预还原为+4价碲,再用Na2S除杂,最后调节除杂后液pH,使碲以TeO2形式沉淀。
1 试验部分
1.1 试验原料及方法
试验料液为铜阳极泥分铜渣经超声强化氧化碱浸所得溶液,pH为13~14,溶液中各主要元素质量浓度见表1。

表1 分铜渣碱浸液中各主要元素质量浓度 mg/L
1.2 试验原理
(1)
还原后液中含有Cu2+、Pb2+等杂质。Cu2+、Pb2+易与S2-结合生成难溶MeS沉淀而被去除。PbS、CuS的Ksp[15]分别为1.3×10-28、6.3×10-36,而二硫化碲易溶于碱性含硫溶液[16],因此可采用Na2S作除杂剂。

(2)

(3)
(4)

(5)
(6)
25 ℃时各反应的平衡常数[17]K1=10-2.2,K2=10-5.03,K3=10-11.41。此时溶液中碲总浓度[Te(Ⅳ)]T计算公式为
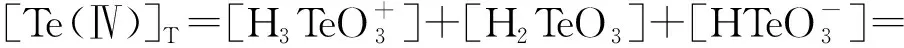
(7)
根据公式(5),绘制lg([Te(Ⅳ]T)-pH关系曲线,如图1所示。
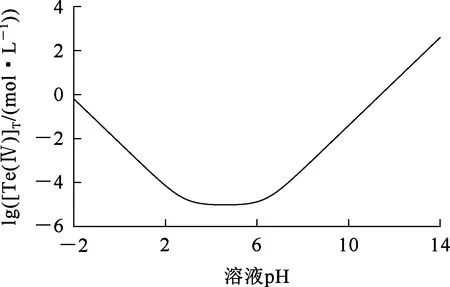
图1 25 ℃时lg([Te(Ⅳ)]T)-pH关系曲线
由图1看出:随溶液pH降低,溶液中+4价碲浓度下降,在pH为3~6时达最低,为10-5mol/L,即此时溶液中的碲基本水解完全;继续降低pH,溶液中碲浓度又有所提高,水解产生的碲沉淀物有部分溶解。因此,要使溶液中的碲尽可能多地沉淀,需控制水解pH为3~6。
2 试验结果与讨论
2.1 碱浸液的预还原
2.1.1 还原时间对预还原的影响
Na2SO3用量为理论用量的1.0倍,反应温度70 ℃,搅拌速度300 r/min,还原时间对碲还原的影响试验结果如图2所示。可以看出:随还原时间延长,碲还原率提高明显;但反应9 min后,再继续反应,碲还原率反而逐渐下降。随反应进行,溶液中生成的+4价碲与Na2SO3反应生成碲单质,导致溶液中+4价碲浓度降低。在反应时间为9 min时,碲还原率最高,为85.21%。
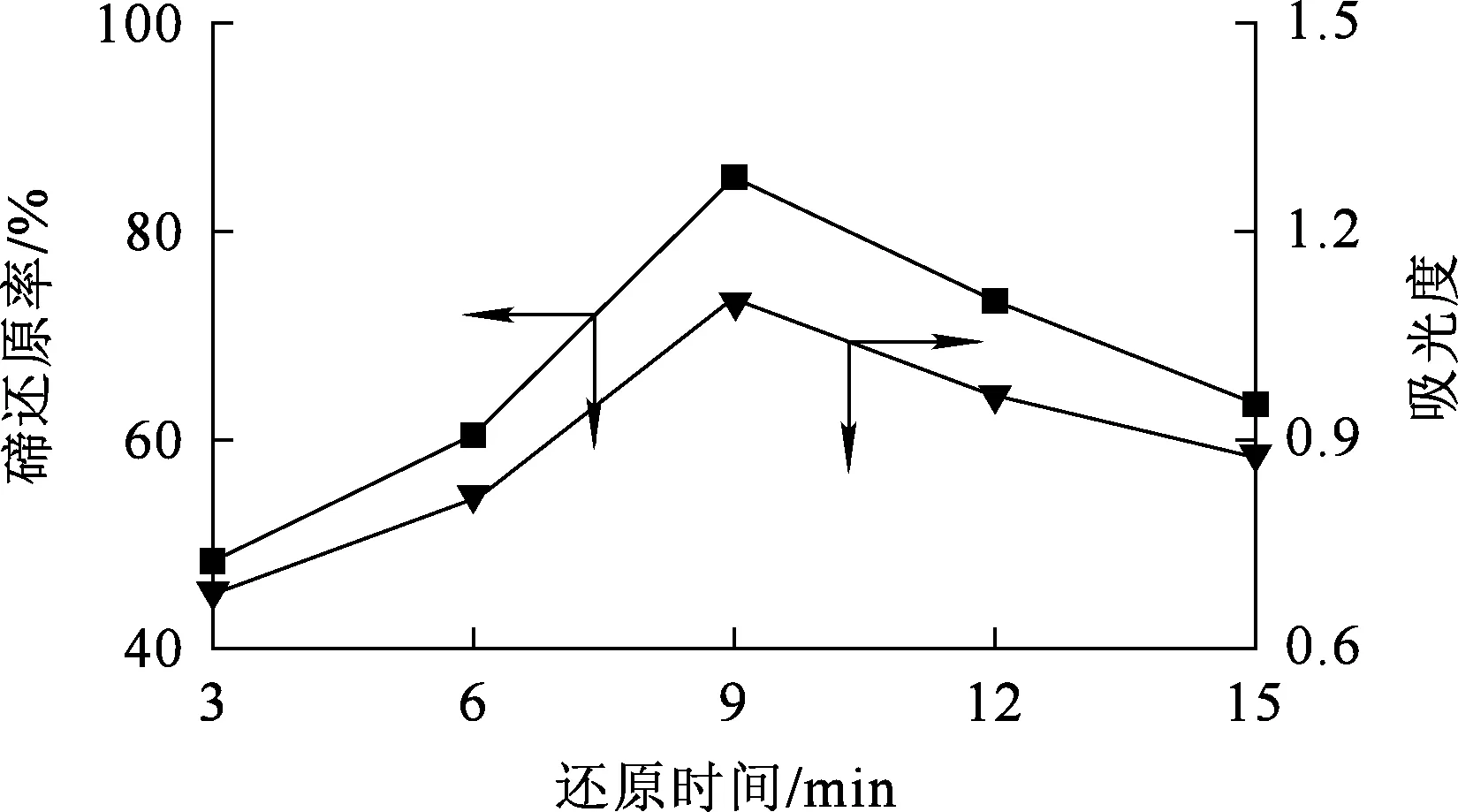
图2 还原时间对碲还原的影响
2.1.2 Na2SO3用量对预还原的影响
还原温度70 ℃,还原时间9 min,搅拌速度300 r/min,Na2SO3用量对碲还原的影响试验结果如图3所示。
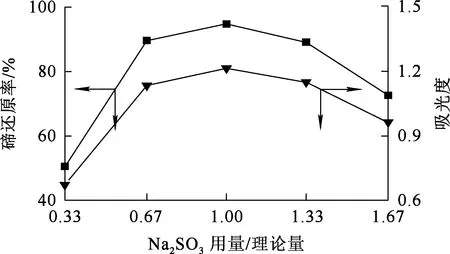
图3 Na2SO3用量对碲还原的影响
由图3看出:随Na2SO3用量增加,碲还原率呈先升高后下降趋势,Na2SO3用量为0.15 g即理论用量的1.0倍时碲还原率最高,为94.75%。这是由于随Na2SO3用量过量,已经被还原的+4价碲被还原为单质碲,致使溶液中+4价碲浓度下降。
2.1.3 还原温度对预还原的影响
Na2SO3用量为理论用量的1.0倍,还原时间9 min,搅拌速度300 r/min,反应温度对碲还原的影响试验结果如图4所示。可以看出:随还原温度升高,碲还原率逐渐提高;温度升至70 ℃时,碲还原率达最大,为92.27%; 但继续升温,碲还原率有所降低。随温度升高,溶液中的+4价碲与Na2SO3的反应加剧,使+4价碲被继续还原为碲单质,导致溶液中+4价碲浓度降低。
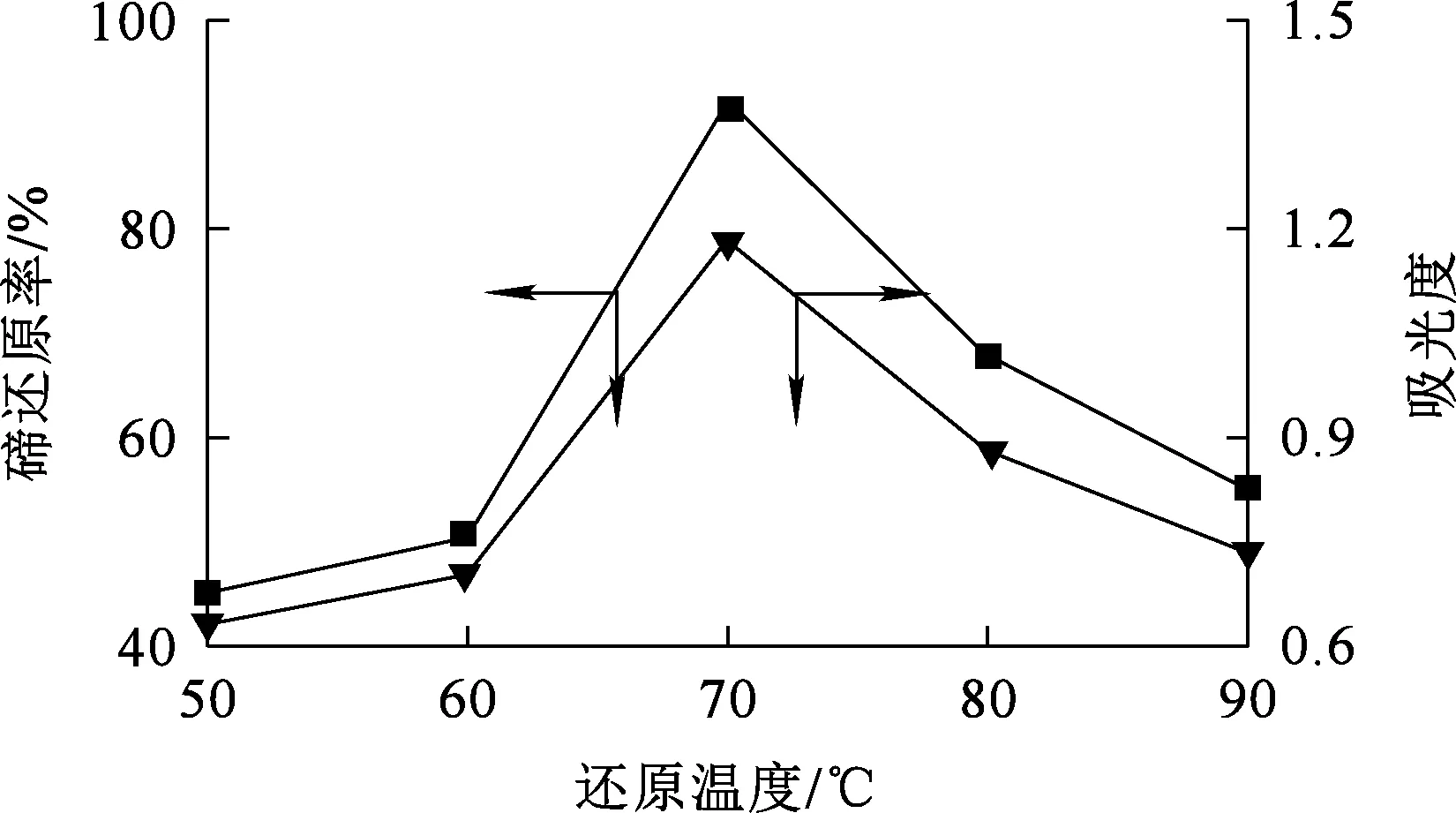
图4 还原温度对碲还原的影响
2.2 预还原后溶液的除杂
2.2.1 反应时间对脱除杂质的影响
Na2S用量为理论用量的1.0倍,反应温度70 ℃,搅拌速度300 r/min,反应时间对脱除杂质Pb2+、Cu2+的影响试验结果如图5所示。
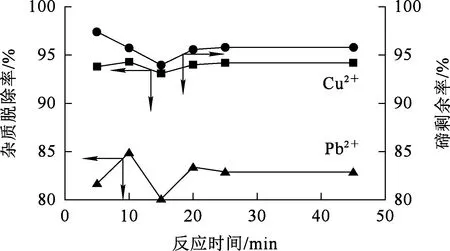
图5 反应时间对脱除杂质Pb2+、Cu2+的影响
由图5看出:反应10 min,溶液中Pb2+、Cu2+脱除率达最大;随反应进行,杂质脱除率略有降低之后保持稳定;溶液中的碲则随反应时间延长先略有降低后趋于稳定。反应初期,部分+4价碲与Na2S反应被还原为碲单质,导致溶液中+4价碲浓度降低。反应时间为10 min时,杂质脱除率较高且碲损失较少。
2.2.2 Na2S添加量对脱除杂质的影响
反应时间10 min,反应温度70 ℃,搅拌速度300 r/min,Na2S添加量对脱除杂质Pb2+、Cu2+的影响试验结果如图6所示。可以看出:Na2S添加量低于理论量的1.0倍时,随Na2S添加量增加,Pb2+脱除率提高明显,之后随Na2S添加量增加,Pb2+脱除率提高幅度不大;Cu2+脱除率随Na2S添加量增加略有提高,之后保持稳定;溶液中碲浓度则呈下降趋势。溶液中的碲与过量的Na2S反应会生成单质碲,为取得较高的Pb2+、Cu2+脱除率及较低的碲损失率,确定Na2S用量以理论量的1.0倍为宜。
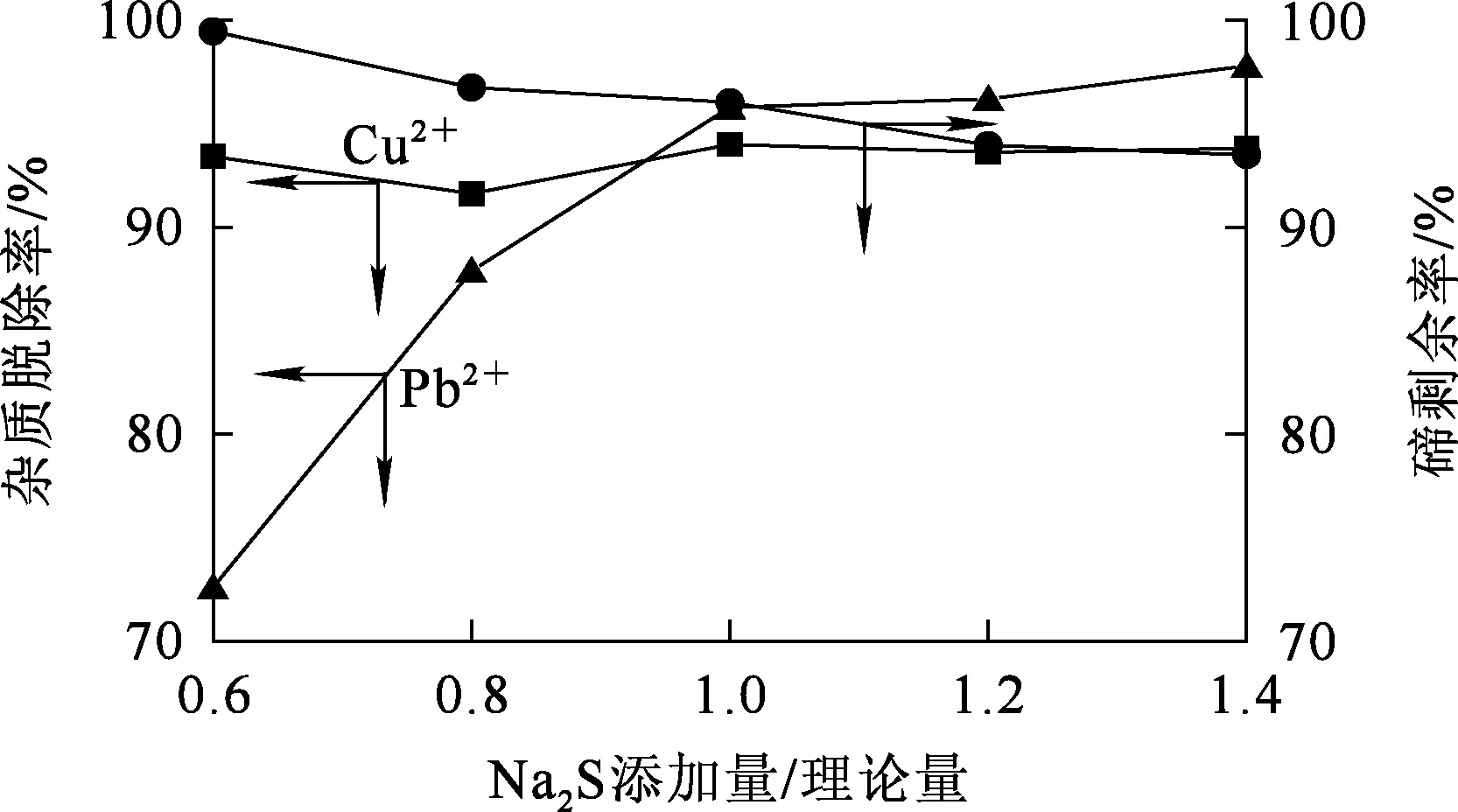
图6 Na2S添加量对脱除杂质Pb2+、Cu2+的影响
2.2.3 反应温度对脱除杂质的影响
反应时间10 min,Na2S用量为理论量的1.0倍,搅拌速度300 r/min,反应温度对脱除杂质Pb2+、Cu2+的影响试验结果如图7所示。
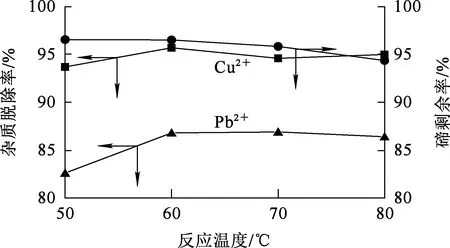
图7 反应温度对脱除杂质Pb2+、Cu2+的影响
由图7看出:随反应温度升高,Pb2+、Cu2+脱除率仅小幅升高后趋于稳定;溶液中碲浓度则在温度高于70 ℃后略有下降。随温度上升,溶液中的部分碲与Na2S反应,+4价碲被还原为单质碲,导致溶液中+4价碲浓度略有降低。综合考虑,确定温度以60 ℃为宜,此条件下,Pb2+、Cu2+脱除率较高分别为86.8%、95.7%,而碲损失较少。
2.3 除杂后液水解沉淀碲
2.3.1 水解时间对碲水解的影响
调节水解终点溶液pH为4左右,水解温度90 ℃,搅拌速度300 r/min,水解时间对碲水解的影响试验结果如图8所示。可以看出:水解时间小于10 min时,碲水解率提高较快,水解10 min时,碲已基本水解完全,水解率为98.16 %;继续水解,碲水解率基本保持稳定不再变化。
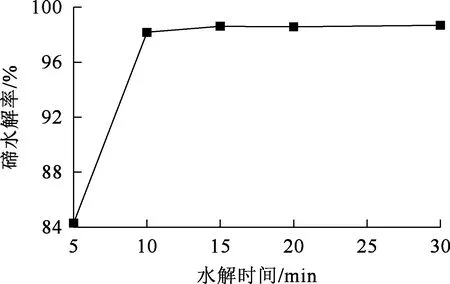
图8 水解时间对碲水解的影响
2.3.2 水解温度对碲水解的影响
水解时间10 min,水解终点溶液pH为4左右,搅拌速度300 r/min,水解温度对碲水解的影响试验结果如图9所示。
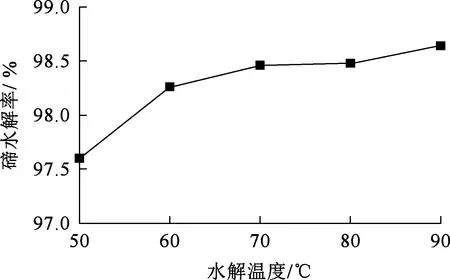
图9 水解温度对碲水解的影响
由图9看出,温度从50 ℃升至90 ℃,碲水解率提高幅度不大,表明温度对碲的水解影响较小。但温度升高有助于沉淀物颗粒长大,方便后续过滤,因此确定水解温度以90 ℃为宜。
2.3.3 水解终点溶液pH对碲水解及TeO2纯度的影响
水解时间10 min,水解温度90 ℃,搅拌速度300 r/min,溶液终点pH对碲水解及TeO2纯度的影响试验结果如图10所示。
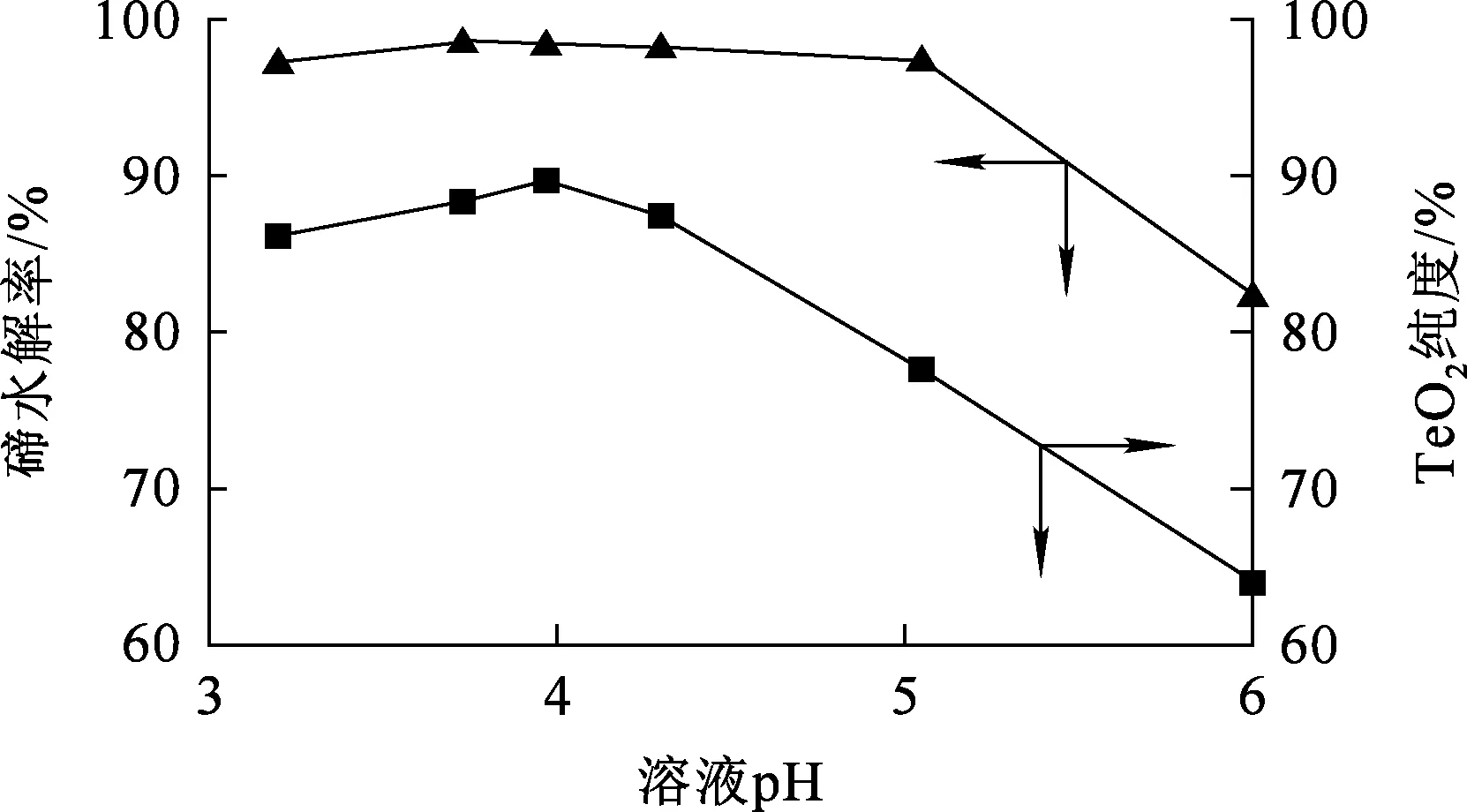
图10 水解终点溶液pH对碲水解及TeO2纯度的影响
由图10看出:随水解终点溶液pH降低,碲水解率提高明显,并在溶液终点pH为4左右达最大,为98.44%;终点pH继续降低,则碲水解率下降。这是由于水解产物TeO2会溶于强酸,此结果与前面的理论分析结论基本一致。为得到较多的碲沉淀物应控制水解终点溶液pH为4左右。
最佳条件下获得的碲水解产物经过滤、烘干,并进行XRD、SEM-EDS分析,结果如图11~13所示。可以看出:水解产物主要是TeO2,颗粒大小不一,纯度为89.69 %。
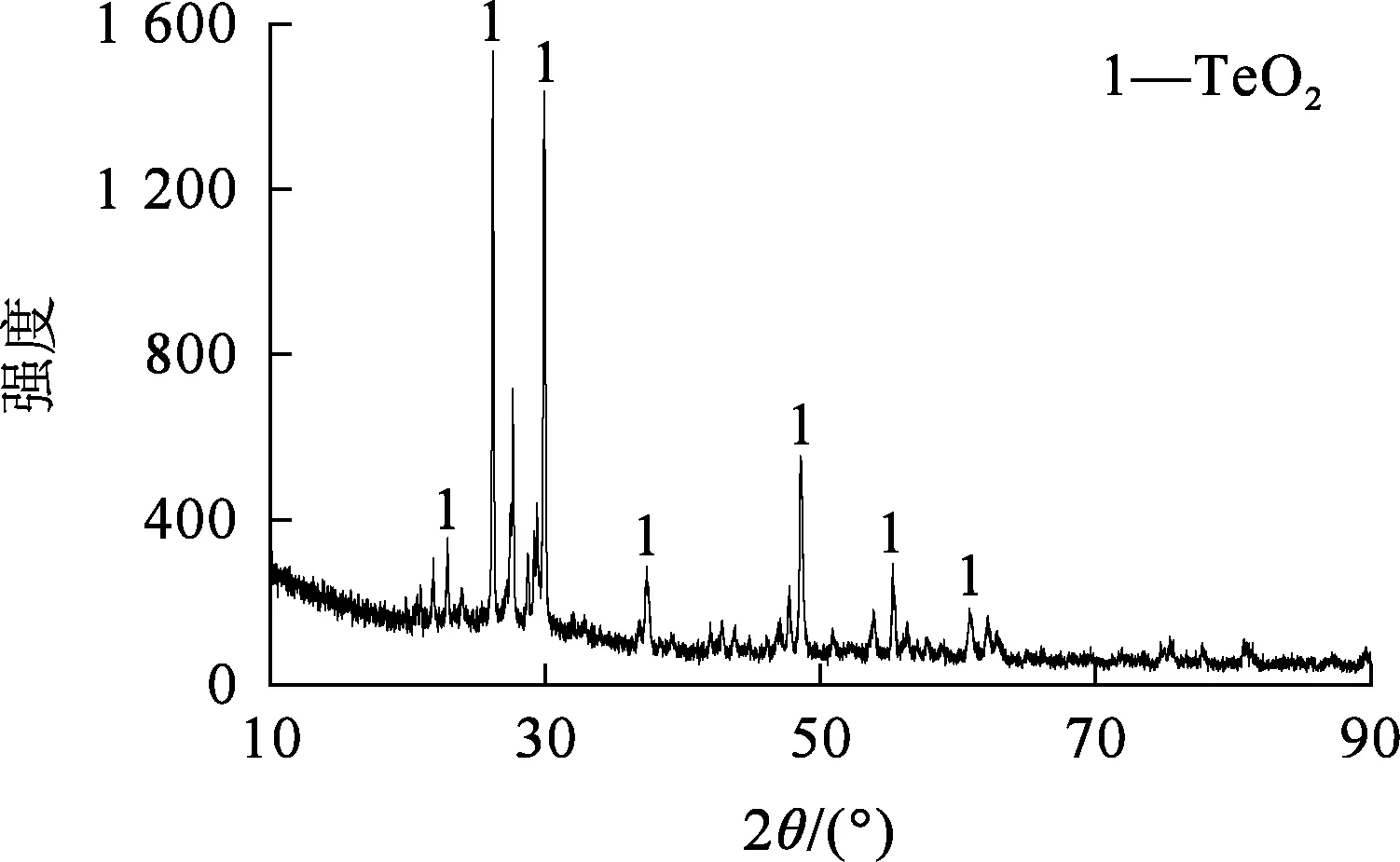
图11 水解产物的XRD图谱
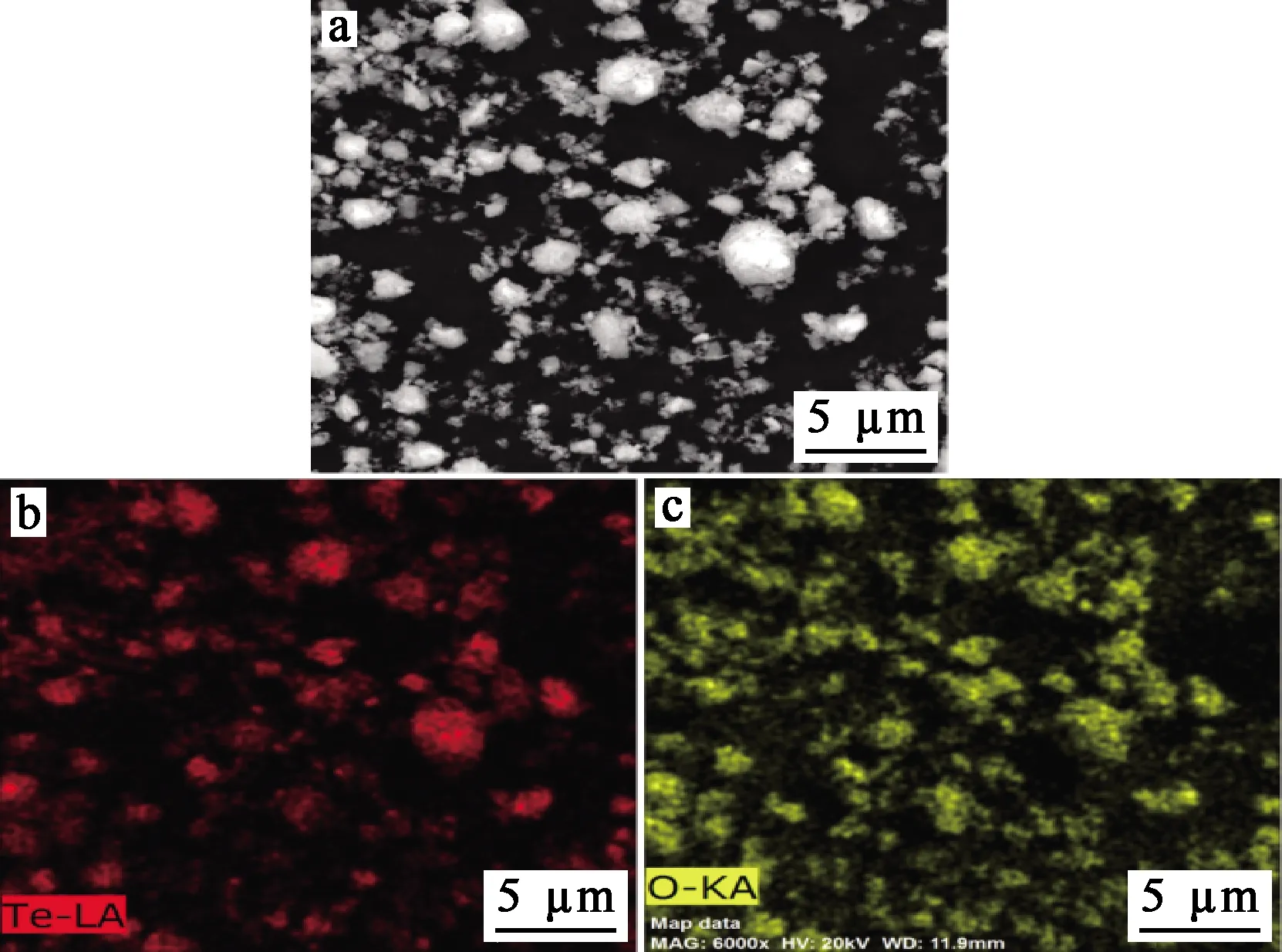
a—水解产物SEM形貌(6 000倍);b—Te元素面扫;c—O元素面扫。图12 水解产物的SEM形貌及面扫描
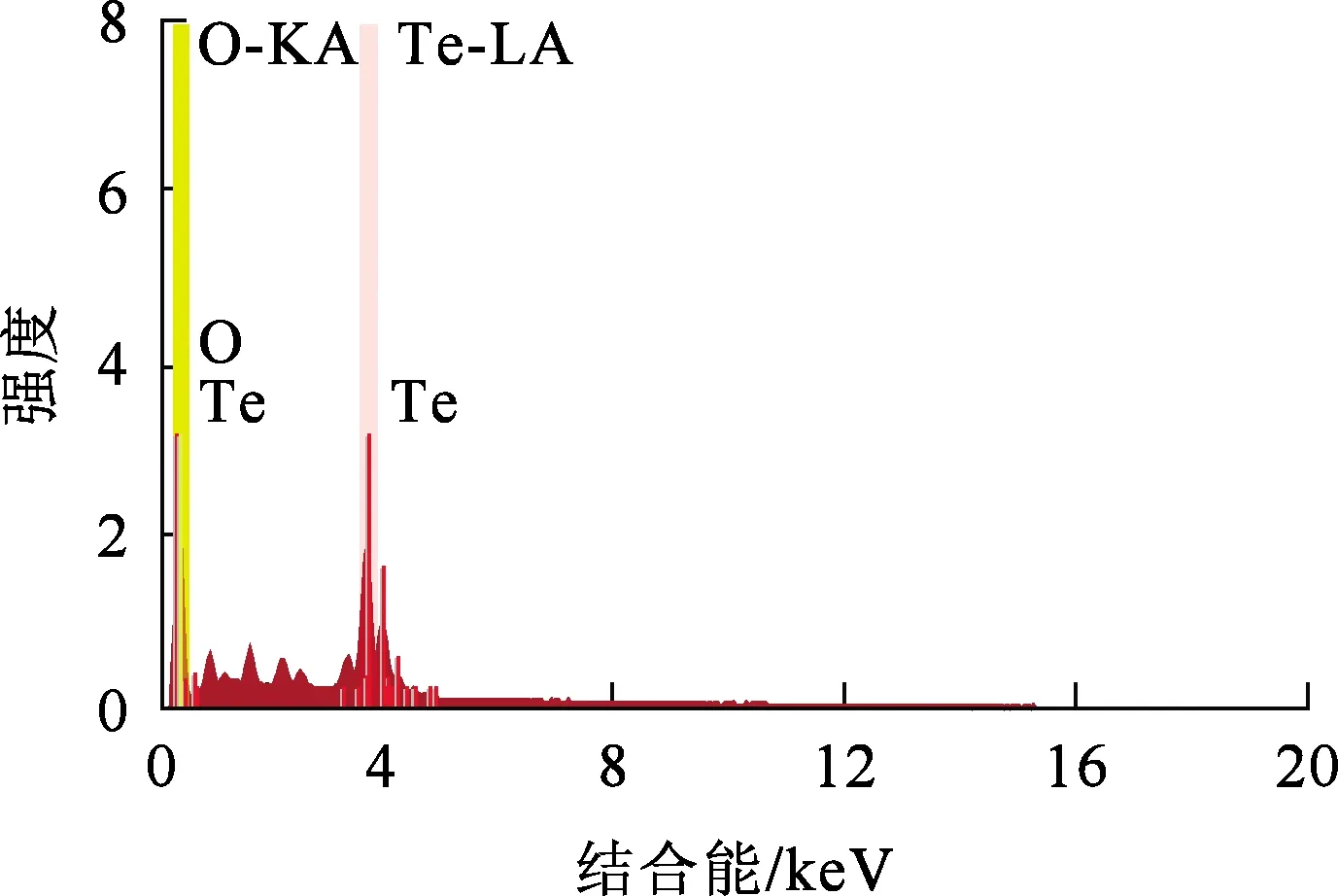
图13 水解产物的EDS分析结果
3 结论
对铜阳极泥分铜渣超声强化氧化碱浸所得含碲溶液,先进行预还原,再对还原后液除杂、调终点pH进行水解,最终获得TeO2粉末。适宜条件下,碲还原率为92.27%,Pb2+、Cu2+脱除率86.8%、95.7%,碲水解率达98.44%,所制得TeO2粉末纯度为89.69%。
