二氧化硅表面化学镀银研究
2021-04-06吴明阳谭晓明熊航行
陈 勇,吴明阳,谭晓明,熊航行,冯 靖,朱 琼
二氧化硅表面化学镀银研究
陈 勇1, 2,吴明阳1,谭晓明1,熊航行1,冯 靖1,朱 琼3
(1. 荆楚理工学院 化工与药学院,湖北 荆门 448000;2. 荆门化工绿色技术研究院,湖北 荆门 448000;3. 湖北本心环保科技有限公司,武汉 430074)
通过二氧化硅(SiO2)表面硅烷偶联剂改性,继续以聚甲基吡咯烷酮(PVP)为稳定剂,银氨溶液为银源,葡萄糖与甲醛为二元还原剂,对SiO2表面化学镀银工艺进行了研究。最佳镀银工艺条件为:当AgNO3/SiO2质量比为1:1,葡萄糖浓度为0.1 g/mL,反应温度为30℃,反应溶液pH值为13.5,能够获得较高导电率的SiO2镀银(SiO2-Ag)复合粒子,最高导电率为2564 S/cm。使用红外光谱、X射线衍射、热重分析和偏光显微镜等表征产物的物化性能,结果表明:PVP参与化学镀银反应,使SiO2-Ag的热失重变大。基于实验结果探讨了二氧化硅化学镀银的反应机理。
二氧化硅;硅烷偶联剂改性;化学镀银;导电性能
SiO2因其具有较大的比表面积,良好的生物相容性,低廉的成本等优点被广泛应用于催化[1]、分离[2]、生物医学[3]和复合材料[4]等领域。银是导电性最好的金属,氧化银同样具有导电性,而且具有极高的化学稳定性[5]。银粉在导电胶粘剂[6]、太阳能和触摸屏导电银浆[7-8]、电磁屏蔽材料[9]和抗菌材料[10]中均有广泛应用。由于银是一种贵金属,昂贵的成本使其在应用中受到限制。因此制备镀银产品代替纯银产品是一种性价比较高的方法,同时由于镀银产品的复合材料特性使其具备纯银未具有的性能。SiO2化学镀银的方法较多,有机械化学改性[11]、化学气相沉积[12]、沉淀法[13]、表面种子法[14]、层层自组装法[15]等。这些方法制备的SiO2导电填料一般都存在银壳层包覆不均匀,Ag与SiO2结合力差,电性能不佳等问题。通过还原剂化学镀银是一种比较简单可靠的镀银方法。
本课题组此前使用分散聚合法制备聚甲基丙烯酸甲酯微球,在其表面覆银得到PMMA-Ag微球[16]。本文采用两步法,先在SiO2表面接枝巯基丙基三甲氧基硅烷偶联剂,然后对改性后的SiO2进行表面化学镀银,以提高SiO2复合粒子的导电性能。通过红外光谱,X射线衍射,热失重仪和偏光显微镜测试SiO2镀银的物化性能,探讨SiO2镀银的机理。
1 实验部分
1.1 试剂及仪器
SiO2(平均粒径100 μm),广州亿峰化工科技有限公司;巯基丙基三甲氧基硅烷,分析纯,武汉克米克生物医药技术有限公司;硝酸银(AgNO3)、聚乙烯吡咯烷酮(PVP,K-30)、氨水(25%)、葡萄糖、甲醛、氢氧化钠和无水乙醇等均为市售分析纯试剂。
四探针电阻率测试仪(RTS-8),广州四探针科技公司;X射线衍射仪(X’Pert PRO),荷兰PANalytical公司;红外光谱仪(Nicolet iS50型),美国赛默飞世尔科技公司;热失重仪(TGA-2),瑞士梅特勒-托利多公司。
1.2 样品的制备
1.2.1 SiO2表面巯基化改性(SiO2-MS)
称取2.0 g SiO2,放入单口烧瓶中,然后加入60.0 g巯基丙基三甲氧基硅烷-乙醇溶液(巯基丙基三甲氧基硅烷与乙醇质量比为1:30),在70℃水浴中回流搅拌4 h。样品冷却后经过过滤,用乙醇清洗3次之后,在真空烘箱中,60℃干燥24 h备用。
1.2.2 SiO2表面包银(SiO2-Ag)
称取2.0 g SiO2-MS于500 mL的三口烧瓶中,加入60.0 g PVP-乙醇溶液(PVP与乙醇质量比为1:30),超声分散均匀。配制银氨溶液(40 mL,AgNO3溶液+一定体积氨水),加入到三口烧瓶中,用0.1 mol/L NaOH溶液将反应体系的pH值调节到13.5。然后将反应体系移至水浴锅中加热,控制反应体系温度为30℃,调节转速为400 r/min。再向恒压漏斗中加入葡萄糖溶液,调节滴速控制在1.5 秒一滴,使其缓慢进行还原反应。待葡萄糖溶液(一定体积)全部滴加完毕后,继续滴加甲醛溶液(一定体积)。甲醛溶液滴加完毕后,停止反应,离心分离。样品用蒸馏水洗涤3次,将得到的样品置于真空干燥箱中,60 ℃干燥24 h,得到SiO2镀银复合粒子。
1.3 表征测试
称取约100 mg样品,在压片机上压制(10 MPa,5 min)成直径为10 mm的薄片,用四探针电阻率测试仪测试样品导电率。将产物分散在乙醇溶液中,取少量溶液滴在载玻片表面,待自然挥发干后,使用偏光显微镜观察样品形貌。用溴化钾压片法在红外光谱仪上测试样品红外光谱图。将样品直接压片,用XRD测试产物的XRD图谱(测试过程选用Cu靶的K射线,工作电压40 kV,工作电流40 mA,扫描角度(2)范围10°~90°,步长0.017°/s)。称取约10 mg样品,在氮气保护下,用热失重仪测试样品的耐热性能,测试温度范围30℃~500℃,升温速率为10℃/min。
2 结果与讨论
2.1 样品制备的影响因素
2.1.1 AgNO3用量对SiO2表面化学镀银的影响
图1为AgNO3用量对SiO2镀银导电性能的影响。当AgNO3/SiO2的质量比小于1.0时,随着AgNO3用量增加,SiO2-Ag导电率增加,这是因为SiO2表面银的厚度增加。继续增加AgNO3用量时,SiO2-Ag导电率下降,由于过量的银离子使其发生自相成核形成纳米银原子,从而降低了SiO2-Ag的导电率,所以AgNO3/SiO2最佳质量比为1.0。

图1 AgNO3用量对SiO2-Ag的导电性能影响
2.1.2 葡萄糖浓度对SiO2表面化学镀银的影响
图2为葡萄糖浓度对SiO2-Ag导电性能影响。当葡萄糖浓度小于0.10 g/mL时,随着葡萄糖浓度的增加,SiO2-Ag导电率增加,这是因为SiO2表面生成了较多的银层,继续增加葡萄糖浓度,SiO2-Ag导电率下降,由于高浓度的葡萄糖使得反应速度过快,银离子来不及在SiO2表面成核反应而自相成核形成纳米银原子,所以降低了导电率。葡萄糖最佳浓度为0.10 g/mL。

图2 葡萄糖浓度对SiO2-Ag的导电性能影响
2.1.3 反应温度对SiO2表面化学镀银的影响
图3为反应温度对SiO2镀银的影响。当温度低于30℃时,随着温度升高,产物导电率增加,这是因为较低的温度使银离子还原速度较低,升高温度可以增加反应速度,SiO2表面还原的银逐渐增多。30℃之后,当继续增加温度,导电率下降,这是因为反应温度过高,银离子都在溶液中快速反应自相成核形成纳米银原子,而包覆到SiO2表面的银较少。所以最佳反应温度为30℃。
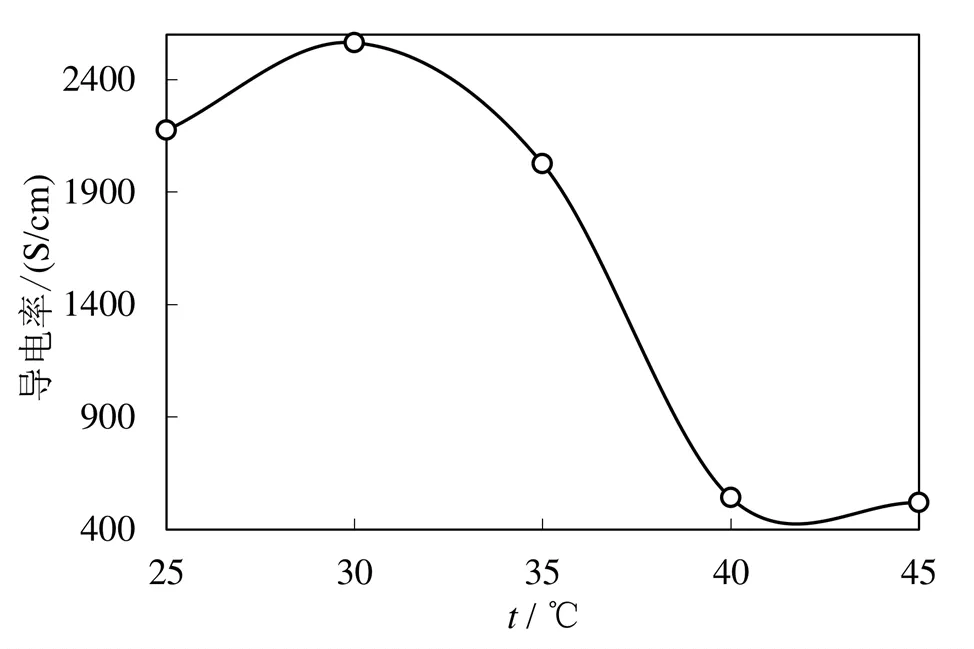
图3 反应温度对SiO2-Ag的导电性能影响
2.1.4 溶液pH值对SiO2表面化学镀银的影响
图4为溶液pH值对镀银的影响。银氨溶液为强碱性,当溶液中pH小于12.9时,由于溶解的银离子较小,所以在SiO2表面还原成银层较薄较少,SiO2-Ag导电率较小,SiO2包银的导电率为1449 S/cm,随着pH值升高,溶解在溶液中的银离子增加,SiO2-Ag导电率升高,当pH为13.5时,导电率最高为2000 S/cm,进一步升高pH时,过量的银离子快速反应容易自相成核形成纳米银原子,使得SiO2-Ag导电率下降,所以溶液最佳pH为13.5。
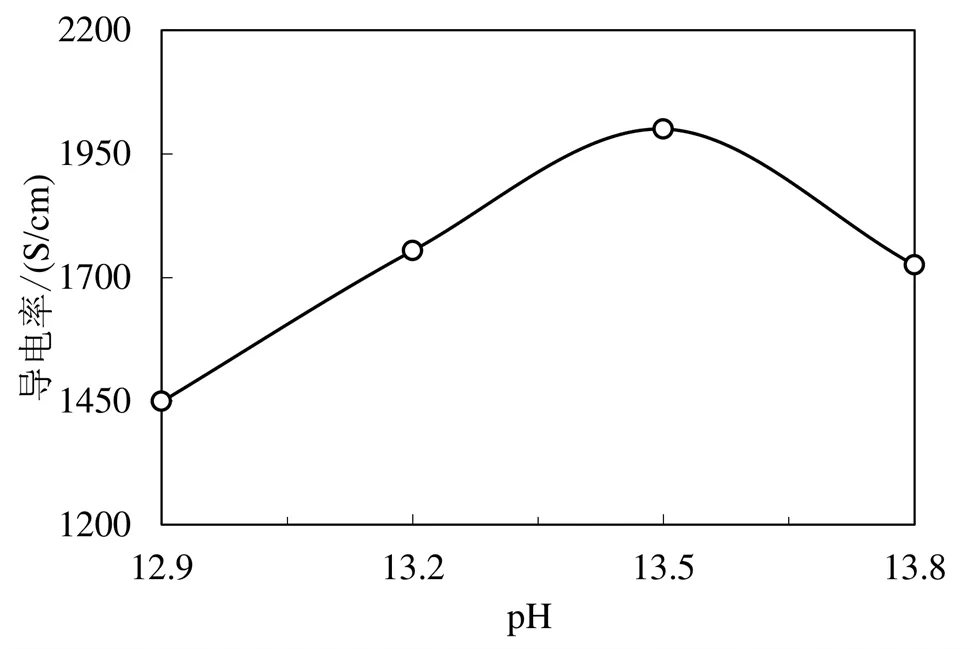
图4 溶液pH值对SiO2-Ag导电性能的影响
2.2 样品表征
2.2.1 红外光谱
图5为样品的红外光谱图。由SiO2的红外光谱曲线可知,在3438 cm-1处的宽峰是SiO2表面的结构水-OH反对称伸缩振动峰,827 cm-1处的尖峰属于Si-OH的弯曲振动吸收峰。SiO2通过硅烷偶联剂表面处理,SiO2表面的化学成分发生了变化。为了确定偶联剂分子是否与SiO2表面作用形成新的化学键,同时通过包银之后,某些化学键被单质银包覆。SiO2-MS红外光谱如图5所示,在3438 cm-1处为Si-OH的吸收峰,由-OH的伸缩振动引起。SiO2-MS多了2356 cm-1和1407 cm-1两个峰,为-SH和-C-SH的伸缩振动峰,同时3438 cm-1宽峰变弱,是由于R-Si-SH接到SiO2的表面,掩盖了-OH的伸缩振动峰。SiO2-Ag的红外光谱中3438 cm-1宽峰消失,827 cm-1峰变弱,证明银覆盖在SiO2的表面。

图5 红外光谱图
2.2.2 X射线衍射
图6为样品的X射线衍射图。SiO2为一种片形晶体结构,X射线衍射测试出现了4个衍射峰(21.0°、36.7°、50.3°、68.4°),与偏光显微镜测试的片形结构相对应。SiO2-Ag总共出现5个衍射峰(38.2°、44.3°、64.5°、77.4°和81.6°),与标准晶态银卡片(JCPDS File04-0783)的(111)、(200)、(220)、(311)和(222)的峰是一致的,可确定SiO2表面的银呈面心立方晶体结构。XRD图谱中未出现其它杂质的衍射峰,尤其是未检出Ag2O衍射峰,表明无其他可检出物相存在。
2.2.3 热失重分析
图7为样品在氮气气氛的热失重曲线。SiO2从室温升温到500℃,残留重量为99.35%,当用偶联剂改性SiO2生成SiO2-MS,从室温加热到500℃,残留总量为98.35%,这是由于包覆在SiO2表面的偶联剂为有机物,高温下容易分解。SiO2-Ag的热失重曲线可知,在500℃残留的质量为90.66%,这是由于在银离子化学反应还原到SiO2表面时,PVP作为稳定剂参与了化学反应,由于PVP是一种高分子,同时跟银一起沉积在SiO2表面,所以造成高温加热SiO2-Ag时,质量损失较大。
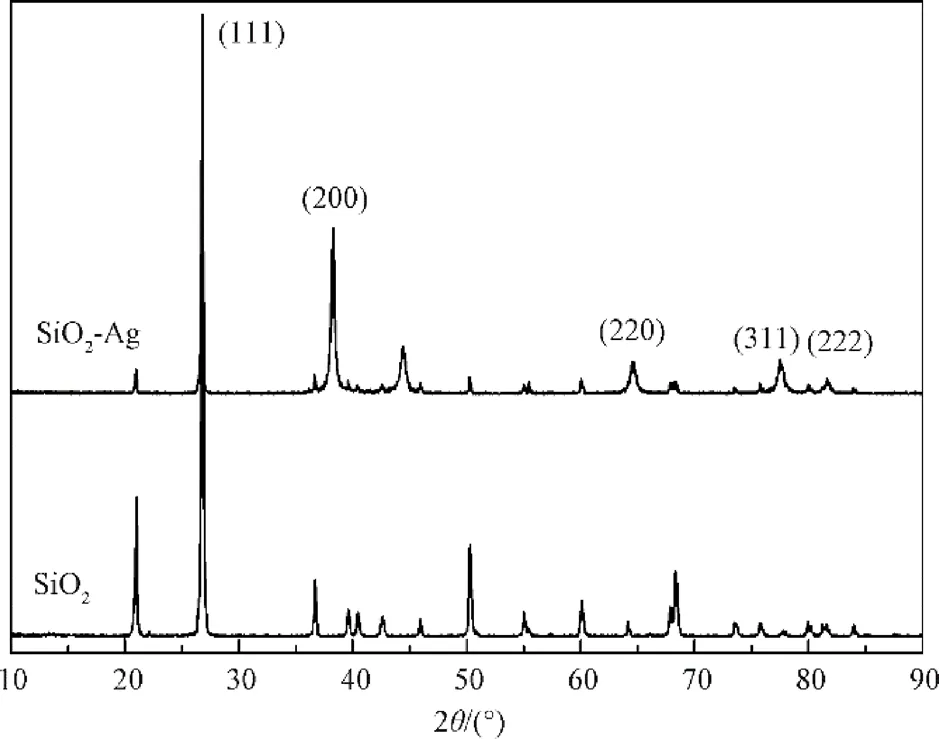
图6 X射线衍射图

图7 热失重图
2.2.4 偏光显微镜测试
图8为SiO2和Ag-SiO2样品的偏光显微镜图。

图8 偏光显微镜图
图8(a)说明SiO2是一种半透明的片状固体,直径约为100 μm左右。图8(b)表明SiO2-Ag片的直径大于100 μm,颜色为黑色,由于银层较厚,表现为一种不透明的晶体。SiO2-Ag体系中看不到微小的颗粒,说明银发生的自相成核形成的单质银较少,证明了银氨溶液中的银被还原到SiO2表面。
2.3 二氧化硅表面化学镀银反应机理探讨
图9为SiO2表面化学镀银反应机理图。

图9 SiO2-Ag反应机理图
Fig 9. The reaction mechanism of SiO2-Ag
图9中,SiO2表面为无机的界面,与银原子的吸附较小,如果不使用偶联剂表面包覆改性,SiO2表面直接进行镀银时,SiO2-Ag的导电率只有253 S/cm。使用巯基硅烷偶联剂改性时,首先硅烷偶联剂与SiO2表面上的羟基反应,形成-SH共价键。同时,巯基硅烷分子的硅醇互相反应形成低聚物网状结构的膜,覆盖在SiO2表面,使无机颗粒表面有机化。在PVP高分子稳定剂作用下,以银氨溶液为银源,银离子与SiO2表面的-SH键合,继续与葡萄糖和甲醛二元还原剂进行化学反应,在SiO2表面化学镀银,形成核壳粒子,提高了SiO2的导电性能。
3 结论
1) 制备条件实验表明,SiO2经过巯基偶联剂改性后,以银氨溶液作为银源,PVP作为稳定剂,葡萄糖和甲醛作为二元还原剂进行化学镀银反应,当AgNO3/ SiO2质量比为1:1,葡萄糖浓度为0.1 g/mL,反应温度为30℃,溶液pH值为13.5,SiO2-Ag的最高导电率为2564 S/cm。
2) 对样品的分析表征表明,通过FTIR,XRD,TGA和偏光显微镜测试样品物化性能,证明了SiO2表面发生了化学镀银反应。该SiO2-Ag具有制备简单、成本低、导电率高等优点,有望在光学、电学、抗菌和电磁屏蔽等诸多领域都有潜在应用前景。
3) 机理探讨认为,巯基偶联剂首先与银离子结合,PVP作为稳定剂防止还原反应自相成核聚集,使用葡萄糖和甲醛二元还原剂,能够控制反应速度和提高还原反应的转化率,提高SiO2-Ag导电性能。
[1] ARIMIK B, GHAFFARI B, VALI H. Synergistic catalysis within core-shell Fe3O4@SiO2functionalized with triethylene glycol (TEG)-imidazolium ionic liquid and tetramethylpiperidine N-oxyl (TEMPO) boosting selective aerobic oxidation of alcohols [J]. Journal of Colloid and Interface Science, 2020, 589: 474-485.
[2] QIAN H, LI W Y, WANG X, et al. Simultaneous growth of graphene/mesoporous silica composites using liquid precursor for HPLC separations [J]. Applied Surface Science, 2020, 537: 148101.
[3] DULSKI M, GAWECKI R, SUOWICZ S, et al. Key properties of a bioactive Ag-SiO2/TiO2coating on NiTi shape memory alloy as necessary at the development of a new class of biomedical materials [J]. International Journal of Molecular Sciences, 2021, 22(2): 507: 2-17.
[4] CHEN L P, REN Z Y, LIU X M, et al. Infrared-visible compatible stealth based on Al-SiO2nanoparticle composite film [J]. Optics Communications, 2020, 482: 126608.
[5] WANG X, GUO J, HU L. Preparation and application of gallium-based conductive materials in the very recent years [J]. Science China Technological Sciences, 2020, 64(4): 681-695.
[6] CHOI H W, SEONG D G, PARK J S. Conductive adhesive electrode exhibiting superior mechanical and electrical properties for attachable electrochromic devices [J]. Organic Electronics, 2020, 87: 1-7.
[7] SINGH P, NAUTIYAL V K, SINGH N, et al. Study of the effective surface plasmon in a nano-composite of silver nanoparticles with a host ZrO2in one-dimensional ternary periodic structure for solar cell application [J]. Physica Scripta, 2021, 96(2): 1-14.
[8] WU C C. Ultra-high transparent sandwich structure with a silicon dioxide passivation layer prepared on a colorless polyimide substrate for a flexible capacitive touch screen panel [J]. Solar Energy Materials and Solar Cells, 2020, 207: 1-8.
[9] LIM G H, KWON N Y, HAN E J, et al. Flexible nanoporous silver membranes with unprecedented high effectiveness for electromagnetic interference shielding [J]. Journal of Industrial and Engineering Chemistry, 2020, 93: 245-252.
[10] PHAM N B T, LE V K T, BUI T T T, et al. Improved synthesis of Ag/SiO2colloidal nanocomposites and their antibacterial activity against ralstonia solanacearum 15 [J]. Journal of Nanoscience and Nanotechnology, 2021, 21(3): 1598-1605.
[11] BOGATYROV V M, GUN’KO V M, GALABURDA M V, et al. The effect of photoactivated transformations of Ag+and Ag0in silica fillers on their biocidal activity [J]. Research on Chemical Intermediates, 2019, 45(8): 3985-4001.
[12] LIU J D, LIU Z W, CHEN Z Q, et al. Thermal diffusion and epitaxial growth of Ag in Ag/SiO2/Si probed by XRD, depth-resolved XPS, and slow positron beam [J]. Applied Surface Science, 2019, 496: 1-5.
[13] MENAZEA A A, ABDELGHANY A M, HAKEEM N A, et al. Nd: YAg nanosecond laser pulses for precipitation silver nanoparticles in silicate glasses: AC conductivity and dielectric studies [J]. Silicon, 2019, 12(1): 13-20.
[14] PHAM X H, HAHM E, HUYNH K H, et al. Sensitive and selective detection of 4-aminophenol in the presence of acetaminophen using gold-silver core-shell nanoparticles embedded in silica nanostructures [J]. Journal of Industrial and Engineering Chemistry, 2019, 83: 208-213.
[15] ZHANG L, LIU Y, LI L, et al. High-performance flexible transparent conductive films enabled by a commonly used antireflection layer[J]. ACS Applied Materials & Interfaces, 2020, 13(2): 2979-2987.
[16] 陈勇, 谭晓明, 熊航行, 等. 聚甲基丙烯酸甲酯微球表面镀银的研究[J]. 贵金属, 2020, 41(1): 37-42.
CHEN Y, TAN X M, XIONG H X, et al. Study on silver plating on the surface of PMMA microspheres [J]. Precious Metals, 2020, 41(1): 37-42.
Study on silver plating on the surface of silicon dioxide
CHEN Yong1, 2, WU Ming-yang1, TAN Xiao-ming1, XIONG Hang-xing1, FENG Jing1, ZHU Qiong3
(1. College of Chemical Engineering and Pharmacy, Jingchu University of Technology, Jingmen 448000, Hubei, China;2. Jingmen Green Chemical Technology Research Institute, Jingmen 448000, Hubei, China;3. Hubei Benxin Environmental Protection Hi-tech Co. Ltd., Wuhan 430074, China)
Silicon dioxide (SiO2) surface was modified by silane coupling agent, then the electroless silver plating process was studied with polymethylpyrrolidone (PVP) as stabilizer, silver ammonia solution as silver source, glucose and formaldehyde as binary reducing agent. The optimal silver plating process conditions were obtained as follows: the mass ratio of AgNO3/SiO2was 1:1, the concentration of glucose was 0.1 g/mL, the reaction temperature was 30℃ and the pH value of the reaction solution was 13.5. The results showed that SiO2-Ag composite particles can be obtained with the highest conductivity 2564 S/cm. The physicochemical properties of SiO2-Ag were characterized by infrared spectrometer, X-ray diffractometer, thermogravimetry and polarizing microscope, and the results showed that PVP participated in the electroless silver plating reaction, which made the thermogravimetry of SiO2-Ag increased. The mechanism of electroless silver plating on SiO2was discussed based on the experimental results.
SiO2; silane coupling agent modification; electroless silver plating; conductivity
TB383.1;O614.122
A
1004-0676(2021)04-0055-06
2021-02-03
湖北省教育厅科学研究项目(B2020198);荆楚理工学院科研项目(ZD202106);荆门市科技局项目(2018YFYB048);荆楚理工学院教育教学研究项目(JX2018-024);湖北省大学生创新创业训练项目(202011336022/202011336023);荆楚理工学院大学生创新创业训练项目(KC2021029)
陈 勇,男,博士,讲师,研究方向:纳米、高分子复合、绿色化工和环境功能材料。E-mail:chenyong3089@126.com
