穿心莲内酯对脓毒症大鼠急性心肺组织损伤和炎症反应的影响*
2021-04-06杨敏华姚友杰王娟陈亚奇刘高仁王森
杨敏华,姚友杰,王娟,陈亚奇,刘高仁,王森
(1.河南中医药大学第二附属医院/河南省中医院急诊内科,郑州 450002;2.郑州大学第一附属医院心内科,郑州 450052;3.河南中医药大学康复学院,郑州 450008)
脓毒症(spesis)是重症监护病房死亡发生的主要原因之一,主要表现为炎症递质大量释放、弥漫性血管内凝血及内皮细胞功能障碍[1]。其中,心脏和肺脏是脓毒症侵犯的常见靶器官,也是造成脓毒症患者死亡的主要原因[2]。脓毒症发生时,伴随着大量炎症细胞浸润,致使促炎-抗炎动态平衡被打破。目前,对脓毒症的治疗主要以控制炎症反应、减轻脏器损伤为主。穿心莲内酯(andrographolide,AG)是从植物穿心莲叶片中提取得到的一种二萜内酯,具有抗病毒、抗炎抗菌、保肝、抗肿瘤、抗氧化和增强免疫等[3-7],在治疗关节炎、神经炎、椎间盘退变等炎症性疾病中已得到广泛应用[8-11]。已有研究表明AG可用于治疗脓毒症[12-14],但AG对脓毒症的具体作用机制尚不清楚。因此,本文用脂多糖诱导建立脓毒症模型大鼠,探讨AG对模型大鼠的心、肺组织损伤和炎症反应的作用及其机制。
1 材料与方法
1.1实验动物 无特定病原体(SPF)级、雄性、8~10周龄、SD大鼠60只,体质量(260.7±21.5)g,购自北京维通利华公司,动物质量合格证号:SCXK(京)2014-0001,动物使用的伦理审批号:LLPZ-012。饲养温度26~28 ℃,相对湿度50%~60%,自由采食和饮水,适应性饲养7 d后进行实验,所有实验符合动物实验学的3R原则。
1.2试剂与仪器 AG粉末购自美国Sigma公司,含量≥98%,批号:365645;利奈唑胺购自中国食品药品检定研究院,含量≥99%,批号:130640-201901,吡咯烷二硫代氨基甲酸酯(pyrrolidine dithiocarbamate,PDTC,购自美国Biovision公司,批号:1676-100);苏木精-伊红(HE)染色试剂盒(批号:D006-1-1)购自南京建成生物工程研究所;酶联免疫吸附测定(ELISA)试剂盒购自美国RB公司;TRIzol试剂盒(批号:15596026)购自美国ThermoFisher公司;BCA蛋白定量试剂盒(P0012S)购自上海碧云天生物技术研究所;抗体购自英国Abcam公司;电化学发光(ECL)化学发光液(批号:WP20005)购自美国Invitrogen公司。聚合酶链反应(PCR)仪、电泳仪及半干转膜仪购自美国伯乐公司;Gel View 6000凝胶成像系统购自广州云星仪器有限公司;多功能酶标仪购自瑞士TECAN公司。
1.3方法
1.3.1建模和分组给药 ①将大鼠随机分为6组,每组10只:正常对照组,模型对照组,AG小剂量、中剂量、大剂量组(LPS+AG 2.5 mg、LPS+AG 5 mg和LPS+AG 10 mg)组,利奈唑胺(linezolid,LNZ)组(LNZ 25 mg)。除正常对照组外,各组大鼠均腹腔注射LPS(10 mg·kg-1)复制脓毒症大鼠模型[15],造模后通过观察大鼠呼吸频率、皮温、心率、口鼻分泌物、精神状态等判断造模成功与否。AG小剂量、中剂量、大剂量组于造模后立即、8 h和16 h给予AG 2.5,5,10 mg·kg-1,利奈唑胺组给予利奈唑胺25 mg·kg-1,正常对照组和模型对照组给予等量0.9%氯化钠溶液。②另取大鼠随机分为5组:正常对照组、模型对照组、AG大剂量组(AG 10 mg)、PDTC+模型组(PDTC 50 mg)和PDTC+AG大剂量组。造模方法、给药方法、取材时间同上。造模24 h后处死大鼠,采样进行后续实验。
1.3.2肺湿/干重比值(W/D)测定 取各组大鼠肺脏,用磷酸盐缓冲液(PBS)充分洗净,吸去多余水分,称定质量,记为湿重(W)。用温箱在80 ℃条件下干燥48 h后,再次称定质量,记为干重(D)。W/D=(湿重-干重)/干重。
1.3.3HE染色检测心肺组织病理损伤 取各组心脏、肺脏用PBS充分洗净,10%中性甲醛固定,经常规脱水、透明、浸蜡和包埋过程,制成切片厚度4 μm。经过HE染色后,在光学显微镜下观察心脏、肺脏病理学改变。
1.3.4ELISA检测大鼠心肌损伤标记物和炎症细胞因子含量 取各组心肌组织适量,制成1:9匀浆液,4 ℃条件下3000 r·min-1×10 min(离心半径r=13.5 cm),收集上清液,严格按照试剂盒操作,测定心肌损伤标记物肌酸激酶同工酶(creatine kinase isoenzyme,CK-MB)、肌钙蛋白I(cardiac troponin I,cTnI)和肌红蛋白(myoglobin,Mb)含量。取各组大鼠眼眶静脉血,4 ℃条件下3000 r·min-1×10 min(离心半径r=13.5 cm),收集上清液,严格按照试剂盒操作,测定炎性细胞因子肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)、IL-6和巨噬细胞炎性蛋白-2(macrophage inflammatory protein-2,MIP-2)的含量。
1.3.5Western blotting检测心肺组织HMGB1、TLR4和NF-κB p65的蛋白表达水平 用RIPA蛋白裂解液提取各组心脏和肺脏总蛋白,用BCA法测定并调平蛋白浓度。每组取等量蛋白质用12%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)分离并转移至聚偏氟乙烯膜。用5%脱脂牛奶室温封闭蛋白质2 h,加入一抗(1:500),4 ℃孵育过夜。第2天弃去一抗,洗膜后,加入对应二抗(1:10 000),室温封闭1 h后,滴加发光液曝光显影。以GAPDH为内参。

2 结果
2.1AG对脓毒症大鼠心、肺组织病理损伤的影响 大鼠心肌组织HE染色结果如图1所示。正常对照组大鼠心肌组织未见明显病理变化,模型对照组大鼠可见心肌纤维排列紊乱、细胞核肿胀、部分心肌纤维断裂、炎性细胞增多等病理改变,AG中剂量、大剂量组和利奈唑胺组大鼠心肌组织中上述病理改变均有不同程度的改善。
大鼠肺脏组织HE染色结果如图1所示:正常对照组大鼠肺组织未见明显病理变化,模型对照组大鼠可见肺泡塌陷,肺泡壁厚度增加,大量炎性细胞浸润等病理学改变;AG中剂量、大剂量组和利奈唑胺组大鼠肺组织病理学改变均得到改善。
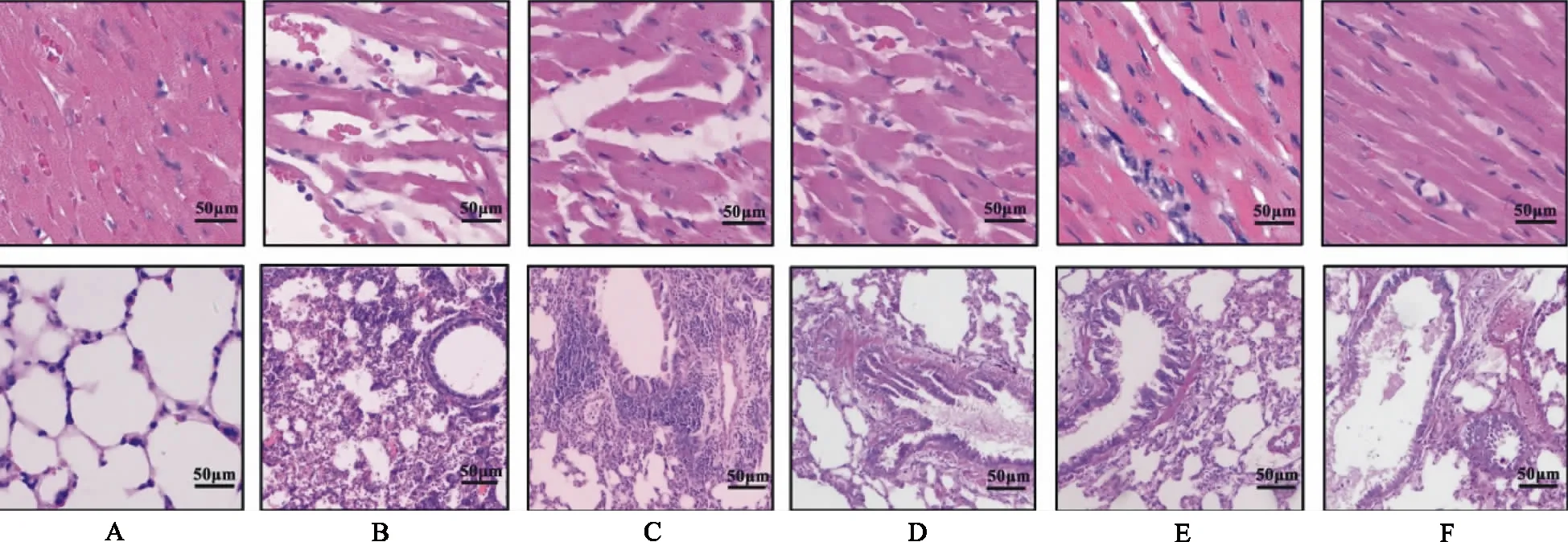
A.正常对照组;B.模型对照组;C.AG小剂量组;D.AG中剂量组;E.AG大剂量组;F.利奈唑胺组。
2.2AG对脓毒症大鼠心肌损伤标记物和肺脏W/D影响 ELISA检测各组心肌组织匀浆中心肌损伤标记物含量,结果见图2。与正常对照组比较,模型对照组大鼠心肌组织匀浆中CK-MB、cTnI和Mb含量显著增加(t=1.631,1.165,1.438,P<0.01);与模型对照组比较,AG治疗组上述指标均有不同程度的降低,其中AG中剂量、大剂量组降低程度差异有统计学意义(F=39.83,33.18,104.6,P<0.05或P<0.01)。
测定各组大鼠肺脏干燥前后两次质量,检测AG对脓毒症大鼠肺脏W/D的影响,结果见图2。与正常对照组比较,模型对照组大鼠肺脏W/D显著增加(t=4.744,P<0.01);与模型对照组比较,AG治疗组大鼠肺脏W/D均下降,其中AG中、大剂量组比值差异有统计学意义(F=38.11,P<0.05或P<0.01)。
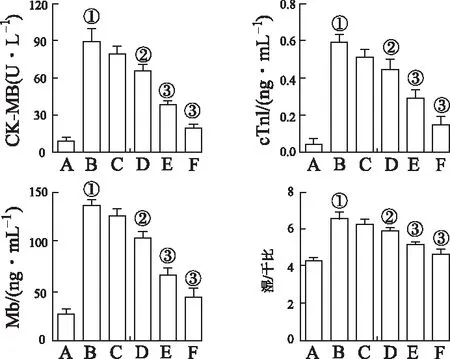
A.正常对照组;B.模型对照组;C.AG小剂量组;D.AG中剂量组;E.AG大剂量组;F.利奈唑胺组;①与正常对照组比较,P<0.01;②与模型对照组比较,P<0.05,③与模型对照组比较,P<0.01。
2.3AG对脓毒症大鼠炎症因子表达的影响 ELISA检测大鼠血清中炎症因子表达水平,结果如图3所示:与正常对照组比较,模型对照组大鼠的TNF-α、IL-1β、IL-6和MIP-2血清表达水平显著上调(t=1.513,1.936,1.399,1.527,P<0.01);与模型组比较,AG治疗组中上述指标表达水平均明显下调,且AG中剂量、大剂量组差异有统计学意义(F=80.93,8.498,38.38,13.99,P<0.05或P<0.01)。
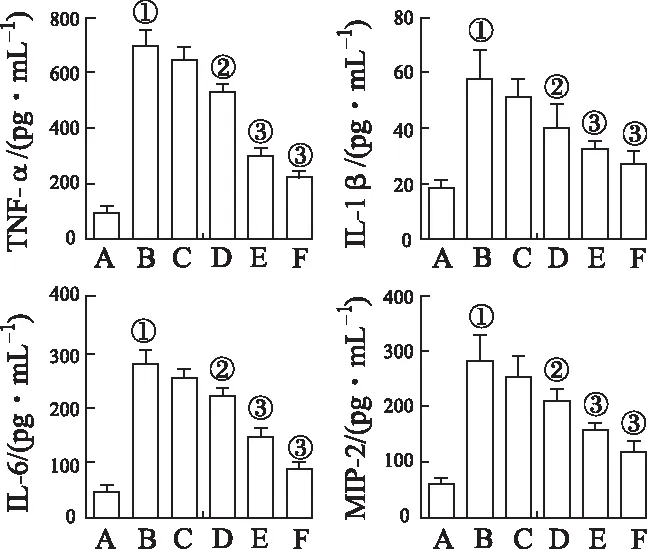
A.正常对照组;B.模型对照组;C.AG小剂量组;D.AG中剂量组;E.AG大剂量组;F.利奈唑胺组①与正常对照组比较,P<0.01;②与模型对照组比较,P<0.05,③与模型对照组比较,P<0.01。
2.4AG对脓毒症大鼠心脏和肺脏组织中HMGB1、TLR4蛋白表达和NF-κB p65磷酸化水平的影响 Western boltting检测大鼠心肺组织中HMGB1、TLR4和p-NF-κB p65蛋白表达水平的影响,结果如图4所示:与正常对照组比较,模型对照组大鼠心、肺组织中HMGB1、TLR4和p-NF-κB p65/NF-κB p65表达水平显著上调(心脏:t=1.086,1.168,1.400;肺脏:t=1.142,1.130,1.138,P<0.01);与模型对照组比较,AG治疗组中上述指标表达水平均明显下调,且AG中大剂量组差异有统计学意义(心脏:F=145.0,84.89,50.86;肺脏:F=52.28,76.15,26.80,P<0.05或P<0.01)。

A.正常对照组;B.模型对照组;C.AG小剂量组;D.AG中剂量组;E.AG大剂量组;F.利奈唑胺组;①与正常对照组比较,P<0.01;②与模型对照组比较,P<0.05,③与模型对照组比较,P<0.01。
2.5AG和(或)PDTC对脓毒症大鼠心肺损伤、炎症因子表达和信号通路活化的影响 HE染色、心肌损伤标记物和肺脏W/D检测结果如图5-A、B和C所示:与正常对照组比较,模型对照组大鼠心脏组织可见明显的排列紊乱、细胞核消融和炎性浸润等病理改变,且心肌损伤标记物含量显著上升(t=1.526,1.241,1.323,P<0.01),肺脏组织也可见肺泡塌陷,肺泡壁厚度增加,炎性浸润等病理学改变,且肺脏W/D也显著增加(t=4.622,P<0.01);与模型对照组比较,AG和/或PDTC治疗组大鼠心肺组织病理学改变得到明显改善,心肌损伤标记物含量和肺脏W/D也显著下降(F=223.2,71.22,73.46,70.92,P<0.01)。
ELISA和Western boltting分别检测炎症因子和炎症信号通路活化情况,结果如图5-D、E和F所示:与正常对照组比较,模型对照组大鼠血清中炎症因子和心肺组织中炎症信号通路蛋白表达水平均显著上调(t=1.404,2.138,1.413,1.511,1.234,1.154,1.504,1.294,1.432,1.390,P<0.01);与模型对照组比较,AG和(或)PDTC治疗组大鼠上述指标均显著下调(F=165.0,15.69,60.34,39.39,37.37,55.11,25.89,79.17,41.54,82.05,P<0.01)。

A.正常对照组;B.模型对照组;C.AG大剂量组;D.PDTC+模型组;E.PDTC+AG大剂量组;①与正常对照组比较,P<0.01;②与模型对照组比较,P<0.01。
上述结果均证明,AG改善脓毒症大鼠心肺损伤和炎症反应的机制与抑制HMGB1/TLR4/NF-κB p65信号通路活化有关。
3 讨论
目前,关于AG在脓毒症的治疗研究尚不多,本文通过腹腔注射脂多糖5 mg·kg-1建立脓毒症模型大鼠,并分3次于造模后立即、8 h和16 h给予AG治疗,造模24 h后,取材进行检测发现:模型对照组动物心脏和肺脏组织发生典型的脓毒症病理学改变;同时,心肌损伤标记物含量明显上升,肺部W/D也增加。结果表明本实验脓毒症模型建立成功。此外,小剂量AG治疗后上述检测指标未见明显改变,中剂量、大剂量AG则有效改善了心脏和肺脏的病理损伤程度,降低了心肌损伤标记物释放和肺脏W/D,其中大剂量组效果更优,仅次于利奈唑胺。综合实验结果,大剂量AG能有效治疗LPS诱导的脓毒症大鼠心、肺组织病理损伤。
研究表明,AG具有较强的抗炎作用,而多种疾病均与炎症因子大量释放有关[11,17]。巨噬细胞炎性蛋白-2(macrophage inflammatory protein-2,MIP-2)是白血病趋化因子家族之一,有助于中性粒细胞聚集到损伤或感染部位,从而调节免疫和炎症反应,是炎症反应的重要部分[18]。研究表明,急性肺损伤发生时,肺脏干湿比及肺泡灌洗液中炎症因子表达水平均发生改变[19]。研究发现,在脓毒症小鼠模型中,AG能通过减少心肌细胞凋亡减轻脂多糖诱导的心脏功能紊乱[20]。本研究结果证明,AG治疗能降低脓毒症大鼠血清中炎症细胞因子(TNF-α、IL-1β、IL-6和MIP-2)含量。
NF-κB是炎症反应最重要的转录调节因子,磷酸化激活后可转移到细胞核内,结合并启动促炎基因表达和炎症反应的扩增,从而导致炎症损伤。因此,抑制NF-κB信号活化是治疗炎症性疾病的重要手段[21]。高迁移率族蛋白B1(high mobility group protein B1,HMGB1)可与内源性配体TLR4结合,使NF-κB磷酸化,激活HMGB1/TLR4/NF-κB信号通路,诱导炎性细胞因子的释放,启动炎症级联反应,造成组织损伤[22]。LIU等[11]研究发现,AG治疗后,能减少脂多糖诱导的髓核细胞凋亡和炎症递质含量,其机制就与抑制NF-κB途径密切相关。另一研究也表明,AG能抑制促炎细胞因子IL-1β对髓核细胞凋亡的诱导作用,同时NF-κB的核易位[16]。本研究发现,脓毒症大鼠心脏和肺脏组织中HMGB1/TLR4/NF-κB信号通路蛋白水平均在AG治疗后显著降低。提示脓毒症大鼠的心肺组织损伤和炎症反应发生与该通路的表达上调有关,为了证明此观点,观察了NF-κB特异性抑制剂—PDTC[23]和(或)AG治疗对上述检测指标的影响,结果发现:PDTC能减轻脓毒症大鼠心肺组织病理损伤、心肌损伤标记物释放、肺脏W/D比值、血清炎症细胞因子含量和HMGB1/TLR4/NF-κB信号通路表达水平,而AG能增加PDTC的上述调节作用。
综上所述,AG能改善心肺组织病理学改变,减少心肌损伤标记物含量,降低肺脏W/D比值,抑制血清中炎症因子TNF-α、IL-1β、IL-6和MIP-2表达,抑制HMGB1、TLR4和p-NF-κB p65表达水平,并能增加NF-κB特异性抑制剂PDTC对脓毒症大鼠心肺组织损伤、心肌损伤标记物、肺脏W/D比值、血清炎性细胞因子含量及炎症通路活化的调节作用。总之,AG能通过抑制HMGB1/TLR4/NF-κB信号通路活化,减轻脓毒症大鼠心肺病理损伤和炎症反应。
