吡喃葡萄糖基咪唑啉盐表面活性剂的波谱学数据分析
2021-03-26陈凤宇肖鑫艳路东亮周中高
谢 倩,周 鑫,陈凤宇,肖鑫艳,路东亮,周中高
吡喃葡萄糖基咪唑啉盐表面活性剂的波谱学数据分析
谢 倩1,2,周 鑫1,陈凤宇1,肖鑫艳1,路东亮1,2,*周中高1,2
(1.赣南师范大学化学化工学院,江西,赣州 341000;2. 江西省高校功能材料化学重点实验室,江西,赣州 341000)
以1-(2,6-二甲基苯基)-1H-咪唑与2-溴乙基葡萄糖苷为原料,一步合成了新化合物溴化1-(2,6-二甲基苯基)-3-[2-(2,3,4,6-四-O-乙酰基-β-D-吡喃葡萄糖基氧基)-乙基]-咪唑盐(化合物1),是一种咪唑啉盐表面活性剂。化合物1的结构中存在糖基,含有多个手性碳原子,导致其核磁共振氢谱和碳谱较为复杂。我们运用液相色谱-高分辨质谱(LC-HRMS)和元素分析(EA)确定了其化学组成,随后通过液体核磁共振波谱技术(包括1D和2D核磁共振手段,如1H NMR、13C NMR、DEPT90、DEPT135、1H-1H COSY、1H-13C HSQC、1H-13C HMBC)对化合物1的氢谱和碳谱信号进行了表征,通过解析对其结构进行了详尽归属。
液体磁共振(NMR);手性表面活性剂;咪唑啉盐;葡萄糖;波谱学数据
全球日益关注生物相容性和可持续资源的利用,糖类化合物在自然界的含量丰富,物美价廉,无毒副作用,且具有独特的手性、生物相容性、水溶性等特性而被广泛应用,是非常好的手性官能团[1-5]。目前,糖类化合物衍生的表面活性剂被广泛研究并产业化,其应用领域包括乳化剂、洗涤剂以及医药输送系统[6-7]。相关研究集中于非离子表面活性剂,利用糖类化合物多羟基为表面活性剂提供亲水性。虽然非离子表面活性剂在增强稳定性方面具有明显优势,但是对pH值变化或电解质不敏感性也限制它的应用[8-9]。然而,涉及离子电荷的糖类化合物衍生的表面活性剂相关研究较少[10]。如典型的阴离子氨基葡萄糖醛酸烷基酯,即氧化的糖苷与羧酸的盐,以及糖类化合物阳离子N-烷基化的氨盐。这是最容易获得的糖基阳离子表面活性剂。但是其化学稳定性差又限制了后续的应用研究,阳离子、阴离子表面活性剂主要受介质影响[9,11]。考虑到生物细胞膜上存在大量的负电荷,阳离子表面活性剂可能会改善载体与细胞靶标之间相互作用,因此,糖基阳离子表面活性剂比阴离子表面活性剂更受青睐,又可以通过多种方式实现将糖类片段引入到氨基或铵基。咪唑啉盐多种多样的合成方法为配体的设计合成提供了新的思路,为减少化学反应步骤并优化产率,先对吡喃葡萄糖基衍生化随后与1-芳基咪唑反应,快速高效获得吡喃葡萄糖基咪唑啉盐表面活性剂,其中芳基咪唑不仅将阳离子引入糖类化合物中,同时还引入了疏水基团[12]。
吡喃葡萄糖基咪唑啉盐表面活性剂(化合物1)中含有5个手性碳和4个全乙酰基,吡喃糖基上的六元杂环(稠环)一般采取椅式和船式构象[13-14],不同构象会对碳氢化学位移产生一定影响,另外C-6上面的两个氢原子,分别对应直立键和平伏键上的氢,它们所处的化学环境不等价,这些因素使吡喃葡萄糖基咪唑啉盐表面活性剂上的部分碳氢化学位移非常接近[12, 15]。通过设计高效表面活性剂,深入理解表面活性剂的化学结构和相应取代基对表面活性剂性能的影响。因此,对吡喃葡萄糖基咪唑啉盐表面活性剂1的结构进行核磁共振(NMR)研究,仅通过一维1H NMR和13C NMR数据难于准确解析和归属,需要借助2D NMR技术,包括同核化学位移相关谱(1H-1H COSY)和异核化学位移相关谱(1H-13C HSQC),特别是异核多碳相关谱(1H-13C HMBC)研究对化合物1的1H和13C NMR的准确解析、归属和验证是非常必要的[16-19]。
以2-溴乙基葡萄糖苷和1-(2,6-二甲基苯基)-1H-咪唑为起始原料,一步制备了空气中稳定、具有一定吸水性的溴化1-(2,6-二甲基苯基)-3-[2-(2,3,4,6-四-O-乙酰基--D-吡喃葡萄糖基氧基)-乙基]-咪唑盐(化合物1)。这个新合成的吡喃葡萄糖基咪唑啉盐表面活性剂,首先用EA和LC-HRMS进行了组成确认,随后通过液体1D和2D NMR技术,包括一维1H、13C、DEPT135和DEPT90,二维1H-13C COSY、1H-13C HSQC和1H-13C HMBC对化合物1的结构进行了详细分析和准确归属。此研究对糖基咪唑啉盐类表面活性剂的制备和结构分析及核磁共振数据解析有一定参考作用。
1 实验部分
1.1 仪器与试剂
液相色谱-高分辨质谱(LC-HRMS)是在H-Class/Xevo G2-S QTof型超高效液相色谱/四极杆飞行时间串联质谱仪上进行测试。CHN元素分析(EA)使用德国Elementar公司Vario Micro cube元素分析仪测试。1H、13C、DEPT、1H-1H COSY、1H-13C HSQC和1H-13C HMBC均在Bruker Avance III-400型超导NMR谱仪测定,使用PABBO-5 mm多核宽带探头。2-溴乙基葡萄糖苷参考文献[10]方法合成,新化合物溴化1-(2,6-二甲基苯基)-3- [2-(2,3,4,6-四-O-乙酰基-β-D-吡喃葡萄糖基氧基)-乙基]-咪唑盐(化合物1)参考文献[20-21]方法合成。1-(2,6-二甲基苯基)-1H-咪唑、甲醇、二氯甲烷和乙腈等化学试剂均购自上海国药集团化学试剂有限公司。柱层析硅胶(200-300目)和GF薄层层析硅胶板均购自青岛海洋化工有限公司。核磁共振样品管(ST-500,NORELL)、氘代试剂CDCl3(99.8%氘代)均购自青岛腾龙微波科技有限公司。
1.2 实验条件
NMR谱图均在室温[(293.0 ± 0.1) ℃]条件下使用Bruker Avance III-400型超导NMR谱仪测定,使用PABBO-5 mm多核宽带探头,以CDCl3为溶剂,以TMS为内标。1H和13C NMR的工作频率分别为400.13、100.76 MHz,谱宽分别为8 223.69 Hz和24 038.46 Hz,COSY、HSQC及HMBC实验均采用标准脉冲程序。COSY的2(1H)和1(1H)维谱宽均为6 009.61 Hz,采样数据点阵2×1= 2 048×256;HSQC的2(1H)和1(13C)维谱宽分别为6 398.86 Hz和22 136.58 Hz,采样数据点阵2×1= 2 048×256;HMBC的2(1H)和1(13C)维谱宽分别为6 393.86 Hz和22 138.80 Hz,采样数据点阵2×1= 4 096×256。
2 结果与讨论
2.1 化合物1的合成
参考文献[20-21]方法,氮气保护,将2-溴乙基葡萄糖苷(3.0 mmol)和1-(2,6-二甲基苯基)-1H-咪唑(3.0 mmol)溶解在25.0 mL无水乙腈中,加热回流反应12 h,用TLC监测反应进程,待反应结束后,用旋蒸除去溶剂,残余物用柱层析提纯(用体积比30/1~10/1的二氯甲烷/甲醇梯度淋洗),真空干燥,得淡黄色粘稠液体,溴化1-(2,6-二甲基苯基)-3-[2-(2,3,4,6-四-O-乙酰基-β-D-吡喃葡萄糖基氧基)-乙基]-咪唑盐(化合物1),1.45 g,产率95%.
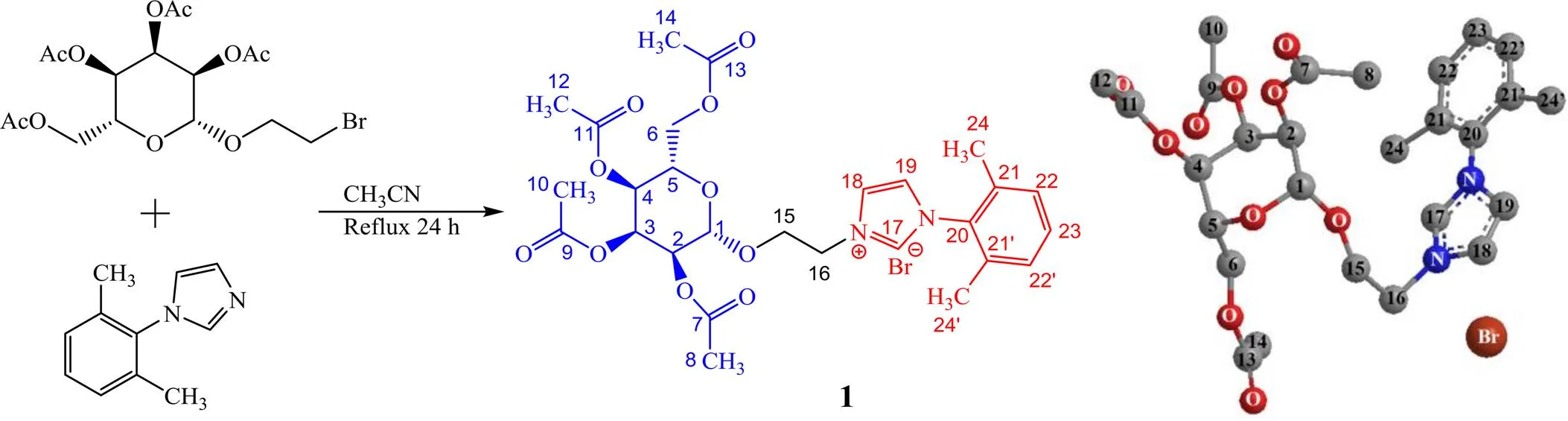
图1 化合物1的合成及其分子构型优化图(Chem 3D)
2.2 化合物1的高分辨质谱分析和元素分析
化合物1的HR-MS和EA都表现出吡喃葡萄糖基咪唑啉盐类表面活性剂的结构特征[10,20-21]。对其高分辨质谱结果进行分析,液相色谱-高分辨质谱ESI源正离子检测得到[M+H]+626.147 1,计算值626.147 5,误差为0.000 4,可以得知化合物1的分子量为627.485 0,分子式为C27H35BrN2O10。化合物1的元素分析C27H35BrN2O10,理论值(%):C 51.68,H 5.62;实测值(%):C 51.70,H 5.61。
2.3 核磁共振谱分析
2.3.1 1D NMR谱图分析
图2是化合物1的核磁共振氢谱,参考化学位移、峰型、峰面积和文献报道类似物的相关核磁共振信息,同时结合电子云密度,可知化合物1咪唑杂环上NCN(H-17)和NCCN(H-18和H-19)的质子酸性会随着溴代咪唑啉盐的形成而有所增加,相比H-18和H-19,H-17的化学位移出现在最低场区域,将H10.02(s, 1H)归属为H-17[12];溴代咪唑啉盐的形成而使得NCCN质子(H-18和H-19)的化学位移和峰型完全不同,其中一个为三重峰8.39(t,= 4.0 Hz,1H),一个为单峰7.48(s, 1H),初步推测H-18为三重峰,H-19为单峰。同时,吡喃葡萄糖的糖环上端基碳H-1较为特殊,只与H-2形成耦合体系,结合有关文献值,可将H5.02(d,= 8.0 Hz)归属为H-1。另外,苯环上两个甲基H-24和H-24’出现在高场,两个峰面积为3的单峰:2.37(s, 3H)和2.39(s, 3H)归属为H-24和/或H-24’,可以看出由于苯环旋转受阻,导致H-24和H-24’不等价而表现为两组信号峰,其它峰的归属需要借助2D NMR技术。
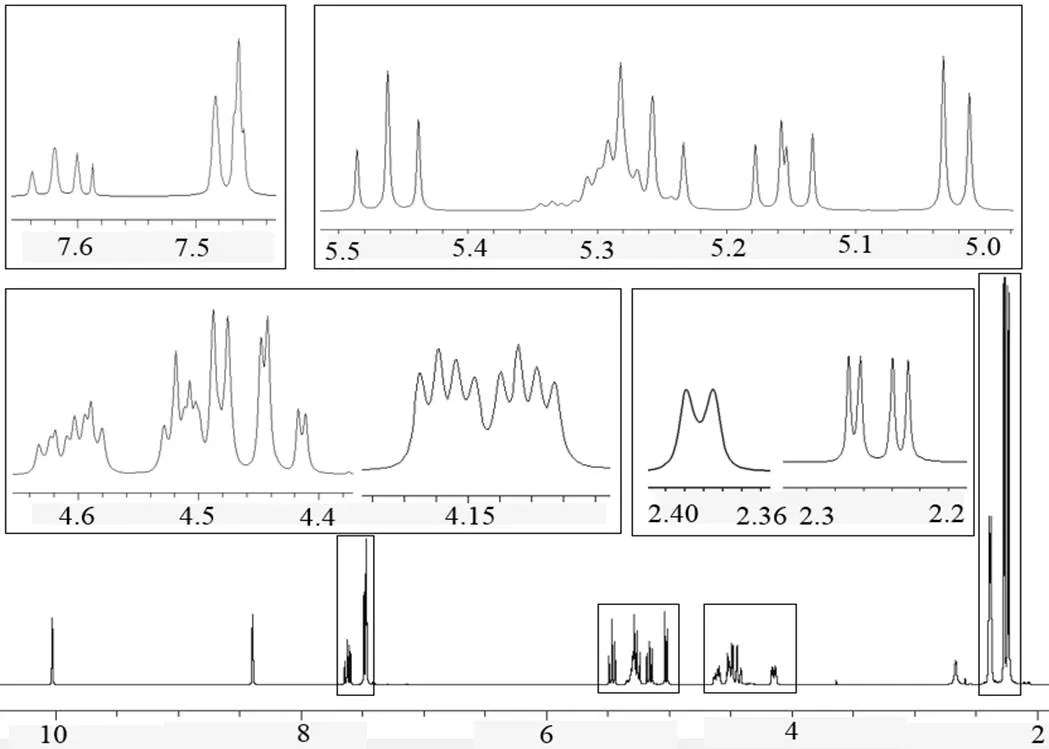
图2 化合物1在CDCl3中的核磁共振1H NMR谱图
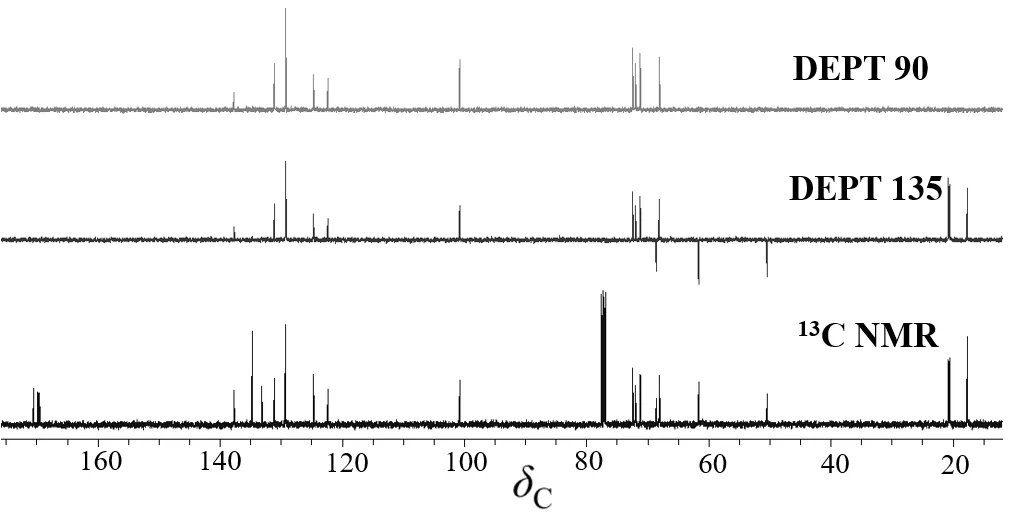
图3 化合物1在CDCl3中的13C NMR谱图
图3是化合物1的13C NMR和DEPT谱对比,通过比较13C NMR、DEPT135和DEPT90,确定该化合物有5个伯碳信号峰(C17.4、20.2、20.3、20.5和20.6),3个仲碳信号峰(C50.2、61.4和68.4)、10个叔碳信号峰(C67.9、70.9、71.8、72.2、100.5、122.1、124.5、129.0、130.9和137.4)和6个季碳信号峰(C132.9、134.5、169.3、169.4、169.7和170.3)。虽然H-24和H-24’不等价,但是C-24和C-24’在13C NMR上仅表现出一组信号峰。仅通过13C NMR和DEPT谱尚不能准确归属,所以需要借助2D NMR技术进一步解析。
2.3.2 2D NMR谱图分析
图4是化合物1的COSY谱,化合物1具有全乙酰吡喃葡萄糖基,吡喃糖基上的六元杂环(稠环)一般采取椅式和船式构象,使用Chem 3D软件的MM2功能对化合物1的分子结构进行优化(图1),可以看出吡喃糖基上的六元杂环是椅式构象,相邻两个碳上的氢原子在COSY谱上呈现交叉峰,可得糖骨架上端基碳上的H-1仅与H-2形成耦合体系,有交叉峰,将H-2归属为H5.16(dd,= 9.6 Hz,= 8.0 Hz, 1H);H-2同时与H-1和H-3耦合,均有交叉峰,将H5.46(t,= 9.6 Hz,1H)归属为H-3;H-3同时与H-2和H-4具有交叉峰,将H5.26(t,= 9.6 Hz, 1H)归属为H-4;
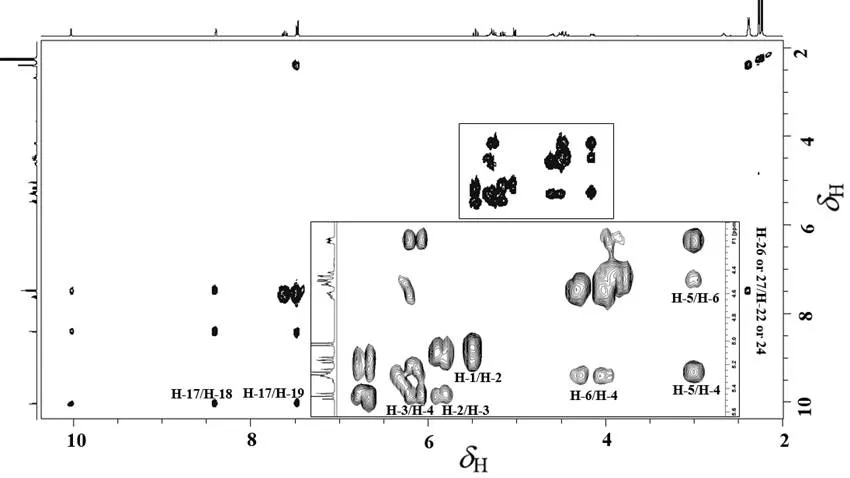
图4 化合物1在CDCl3中的COSY NMR谱(293 K)
由于全乙酰吡喃葡萄糖基稠环是椅式构象,其中C-5也具有手性,另外C-6上面的两个氢原子(H-6与H-6)分别对应直立键和平伏键的位置,它们所处的化学环境不等价而导致其化学位移不同,借助异核多量子相干实验,特别是二维1H-13C HSQC和1H-13C HMBC,将H4.61(m, 1H)归属为H-6,H4.51(m, 1H)归属为H-6。H-5同时与H-4、H-6和H-6存在耦合,其信号峰的受到多种氢的耦合,峰型较为复杂,将H4.14(m, 1H)归属为H-5。
图5是化合物1的HSQC NMR谱,由图可得,C100.5与H-1相关,归属为C-1;C71.0与H-2相关,归属为C-2;C72.2与H-3相关,归属为C-3;C67.9与H-4相关,归属为C-4;C71.8与H-5相关,归属为C-5。C137.4与H-17相关,归属为C-17;C68.3与H4.61(m, 1H)和H4.50(m, 1H)均有相关,即H-6、H-6,归属为C-6;C137.2与H-17相关,归属为C-17;C130.9对应的H-23只有1个质子,所以归属为C-23;C129.0对应的H-22和H-22’有2个质子,归属为C-22和C-22’。结合DEPT135,剩余2个未归属仲碳信号峰(C50.2和61.4)分别对应C-15和C-16。C124.5与H8.39(t,= 4.0 Hz, 1H)(H-18或H-19)相关,C122.1与H7.48(br, 1H)(H-18或H-19)相关,归属为C-18或C-19,准确归属需要借助二维HMBC谱[17]。
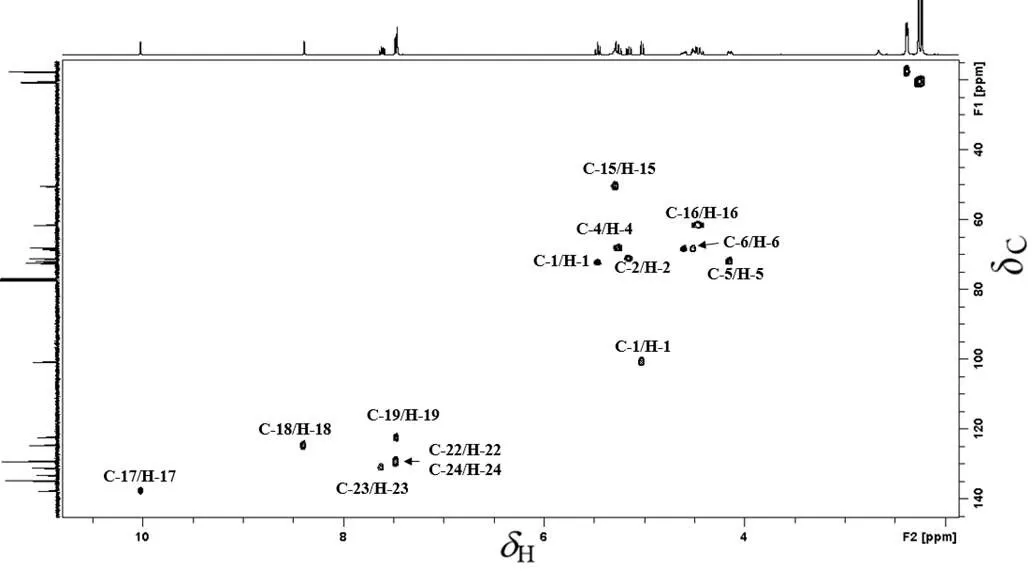
图5 化合物1在CDCl3中的1H-13C HSQC谱图(293 K)
由于化合物存在4个乙酰基,分别存在4个季碳信号峰(C169.3、169.4、169.6、170.3)和4个伯碳信号峰(C20.2、20.3、20.4、20.6)未归属,2个仲碳(C50.2和61.4),另外还有2个叔碳(C124.5和122.1)和苯环上的2个季碳信号峰(C134.5和132.9),无法准确归属,还需要进一步借助二维异核多量子相干实验,特别是HMBC谱来解析。
图6是化合物1的异核多碳相关谱(HMBC)谱图,首先从C-15和C-16入手,即2个仲碳(C50.2和61.4),C50.2与H-18有交叉峰,归属为C-16;C61.4与H-1有交叉峰,归属为C-15;其中2个叔碳(C124.5和122.1)是咪唑杂环上的,C124.5与H-16有交叉峰,归属为C-18,同时它与H-19相关;C122.1只与H-17有交叉峰,归属为C-19;C134.5与H-23有交叉峰,归属为C-21/C-21’,C132.9与H-22有交叉峰,归属为C-20。
到此为止,尚余4个乙酰基对应的4个季碳信号峰(C169.3、169.4、169.6、170.3)和4个伯碳信号峰(C20.2、20.3、20.4、20.6)未归属。通过HMBC谱图,化合物1中4个难以区分的伯碳氢分别与糖基稠环上对应碳有相关峰,它们的归属也就显而易见,H2.27(s, 3H)与C-4有交叉峰,归属为H-12;H2.26(s, 3H)与C-2有交叉峰,归属为H-8;H2.23(s, 3H)与C-3有交叉峰,归属为H-10;H2.24(s, 3H)与C-6有交叉峰,归属为H-14。同时C170.3即C-13与H2.24(s, 3H)有交叉峰,归属为H-14;C169.6即C-9与H2.23(s, 3H)有交叉峰,归属为H-10;C169.4即C-7与H2.26(s, 3H)有交叉峰,归属为H-8;剩下一个为H-12。化合物1中4个伯碳(C20.2、20.3、20.4、20.6)无法通过HSQC谱图归属,因为它们化学位移差值太小。
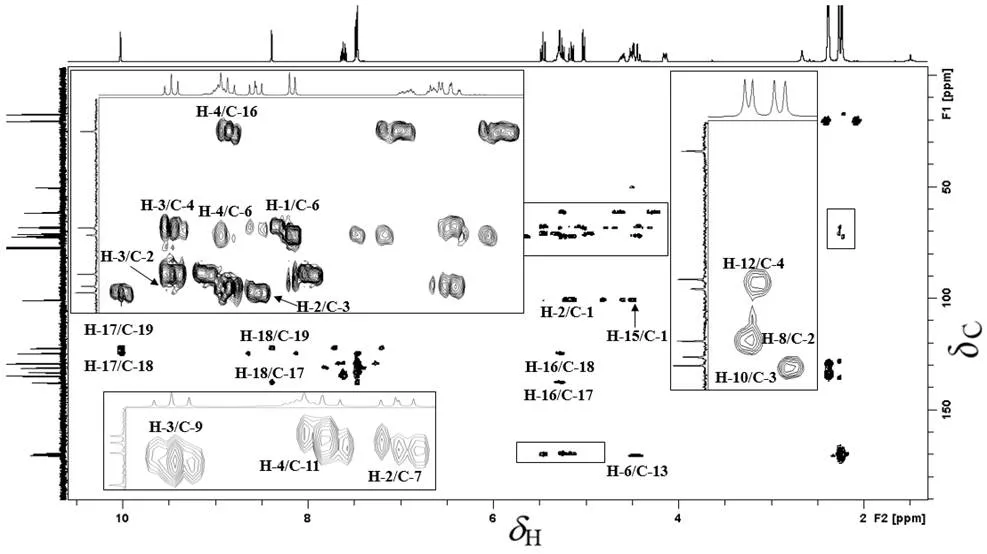
图6 化合物1在CDCl3中的1H-13C HMBC谱图(293 K)
表1 化合物1的H NMR和C NMR归属
Table 1 Belonging of Compound 1 in H NMR and C NMR
PositiondCdH (J/Hz)HSQCCOSYHMBC 1100.55.02 (d, J = 8.0 Hz)+H-2H-2, H-5, H-15 271.05.16 (dd, J = 9.6 Hz, J = 8.0 Hz)+H-1, H-3H-1, H-3, H-8 372.25.46 (t, J = 9.6 Hz)+H-2, H-4H-1, H-2, H-4, H-10 467.95.26 (t, J = 9.6 Hz)+H-3, H-5H-3, H-5, H-6a, H-6e, H-10 571.84.13 (m)+H-4, H-6aH-1, H-4, H-6a, H-6e 6a68.34.61 (m)+H-5H-4, H-5, H-14 6e68.34.50 (m)+/H-4, H-5, H-14 7169.4///H-2, H-8 820.42.26 (s)+/H-2, H-7 9169.6///H-3, H-10 1020.22.23 (s)+/H-3, H-9 11169.3///H-4, H-12 1220.62.27 (s)+/H-4, H-11 13170.3///H-6, H-14 1420.32.24 (s)+/H-6, H -13 1561.44.46 (m)+H-16H-1, H -16 1650.25.28 (m)+H-15H-15, H-17, H -18 17137.410.02 (s)+H-18, H-19H-16, H-18, H -19, H-20 18124.58.39 (t, J = 4.0 Hz)+H-17, H-19H-16, H-17, H -19 19122.17.48 (br)+H-17, H-18,H-24, H-24’H-17, H-18 20132.9///H-17, H-19, H-22, H-22’, H-24, H-24’ 21134.5///H-22, H-23, H-24 21’134.5///H-23, H-22’, H-24’ 22129.07.47 (m)+H-23H-23, H-22’, H-24 22’129.07.47 (m)+H-23H-22, H-23, H-24’ 23130.97.62 (m)+H-22, H-22’H-22, H-22’ 2417.42.37 (s) or 2.39 (s)+H-19H-22 24’17.42.37 (s) or 2.39 (s)+H-19H-22’
化合物1的详细结构经过异核多碳相关谱的解析和验证,主要是将化合物1中较难归属的一系列数据进行解析,包括吡喃葡萄糖基上乙酰基对应季碳和伯碳上碳氢化学位移,以及咪唑杂环骨架上叔碳和苯环上季碳的碳氢化学位移归属方面起到了重要作用。同时对HMBC的解析也反过来验证了前面的COSY和HSQC的分析结果[15]。
化合物1是一个新的化合物,通过对它进行液体核磁共振包括一维技术(1H、13C NMR、DEPT135和DEPT45)和同核与异核二维技术(COSY、HSQC和HMBC)的分析,对相关类似物归属的特征信号峰、化合物1的1H和13C NMR信号全归属见表1。
3 小结
本研究首次制备了手性吡喃葡萄糖基表面活性剂溴化1-(2,6-二甲基苯基)-3-[2-(2,3,4,6-四-O-乙酰基-β-D-吡喃葡萄糖基氧基)-乙基]-咪唑盐。运用LC-HRMS和EA确认了它的化学组成,通过液体核磁共振波谱1D和2D技术对它的氢谱和碳谱信号进行了解析和详尽的全归属。特别是异核多碳相关谱在氢谱和碳谱信号解析方面起到重要作用,将难以归属的一系列信号峰进行反复推敲和前后验证,包括吡喃葡萄糖基上、乙酰基上对应的季碳和伯碳上碳氢化学位移,氮杂环骨架上叔碳以及苯环上季碳的碳氢化学位移。同时异核多碳相关谱的解析也反过来验证了同核化学位移相关谱和异核化学位移相关谱的分析结果。此研究工作对手性基咪唑啉盐类表面活性剂的制备和结构分析,特别是核磁共振数据解析有一定参考作用。
[1] Marradi M, Chiodo F, García I, et al. Glyconanoparticles as multifunctional and multimodal carbohydrate systems[J]. Chem. Soc. Rev., 2013, 42(11): 4728-4745.
[2] Woodward S, Diéguez M, Pàmies O. Use of sugar-based ligands in selective catalysis: recent developments[J]. Coord. Chem. Rev., 2010, 254(17-18): 2007-2030.
[3] Zhang X, Wilson K, Lee A F. Heterogeneously catalyzed hydrothermal processing of C5–C6sugars[J]. Chem. Rev., 2016, 116: 12328.
[4] Kaur N, Chopra H K. Synthesis and applications of carbohydrate based chiral ionic liquids as chiral recognition agents and organocatalysts[J]. J. Mol. Liq., 2020, 298(15): 111994.
[5] 胡文杰,朱立成,殷帅文,等. 油樟叶精油不同馏分化学成分及其抗氧化能力评价[J]. 井冈山大学学报: 自然科学版, 2019, 40(5): 26-33.
[6] Goh E W, Heidelberg T, Duali Hussen, et al. Imidazolium-linked azido-functionalized guerbet glycosides: Multifunctional surfactants for biofunctionali- zation of vesicles[J]. ACS Omega, 2019, 4(16): 17039-17047.
[7] Wang Y, Carder H M, Wendlandt A E. Synthesis of rare sugar isomers through site-selective epimerization[J]. Nature, 2020, 578: 403-408.
[8] Ginzburg A L, Truong L, Tanguay R L, et al. Synergistic toxicity produced by mixtures of biocompatible gold nanoparticles and widely used surfactants[J]. ACS Nano, 2018, 12(6): 5312-5322.
[9] Bhadani A, Misono T, Singh S, et al. Structural diversity, physicochemical properties and application of imidazolium surfactants: Recent advances[J]. Adv. Colloid Interface Sci., 2016, 231: 36-58.
[10] Salman A A, Tabandeh M, Heidelberg T, et al. Alkyl- imidazolium glycosides: non-ionic—cationic hybrid surfactants from renewable resources[J]. Carbohydr. Res., 2015, 412: 28-33.
[11] Imbrich D A, Frey W, Naumann S, et al. Application of imidazolinium salts and n-heterocyclic olefins for the synthesis of anionic and neutral tungsten imido alkylidene complexes[J]. Chem. Commun., 2016, 52(36): 6099-6102.
[12] Zhao W, Ferro V, Baker M V. Carbohydrate–N- heterocyclic carbene metal complexes: synthesis, catalysis and biological studies[J]. Coord. Chem. Rev., 2017, 339: 1-16.
[13] Kaur N, Singh A, Chopra H K. Exploring low-cost natural precursors as chiral building blocks in synthesis: Chiral carbohydrate-ionic liquids[J]. Mini-Rev. Org. Chem., 2018, 15(3): 208-219.
[14] Shi J C, Lei N, Tong Q S, et al. Synthesis of chiral imidazolinium carbene from a carbohydrate and its Rhodium(I) complex[J]. Eur. J. Inorg. Chem., 2007, 2007(15): 2221-2224.
[15] 周中高,元洋洋,黄丽,等. 葡糖衍生手性N-杂环卡宾前体波谱学数据分析[J].波谱学杂志,2018,35(2): 215-225.
[16] 周中高,刘沛,童庆松,等. 甲基 3-脱氧-3-(2-羟基苄叉氨基)-4, 6-O-苄叉基-α-D-阿卓吡喃糖苷的 NMR 研究[J]. 福建师范大学学报:自然科学版, 2009, 25(5): 78-80.
[17] 元洋洋,刘金香,黄丽,等. 含葡糖单元N-杂环卡宾前体的结构确认[J]. 赣南师范大学学报:自然科学版, 2017, 2017(6): 74-79.
[18] 蓝倩,元洋洋,李美,等. 非膦钯催化Suzuki偶联反应[J]. 井冈山大学学报: 自然科学版, 2017, 38(6): 30-34.
[19] 许瑞波,杨雯雯,万蓓蓓. 连云港山楂叶黄酮的超声提取及体外活性研究[J]. 井冈山大学学报: 自然科学版, 2016, 36(6): 24-29.
[20] Zhou Z, Zhao Y, Zhen H, et al. Poly(ethylene glycol)- and glucopyranoside-substituted N-heterocyclic carbene precursors for the synthesis of arylfluorene derivatives using efficient palladium-catalyzed aqueous Suzuki reaction[J]. Appl. Organomet. Chem., 2016, 30(11): 924-931.
[21] Zhou Z, Qiu J, Xie L, et al. Synthesis of chiral imidazolium salts from a carbohydrate and their application in Pd-catalyzed Suzuki–Miyaura reaction[J]. Catal. Lett., 2014, 144(11): 1911-1918.
The Spectral Analysis of Glucopyranosyl Imidazolinium Surfactants
XIE Qian1,2, ZHOU Xin1, CHEN Feng-yu1, XIAO Xin-yan1, LU Dong-liang1,2,*ZHOU Zhong-gao1,2
(1.College of Chemistry and Chemical Engineering, Gannan Normal University, Ganzhou, Jiangxi 341000, China;2.Key Laboratory of Jiangxi University for Functional Materials Chemistry, Ganzhou, Jiangxi 341000, China)
1-(2,6-dimethylphenyl)-3-[2-(2,3,4,6-tetra-O-acetyl--D-glucopyranosyloxy)-ethyl]-imidazolinium salt (Compound 1) is synthesized by 1-(2,6-dimethylphenyl)-1H-imidazole and 2-bromoethylglucoside, which is a glucose-derived chiral imidazolinium surfactants. The structure of compound 1 has sugar groups and multiple chiral carbon atoms, which makes its1H nd13C NMR spectrum more complicated. Herein, we used liquid chromatography-high resolution mass spectrometry (LC-HRMS) and elemental analysis (EA) to determine its chemical composition, and subsequently characterized the hydrogen and carbon spectrum signals of compound 1 by liquid NMR spectroscopy (including1H,13C, DEPT90, DEPT135,1H-1H COSY,1H-13C HSQC and1H-13C HMBC), finally, the1H and13C NMR chemical shift was completely assigned.
liquid NMR; chiral surfactants; imidazolinium salt; glucose; spectroscopy data
O482.53
A
10.3969/j.issn.1674-8085.2021.02.005
1674-8085(2021)02-0026-06
2021-01-02;
2021-01-27
国家自然科学基金项目(21562002);大学生创新创业训练计划项目(CX190009);江西省学位与研究生教育教学改革研究项目(JXYJG-2017-135);研究生优质课程项目
谢 倩(1998-),女,江西赣县人,硕士生,主要从事有机功能材料合成及性能研究(E-mail:1343936818@qq.com);
周 鑫(2000-),女,江西南昌人,赣南师范大学化学化工学院2018级化学专业本科生(E-mail:912296685@qq.com);
陈凤宇(1997-),女,内蒙古赤峰人,赣南师范大学化学化工学院2016级材料化学专业本科生(E-mail:1041673986@qq.com);
肖鑫艳(1998-),女,江西信丰人,赣南师范大学化学化工学院2017级应用化学专业本科生(E-mail:2640861103@qq.com);
路东亮(1985-),男,河南林州人,讲师,硕士生导师,博士,主要从事手性不对称催化研究(E-mail:ludl201306@163.com);
周中高(1982-),男,江西赣州人,副教授,博士,硕士生导师,主要从事有机功能材料合成及绿色手性催化剂性能研究(E-mail:zhgzhou@foxmail.com).
