新型β内酰胺类-β内酰胺酶抑制剂复方制剂研究进展
2021-03-25黄晓岚卞星晨黄志伟毋海兰
黄晓岚,卞星晨,黄志伟,毋海兰,张 菁
数十年来,β内酰胺类抗菌药物一直被用于治疗各种感染,占全球抗菌药物使用量的60%[1],是抗感染治疗主要药物之一。青霉素和头孢菌素分别于20世纪40年代和60年代应用于临床,选择性压力很快促使超广谱β内酰胺酶 (extendedspectrum β-lactamases,ESBL)和头孢菌素酶(AmpC酶)的产生,对β内酰胺类抗菌药物的使用构成了严重威胁。ESBL大多数来自A类TEM、SHV、CTX-M家族(Ambler分类法),可以水解青霉素类、头孢菌素和单环β内酰胺类抗菌药物,却对碳青霉烯类抗菌药物的水解能力较弱。随后,于1985年发现了以亚胺培南为代表的碳青霉烯类抗菌药物,这类药物具有很强的抗菌活性[2]。然而,随着其广泛使用,产生了新的能够水解碳青霉烯类的β内酰胺酶。其中,肺炎克雷伯菌碳青霉烯酶(Klebsiella pneumoniaecarbapenemase,KPC)最为常见[3]。为了应对这一挑战,β内酰胺类-β内酰胺酶抑制剂复方制剂逐渐进入临床。
第一代β内酰胺酶抑制剂(克拉维酸、舒巴坦和他唑巴坦)主要抑制A类(碳青霉烯酶除外)和某些C类丝氨酸β内酰胺酶,但对绝大部分B、C、D类酶没有抑制作用[4]。而新一代β内酰胺酶抑制剂(阿维巴坦、法硼巴坦和雷利巴坦)则表现出广谱抑制活性,包括KPC在内的大部分A类、C类和某些D类β内酰胺酶,备受临床青睐。美国食品药品监督管理局(FDA)分别于2014年12月、2015年2月、2017年8月和2019年7月批准头孢洛扎-他唑巴坦(ceftolozane-tazobactam)、头孢他啶-阿维巴坦(ceftazidime-avibactam)、美罗培南-法硼巴坦(meropenem-vaborbactam)和亚胺培南-西司他丁-雷利巴坦(imipenem-cilastatin-relebactam)上市[5]。本文综述4种酶抑制剂的抑酶谱,头孢他啶-阿维巴坦、头孢洛扎-他唑巴坦、美罗培南-法硼巴坦、亚胺培南-西司他丁-雷利巴坦的体外抗菌活性、药动学(PK)、药效学(PD)、PK/PD以及临床疗效和安全性等,供临床合理应用该类药物作参考。
1 抑酶谱
他唑巴坦作为第一代β内酰胺酶抑制剂,与新头孢菌素类抗菌药物头孢洛扎组成复方制剂可抑制A类β内酰胺酶,如CTX-M、SHV和TEM,但不能抑制碳青霉烯酶。作为新一代β内酰胺酶抑制剂,阿维巴坦和雷利巴坦不含有β内酰胺环结构,因此不易被水解,有着更广泛的抑酶谱和可逆的抑酶效果,能抑制包括碳青霉烯酶在内的A类和C类酶。同时,阿维巴坦对D类酶(如OXA-48)具有抑制作用[3]。法硼巴坦是新型的硼酸复合物酶抑制剂,可抑制A类(尤其是KPC)和C类β内酰胺酶,对D类β内酰胺酶不起作用。值得注意的是,上述4种抑制剂均无法抑制B类β内酰胺酶。表1汇总了4种酶抑制剂的抑酶谱[6]。

表1 4种酶抑制剂抑酶谱
2 体外抗菌活性
头孢洛扎-他唑巴坦、头孢他啶-阿维巴坦、美罗培南-法硼巴坦和亚胺培南-西司他丁-雷利巴坦对大多数肠杆菌科细菌、铜绿假单胞菌和流感嗜血杆菌均具有较强抗菌、抑酶作用,但对不动杆菌属作用较弱,对嗜麦芽窄食单胞菌、粪肠球菌和屎肠球菌无抗菌作用[3]。表2总结了4种β内酰胺类-β内酰胺酶抑制剂复方制剂体外抗菌活性[7-13]。

表2 β内酰胺类-β内酰胺酶抑制剂复方制剂体外抗菌活性
3 PK
4种抗菌药物与配伍的4种β内酰胺酶抑制剂的PK相似且符合线性PK特征,联合给药对单一成分PK无影响,并且未发现药物相互作用。研究显示,多次静脉输注给药后,均无明显蓄积现象。
该4种复方制剂均通过肾脏排泄,清除率随着肾功能的下降而降低。因此,对于头孢他啶-阿维巴坦、头孢洛扎-他唑巴坦和美罗培南-法硼巴坦,患者估计肾小球滤过率(eGFR)<50 mL · min-1·1.73 m2时需及时调整剂量;对于亚胺培南-西司他丁-雷利巴坦,eGFR<90 mL · min-1· 1.73 m2时应及时调整剂量,并且当eGFR<15 mL · min-1·1.73 m2不应使用该药,除非患者进行血透。另外,对于该4种复方制剂,均建议终末期肾病(end stage renal disease, ESRD)血液透析的患者在透析结束后给药[14-17]。4种复方制剂的PK参数总结见表3[18-19]。
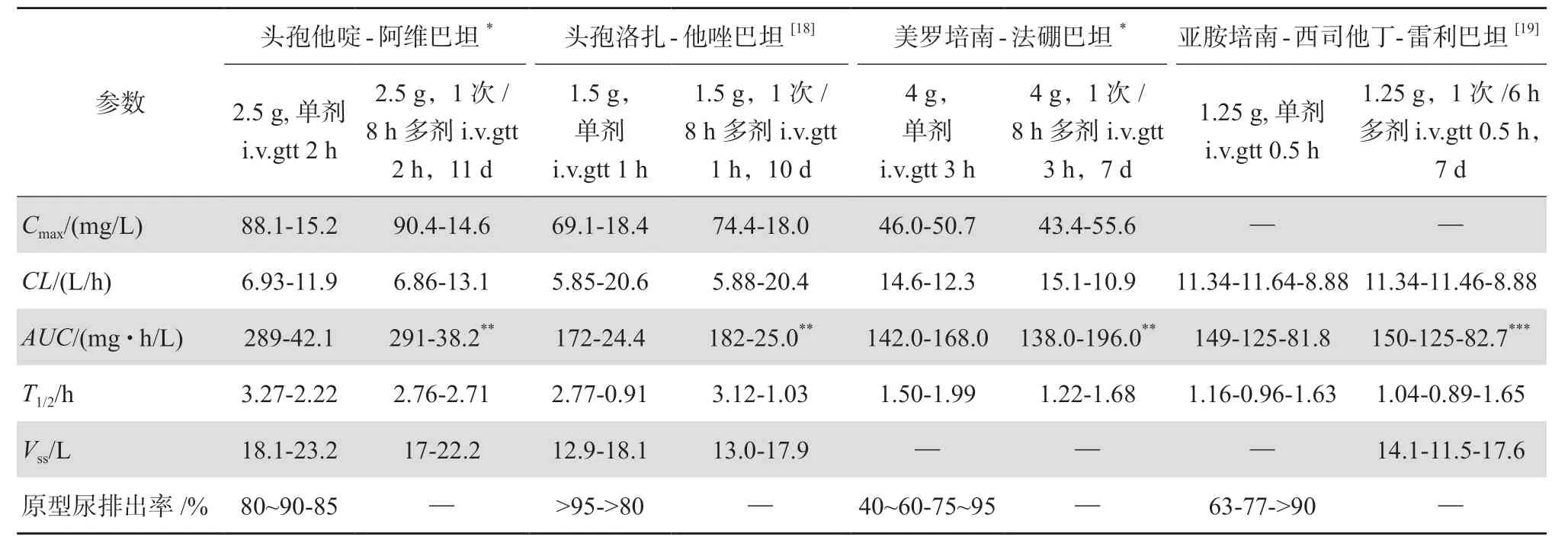
表3 β内酰胺类-β内酰胺酶抑制剂复方制剂PK参数
4 PK/PD
既往大多只研究了β内酰胺类抗菌药物的PK/PD特性,描述β内酰胺酶抑制剂的PK/PD数据很少。表4对β内酰胺酶抑制剂相关的PK/PD研究进行了总结[20-26]。
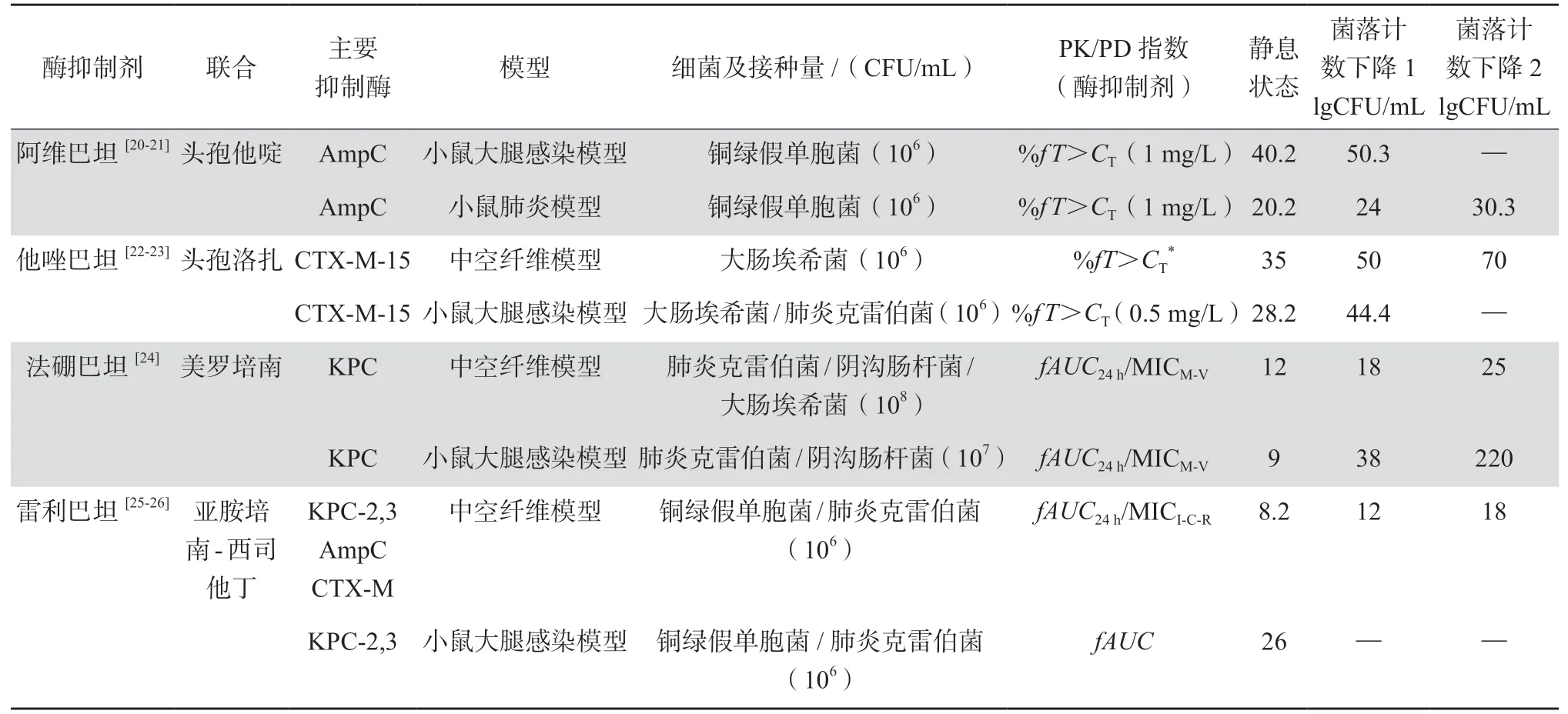
表4 酶抑制剂的PK/PD指数和靶值
早期通过大量研究证实β内酰胺类抗菌药物多为时间依赖性,与其疗效最相关的PK/PD指数为游离药物浓度高于MIC的时间占给药间隔的百分比,即%ƒT>MIC[27]。
近年来的研究证实,阿维巴坦、他唑巴坦、法硼巴坦和雷利巴坦的加入均可增强与之配伍的β内酰胺类药物的抗菌作用[1]。体外研究显示,β内酰胺酶抑制剂与疗效最相关的PK/PD指数可能不同。阿维巴坦和他唑巴坦的疗效相关PK/PD指数为%f T>CT(CT为阈值浓度)。其中,阿维巴坦CT为1 mg/L[28];而他唑巴坦PK/PD靶值研究表明,CT可能与β内酰胺酶表达水平有关[22]。而与法硼巴坦疗效最为相关的PK/PD指数为fAUC24h/MIC,其中MIC为联合8 mg/L法硼巴坦时美罗培南的MIC值[24],与雷利巴坦疗效最为相关的PK/PD指数为fAUC24h/MIC,其中MIC为联合4 mg/L雷利巴坦时亚胺培南的MIC值[26]。
5 临床疗效及安全性
自2014年以来,FDA及EMA相继批准了4种新型β内酰胺类-β内酰胺酶抑制剂复方制剂。截至目前,中国仅批准了头孢他啶-阿维巴坦上市。表5总结了经FDA、EMA、CDE批准的该4种复方制剂的相关适应证等内容。具体临床研究内容可见表6[29-39]。
5.1 复杂性尿路感染(cUTI)
Wagenlehner等[29]开展的一项Ⅲ期临床试验比较了头孢他啶-阿维巴坦(2 g-0.5 g,1次/8 h)和多立培南(0.5 g,1次/8 h)治疗包括急性肾盂肾炎在内的cUTI的疗效和安全性。FDA联合终点结果表明,头孢他啶-阿维巴坦与多立培南相比,显示出非劣效性:①第5天访视症状缓解患者的比例分别为70.2%和66.2%;②治疗访视(test of cure)时微生物学清除且症状缓解患者的比例分别为71.2%和64.5%。EMA指导下的主要终点是微生物改良意向治疗(microbiological modified intent-to-treat, mMITT)人群在治疗访视时微生物学清除患者的比例,头孢他啶-阿维巴坦组和多立培南组分别为77.4%和71.0%,头孢他啶-阿维巴坦在5%显著性水平上显示出优越性。安全性方面,头孢他啶-阿维巴坦组和多立培南组分别有36.2%和31.0%的受试者至少发生过1次不良事件,大多为轻度或中度。
Wagenlehner等[30]开展的另一项Ⅲ期临床试验,患者以1∶1的方式随机接受头孢洛扎-他唑巴坦(1.5 g,1次/8 h)联合甲硝唑(0.5 g,1次/8 h)或左氧氟沙星(0.75 g,1次/8 h)治疗。FDA指导下的主要复合终点为mMITT人群在治疗访视时的临床治愈率和微生物学清除率,结果显示头孢洛扎-他唑巴坦疗效优于左氧氟沙星(76.9%和68.4%)。头孢洛扎-他唑巴坦组与左氧氟沙星组的不良事件发生率相似,分别为34.7%和34.4%,最常见的不良反应是头痛和胃肠道症状。
Kaye等[31]开展一项Ⅲ期临床试验,患者以1∶1的方式随机接受美罗培南-法硼巴坦 (2 g-2 g,1次/8 h)或哌拉西林-他唑巴坦 (4 g-0.5 g,1次/8 h)治疗。美罗培南-法硼巴坦与哌拉西林-他唑巴坦相比,前者在FDA和EMA指导下的主要终点结果均显示出非劣效性。安全性方面,美罗培南-法硼巴坦组和哌拉西林-他唑巴坦组的不良反应率分别为39.0%和35.5%,美罗培南-法硼巴坦组最常见的不良反应为轻度头痛。
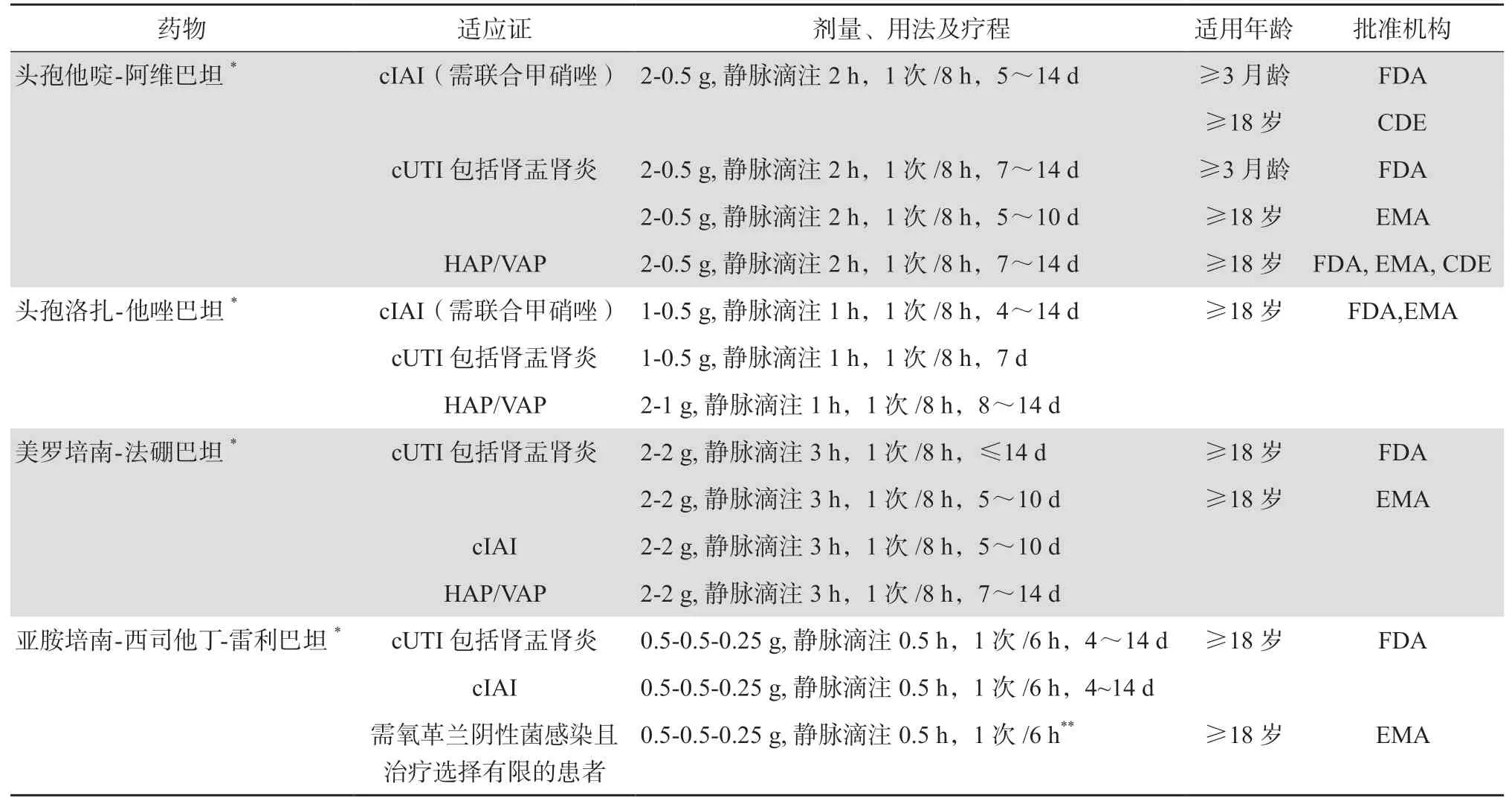
表5 4种批准上市的β内酰胺类-β内酰胺酶抑制剂复方制剂适应证等
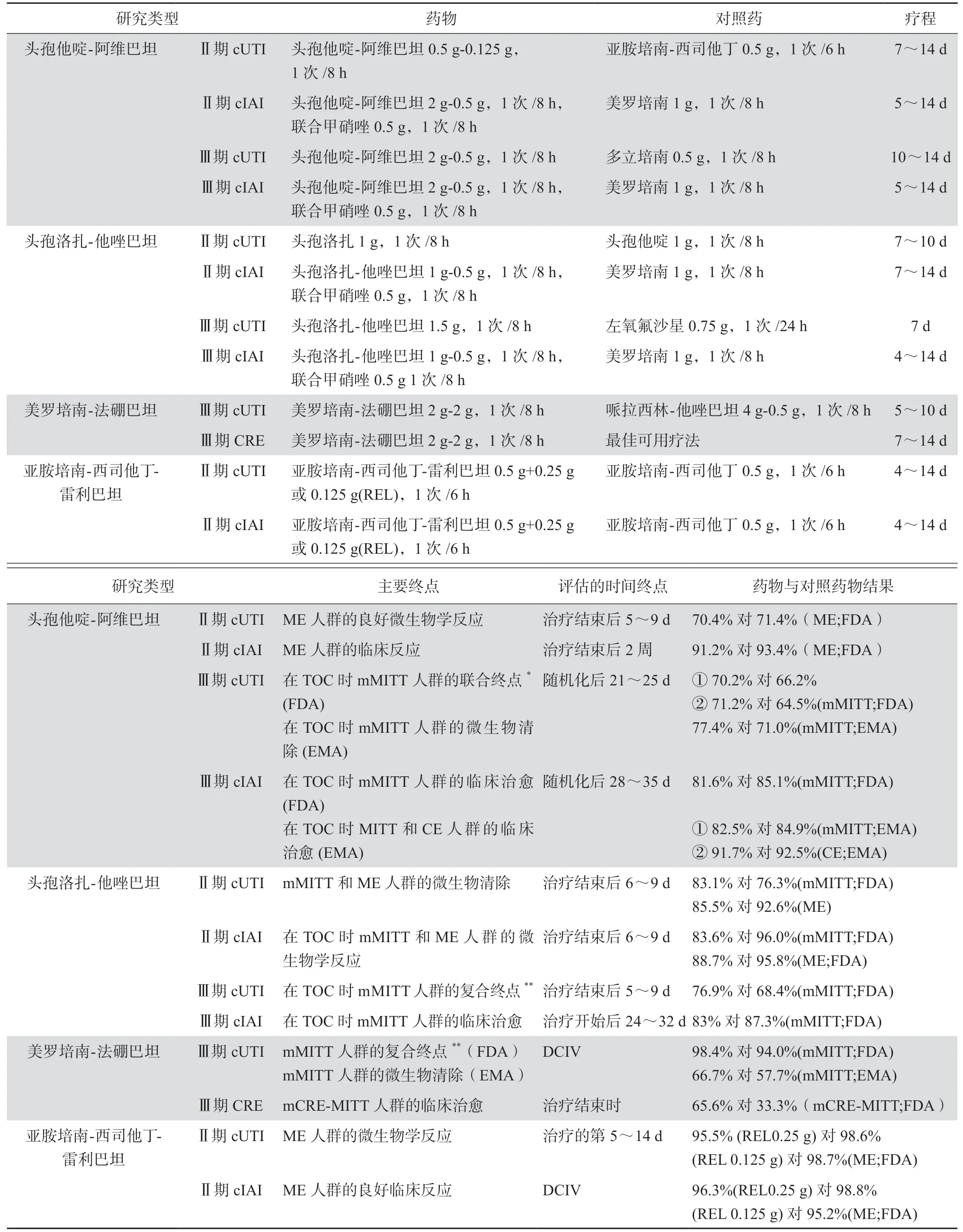
表6 β内酰胺类-β内酰胺酶抑制剂复方制剂临床研究
Sims等[32]开展的一项多中心、随机对照、双盲的Ⅱ期临床试验,将患者以1∶1∶1的方式随机分组,接受亚胺培南-西司他丁(0.5 g,1次/6 h)与不同剂量的雷利巴坦 (0.25 g或0.125 g)治疗。FDA指导下的主要终点为微生物可评估人群(microbiologically evaluable, ME)的微生物学反应,显示亚胺培南-西司他丁-雷利巴坦 250 mg组、125 mg组和单用亚胺培南-西司他丁组的微生物反应率分别为95.5%、98.6%和98.7%,证实亚胺培南-西司他丁-雷利巴坦与亚胺培南-西司他丁单独给药相比并不逊色。安全性方面,在接受治疗的三组患者中,不良反应率分别为28.3%、29.3%和30.0%,最常见的与治疗相关的不良反应是腹泻、恶心和头痛。
5.2 复杂性腹腔内感染(cIAI)
Mazuski等[33]开展的一项Ⅲ期随机、双盲临床试验,比较了头孢他啶-阿维巴坦联合甲硝唑或美罗培南治疗cIAI的疗效和安全性。患者以1∶1的方式随机接受头孢他啶-阿维巴坦(2 g-0.5 g,1次/8 h)联合甲硝唑(0.5 g,1次/8 h)或美罗培南(1 g,1次/8 h)治疗。FDA和EMA的主要终点为各分析人群的临床治愈率,结果显示头孢他啶-阿维巴坦联合甲硝唑在所有分析人群中的疗效均不逊于美罗培南,分别为81.6%和85.1%(mMITT人群,FDA),82.5%和84.9%(MITT人群,EMA),91.7%和92.5%(临床可评估人群,EMA)。安全性方面,头孢他啶-阿维巴坦组和美罗培南组的不良反应事件发生率相似,分别为45.9%和42.9%,最常见的是胃肠道反应。
Solomkin等[34]开展的一项Ⅲ期临床试验,患者以1∶1的方式随机接受头孢洛扎-他唑巴坦 (1.5 g,1次/8 h)联合甲硝唑(0.5 g,1次/8 h)或美罗培南(1 g,1次/8 h)治疗。FDA指导下的主要复合终点为mMITT人群在TOC时的临床治愈率,结果显示头孢洛扎-他唑巴坦联合甲硝唑的疗效不逊于美罗培南,分别为83%和87.3%。头孢洛扎-他唑巴坦组和美罗培南组的不良事件发生率相似,分别为44.0%和42.7%,最常见的不良反应是恶心和腹泻。
Lucasti等[35]开展的一项Ⅱ期临床试验,主要终点为ME人群在停止静脉治疗(DCIV)后的良好临床反应率。结果显示亚胺培南-西司他丁-雷利巴坦500 mg+250 mg组、500 mg+125 mg组和单用亚胺培南-西司他丁500 mg组的良好临床反应率分别为96.3%、98.8%和95.2%。安全性方面,所有治疗组与药物相关的不良反应事件发生率总体相似,大多为腹泻、恶心和呕吐。
5.3 碳青霉烯类耐药肠杆菌科细菌(CRE)
Wunderink等[36]开展了一项Ⅲ期研究,旨在评价美罗培南-法硼巴坦(2 g-2 g,1次/8 h)与最佳可用疗法(best-available therapy,BAT)治疗CRE感染的疗效和安全性。FDA指导下的主要终点为CRE感染的MITT(mCRE-MITT)人群的临床治愈率,美罗培南-法硼巴坦和BAT组(包括多黏菌素、碳青霉烯类、氨基糖苷类、替加环素的单药或联合治疗;头孢他啶-阿维巴坦的单药治疗)的临床治愈率分别为65.6%和33.3%。在安全性方面,美罗培南-法硼巴坦组大约有10%患者出现与治疗相关的不良反应,包括腹泻、贫血和低钾血症;而BAT组约10%患者出现败血症、感染性休克、腹泻、贫血、低血压和急性肾功能衰竭等不良反应。因此,与BAT相比,美罗培南-法硼巴坦用于治疗CRE感染可提高临床治愈率和降低肾毒性。
6 结语
新一代β内酰胺酶抑制剂表现出更广泛的抑酶作用,与β内酰胺类抗菌药物联合后显示出良好的临床疗效,是临床用于治疗产β内酰胺酶细菌感染的重要选择。但目前有一些报告提示某些菌株可能对头孢他啶-阿维巴坦产生耐药性,且产B类β内酰胺酶细菌感染的问题依然严峻。因此,如何有效预防耐药性的发生,并寻找新的药物组合以解决产B类β内酰胺酶耐药菌株的问题,是今后临床研发的方向。
