替吉奥在消化道肿瘤患者化疗中的应用及预后
2021-03-22吴晓玲傅育卡陈章兴
吴晓玲 傅育卡 陈章兴
近些年来,随着人们生活水平的提升及生活习惯的改变等多种因素的出现,我国肿瘤疾病的发病率呈现出上升趋势,并且逐渐趋于年轻化[1]。其中消化道肿瘤是临床常见的肿瘤之一,包括良性病变与恶性病变,前者通常患者全身一般无明显症状,死亡率较低,预后情况较为良好;后者生长速度较快,侵袭性生存,容易发生转移,治疗以后容易复发,可危及患者生命安全[2]。因此,对于恶性消化道肿瘤患者的治疗称为了临床的一大难点。由于患者在早期并未出现明显的临床症状,许多患者在入院确诊时已经进入了中期或者晚期,临床上常常以手术治疗为主,但疾病难以根除,常常采用化疗缓解病情进展[3]。随着消化道肿瘤患者的增多,常规化疗效果的局限性也随之显现。鉴于此,本文将对口服替吉奥进行化疗治疗对消化道肿瘤患者生存质量与药副反应发生情况进行分析,具体内容如下。
1 资料与方法
1.1 一般资料
选取本院2018年1月-2020年2月收治的165例消化道肿瘤患者作为研究对象。纳入标准:(1)确诊为消化道肿瘤;(2)预计生存时间超过3个月;(3)年龄在18周岁以上;(4)临床资料完整[4]。排除标准:(1)合并重度血小板减低;(2)合并严重心、肝、肾功能不全;(3)造血系统严重疾病;(4)患有精神病;(5)严重感染性疾病;(6)对本研究所用药物过敏;(7)口服药物禁忌证;(8)配合不佳[5]。按照治疗方法分为对照组(80例)和研究组(85例)。对照组男46例,女34例;年龄43~80岁,平均(57.69±10.22)岁;食管癌23例,结直肠癌26例,胃癌31例。研究组男50例,女35例;年龄44~80岁,平均(58.15±10.28)岁;食管癌26例,结直肠癌25例,胃癌34例。两组一般资料对比差异无统计学意义(P>0.05),有可比性。患者对研究知情同意并签署了相关协议,研究获得医院伦理委员会批准。
1.2 方法
对照组采用常规化疗治疗,研究组在常规化疗治疗基础上口服替吉奥进行化疗治疗。对照组接受常规化疗治疗,给予患者氟尿嘧啶(天津金耀药业有限公司,国药准字H12020959),采用静脉滴注的方式,2 d进行1次氟尿嘧啶治疗,每次治疗必须间隔24 h以上,0.25~0.75 g/次。1个疗程为10 d,1个疗程内,氟尿嘧啶的总用量不超过10 g,治疗2个疗程。
研究组口服替吉奥治疗(江苏恒瑞医药股份有限公司,国药准字H20100135),剂量为60~80 mg/m2,2次/d,每次均在饭后服用,1个疗程为14 d,在第1个疗程结束后,间隔7 d开始第2个疗程的治疗,治疗2个疗程。
1.3 观察指标及评价标准
对比两组无进展生存期、疾病控制、生存质量评分、药副反应发生情况。
无进展生存期:患者从接受治疗开始,到观察到疾病进展的这段时间。疾病控制情况:(1)完全缓解:患者的肿瘤病灶消失;(2)部分缓解:患者的肿瘤病灶明显缩小,病灶基线长径总和缩小幅度>30%;(3)稳定:患者的肿瘤病灶经治疗后没有变化,或者病灶基线长径总和缩小幅度≤30%,或者病灶基线长径总和增大幅度<20%;(4)进展:患者的原有肿瘤病灶明显增加,其病灶基线长径总和增大幅度≥20%,或有新病灶出现。疾病控制率=(完全缓解+部分缓解+稳定)/总例数×100%[6]。生存质量:采用QOL量表评定完成2个疗程的治疗后患者生存质量,该量表共10项问题,满分为60分,51~60分为良好,41~50分为较好,31~40分为一般,21~30分为差,≤20分为极差[7]。
1.4 统计学处理
本研究数据采用SPSS 23.0统计学软件进行分析和处理,计量资料以(±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组无进展生存期及疾病控制情况对比
对照组无进展生存期(2.91±0.68)个月,比研究组的(4.92±0.73)个月短(P<0.05)。研究组疾病控制率明显高于对照组(P<0.05),见表1。

表1 两组疾病控制情况对比 例(%)
2.2 两组生存质量对比
研究组生存质量评分级别的良好率、较好率均高于对照组(P<0.05),见表2。与治疗前相比,两组生存质量评分均增高,研究组生存质量评分高于对照组(P<0.05),见表3。

表2 两组生存质量对比 例(%)
表3 两组治疗前后生存质量评分对比 [分,(±s)]
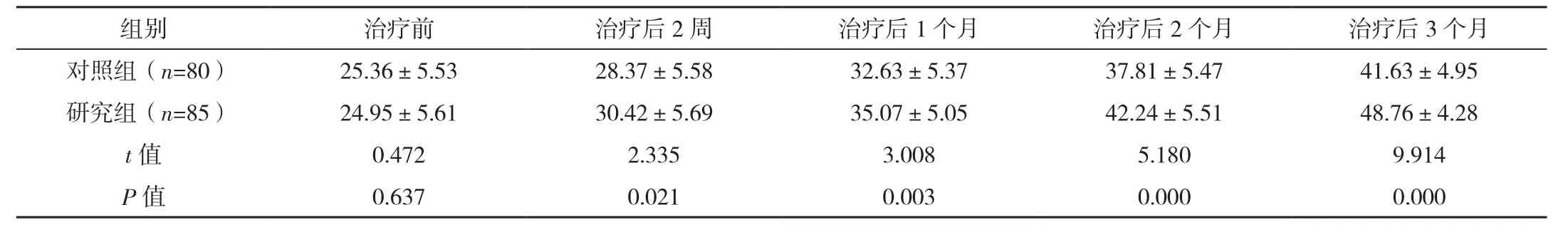
表3 两组治疗前后生存质量评分对比 [分,(±s)]
组别 治疗前 治疗后2周 治疗后1个月 治疗后2个月 治疗后3个月对照组(n=80) 25.36±5.53 28.37±5.58 32.63±5.37 37.81±5.47 41.63±4.95研究组(n=85) 24.95±5.61 30.42±5.69 35.07±5.05 42.24±5.51 48.76±4.28 t值 0.472 2.335 3.008 5.180 9.914 P值 0.637 0.021 0.003 0.000 0.000
2.3 两组药副反应发生情况对比
研究组药副反应发生率明显低于对照组(P<0.05),见表4。

表4 两组药副反应发生情况对比 例(%)
3 讨论
胃癌、食管癌、结肠癌、直肠癌等是我国临床上较为常见的几种消化道肿瘤。对于肿瘤患者而言,肿瘤一旦发展到晚期,癌细胞就会向其全身进行转移、扩散,直接造成患者体内其他器官受到严重的损伤,导致患者出现相关的并发症和功能性的障碍,引发躯体出现各种不适症状[8]。严重影响到患者的身心健康,同时又极大地降低了患者的生存质量,给患者增添痛苦。因此,对消化道肿瘤的治疗效果的研究具有重要意义。在用药研究上,关于药物对肿瘤进展改善的效果十分重视,此外,由于肿瘤患者机体本身就受到了侵害,导致其功能降低,若药物副作用过大会影响到整体疗效,对药副作用的控制也非常重视。
在既往临床中治疗消化道肿瘤时,较为常用的药物为铂类、拓扑异构酶抑制剂、氟尿嘧啶类及紫杉类,由于近年来消化道肿瘤患者不断增多,基础临床药物在疗效上的缺陷也随之显现出来,为提高治疗效果,对新药物的疗效研究成为重要的课题之一[9]。替吉奧是一种复方抗肿瘤化疗药物,该药物由日本首先研究开发,与以往临床上常采用的抗癌药物不同的是,该药物为口服用药[10]。替吉奧的成分主要为替加氟、奥替拉西钾、吉美嘧啶等。替加氟具有较高的口服生物利用度,当患者服用该药物后,替加氟能转变为具有抵抗肿瘤作用的5-FU[11]。其中的奥替拉西钾能有效降低对患者的毒副作用,减少化疗后的不良反应,提高了用药安全性及患者依从度[12]。吉美嘧啶属于一种生化调节剂,能够对酶分解患者体内氟尿嘧啶的这一过程产生抑制,促使氟尿嘧啶在患者的血浆、肿瘤组织中的浓度在较长的一段时间为处于稳定状态,该项优势有利于增强该药物的抗肿瘤活性[13]。在此次研究中,与接受常规化疗治疗的患者相比,接受替吉奥治疗的患者,其无进展生存期更长,疾病控制率更高,生存质量评分级别的良好率、较好率均更高,并且药副反应发生率更低。表明替吉奥不仅提升了消化道肿瘤的病情控制效果,延长了患者的生存期,并且提升了患者的生存质量,且该药物的用药安全性得以保证。在临床治疗上,为了进一步提高治疗效果,替吉奥还可以与其他抗癌药物进行联用,但需要注意的是,替吉奥不可与其他氟尿嘧啶类药物、亚叶酸、抗真菌药等药物进行联用,因为与上述药物联合会造成患者出现严重的血液循环类疾病[14]。因此,临床医生在治疗消化道肿瘤患者时,应严格掌握所选取的化疗药物的配伍禁忌等。
综上所述,在常规胡化疗治疗基础上,采用口服替吉奥进行化疗治疗消化道肿瘤,能有效延长患者的无进展生存期,提升疾病控制率,提高患者的生存质量,并且该药物的使用并未增加反而减少了药副反应,具有较高的用药安全性。
