甲磺酸阿帕替尼对晚期宫颈癌患者预后的影响研究
2021-03-22唐晓红周自纯伊富芳
唐晓红,周自纯,伊富芳
平顶山市妇幼保健院产后保健科,河南 平顶山 467000
宫颈癌是影响女性健康的第三大恶性肿瘤,据统计,全球每年有56.9万例新发确诊,死亡例数约为31.1万例。手术根治性切除、放疗和化疗是临床治疗宫颈癌的主要手段,可有效延长患者中位无进展生存期,但仍有部分患者出现肿瘤复发或转移。对于复发或转移性晚期宫颈癌患者,一般根据患者具体状况采取个体化治疗方案,一线治疗方案包括化疗、局部姑息放疗及生物靶向治疗,传统化疗因效果不佳且不良反应大,使患者生活质量大幅度下降,局部姑息放疗仅对寡转移病灶或发生骨转移的患者有效,故靶向性的生物制剂成为临床关注的重点。临床用于靶向性治疗的药物有甲磺酸阿帕替尼、贝伐珠单抗及舒尼替尼等,主要作用机制为抗血管生成。甲磺酸阿帕替尼主要作用于血管内皮生长因子受体2(vascular endothelial growth factor receptor 2,VEGFR2),是中国自主研发的口服抗肿瘤药物,经大量临床研究验证安全有效,可作为晚期胃癌、肝癌等一、二线治疗失败后的治疗方案。本研究探讨甲磺酸阿帕替尼在晚期宫颈癌中的应用效果及对预后的影响,现报道如下。
1 资料与方法
1.1 一般资料
收集2014年6月至2017年6月平顶山市妇幼保健院收治的标准方案治疗失败后采取甲磺酸阿帕替尼治疗的晚期宫颈癌患者的病历资料。纳入标准:均经过病理学检查确诊为晚期宫颈癌,且经标准方案治疗失败;美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)体力状况评分≤1分。排除标准:治疗前心、肝、肾功能及血压异常(药物控制效果不佳);临床及随访资料不全。根据纳入、排除标准,共纳入120例晚期宫颈癌患者,按治疗方案的不同分为观察组75例和对照组45例。对照组采取二线或二线以上化疗方案,观察组采取甲磺酸阿帕替尼联合二线或二线以上化疗方案。两组患者各临床特征比较,差异均无统计学意义(P
>0.05)(表1)。
表1 两组患者的临床特征
1.2 治疗方法
对照组根据患者具体状况采取二线或二线以上化疗,药物包括多西他赛、长春瑞滨、伊立替康、拓扑替康、氟尿嘧啶、铂类等,14天为1个化疗周期,共化疗6个周期。观察组给予甲磺酸阿帕替尼联合二线或二线以上化疗药物(同对照组)治疗,甲磺酸阿帕替尼用法用量:饭后半小时口服,剂量为500 mg/d,28天为1个治疗周期,连续服用3个周期。
1.3 疗效评价
评价标准:完全缓解(CR),肿瘤病灶消失且未发现新病灶;部分缓解(PR),肿瘤最大径缩小≥30%;疾病稳定(SD),肿瘤最大径缩小<30%或增大<20%;疾病进展(PD):肿瘤最大径增大≥20%或有新的病灶。客观有效率(objective response rate,ORR)=(CR+PR)例数/总例数×100%;疾病控制率(disease control rate,DCR)=(CR+PR+SD)例数/总例数×100%。
1.4 观察指标
①评价患者治疗期间的不良反应,包括高血压、手足综合征、蛋白尿、便秘或腹泻、乏力、肾功能受损等,参照抗肿瘤药物不良反应评价标准进行分级,并计算不良反应总发生率。②分析从化疗之日起3年内的随访资料,绘制生存曲线并计算中位总生存时间(overall survival,OS)及中位无进展生存时间(progression-free survival,PFS)。
1.5 统计学分析
采用SPSS 22.0软件对数据进行分析,符合正态分布且方差齐的计量资料以均数±标准差(x-
±s
)表示,多组比较采用单因素方差分析,两组比较采用两独立样本t
检验;计数资料以例数及率(%)表示,组间比较采用χ
检验;以Kaplan-Meier法绘制生存曲线,采用Log-rank法进行检验;多因素分析采用Cox比例风险回归模型;以P
<0.05为差异有统计学意义。2 结果
2.1 近期疗效的比较
观察组患者ORR、DCR分别为61.33%(46/75)、86.67%(65/75),均高于对照组的42.22%(19/45)、71.11%(32/45),差异均有统计学意义(χ
=4.138、4.393,P
<0.05)。(表2)
表2 两组患者的近期疗效[n(%)]*
2.2 不良反应发生情况的比较
两组患者不良反应主要为1级和2级,无4级不良反应,最常见的为高血压、手足综合征及蛋白尿,两组患者不良反应总发生率比较,差异无统计学意义(P
>0.05)。(表3)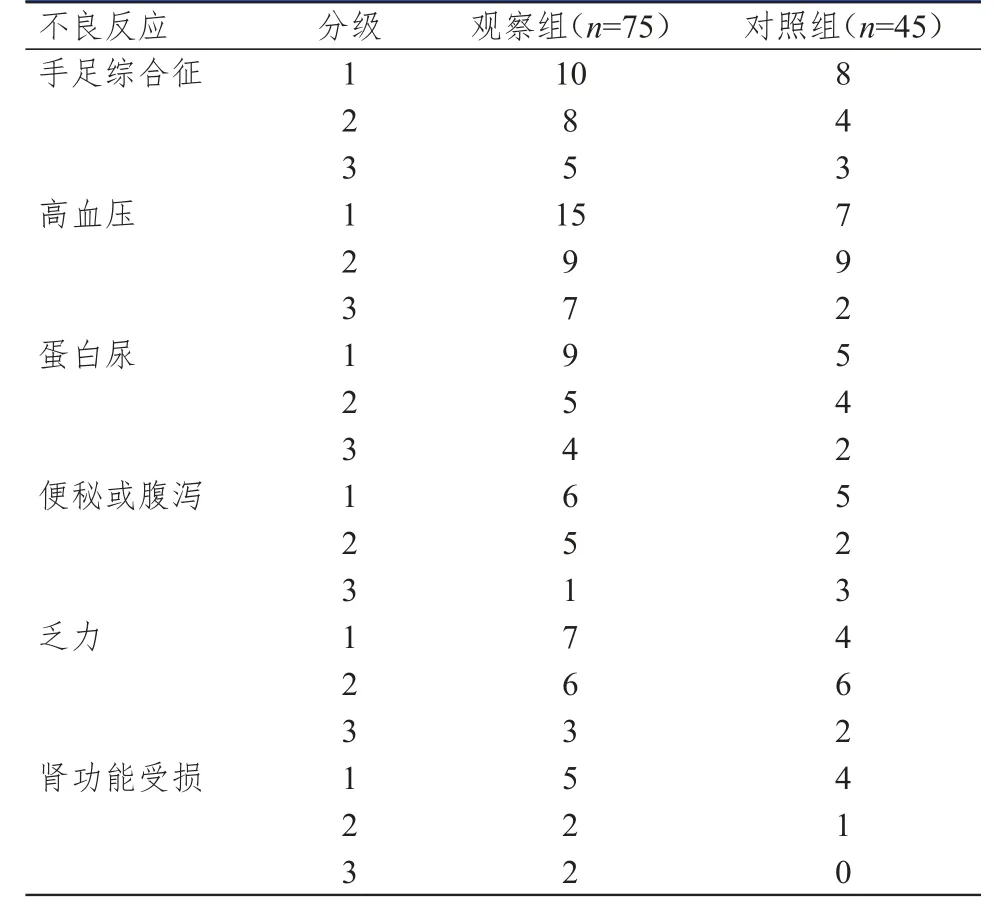
表3 两组患者不良反应发生情况
2.3 生存分析
观察组患者1年、2年、3年生存率分别为88.00%、38.70%、21.30%,对照组患者1年、2年、3年生存率分别为61.70%、25.10%、16.00%。观察组患者中位OS为20.00个月,长于对照组的14.68个月,差异有统计学意义(χ
=4.233,P
=0.040)。观察组患者中位PFS为15.20个月,长于对照组的10.98个月,差异有统计学意义(χ
=3.992,P
=0.046)。(图1、图2)
图1 观察组(n=75)与对照组(n=45)患者的生存曲线

图2 观察组(n=75)与对照组(n=45)患者的无进展生存曲线
2.4 晚期宫颈癌患者预后影响因素的单因素分析
不同年龄、ECOG评分、病理类型的晚期宫颈癌患者3年生存率比较,差异均无统计学意义(P
>0.05);不同肿瘤转移部位数量、临床分期及治疗方案的宫颈癌患者3年生存率比较,差异均有统计学意义(P
<0.05)。(表4)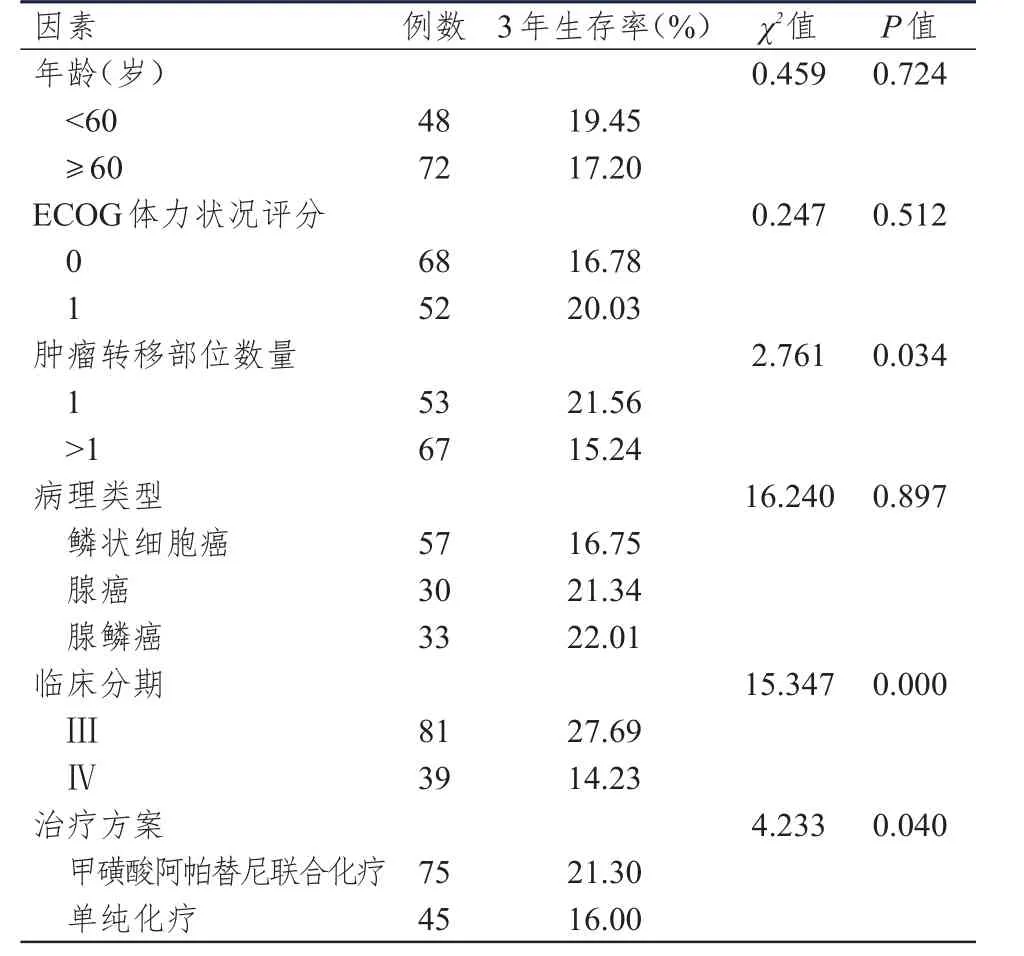
表4 晚期宫颈癌患者预后影响因素的单因素分析(n=120)
2.5 晚期宫颈癌患者预后影响因素的多因素分析
以单因素分析中差异有统计学意义的因素为自变量,OS为因变量,Cox比例风险回归分析结果显示,肿瘤转移部位数量>1个、临床分期为Ⅳ期、单纯化疗均是影响晚期宫颈癌患者OS的独立危险因素(P
<0.05)。(表5)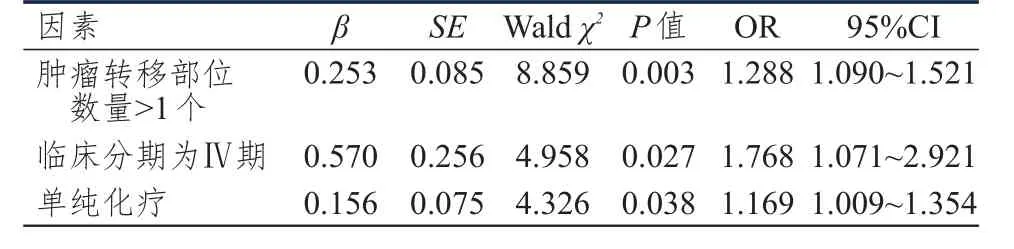
表5 晚期宫颈癌患者预后影响因素的Cox比例风险回归分析
3 讨论
宫颈癌是女性生殖系统常见恶性肿瘤,发病率仅次于乳腺癌,而且易发生复发或远处转移,预后不良。随着近年中国对宫颈癌知识的普及以及宫颈癌疫苗的推广,宫颈癌患者的5年生存率得到改善,但也仅仅在50%左右。相关报道显示,肿瘤的局部复发或远处转移是影响宫颈癌生存率的主要原因,约35%的患者初治后2年内再次复发或发生转移,由于不能再次进行手术或放疗,化疗成为这类患者主要的治疗手段,但疗效有限,不良反应严重。因此,寻找一种新的抗肿瘤药物用于标准方案治疗失败后的晚期宫颈癌患者成为临床亟待解决的问题。
随着生物医药的大力发展以及肿瘤机制研究的深入,针对肿瘤的靶向制剂成为临床研究的热点。研究显示,血管生成是维持组织新陈代谢的基本条件,但肿瘤血管形成会促使大量的氧气和营养物质被输送到肿瘤组织,导致肿瘤体积快速增长,进而引发血管生成增多,如此恶性循环最终造成肿瘤失控发生转移。因此,通过抗血管生成抑制肿瘤生长可作为治疗恶性肿瘤的一种有效途径。目前临床常见的抗血管生成药物有阿帕替尼、贝伐珠单抗及舒尼替尼等,临床仅推荐贝伐珠单抗作为复发或转移性晚期宫颈癌的一线药物,但长期用药不良反应多,如高血压、蛋白尿、栓塞等,而二线治疗方案尚无定论,免疫治疗是其中一个研究方向。最新研究显示,帕博利珠单抗作为二线药物治疗晚期宫颈癌,疗效尚可,但进口药物昂贵的价格导致临床应用受限。甲磺酸阿帕替尼是中国自主研发的抗血管生成药物,于2014年被国家批准作为晚期胃癌或胃-食管结合部腺癌三线及以上的治疗药物,而且在其他恶性肿瘤包括肝癌、肺癌、骨肉瘤、结直肠癌中也有较好的效果。甲磺酸阿帕替尼是作用于VEGFR2的酪氨酸激酶抑制剂,通过选择性地与VEGFR2胞内酪氨酸ATP结合位结合,使酪氨酸激酶的活性受到抑制,从而阻断下游信号通路,抑制肿瘤血管生成。
本研究结果显示,观察组患者ORR、DCR分别为61.33%、86.67%,均高于对照组的42.22%、71.11%,表明甲磺酸阿帕替尼对晚期宫颈癌患者的近期疗效显著。进一步分析两组生存情况显示,观察组患者中位OS及中位PFS均长于对照组,提示在二线治疗宫颈癌失败后甲磺酸阿帕替尼可作为后续治疗的选择,改善患者远期预后。关于阿帕替尼的体外细胞实验显示,一定浓度的阿帕替尼可抑制人宫颈癌细胞(SiHa)和人子宫鳞状细胞癌细胞(HCC94)的增殖,而且对化疗药物紫杉醇有增效作用。还有研究指出,阿帕替尼联合放疗对细胞分裂暂停期(G期)/DNA合成前期(G期)有明显的阻滞作用,在促进HaLa细胞凋亡方面作用不明显,其相关作用机制尚不清楚。比较两组患者不良反应发生情况发现,大多数患者不良反应为1级和2级,少数为3级,未发生严重的4级不良反应,而且高血压的发生率最高,其次是手足综合征和蛋白尿,但两组比较差异无统计学意义。本研究与既往临床研究结果一致,在甲磺酸阿帕替尼剂量减少或对症治疗后,患者的不良反应可降低至1级或消失,提示甲磺酸阿帕替尼具有较高的安全性,不会增加放化疗的不良反应。本研究进一步研究发现,晚期宫颈癌患者的3年生存率与患者年龄、ECOG体力状况评分、病理类型无关,而与肿瘤部位转移数量、临床分期、治疗方案有关。多因素Cox比例风险分析结果显示,临床肿瘤转移部位数量>1个、临床分期为Ⅳ期、单纯化疗均是影响晚期宫颈癌患者OS的独立危险因素,与既往研究结果一致。
综上所述,在标准化疗方案治疗失败后,甲磺酸阿帕替尼可明显改善晚期宫颈癌患者的近期及远期预后,且不良反应症状较轻,显示了较好的安全性。
