单肺通气期间出现低氧血症的病例分析1例
2021-03-19刘倩周瑜王小雨顾小萍
刘倩,周瑜,王小雨,顾小萍
(南京大学医学院附属鼓楼医院麻醉科,江苏 南京 210008)
1 患者资料
患者,男,76岁,身高175 cm,体质量89 kg,BMI 29.1 kg/m2,2011年,外院体检行胸部CT发现左肺上叶结节(体积不详),后每年定期复查,2013年结节体积增长至1.8 cm×1.0 cm,2014年复查胸部CT发现结节体积较前有增大、 实变倾向,周围见片状模糊影,边缘见支气管影,内可见空泡影,临近斜裂胸膜局部增厚,考虑早期肺癌可能,于2014年9月28日以“左肺占位”收入南京鼓楼医院。 既往有高血压病史,血压(BP)最高150/100 mmHg,服用氯沙坦钾氢氯噻嗪片降压治疗,检测BP波动在140~150/90~95 mmHg; 血糖偏高 2年,空腹血糖波动在6.0~6.5 mmol/L,未明确诊断糖尿病; 房颤病史3年,先后服用华法林、 阿司匹林肠溶片抗凝抗血小板治疗,后自行停用,入院时口服酒石酸美托洛尔片控制心室率。 结合病史、 检验检查报告等入院初步诊断为: (1)左肺占位; (2)高血压病2级(很高危); (3)持续性房颤。 入院后完善相关检查,继续行降压、 控制心室率治疗,予依诺肝素钠术前抗凝。 1 d后出现上呼吸道感染症状,予药物治疗,5 d后好转。 心脏彩超示: 左心房、 右心房增大,室间隔基底部增厚,三尖瓣中度、 二尖瓣轻中度反流,主动脉瓣钙化,轻度肺动脉高压[肺动脉收缩压(SBP)约 36 mmHg],EF值61%。 肺功能: 最大通气量偏低,F-V曲线示小气道气流受限,中度混合型通气功能障碍。 动态心电图示持续性心房颤动,最长R-R间期2.16 s,共67次室性早搏,间歇性T波低平。 结合相关检查及外院联合会诊,考虑为瘢痕基础上发生的恶性病变(瘢痕腺癌),建议手术治疗。 入院第23天,入手术室拟行“电视辅助胸腔镜(VATS)下左上肺肿块楔形切除术+淋巴清扫术”。
8: 00入室,入室后在局麻下行左侧桡动脉穿刺测压,心电监护动脉血压(IBP)124~146/86~92 mmHg,心电监护提示房颤心率,呼吸频率(RR) 30次/min; 吸纯氧状态下脉搏血氧饱和度(SpO2) 100%。 麻醉前评估: 左肺占位,高血压病2级(很高危),持续性房颤,ASA分级Ⅲ级。 8: 30全身麻醉诱导,依次给予咪达唑仑6 mg,维库溴铵12 mg,芬太尼0.75 mg,依托咪酯20 mg。 5 min后行双腔气管导管(F35R)右管插管,通气良好,纤维支气管镜确定导管定位良好,机控呼吸,RR 12次/min,氧流量 2 L/min,双肺通气。
9: 00行颈内静脉穿刺置管; 9: 20改右侧卧位,纤维支气管镜确定主管对位良好,行血气分析pH 7.40,动脉血二氧化碳分压(PaCO2) 41 mmHg,动脉血氧分压(PaO2) 231 mmHg,SpO2100%。
9: 30手术开始,予以右侧单肺通气(OLV),潮气量(VT)350 mL,RR 14次/min,气道峰压(Ppeak) 25 mmHg,麻醉维持: 2%丙泊酚20 mL/h,维库溴铵3 mg/h,瑞芬太尼0.5 mg/h,七氟醚1%间断吸入,IBP波动在88~120/57~70 mmHg,当SBP低于 90 mmHg时,停用七氟醚,予苯肾上腺素80 μg 静脉注射,同时丙泊酚减量至16 mL/h,瑞芬太尼 0.3 mg/h,IBP上升至正常。 SpO296%~98%。
10: 10,即OLV 40 min左右,患者出现SpO2缓慢降低,从96%降低至86%,IBP 92~100/55~62 mmHg,Ppeak 29 mmHg,立即予纤支镜检确定导管在位,手控呼吸,SpO2有所上升,约为90%,增大VT至450 mL,机控呼吸,10: 23行血气分析 pH 7.38,PaCO244 mmHg,PaO256 mmHg,SpO288%,PaO2低于60 mmHg,考虑患者有低氧血症,予短时双肺通气后再行OLV,减浅麻醉,停用吸入麻醉药,丙泊酚减量至12 mL/h,瑞芬太尼0.15 mg/h,苯肾上腺素100 μg间断静脉注射,维持IBP在120~ 140/70~80 mmHg,患者SpO2上升至100%。 手术切除病肺后,改为双肺通气。 11: 05手术结束,换双腔管为单管。 手术时间95 min,出血20 mL,尿量300 mL,补液量1500 mL,晶体液500 mL,胶体液1000 mL。 术后患者生命体征平稳,行血气分析检查正常,送患者回胸科监护室。
2 讨论
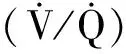
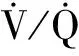
2.1 手术因素
2.1.1 手术体位 手术体位的变化通过影响肺血管血流引起肺内氧合的改变,重力作用是分流率和灌注的主要决定因素。 在侧卧位由于重力作用,非通气肺血流流向通气侧,从而有效减少肺内分流。 而仰卧位时肺部血流没有重力作用下的再分配,术侧肺有血流而无通气加重肺内分流,引起低氧血症。
2.1.2 术侧位置 左肺比右肺小约10%,左肺血流通常比右肺少,所以与右侧肺相比,左侧肺开胸术中氧合较好,出现低氧血症的机会较小。
2.2 麻醉因素
2.2.1 气管导管位置、 气囊压力及通畅性 双腔气管导管位置不当是引起OLV患者术中出现低氧血症的常见原因。 气囊压力过大致使气囊过度膨胀可能会覆盖到导管前端引起气道阻塞; 另外,反复的插管刺激可引起气道分泌物增多,堵塞气管导管,引起通气障碍而出现低氧血症。
2.2.2 麻醉药物 麻醉药物对于OLV下发生低氧血症的影响存在争议。 有研究发现,与七氟醚麻醉相比,丙泊酚能改善开胸肺叶切除术患者OLV期间的氧合和分流率[3]。 也有研究报道[4],丙泊酚对OLV或双肺通气时血流动力学和PaO2的影响与异氟醚相比无明显差异。
2.2.3 通气管理 OLV期间VT过低、 吸氧浓度过高容易引起患者肺不张,而VT过大、 呼气末正压(PEEP)值选择不当可能会导致患者通气肺过度膨胀,引起通气性肺损伤,这些因素可能会引起术中低氧血症的发生。
2.2.4 液体管理 快速过量补充晶体液稀释静脉血,使分流增加; 另外,在OLV过程中,心输出量会影响动脉氧合[5]。
2.3 患者因素
2.3.1 术前肺功能状态 通常肺功能异常在OLV过程中容易发生低氧血症,但并不是所有的肺功能指标都是可靠的指标。 Slinger等[6]研究发现,第1秒用力呼气量(FEV1)越小,OLV时氧合越好,FEV1与PaO2呈负相关。 这可能是在OLV期间,通气肺内的空气滞留可能产生呼气末自正压,从而降低通气肺内肺不张的可能性并改善氧合。
2.3.2 术前术侧的通气/血流匹配 如术侧有巨大的肿块或肺大泡,大的中心肿瘤对非依赖性肺的灌注较少,对依赖性肺的灌注较多,进行非依赖性肺切除时氧合反而得到更好的维持。 相反,小肿瘤(即孤立结节)患者在OLV期间有更多的灌注到非依赖性肺,这些患者在术中有出现短暂低氧血症的倾向。
2.3.3 患者体质量 肥胖患者因自身生理病理变化影响通气和氧合。 在一项研究中[7],与非肥胖患者相比,14例BMI>30 kg/m2的胸外科手术期间需要OLV的肥胖患者在术中及术后出现低氧血症的次数更多。
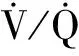
对于接受肺叶切除术患者,OLV是常用的保持通气和氧合的操作技术,可以促进CO2的消除,减少术后肺功能损伤。 尤其是长时间OLV是导致患者术中出现低氧血症的危险因素之一。 对于如何预防和减少术中OLV患者发生低氧血症是麻醉医生在围术期需要关注的问题。
(1)改善术前肺功能: 术前检查或OLV前双肺通气时的血气分析发现异常低的PaO2可能是一个可靠的肺功能异常的指标,可以预测OLV期间的低氧血症。 Slinger等[6]发现,在自主呼吸期间,甚至在双肺通气期间,PaO2水平与OLV期间的PaO2呈强正相关。 术前改善肺功能不仅能减少术后肺部并发症,而且能改善OLV时的氧合,包括物理治疗、 药物扩张支气管和排出分泌物。
(2)关注肺部血流灌注: 由于肺内分流依赖于未氧合的血液占心输出量的百分比,不通气肺灌注越少,通气肺灌注越多,OLV时PaO2越高。 术前测量两肺之间的灌注分布可能有助于预测OLV期间的低氧血症。 很多接受胸外科大手术的患者可能在手术前做了灌注扫描,所以麻醉医生需要提前了解扫描的结果,提前做好应急准备。
(3)通气策略: 术中根据患者的情况和现有的最佳临床证据来制定最适合患者需要的通气策略。 指南指出[8],压力控制或压力控制保证容量可用于OLV的肺切除患者; 推荐保护性机械通气即VT为 6~8 mL/kg,PEEP为5 cmH2O,控制Ppeak<40 cmH2O。 OLV条件下提高肺顺应性,获得较好的肺通气量,以改善患者的低氧血症。 通过吸气时间的相对延长 [降低RR和吸呼比(I∶E)],可使通气量增加,气道内压力降低,提高肺顺应性。 有报道称,与1∶2相比,I∶E设置1∶1可以降低气道压力,改善肺顺应性[9],这与指南中推荐是一致的。 指南[8]还建议术侧肺行持续气道正压或高频通气可减少该侧肺血流,提高氧合,可用于肺叶切除和OLV的患者,有利于改善短期氧合。
(4)药物选择: 右美托咪定静脉滴注联合吸入异氟醚可增强HPV,从而在OLV期间改善氧合[10]。 丙泊酚或异氟醚似乎对动脉氧合没有显著影响,可作为胸外科手术的合适麻醉药物,使术中CO2梯度范围正常化[11]。
对于需要术中OLV的患者,麻醉医生在术前评估时需充分了解患者各项生理机能,预测可能造成术中出现低氧血症的影响因素,制定合理的麻醉及管理方案,以减少术中低氧血症的发生; 当OLV患者术中出现低氧时,即时给予纠正,迅速诊断病因,确保麻醉手术中患者氧合正常和患者生命安全。
