宽苞糙苏根降三萜化学成分研究
2021-03-17邓瑞雪黄玉阳许艺凡
邓瑞雪,黄玉阳,许艺凡,刘 普
宽苞糙苏根降三萜化学成分研究
邓瑞雪,黄玉阳,许艺凡,刘 普*
洛阳市天然产物功能因子研究及产品开发重点实验室,河南科技大学化工与制药学院,河南 洛阳 471023
研究宽苞糙苏var根降三萜类化学成分。用硅胶柱色谱、凝胶柱色谱、以及制备高效液相色谱等多种色谱分离手段进行分离纯化,用有机波谱手段鉴定分离得到的化合物结构。从宽苞糙苏根的95%乙醇提取物中分离得到8个降三萜类化合物,分别鉴定为糙苏醛A(1)、糙苏酮(2)、糙苏四醇A(3)、糙苏四醇 B(4)、糙苏六醇A(5)、糙苏六醇B(6)、糙苏六醇C(7)、糙苏六醇D(8)。化合物1为新化合物,化合物3、4、6~8为首次从宽苞糙苏中分离得到的化合物,这些化合物表现出一定的肿瘤细胞抑制活性。
宽苞糙苏;降三萜;抗肿瘤;糙苏醛A;糙苏四醇A;糙苏六醇B
糙苏属Linn.是被子植物门木兰纲野芝麻亚族下的1个属,该属植物多为多年生草本,全球共有约100种,分布于地中海,亚洲中部至东部。我国有60余种(变种/变型),分布于全国各地,西南各省区种类最多[1-2]。药用植物糙苏Turcz. 生长于疏林下或草坡上,广泛分布在全国各地。民间以糙苏根入药,性苦、辛,微温,具有消肿、生肌、续筋、接骨,以及补肝、肾,强腰膝、安胎等功效[3-4]。研究发现,药用植物糙苏中主要化学成分有苯乙醇苷类、三萜类、二萜类、环烯醚萜苷类、黄酮类、多糖和挥发油等[5-15]。课题组前期研究了湖北恩施土家药“四楞麻”(糙苏根)的化学成分及其活性,从中分离得到一系列结构新颖的28-降齐墩果烷型螺环三萜(降三萜)类化合物,活性测试显示该类化合物具有较好的生物活性[16-21]。宽苞糙苏Turcz. var.Sun ex C. H. Hu为药用植物糙苏的1个变种。课题组前期对宽苞糙苏的化学成分进行了初步研究,发现其中也含有降三萜类化合物[22]。为了进一步阐明宽苞糙苏降三萜类化合物结构及活性特点,本研究对其降三萜类化学成分进行了分离鉴定,采用硅胶柱色谱、凝胶柱色谱以及制备高效液相色谱等多种分离方法,从宽苞糙苏的95%乙醇提取物中分离得到8个降三萜类化合物(图1),分别鉴定为糙苏醛A(phlomisal A,1)、糙苏酮(phlomisone,2)、糙苏四醇A(phlomistetraol A,3)、糙苏四醇A(phlomistetraol B,4)、糙苏六醇A(phlomishexaol A,5)、糙苏六醇B(phlomishexaol B,6)、糙苏六醇C(phlomishexaol C,7)和糙苏六醇D(phlomishexaol D,8)。其中,化合物1为新化合物,化合物3、4、6~8为首次从宽苞糙苏中分离得到的化合物,这些降三萜类化合物表现出一定的抑制肿瘤细胞活性。该研究为宽苞糙苏的研究开发利用奠定了基础。
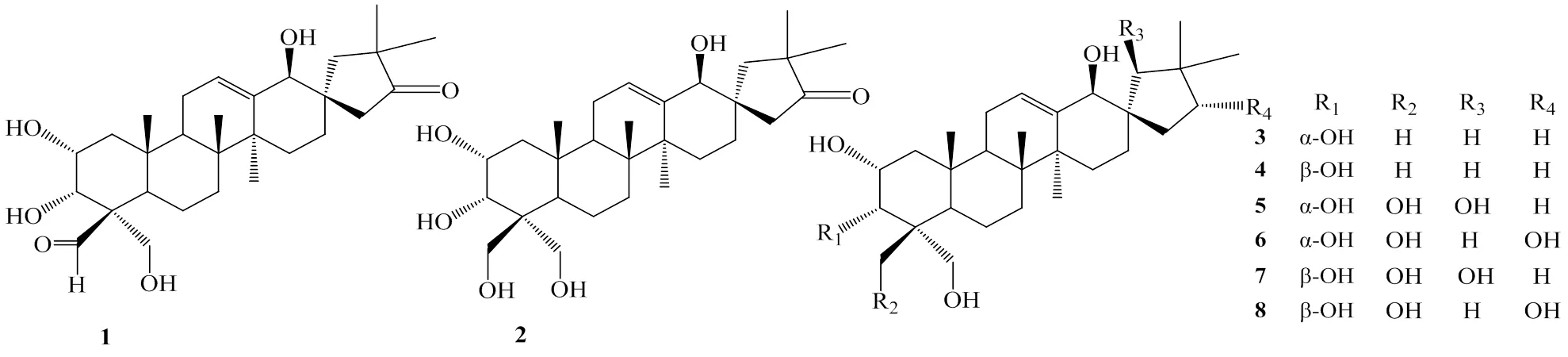
图1 化合物1~8的结构
1 仪器与材料
Bruker AVANCE 400 MHz核磁共振仪(Bruker公司,瑞士);Alliance 2695,Quattro Micro TM ESI液质联用色谱仪(Waters公司,美国);Waters 600制备高效液相色谱仪(Waters公司,美国);制备HPLC色谱柱:YMC SL12S05-2520 WT柱(250 mm×20 mm,5 μm,YMC公司),YMC ODS-A柱(250 mm×22 mm,10 μm,YMC公司);凝胶色谱柱(Toyopearl HW-40C,Tosoh公司);柱色谱和薄层色谱用硅胶(青岛海洋化工厂);所用试剂均为分析纯。
药材根于2015年9月采自河南省嵩县车村镇,由河南农业大学农学院高致明教授鉴定宽苞糙苏Turcz. var.Sun ex C. H. Hu的根,标本(FNS2015012)存放于河南科技大学天然产物资源标本馆。
实验用人非小细胞肺癌A549细胞、人宫颈癌HeLa细胞、小鼠成纤维L929细胞、人结肠癌HT-29细胞、人结肠癌HCT-116细胞、人脐静脉内皮HUVEC和人正常干细胞WRL-68由河南科技大学第一附属医院提供。其他生化试剂购自洛阳市洛龙区科迈教学仪器经销部。
2 提取与分离
取自然干燥的宽苞糙苏根10.5 kg,粉碎后用95%乙醇加热回流提取3次,每次4 h,提取液减压浓缩得乙醇粗提物浸膏。取乙醇粗提物加入适量的蒸馏水搅拌,制备得到乙醇混悬液。然后依次加入不同溶剂分别萃取,收集萃取液减压浓缩除去溶剂,得石油醚浸膏55 g、醋酸乙酯浸膏83 g、正丁醇浸膏410 g。
取糙苏根醋酸乙酯萃取层浸膏80 g,采用硅胶柱色谱分离,分别用氯仿-甲醇(15∶1、12∶1、9∶1、5∶1、3∶1、1∶1)梯度洗脱,经过薄层色谱(TLC)分析合并获得到22个流分Fr. 1~22。Fr. 8(3.6 g)采用硅胶柱色谱分离,氯仿-甲醇(15∶1、13∶1、11∶1、9∶1、7∶1、5∶1)梯度洗脱,得到组分Fr. 8.1~8.8。Fr. 8.3(569 mg)采用半制备高效液相色谱分离 [体积流量5 mL/min,甲醇-水(3∶7),色谱柱ODS-AQ],得到化合物3(R=12.65 min,14.6 mg)和6(R=18.23 min,12.3 mg)。Fr. 8.6(765 mg)采用半制备高效液相色谱分离[体积流量5 mL/min,甲醇-水(3∶7),色谱柱ODS-AQ],得到化合物4(R=9.36 min,8.9 mg)、7(R=12.37 min,20.3 mg)和8(R=17.66 min,15.4 mg)。Fr. 12(2.5 g)经过TLC分析,采用半制备高效液相色谱分离[体积流量5 mL/min,流动相甲醇-水(4∶6)],色谱柱ODS-AQ],得到化合物1(18.5 mg)。Fr. 14(5.8 g)采用硅胶柱色谱分离,氯仿-甲醇(8∶1、6∶1、4∶1、5∶1、3∶1、1∶1)梯度洗脱,得到组分Fr. 14.1~14.4。Fr. 14.4以半制备高效液相色谱分离[体积流量5 mL/min,流动相甲醇-水(8∶2),色谱柱ODS-AQ],得到化合物2(R=15.61 min,35.6 mg)。Fr. 17(3.3 g)经过Sephadex LH-20凝胶柱分离得到流分Fr. 17.1~17.4,Fr. 17.4采用半制备高效液相色谱分离[体积流量5 mL/min、流动相甲醇-水(4∶6)、色谱柱ODS-AQ],得到化合物5(R=13.47 min,9 mg)。
3 结构鉴定
化合物1的1H-NMR (600 MHz, C5D5N) 表明化合物有5个甲基单峰信号H0.91 (3H, s), 0.97 (3H, s), 1.02 (3H, s), 1.17 (3H, s), 1.34 (3H, s);3个与吸电子相连次甲基质子峰信号H4.18 (1H, brs), 4.51 (1H, m), 5.22 (1H, br s);1个和吸电基团相连的亚甲基质子信号H4.33 (2H, d,= 11.0 Hz);1个双键质子信号H6.22 (1H, brs) 和1个醛基质子信号H10.17 (1H, s)。
化合物1的13C-NMR (150 MHz, C5D5N) 和DEPT谱数据,在低磁场区域可以观测到1个酮羰基碳信号C221.8,1个醛羰基碳信号C205.5 (s)] 和1个双键碳信号C119.3 (d), 142.0 (s);还可以在中低磁场区域观测到3个吸电子基团取代次甲基碳信号C65.6, 74.7, 69.3和1个吸电基团取代的亚甲基碳信号C63.3;较高场可以看到5个甲基碳信号C16.2, 17.7, 22.5, 28.8, 25.3;9个亚甲基的碳信号C45.8, 17.9, 34.2, 23.3, 27.4, 35.3, 39.4, 41.0, 50.3,2个次甲基的碳信号C42.6, 46.4;6个季碳信号: 59.1, 39.3, 38.5, 43.9, 43.0, 44.9(表1)。以上波谱数据显示该化合物的碳数目为29,其中存在1个双键碳信号,4个与羟基基团相连接的碳信号,1个醛羰基碳信号和1个酮羰基碳信号。
从以上波谱数据信息可以看出化合物1和从糙苏中分离得到的28-降齐墩果烷型螺环三萜类化合物波谱特征相似[16-21],因此推测化合物1也为齐墩果烷型的降三萜类化合物。从化合物的氢谱数据和碳谱数据可以看出,化合物1与从该植物中分离得到的降三萜类化合物phlomisone的核磁共振数据非常相似[20-21]。与化合物phlomisone相比,化合物1少了一组被羟基取代的次甲基质子信号和与吸电子基团氧相连的碳信号,多了1个醛基质子信号和醛羰基碳信号,推测化合物1可能为化合物phlomisone中的1个仲醇基团被氧化为醛基基团。
从化合物1的HMBC相关可以推出,化合物1分子中的4个羟基分别连在C-2、C-3、C-18和C-23上(表1和图2)。H-19 到C-18、C-20、C-21和C-22的HMBC相关,从H-29到C-19, C-20和C-21的HMBC相关,以及从H-22到C-18, C-19, C-20和C-21的HMBC相关可以推测酮羰基在C-21位上。同样,从化合物1的H-23到C-24, H-3到C-24, H-5到C-24的HMBC相关可以看出,化合物1中醛基连接在C-24位。从H-5和H-23的NOESY相关可以推测C-23位有羟基取代。
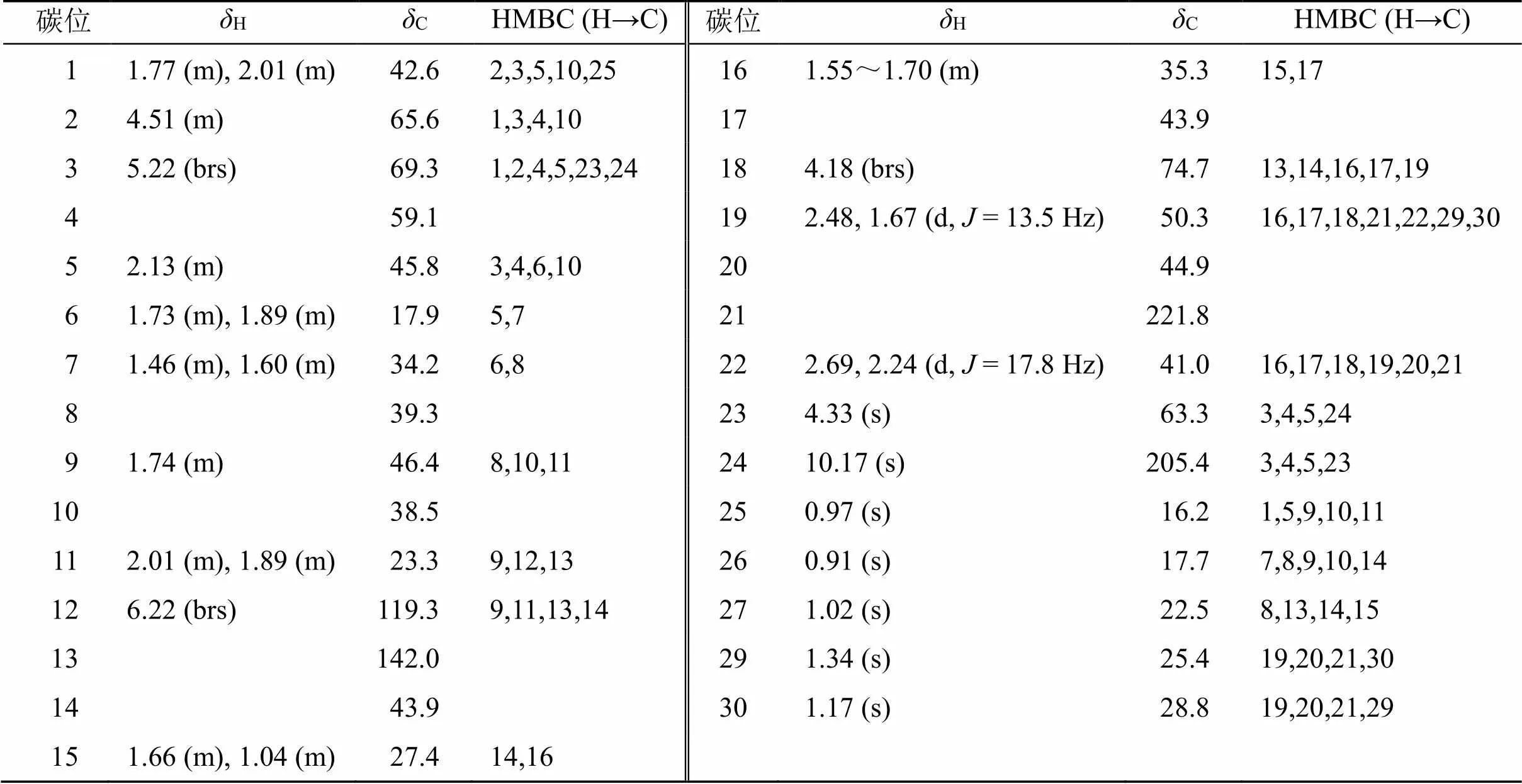
表1 化合物1的核磁共振数据(600/150 MHz, C5D5N)
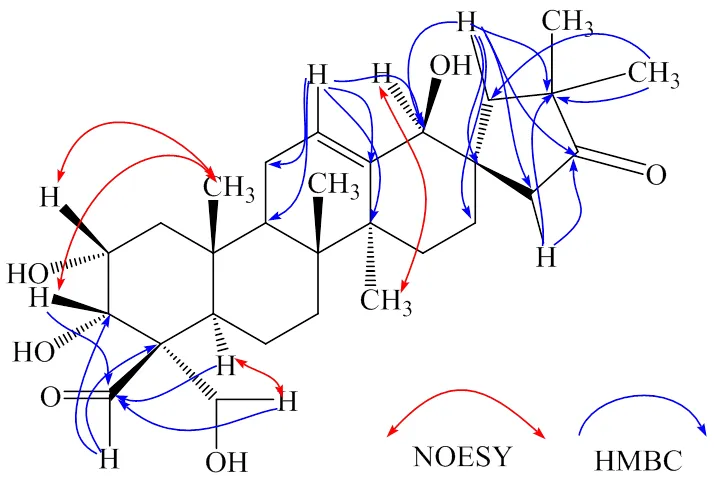
图2 化合物1的主要HMBC和NOESY相关
化合物1的相对构型可以通过NOESY相关来确定。从化合物1中H-2和H-25,以及H-3和H-25之间的NOESY相关可以推测C-2和C-3的羟基为α构型;从H-18和H-27的NOESY相关可以推测C-18的羟基为β构型。因此化合物1的相对构型与文献报道的化合物phlomisone一致[20-21]。故化合物1鉴定为(17)-2α,3α,18β,23-tetrahydroxy-19(18→17)- abeo-28-norolean-12-en-21-oxo-24-aldehyde,通过检索SciFinder,发现该化合物为未见文献报道的新化合物,命名为糙苏醛A。
化合物2:白色晶体(甲醇);mp 289.5~290.5 ℃;ESI-MS:513 [M+Na]+,分子式为C29H46O6;1H-NMR (400 MHz, C5D5N): 0.97 (3H, s, H-26), 1.10 (3H, s, H-27), 1.18 (3H, s, H-25), 1.22 (3H, s, H-29), 1.39 (3H, s, H-30), 1.90, 2.55 (各1H, d,= 13.5 Hz, H-19), 2.21, 2.75 (各1H, d,= 17.6 Hz, H-22), 4.10, 4.27 (各1H, d,= 11.0 Hz, H-24), 4.25 (1H, brs, H-18), 4.44, 4.65 (各1H, d,= 11.1 Hz, H-23), 4.52 (1H, m, H-2), 5.14 (1H, brs, H-3), 6.25 (1H, brs, H-12);13C-NMR (100 MHz, C5D5N): 44.0 (C-1), 66.9 (C-2), 74.3 (C-3), 48.1 (C-4), 45.5 (C-5), 19.5 (C-6), 35.3 (C-7), 40.3 (C-8), 48.5 (C-9), 38.8 (C-10), 24.1 (C-11), 120.0 (C-12), 142.7 (C-13), 44.7 (C-14), 28.3 (C-15), 36.1 (C-16), 43.7 (C-17), 75.5 (C-18), 51.1 (C-19), 45.8 (C-20), 222.1 (C-21), 41.8 (C-22), 69.8 (C-23), 64.7 (C-24), 18.0 (C-25), 18.3 (C-26), 23.5 (C-27), 26.2 (C-28), 29.5 (C-29)。以上波谱数据与文献报道的数据基本一致[20-21],故鉴定化合物2为糙苏酮。
化合物3:白色无定形粉末;ESI-MS:483 [M+Na]+,分子式为C29H48O4;1H-NMR (400 MHz,CD3OD): 0.80 (3H, s, H-24), 0.98 (3H, s, H-26), 1.02 (3H, s, H-29), 1.03 (3H, s, H-30), 1.08 (3H, s, H-25), 1.14 (3H, s, H-27), 3.41, 3.54 (各1H, d,= 11.0 Hz, H-23), 3.61 (1H, brs, H-3), 3.90 (2H, m, H-2, 18), 5.78 (1H, brs, H-12);13C-NMR (100 MHz, CD3OD): 42.7 (C-1), 67.3 (C-2), 78.9 (C-3), 42.7 (C-4), 44.5 (C-5), 19.1 (C-6), 34.7 (C-7), 40.8 (C-8), 48.3 (C-9), 39.3 (C-10), 24.0 (C-11), 119.2 (C-12), 143.7 (C-13), 45.4 (C-14), 28.2 (C-15), 37.1 (C-16), 51.2 (C-17), 76.4 (C-18), 53.1 (C-19), 39.9 (C-20), 43.1 (C-21), 30.8 (C-22), 71.4 (C-23), 17.8 (C-24), 17.9 (C-25), 18.3 (C-26), 23.6 (C-27), 30.5 (C-28), 30.7 (C-29)。以上波谱数据与文献报道的数据基本一致[20],故鉴定化合物3为糙苏四醇A。
化合物4:白色无定形粉末;ESI-MS:483 [M+Na]+,分子式为C29H48O4;1H-NMR (400 MHz, CD3OD): 0.71 (3H, s, H-24), 0.98 (3H, s, H-25), 1.02 (3H, s, H-29), 1.04 (3H, s, H-30), 1.10 (3H, s, H-26), 1.12 (3H, s, H-27), 3.26, 3.51 (各1H, d,= 11.0 Hz, H-23), 3.38 (1H, d,= 9.6 Hz, H-3), 3.74 (1H, m, H-2), 3.90 (1H, brs, H-18), 5.78 (1H, brs, H-12);13C-NMR (100 MHz, CD3OD): 48.1 (C-1), 69.8 (C-2), 78.3 (C-3), 44.2 (C-4), 48.2 (C-5), 19.1 (C-6), 34.6 (C-7), 40.7 (C-8), 48.6 (C-9), 39.0 (C-10), 24.1 (C-11), 119.2 (C-12), 143.7 (C-13), 45.3 (C-14), 28.1 (C-15), 37.0 (C-16), 31.2 (C-17), 76.4 (C-18), 53.1 (C-19), 39.8 (C-20), 43.1 (C-21), 30.7 (C-22), 66.3 (C-23), 14.1 (C-24), 18.1 (C-25), 18.2 (C-26), 23.7 (C-27), 30.5 (C-28), 30.5 (C-29)。以上波谱数据与文献报道的数据基本一致[20],故鉴定化合物4为糙苏四醇B。
化合物5:白色无定形粉末;ESI-MS:515 [M+Na]+,分子式为C29H48O6;1H-NMR (400 MHz, C5D5N): 1.09 (3H, s, H-27), 1.12 (3H, s, H-26), 1.19 (3H, s, H-25), 1.27 (3H, s, H-30), 1.32 (3H, s, H-29), 4.14, 4.28 (各1H, d,= 11.1 Hz, H-24), 4.48 (1H, m, H-2), 4.50, 4.66 (各1H, d,= 11.1 Hz, H-23), 4.53 (1H, brs, H-18), 4.75 (1H, s, H-19), 4.92(1H, brs, H-3), 6.36 (1H, brs, H-12);13C-NMR (100 MHz, C5D5N): 44.0 (C-1), 67.1 (C-2), 74.3 (C-3), 48.1 (C-4), 45.5 (C-5), 19.6 (C-6), 35.2 (C-7), 40.4 (C-8), 48.6 (C-9), 38.8 (C-10), 24.2 (C-11), 119.2 (C-12), 144.3 (C-13), 44. 5 (C-14), 27.3 (C-15), 29.3 (C-16), 51.9 (C-17), 73.8 (C-18), 82.7 (C-19), 43.1 (C-20), 38.8 (C-21), 28.4 (C-22), 69.6 (C-23), 64.8 (C-24), 17.9 (C-25), 18.4 (C-26), 23.6 (C-27), 22.5 (C-28), 29.8 (C-29)。以上波谱数据与文献报道的数据基本一致[20],故鉴定化合物5为糙苏六醇A。
化合物6:白色无定形粉末;ESI-MS/: 515 [M+Na]+,分子式为C29H48O6;1H-NMR (400 MHz, CD3OD): 0.96 (3H, s, H-26), 0.97 (3H, s, H-30), 1.02 (3H, s, H-27), 1.06 (3H, s, H-25), 1.14 (3H, s, H-29), 3.45 (1H, d,= 4.1 Hz, H-21), 3.60, 3.70 (各1H, d,= 11.1 Hz, H-24), 4.16 (2H, m, H-2, 18), 3.71, 3.91 (各1H, d,= 11.1 Hz, H-23), 4.02 (1H, brs, H-3), 5.83 (1H, brs, H-12);13C-NMR (100 MHz, CD3OD): 43.0 (C-1), 67.2 (C-2), 73.8 (C-3), 48.0 (C-4), 45.1 (C-5), 19.6 (C-6), 35.3 (C-7), 40.8 (C-8), 48.8 (C-9), 39.1 (C-10), 24.2 (C-11), 120.1 (C-12), 143.1 (C-13), 45.0 (C-14), 28.5 (C-15), 38.5 (C-16), 48.5 (C-17), 75.2 (C-18), 50.1 (C-19), 45.1 (C-20), 82.0 (C-21), 39.5 (C-22), 69.1 (C-23), 64.6 (C-24), 17.7 (C-25), 18.1 (C-26), 23.3 (C-27), 24.1 (C-28), 29.3 (C-29)。以上波谱数据与文献报道的数据基本一致[20],故鉴定化合物6为糙苏六醇B。
化合物7:白色无定形粉末;ESI-MS/: 515 [M+Na]+,分子式为C29H48O6;1H-NMR (400 MHz, C5D5N): 1.08 (3H, s, H-27), 1.15 (3H, s, H-26), 1.20 (3H, s, H-25), 1.29 (3H, s, H-29), 1.31 (3H, s, H-30), 4.15, 4.28 (各1H, d,= 11.2 Hz, H-24), 4.51 (1H, m, H-2), 4.47, 4.65 (各1H, d,= 11.4 Hz, H-23), 4.55 (1H, brs, H-18), 4.76 (1H, s, H-19), 4.42 (1H, d,= 9.7 Hz, H-3), 6.31 (1H, brs, H-12);13C-NMR (100 MHz, C5D5N): 48.3 (C-1), 69.6 (C-2), 80.1 (C-3), 48.4 (C-4), 49.1 (C-5), 19.5 (C-6), 34.3 (C-7), 40.4 (C-8), 48.6 (C-9), 38.7 (C-10), 24.2 (C-11), 119.2 (C-12), 144.3 (C-13), 44.6 (C-14), 27.3 (C-15), 28.4 (C-16), 51.5 (C-17), 73.8 (C-18), 82.8 (C-19), 43.2 (C-20), 38.8 (C-21), 29.4 (C-22), 69.6 (C-23), 64.5 (C-24), 18.1 (C-25), 18.4 (C-26), 23.7 (C-27), 29.9 (C-28), 22.5 (C-29)。以上波谱数据与文献报道的数据基本一致[19],故鉴定化合物7为糙苏六醇C。
化合物8:白色无定形粉末;ESI-MS/: 515 [M+Na]+,分子式为C29H48O6;1H-NMR (400 MHz, C5D5N): 1.07 (3H, s, H-26), 1.08 (3H, s, H-29), 1.10 (3H, s, H-27), 1.21 (3H, s, H-25), 1.32 (3H, s, H-30), 3.84 (1H, m, H-21), 4.12, 4.26 (各1H, d,= 11.2 Hz, H-24), 4.33 (2H, m, H-2, 18), 4.46, 4.66 (各1H, d,= 11.2 Hz, H-23), 4.40 (1H, d,= 9.7 Hz, H-3), 6.33 (1H, brs, H-12);13C-NMR (100 MHz, C5D5N): 48.4 (C-1), 69.5 (C-2), 80.2 (C-3), 48.3 (C-4), 49.1 (C-5), 19.6 (C-6), 34.2 (C-7), 40.3 (C-8), 48.6 (C-9), 38.8 (C-10), 24.1 (C-11), 119.7 (C-12), 143.5 (C-13), 44.6 (C-14), 28.2 (C-15), 38.1 (C-16), 49.7 (C-17), 74.6 (C-18), 49.9 (C-19), 44.9 (C-20), 81.5 (C-21), 39.8 (C-22), 69.7 (C-23), 64.8 (C-24), 17.9 (C-25), 18.3 (C-26), 23.5 (C-27), 29.5 (C-29), 25.0 (C-30)。以上波谱数据与文献报道的数据基本一致[19],故鉴定化合物8为糙苏六醇D。
4 抑制肿瘤细胞活性测试
采用MTT方法[23],评价了分离得到的降三萜类化合物对待测细胞株的抑制作用。
降三萜类化合物抑制肿瘤细胞的活性见表2。研究结果显示,分离得到的降三萜类化合物对多种肿瘤细胞株均具有一定的抑制作用。所有8个化合物对3种肿瘤细胞A549、HT-29和HCT-116均具有较强的抑制作用,其IC50值均小于50 μg/mL;化合物1、2、4和6~8对肿瘤细胞株Hela和L929表现出较强的抑制作用。所有化合物对HUVEC和WRL-68细胞的抑制作用较弱,这表明降三萜类化合物对正常细胞株没有明显的毒性作用。
5 讨论
采用多种分离方法,从宽苞糙苏根的95%乙醇提取物中分离得到8个28-降齐墩果烷型螺环三萜类化合物,其中,化合物1为新化合物,化合物3、4和6~8为首次从宽苞糙苏中分离得到的化合物。
28-降齐墩果烷型螺环三萜类化合物是一种结构罕见的化合物,生源关系的研究推测该类化合物可能由齐墩果烷型三萜转化得到[20]。28-降齐墩果烷型螺环三萜目前只在唇型科(Labiatae)糙苏属Linn. 植物Falc. ex Benth.[24]和Poir.[25],钩萼草属Benth.植物Benth.[26],钩子木属Kud. 植物(Rehd.) Kudo[27]以及益母草属Linn.植物益母草Sweet[28]等植物中被分离得到。由于从这些植物中分离得到的该类化合物数量和质量都比较少,尚未有关于该类型化合物活性研究的文献报道。课题组从药用植物糙苏及其变种宽苞糙苏中分离得到一系列28-降齐墩果烷型螺环三萜类化合物。从文献报道可以看出,28-降齐墩果烷型螺环三萜目前只在唇形科植物中被发现,并在糙苏属植物中分布较多。上述研究揭示28-降齐墩果烷型螺环三萜类化合物有可能是唇形科,尤其是糙苏属植物中的具有代表性的活性成分,该类成分在糙苏属的其它物种中也可能有分布。因此有必要对28-降齐墩果烷型螺环三萜类化合物进行深入的化学成分的分离和活性测定的研究。

表2 分离得到的化合物的抗肿瘤活性
利益冲突 所有作者均声明不存在利益冲突
[1] 中国植物志编辑委员会. 中国植物志(第66卷) [M]. 北京: 科学出版社, 1977: 119-905.
[2] Li M X, Shang X F, Jia Z P,. Phytochemical and biological studies of plants from the genus[J]., 2010, 7(2): 283-301.
[3] 中国科学院植物研究所. 中国高等植物图鉴(第二册)[M]. 北京: 科学出版社, 1980: 650.
[4] 南京中医药大学. 中药大辞典[M]. 上海: 上海科学技术出版社, 2006: 3759.
[5] Shang X F, Wang J H, Li M X,. Antinociceptive and anti-inflammatory activities ofTurcz. extract [J]., 2011, 82(4): 716-721.
[6] 易进海, 钟炽昌, 罗泽渊, 等. 糙苏属和独一味属植物的化学成分及其分类学的意义 [J]. 中草药, 1992, 23(7): 382-384.
[7] But P P H, Kimura T, Sung C K,.[M]. New Jersey: World Scientific Publishing, 1997: 137.
[8] 田光辉, 刘存芳, 赖普辉, 等. 糙苏叶子挥发油成分及其生物活性的研究 [J]. 食品工业科技, 2008, 29(5): 106-109.
[9] 田光辉, 刘存芳, 危冲, 等. 中药糙苏中的多糖研究 [J]. 食品科技, 2009, 34(6): 206-209.
[10] Chu S S, Liu Q Z, Jiang G H,. Chemical composition and insecticidal activity of the essential oil derived fromagainst two grain storage insects [J]., 2013, 16(1): 51-58.
[11] Guo S J, Gao L M, Cheng D L. Iridoids from[J]., 2001, 56(2): 178-180.
[12] 赵静, 杨秀伟, 付宏征, 等. 糙苏化学成分的研究 [J]. 中草药, 1999, 30(2): 3-5.
[13] 刘世旺, 付宏征, 林文翰. 糙苏的化学成分研究 (I) [J]. 中草药, 1999, 30(3): 3-5.
[14] 杨永利, 郭守军, 孙坤, 等. 中药糙苏亲水性化学成分的研究 [J]. 兰州大学学报, 2004, 40(2): 67-71.
[15] Ding M M, Yan F L, Tan J,. Two new dammarane-type glycosides from[J]., 2014, 28(1): 18-23.
[16] Liu P, Yao Z, Li H Q,. Four new nortriterpenoids from[J]., 2007, 90(3): 601-606.
[17] Liu P, Li L Y, Niu R Q,. Two novel nortriterpenes from the roots of[J]., 2008, 19(10): 1228-1230.
[18] Liu P, Deng R X, Yin W P,. A new nortriterpenoid from[J]., 2010, 46(4): 566-568.
[19] Deng R X, Duan W L, Liu P,. Secondary metabolites from the roots of[J]., 2011, 13(3): 230-237.
[20] Liu P, Yao Z, Zhang W,. Novel nortriterpenes from[J].(Tokyo), 2008, 56(7): 951-955.
[21] Liu P, Qiao W, Jia W,. (17)-2α,3α,18β,23,24- Pentahydroxy-19(18→17)-abeo-28-norolean-12-en-21- one from the rhizome of[J]., 2006, 62(3): o919-o921.
[22] 张丽娜, 邓瑞雪, 王玉, 等. 宽苞糙苏根化学成分研究 [J]. 中国药学杂志, 2019, 54(6): 450-456.
[23] Gao J Y, Zhao H Y, Hylands P J,. Secondary metabolite mapping identifiesinhibitors of human lung cancer cells [J]., 2010, 53(3): 723-728.
[24] Kumar R, Bhan S, Kalla A K,. 28-Noroleana-16, 21-diene triterpenes fromspectabilis [J]., 1992, 31(8): 2797-2799.
[25] Çalış İ, Kırmızıbekmez H, Taşdemir D,. Two new triterpene and a new nortriterpene glycosides from[J]., 2004, 87(3): 611-619.
[26] Luo Y G, Feng C, Tian Y J,. Three novel nortriterpenoids fromBenth. (Labiatae) [J]., 2003, 59(41): 8227-8232.
[27] Peng S L, Li R, Bao T N,. A new nortriterpenoid from[J]., 2005, 76(7/8): 625-628.
[28] 郑玉清, 闫合, 韩婧, 等. 中药茺蔚子中一个新C-28降三萜 [J]. 中国中药杂志, 2012, 37(14): 2088-2091.
Study on nortriterpenes from roots ofvar.
DENG Rui-xue, HUANG Yu-yang, XU Yi-fan, LIU Pu
Luoyang Key Laboratory of Natural Products Functional Factor Research and Development, Chemical Engineering & Pharmaceutical College, Henan University of Science and Technology, Luoyang 471023, China
To study the nortriterpenes from the root ofvar.The chemical constituents were isolated by repeated column chromatographies (Toyopearl HW-40C and preparative HPLC). The structures were elucidated on the basis of spectral data analysis.Eight nortriterpenes were isolated from the 95% ethanol aqueous extract ofvarand the structures were identified as phlomisal A (1), phlomisone (2), phlomistetraol A (3), phlomistetraol B (4), phlomishexaol A (5), phlomishexaol B (6), phlomishexaol C (7), and phlomishexaol D (8).Compound 1 is a new compound, and compounds 3, 4, 6—8 are isolated from this plant for the first time. All the nortriterpenes display varying degrees of antitumor activities against cancer cells.
Turcz var.Sun ex C H Hu; nortriterpene; antitumor activities;phlomisal A; phlomistetraol A; phlomishexaol B
R284.1
A
0253 - 2670(2021)06 - 1555 - 07
10.7501/j.issn.0253-2670.2021.06.002
2020-07-08
河南省高校科技创新人才支持计划(20HASTIT008);国家自然科学基金-河南联合基金资助项目(U1404831)
邓瑞雪(1978—),女,博士,副教授,从事天然有机化学研究。
刘 普(1978—),男,博士,教授,研究方向为天然产物化学。E-mail: liuputju@163.com
[责任编辑 王文倩]
