食品微生物检验室间比对结果与分析
2021-03-11金倩仪
◎ 金倩仪
(中山市食品药品检验所,广东 中山 528437)
通过室间比对和盲样考核是一种提升食品微生物实验室检测能力的常见方式,因此,实验室会每年定期参加不同的能力验证以促进实验室检测能力稳步提升。2020 年,中山市食品药品检验所参与了由广东省市场监督管理局组织的“2020 年食品安全抽检监测工作承检机构微生物检验实验室间比对”,现将有关实验报道如下,以其为今后食品微生物检测工作提供参考。
1 材料与方法
1.1 检测样品
由广东省微生物分析检测中心提供的4 个不同冻干样品(菌落总数1 个、大肠菌群1 个以及沙门氏菌2 个),采用西林瓶真空密闭包装,分别编号为A1、E1、S34 和S78。
1.2 试剂与仪器
1.2.1 试剂
磷酸盐缓冲液、平板计数琼脂、结晶紫中性红胆盐琼脂(VRBA)、煌绿乳糖胆盐肉汤(BGLB)、缓冲蛋白胨水、TTB 增菌液、SC 增菌液、BS 琼脂、三糖铁、革兰氏染色液、赖氨酸脱羧酶肉汤及氨基酸脱羧酶对照均购自北京陆桥技术有限公司;沙门氏菌属诊断血清购于泰国S&A 公司;沙门显色培养基购自法国科玛嘉;API 20E 革兰氏阴性细菌鉴定卡和VIDAS沙门氏菌属筛检试剂条均购于梅里埃诊断产品(上海)有限公司。
1.2.2 仪器
电子天平、生化培养箱、电子显微镜、生物安全柜、均质器、VITEK 2 Compact 全自动微生物分析系统、mini-VIDAS 全自动免疫荧光分析仪。
1.3 检验环境
整个实验在二级生物安全实验室进行,遵循无菌操作原则进行。
1.4 检验方法
菌落总数、大肠菌群、沙门氏菌的检验方法如表1。

表1 实验室间比对微生物检验项目和方法列表
1.5 样品制备
按作业指导书上样品处理的操作方法,在生物安全柜内无菌操作开启样品后,将粉末按步骤溶解于100 mL 磷酸盐缓冲液作为样品原液,按相应方法进行检验。
1.6 菌落总数的检验
取25 mL 样品混悬液于225 mL 的磷酸盐缓冲液中,用均质器拍打混匀,作为第一稀释度。再取1 mL(1 ∶10)的样品匀液于9 mL 磷酸盐缓冲液中,振荡混匀作为第二稀释度。按照同样的步骤做到第八稀释度。吸取1 mL 稀释液于无菌平皿内倒入平板计数琼脂,(36±1)℃倒置培养(48±2)h[1]。
1.7 大肠菌群计数的检验
样品稀释同1.6。样品稀释至第七稀释度,吸取1 mL稀释液于无菌平皿内倒入VRBA 琼脂,(36±1)℃倒置培养18 ~24 h。从VRBA 平板上挑取10 个不同类型的典型可疑菌落,少于10 个菌落的挑取全部典型可疑菌落。分别移种于BGLB 肉汤管内,(36±1)℃培养24 ~48 h,观察产气情况。凡BGLB 肉汤管产气,即可报告为大肠菌群阳性[2]。
1.8 沙门氏菌的检验
1.8.1 前增菌
取25 mL 样品混悬液于225 mL 的缓冲蛋白胨水中,振荡混匀,于(36±1)℃培养8 ~18 h[3]。
1.8.2 增菌
各取1 mL 轻摇培养过的混匀液于10 mL 的TTB增菌液、SC 增菌液中培养。TTB 增菌液需在(42±1)℃培养箱内培养18 ~24 h;SC 增菌液需在(36±1)℃培养箱内培养18 ~24 h[3]。
1.8.3 分离培养
用无菌接种环挑取增菌后的TTB 增菌液和SC 增菌液各一环,分别划线接种BS 平板,沙门氏显色培养基平板。两种平板菌在(36±1)℃环境下培养,其中BS 平板需要培养40 ~48 h,而沙门显色培养基平板需要培养18 ~24 h。
2 结果与分析
2.1 菌落总数的结果
菌落总数检验结果如表2,因为菌落总数的计数方法是取30 ~300 CFU 菌落数,只有稀释度为10-3的平板在计数范围内,所以结果为5×104CFU·mL-1。

表2 菌落总数实验结果表
2.2 大肠菌群计数的结果
大肠菌群计数结果如表3,因为大肠菌群计数方法是取15 ~150 CFU 菌落数,只有稀释度为10-2的平板在计数范围内,所以通过计算得到了7 550 CFU·mL-1的检测值,经过第3 位数字“四舍五入”的修约后得到了7.6×103CFU·mL-1的结果。

表3 大肠菌群计数实验结果表
2.3 沙门氏菌的结果
2.3.1 样品S34 的结果
经过mini-VIDAS 进行初筛得到了阳性的结果,结合划线后的亚硫酸铋琼脂平板上生长黑色有金属光泽菌落,菌落周围培养基呈棕色;沙门显色培养基上生长淡紫色圆形菌落,以上现象均是沙门氏菌的可疑现象,需要进一步做生化试验。三糖铁琼脂的结果为斜面产碱变红,底层产酸变黄,产气,产硫化氢;赖氨酸脱羧酶试验结果为阳性,两个试验结果可初步判断为可疑沙门菌属。笔者运用了API 和VITEK2-Compact 两种方法进行了确证,反馈的结果都是Salmonellagroup 99%,结果可见图1、图2。同时还做了血清试验,O 多价和H 多价血清均凝集。因此样品S34 的结果报告是检出了沙门氏菌。

图1 样品S34 API20E 的结果图
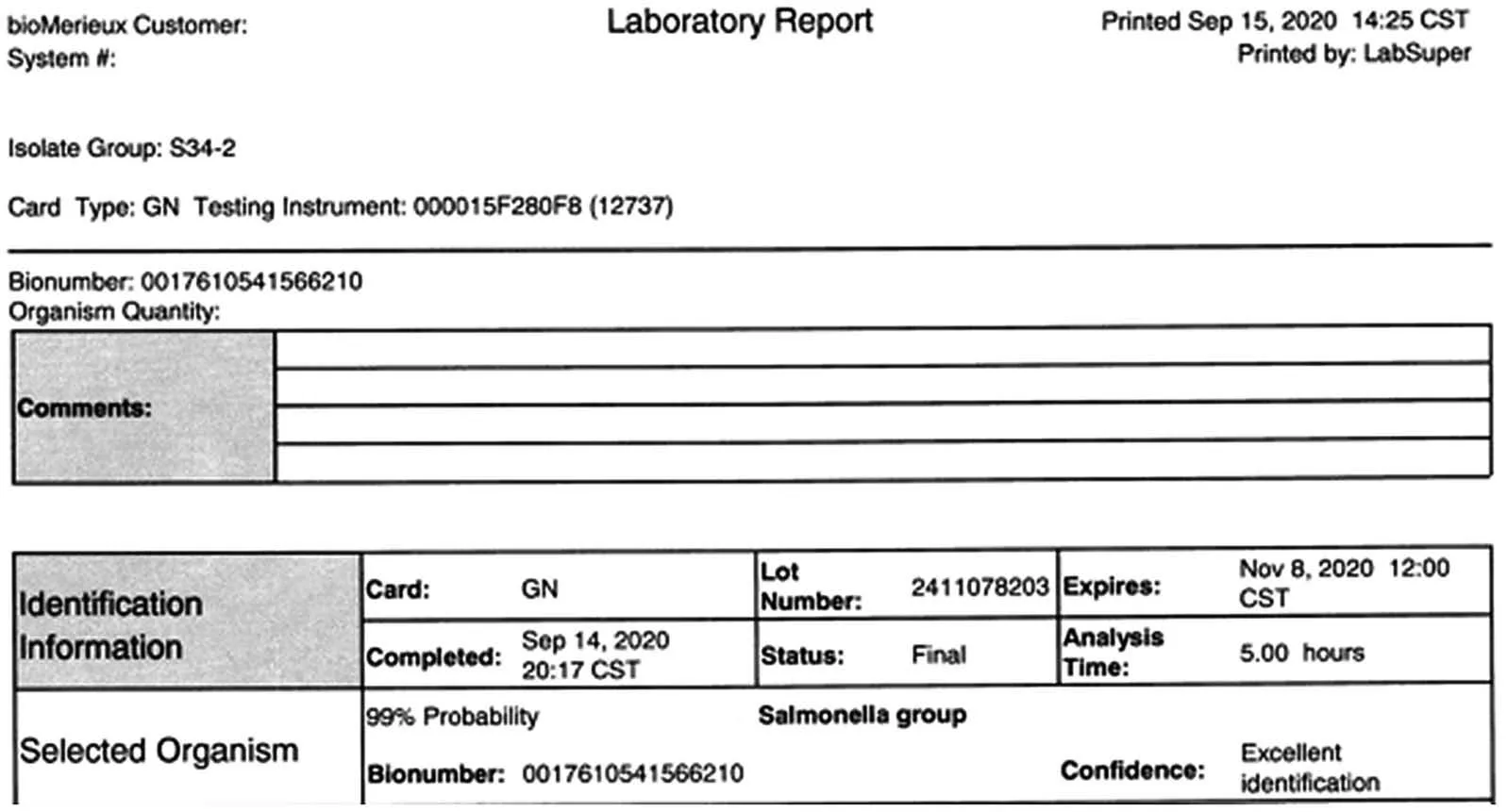
图2 样品S34 VITEK2 的结果图
2.3.2 样品S78
经过mini-VIDAS 进行初筛得到了阴性的结果,见表4,结合划线后的亚硫酸铋琼脂平板上未见菌落生长;沙门显色培养基上生长蓝色圆形菌落,以上现象可判断为未检出沙门氏菌。因此样品S78 的结果报告是未检出沙门氏菌。

表4 Mini VIDAS 结果表
2.4 结果反馈
2020 年食品安全抽检监测工作承检机构微生物检验实验室间比对结果如表5。

表5 2020 年食品安全抽检监测工作承检机构微生物检验实验室间比对情况表
3 结论
参加本次室间比对的实验室共有44 家,其中有4家的结果为不满意,有2 家的结果为基本满意,其余的38 家实验室反馈结果均为满意。出现不满意结果的实验室,有3 家都是在考核沙门氏菌出现假阴性或假阳性的结果;剩下1 家是在大肠菌群计数时结果超出考核范围。沙门氏菌检验出现的问题可以能是因为消毒工作没做好、操作人员判断典型菌落时出现了偏差而没有进行下一步鉴定或是挑取错误、样品前处理时没做好导致实验失败等。因此,在对待可疑样品时应采取多种方法来鉴定,以免造成错检或漏检[4]。
在进行沙门氏菌检验时,应在增菌后通过mini-VIDAS 进行初筛,如果出现阳性的结果应更加谨慎的对待该样品。mini-VIDAS 检测方法既快速准确又可以避免人工检测造成的误差,与传统方法互补[5],不过检验费用较为昂贵。在后续的鉴定中笔者实验室会使用传统方法同时再结合API 法和VITEK2-Compact 两种方法来确证,API 法能够提高检测效率还能弥补传统方法的不足[6];全自动微生物生化鉴定系统在实操中会更加便利,生化结果准确而且快速。虽然相对人工进行的传统生化试验这两种方法成本都更高,但是检测时间更短,而且结果影响因素更少,得到的结果更加准确可靠。通常会用这两种方法来互相确证试验结果,如果结果存在较大偏差时,应及时重做试验发现问题。
