高孕激素状态促排卵与拮抗剂方案在卵巢储备功能减退的年轻人群中体外受精-胚胎移植结局比较
2021-03-10杨松青周黎明王丽萍姚秋萍
杨松青 周黎明 王丽萍 姚秋萍 金 敏▲
1.浙江大学医学院附属第二医院生殖中心,浙江杭州 310009;2.浙江省宁波市妇女儿童医院生殖中心,浙江宁波 315000;3.浙江省嘉兴市妇幼保健院生殖中心,浙江嘉兴 314051
卵巢储备功能减退(diminished ovarian reserve,DOR)指由于年龄、遗传因素、医源性或手术原因导致的卵巢内存留卵子的质量和数量下降,其约占不孕症的10%,且呈上升趋势[1-2]。目前,年轻生育人群中卵巢储备功能减退现状凸显,已成为导致女性生育力下降甚至不孕的重要因素。卵巢储备功能减退不仅影响患者本身的健康,还会影响家庭的和谐稳定,使得患者的心态和精神遭受折磨。本研究回顾性分析了 2013 年 3 月至 2019 年 12 月在浙江大学医学院附属第二医院、嘉兴市妇幼保健院和宁波市妇女儿童医院生殖中心运用高孕激素状态促排卵(progestin primed ovanrian stimalation regimen,PPOS)方案或拮抗剂方案(gonadotropinreleasing hormone antagonist regimen,GnRH-ant)的284例年轻 DOR 患者体外受精-胚胎移植(In Vitro Fertilization-Embryo transfer,IVF-ET)的疗效,旨在为该人群选择更佳的促排卵方案。
1 资料与方法
1.1 一般资料
回顾性分析2013年3月至2017年12月在浙江大学医学院附属第二医院、嘉兴市妇幼保健院和宁波市妇女儿童医院生殖中心进行IVF-ET的284例年轻DOR患者的临床资料。纳入标准:①24岁≤年龄≤35岁;②0.1 ng/ml<抗苗勒管激素(AMH)≤1.1 ng/ml且窦卵泡数(AFC)≤7个;③PPOS或GnRH-ant方案促排。排除标准:①染色体异常者;②严重的全身性疾病不宜妊娠;③因自身原因取消周期者;④既往周期取消>2次。研究方案相关医院医学经伦理委员会审批通过,患者及家属知情并同意。
按AMH水平及促排卵方案分组,其中A组:0.1 ng/ml<AMH≤0.5 ng/ml,PPOS方案,30个周期;B组:0.1 ng/ml<AMH≤0.5 ng/ml,GnRH-ant方案,66个周期;C组:0.5 ng/ml<AMH≤1.1 ng/ml,PPOS方案,38个周期;D组:0.5 ng/ml<AMH≤1.1 ng/ml,GnRH-ant方案,150 个周期。
1.2 促排卵方案及扳机时机
①GnRH-ant方案[3]:卵泡早期开始注射外源性促性腺激素(Gn),中晚期添加拮抗剂至扳机日。②PPOS方案[4]:卵泡早期添加外源性孕激素与Gn。促排过程中根据患者卵泡生长情况和激素变化给予个体化调整。
当优势卵泡直径≥18 mm和(或)成熟卵泡≥3枚,血雌二醇(E2)水平与成熟卵泡数相符,给予HCG扳机,36 ~ 37 h后经阴道B超引导下取卵。
1.3 胚胎观察及评分
体外胚胎受精并根据伊斯坦布尔共识和Gardner标准胚胎评分[5-6]。1期为囊胚腔占囊胚总体积的1/2以下;2期为囊胚腔占囊胚总体积的1/2以上;3期为完全扩张囊胚,囊胚腔占满整个囊胚;4期为扩张后囊胚,囊胚腔体积较早期囊胚明显扩大,透明带变薄;5期为正在孵出的胚胎,囊胚正在从透明带破裂口孵出;6期为孵化出的胚胎,囊胚完全从透明带逸出。内团细胞中A级为细胞数目多,排列紧密,B级为细胞数目少且排列松,C级为细胞数目少;滋养层:A级为上皮细胞含有较多细胞组成且结构紧密,B级为上皮细胞层的细胞不多且结构松散,C级为上皮细胞为稀疏的细胞组成。
可利用卵裂期胚胎:D2、2-5细胞、≥Ⅱ级或D3、≥4细胞、≥Ⅱ级;优质卵裂期胚胎:D2、4细胞、I级、碎片≤ 5% 或 D3、7-9细胞、I级、碎片≤10%。其中D2胚胎的评分仅限于培养到D2就进行移植、冷冻的胚胎。可利用卵裂期胚胎可进行移植、冷冻或在患者要求下进一步培养囊胚。囊胚形成:≥2期;可利用囊胚:≥3期,内细胞团或滋养层不同时为C级。可利用胚胎包括移植和冷冻胚胎,周期取消为无可利用胚胎。相关计算公式参照《辅助生殖技术临床关键指标质控专家共识》[7]。
1.4 胚胎冷冻及移植
全胚冷冻标准:①PPOS方案促排;②移植日宫腔有积液;内膜厚度<7 mm或>16 mm;发热、阴道炎、急性盆腔炎等急性炎症期;合并其他不宜移植的内外科疾病;③患者要求。GnRH-ant方案也可采用鲜胚移植。冻胚解冻移植至少在取卵术后第2个月经周期启动。
1.5 黄体支持及妊娠结果随访
冻胚移植采用激素替代方案至达到子宫内膜转化标准后给予黄体支持,并在对应时期移植胚胎。2周后测血清人绒毛膜促性腺激素(HCG),如阴性则停用黄体支持。血HCG阳性者4 ~ 6周后行阴道超声,观察到孕囊则为临床妊娠;血HCG一过性阳性,超声未见孕囊则为生化妊娠。临床妊娠者继续黄体支持7 ~ 8周,妊娠28周前妊娠丢失记为流产。
1.6 统计学方法
采用SPSS 26.0统计学软件对数据进行统计分析,用中位数-四分位距[四分位距为(P75- P25)/2]描述非正态分布数据,组间比较用Mann-Whitney U检验;计数资料用[n(%)]描述,组间比较用χ2检验。相关性分析后行多元线性回归及广义估计方程分析。P<0.05为差异有统计学意义。
2 结果
2.1 一般资料比较
与B组比较,A组AFC较少(P<0.05),其他指标差异均无统计学意义(P>0.05);C组与D组各指标比较差异均无统计学意义(P>0.05)。见表1。

表1 年轻的卵巢储备功能减退患者不同组间一般临床特征比较
2.2 促排卵情况比较
收集四组患者的促排卵相关指标:Gn用量、HCG日性激素水平(LH、E2)及获卵数、成熟卵子数(MⅡ卵子数)、可利用卵裂期胚胎数、优质卵裂期胚胎数、囊胚形成数、可利用胚胎数(包括卵裂期胚胎及囊胚期胚胎)、MⅡ率、可利用卵裂期胚胎率、优质卵裂期胚胎率、囊胚形成率、可利用胚胎率、周期取消率。与B组比较,A组患者的Gn用量、获卵数及MⅡ卵数较少,HCG日LH水平较高(P<0.05),余指标差异均无统计学意义(P>0.05)。与D组比较,C组患者的Gn较少,HCG日LH水平较高(P<0.05),其余指标差异均无统计学意义。见表2。

表2 年轻的卵巢储备功能减退患者不同组间促排卵情况比较
2.3 胚胎移植情况及结局
本研究比较了未行鲜胚移植的已完结促排周期(无剩余冻胚数且至少随访至孕中期)的妊娠结局,共130个周期,其中有58个取消周期,3个取消移植周期(共7个胚胎),余69个周期中共移植75次(共197个冻胚)。
比较A组与B组及C组与D组:妊娠结局(生化妊娠率、临床妊娠率、着床率、流产率)差异无统计学意义(P<0.05)。见表3。
2.4 回归分析
相关性分析后行多元线性回归分析:获卵数与不同促排方案无明显相关性,见表4 ~ 5。未行鲜胚移植的已完结周期的临床妊娠广义估计方程表明其与不同促排方案无明显相关性,见表6。

表3 年轻的卵巢储备功能减退患者未行鲜胚移植的已完结促排周期的妊娠结局比较

表4 获卵数与其他因素相关性分析

表5 获卵数多元线性回归
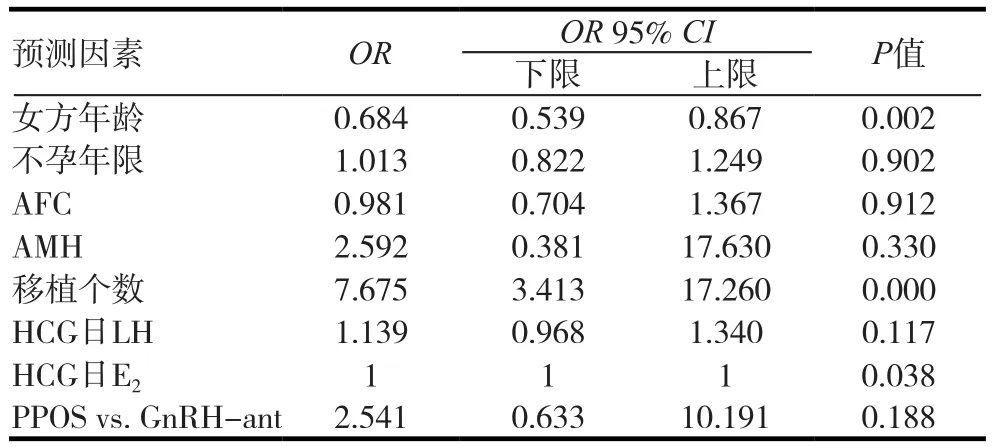
表6 未行鲜胚移植的已完结周期的临床妊娠广义估计方程分析
3 讨论
近年来,AMH对卵巢储备功能评估的价值受到广泛肯定,对IVF结局预测有一定的意义。AMH是卵巢窦前卵泡和小窦卵泡颗粒细胞分泌的一种糖蛋白,具有稳定性,其检测不受月经周期影响[8],且与AFC、年龄密切相关[9-10],能优于其他指标更早地反映卵巢储备功能随年龄增长呈现的下降趋势[11],是目前最灵敏的评估手段。Seifer等[10]研究表明在24岁≤年龄≤35岁时,血清AMH中位值平均每年下降0.2 ng/ml,35岁后下降至0.1 ng/(ml·年)。临床上常定义AMH<1.1 ng/ml为卵巢储备减退,同时有研究表明[12-13]0.5 ng/ml可进一步作为 AMH 预测辅助生殖妊娠结局的节点。AFC是指在月经早期应用超声测量并计数直径为2 ~ 8 mm的可见卵泡数,也是评估卵巢功能的良好指标[9]。目前,AMH结合AFC是临床上应用最广泛、最有效的卵巢评估手段。
DOR患者促排卵通常伴有获卵数少,卵子质量不佳,可利用胚胎少甚至无可利用胚胎,导致周期取消率高和周期妊娠率低等情况。对于年轻的DOR患者,临床医师面临的挑战是采用何种促排卵方案以获得良好的效益。本研究回顾性分析三家生殖中心的年轻DOR患者使用PPOS方案与GnRH-ant方案的促排卵疗效,尝试在有限样本量下比较方案的可行性,具有一定的临床意义。
目前,临床医生有倾向性地在卵巢功能特别差的患者中尝试PPOS方案,这可能是A组AFC少于B组的原因,使得A组获卵数及MⅡ卵数较少(P<0.05),但比较两组的胚胎数量与质量,差异无统计学意义。获卵数多元线性回归分析及已完结促排周期临床妊娠广义估计方程分析均表明,其各自与不同促排方案无明显相关性,再次验证了本研究结论的可靠性。其中,AMH值与获卵数正相关,与临床妊娠无明显相关,提示在年轻的DOR患者中,AMH的下降会减少获卵数,但一旦获得卵子,患者有可能获得良好临床妊娠结局,这与以往文献相一致[14-15]。提醒临床医师不能因AMH低值而放弃对年轻DOR患者启动促排卵周期,反而由于年龄与临床妊娠的负相关,应该采取更积极的措施,把握年龄优势。
本研究中PPOS方案均采用FET,拮抗剂方案则采用鲜胚和(或)冻胚移植。但由于DOR患者单一取卵周期可利用胚胎数较少,各中心往往利用胚胎冷冻技术累积胚胎,其中B组冻胚周期率为71.7%(33/46)、D 组为 66.4%(87/131),与 PPOS方案(A组、C组)中100.0%的冻胚周期率相比,同样产生了大部分胚胎冷冻费用。GnRH-ant方案中使用的拮抗剂价格昂贵、需皮下注射,而PPOS方案使用的外源性孕激素,价格实惠,只需口服或阴道填塞,用药方便,减轻患者痛苦,且Gn用量较拮抗剂方案明显减少,进一步降低患者费用。本研究推测PPOS方案可能具有更好的费效比,更具有优势。
本研究为多中心回顾性研究,更能够全面反映总体的情况。但具有局限性:①本研究纳入的三个中心回顾性研究,方案用药有少许不同;②截至2020年6月11日,本研究中有近31.1%胚胎尚未移植,临床妊娠GEE分析纳入周期数少于实际促排周期,降低效能。
