基于全方特征图谱质量表征的芩连制剂质量评价研究
2021-03-09熊少哲易剑平范国强顾海鸥王志斌
彭 平,熊少哲,张 蓓,易剑平,杜 菁,杨 璇,范国强,顾海鸥,王志斌*
1.北京同仁堂科技发展股份有限公司制药厂,北京 100079
2.中国北京同仁堂(集团)有限责任公司,北京 100079
芩连制剂所涉及的中成药有芩连片、芩连胶囊、芩连丸,其处方由黄芩、连翘、黄连、川黄柏、赤芍、甘草6 味药味组成,具有清热解毒、消肿止痛的功效,其中芩连片收载于《中国药典》2020年版,3 个剂型的芩连药物处方制法均为黄芩、连翘、川黄柏、甘草合并提取,黄连、赤芍粉碎,混合后经不同制剂工艺而得。
现有中成药质量标准中,对其原料的质量控制包括黄连、赤芍药味的显微鉴别项,黄连、黄芩、赤芍药味的薄层鉴别项,黄芩药味的含量测定项。其中对黄连、川黄柏药物的薄层鉴别项以盐酸小檗碱为对照,缺失专属性同时缺少对主要指标成分的定量测定[1];对连翘、甘草药味缺少相应的质量控制方法。有文献报道采用RP-HPLC 等色谱方法建立了芩连片中黄芩苷、盐酸小檗碱、芍药苷、甘草苷、连翘苷等指标性成分的含量测定方法,进一步完善了芩连片复方药物的质量控制[2-6],但研究发现不同芩连制剂中指标性成分含量差异较大,普通液相色谱法受限于最低检测限和测定回收率范围,难以实现对芩连制剂整体质量表征的广泛测定;且现有研究方法对组方药物质量的控制还有遗漏,不能有效控制川黄柏、赤芍药味的特征性质量。
经过对芩连制剂处方药味原料质量研究的相关文献分析发现,赤芍、川赤芍及其易混品白芍药材质量差异成分包括芍药苷、芍药内酯苷、1,2,3,4,6-五-O-倍酰-D-葡萄糖(PGG)[7-10],黄连和川黄柏及关黄柏质量差异成分是盐酸黄柏碱、盐酸巴马汀[11-13],综合连翘、黄芩、甘草药材的《中国药典》指标性成分连翘苷、连翘酯苷A、甘草苷、甘草酸、黄芩苷、汉黄芩苷以及盐酸小檗碱,共计12 个指标性成分含量是芩连片质量评价的主要指标[14-19]。因此,本实验将采用分离效能和灵敏度均较高的UPLC-PDA 色谱法[20],以芩连片为研究载体,建立其特征图谱质量表征方法,同时测定芩连片中12个指标成分的含量,并应用于该类中成药的质量评价之中,为其质量表征与控制提供方法支持。
1 仪器与材料
1.1 仪器
Waters Acquity HClass 超高效液相色谱仪,包括四元溶剂管理器,PAD 检测器,在线温度控制器,样品管理器,Empower 工作站,美国Waters 公司;KQ-250 DE 型数控超声波清洗机,昆山超声仪器有限公司;Mettler ML 204 型电子分析天平、Mettler XP 205 型电子分析天平,瑞士梅特勒-托利集团;0.22 μm 微孔滤膜,天津津腾实验设备有限公司。
1.2 材料
试药:乙腈,默克公司,色谱纯;甲酸,分析纯,天津光复精细化工研究所;乙酸铵,分析纯,南开大学精细化学实验厂;超纯水,Milli-Q 超纯水仪制备。
对照品:盐酸小檗碱(质量分数86.7%,批号110713-201814)、盐酸巴马汀(质量分数86.8%,批号110732-201611)、盐酸黄柏碱(质量分数95.8%,批号111895-201303)、黄芩苷(质量分数93.3%,批号110715-201318)、汉黄芩苷(质量分数98.5%,批号112002-201702)、甘草酸按(质量分数93.0%,批号110731-201619)、甘草苷(质量分数93.7%,批号111610-201106)、芍药苷(质量分数95.1%,批号110736-201943)、连翘酯苷A(质量分数94.1%,批号 111810-201405)、盐酸黄连碱(质量分数95.1%,批号112026-201601)均购自中国食品药品检定研究院;芍药内酯苷(质量分数≥98%,批号YZ3O10H101115)、连翘苷(质量分数98%,批号Z17A8X34077)、表小檗碱(质量分数98%,批号W06M8Z30708)、连翘酯素(质量分数97%,批号YZ3O10H101115)、PGG(质量分数98%,批号P28M9F54631)购自上海源叶生物科技有限公司。
研究用饮片:黄连Coptis chinensisFranch、黄柏Phellodendron chinenseSchneid(川黄柏)、连翘Forsythia suspensa(Thunb.) Vahl(青翘)、黄芩Scutellaria baicalensisGeorgi、甘草Glycyrrhiza uralensisFisch.、赤芍Paeonia lactifloraPall.均由北京同仁堂科技发展股份有限公司提供,由北京同仁堂科技发展股份有限公司工程师刘博譞鉴定,均符合《中国药典》2020年版要求。
芩连制剂中成药样品:芩连片,北京同仁堂科技发展股份有限公司制药厂(S1、S2)、牡丹江灵泰药业股份有限公司(S3)、哈尔滨三木制药厂(S4、S5)、山东孔府制药有限公司(S6);芩连胶囊,成都迪康药业股份有限公司(S7、S8)、吉林敖东集团力源制药股份有限公司(S9、S10);芩连丸,四川旭华制药有限公司(S11)均为市场购买,生产厂家分别编号M1~M7。
2 方法与结果
2.1 样品处理方法
2.1.1 对照品溶液的制备 分别用70%甲醇配制供定量用的对照品溶液,取连翘酯苷A、盐酸黄柏碱、芍药苷、芍药内酯苷、甘草苷、黄芩苷、PGG、连翘苷、盐酸小檗碱、巴马汀、甘草酸、汉黄芩苷对照品适量,精密称定,加70%甲醇制成含连翘酯苷A 20 µg/mL、盐酸黄柏碱15 µg/mL、芍药内酯苷20µg/mL、芍药苷350 µg/mL、甘草苷20 µg/mL、黄芩苷450 µg/mL、PGG 25 µg/mL、连翘苷20 µg/mL、盐酸小檗碱250 µg/mL、巴马汀30 µg/mL、甘草酸50 µg/mL、汉黄芩苷100 µg/mL 的混合对照品溶液,即得。
2.1.2 供试品溶液的制备 取装量差异项下芩连制剂成品约10 g,磨成细粉,取约0.5 g,精密称定,置于具塞三角瓶中,精密加入70%甲醇25 mL,称定质量,加热回流处理90 min,放冷,用提取溶剂补足减失的质量,用0.22 μm 微孔滤膜滤过,取续滤液,即得供试品溶液。
2.2 芩连制剂特征图谱质量表征方法
2.2.1 色谱条件 色谱柱为Waters Cortecs T3 柱(100 mm×2.1 mm,1.6 µm);柱温30 ℃;流动相乙腈(含0.02%甲酸,A)-(10 moL/L 乙酸铵-0.09%甲酸缓冲液,B),梯度洗脱:0~10 min,10%~12%A;10~11 min,12%~15% A;11~18 min,15%~16% A;18~32 min,16% A;32~35 min,16%~19% A;35~40 min,19%~21% A;40~45 min,21%~50% A;45~48 min,50%~90% A;48~52 min,90%A;52~55 min,90%~10% A;55~60 min,10% A;体积流量0.3 mL/min;检测波长230 nm(连翘酯苷A 含量测定检测波长330 nm);进样体积1 μL。
2.2.2 系统适用性 取对照品溶液和供试品溶液适量,在“2.2.1”项色谱条件下进样测定,结果见图1、2,结果表明,理论塔板数按黄芩苷峰计均大于30 000,12 个主要指标性成分色谱峰的分离度均大于1.5,表明系统适用性符合相关测定要求。
2.2.3 特征峰指认 分别取芩连制剂处方6 味药物,采用已建立的样品处理方法,在“2.2.1”项色谱条件下进样测定,标记了38 个含量较高且色谱分离效果稳定的特征色谱峰,采用对照品标记了其中15 个主要色谱峰化学结构。其中包括黄连特征峰3个,黄柏特征峰1 个,黄连、黄柏同源特征峰6 个,赤芍特征峰7 个,连翘特征峰8 个,黄芩特征峰11个,甘草特征峰2 个。结果见表1。
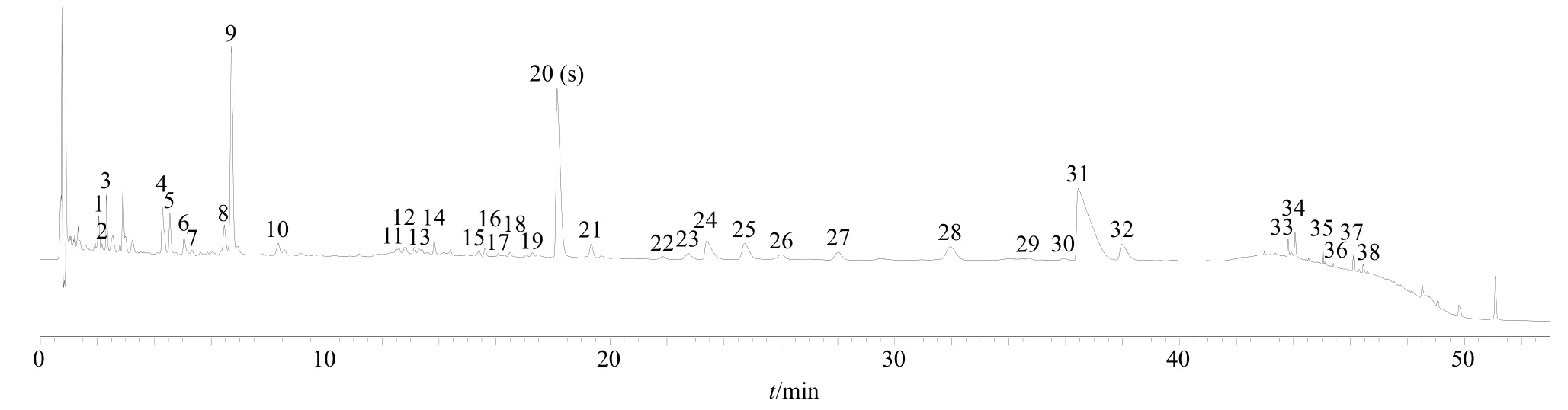
图1 芩连制剂样品 (S1) 的全方特征指纹图谱Fig.1 Whole prescription characteristic spectrum of Qinlian preparation sample (S1)
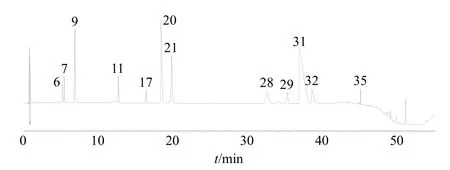
图2 12 个指标成分混合对照品溶液色谱图Fig.2 Chromatograms of solutions of 12 index ingredients mixed control solution
2.2.4 指标性成分含量测定专属性考察 按照芩连制剂处方配比,分别配制芩连制剂缺黄芩、缺黄连和黄柏、缺黄柏、缺黄连、缺连翘、缺赤芍、缺甘草阴性样品,按照芩连制剂供试品处理方法处理各芩连制剂阴性样品溶液,在“2.2.1”项色谱条件下进样测定,见图3、4。在本色谱条件下,检测波长为230 nm 下赤芍中指标性成分芍药苷、芍药内酯苷、PGG 色谱峰处无明显干扰,黄连中指标性成分盐酸巴马汀色谱峰处无明显干扰,黄柏中指标性成分盐酸黄柏碱色谱峰处无明显干扰,黄柏和黄连中指标性成分盐酸小檗碱色谱峰处无明显干扰,连翘中指标性成分连翘苷色谱峰处无明显干扰,甘草中指标性成分甘草苷、甘草酸色谱峰处无明显干扰,黄芩中指标性成分黄芩苷、汉黄芩苷色谱峰处无明显干扰;检测波长330 nm 下连翘中指标性成分连翘酯苷A 色谱峰无明显干扰。
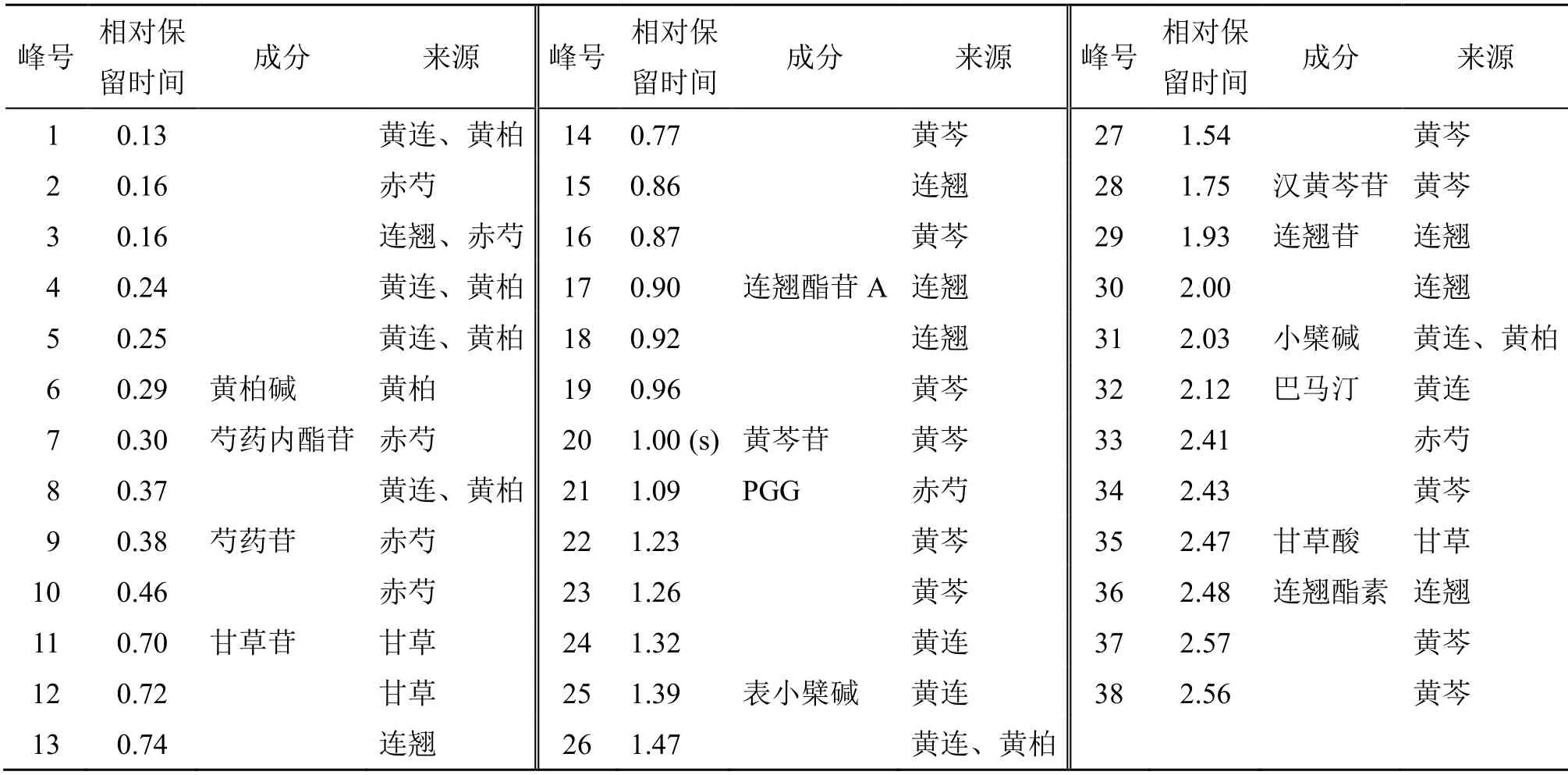
表1 芩连制剂特征图谱中38 个特征峰信息Table 1 Information of 38 characteristic peaks in characteristic map of Qinlian preparation
2.2.5 精密度考察 取同一芩连制剂供试品溶液,在“2.2.1”项色谱条件下进样测定,连续进样6 针测定,记录芩连制剂特征图谱中38 个特征峰峰面积和保留时间,得芩连制剂供试品溶液特征图谱中38个特征峰峰时间和峰面积的精密度结果,各色谱峰相对保留时间和峰面积RSD 值均小于3%,表明仪器精密度符合要求。
2.2.6 稳定性考察 取同一芩连制剂供试品溶液,在“2.2.1”项色谱条件下进样测定,分别于超声处理后0、3、6、9、12、24 h 进样,记录芩连制剂特征图谱中38 个特征图谱峰面积,得芩连制剂供试品溶液特征图谱中38 个特征峰峰面积和相对保留时间的稳定性结果,各色谱峰峰面积RSD 值均小于5%,表明方法稳定性符合要求。
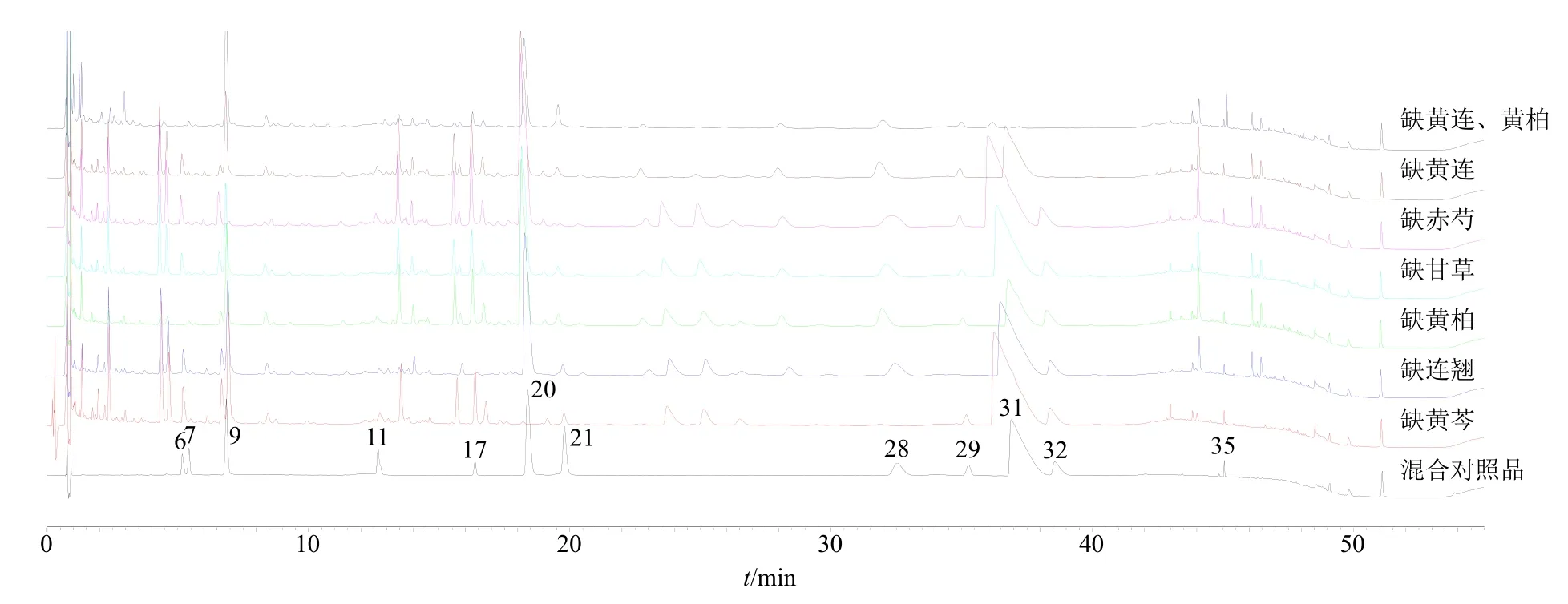
图3 检测波长230 nm 下芩连制剂阴性样品与混合对照品液相色谱图对比图Fig.3 Chromatograms of negative samples of Qinlian preparation under detection wavelength of 230 nm compared with those of mixed controls
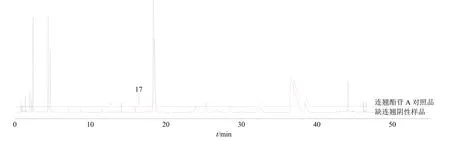
图4 检测波长330 nm 下芩连制剂阴性样品与连翘酯苷A 对照品液相色谱图对比图Fig.4 Chromatograms comparison of negative sample of Qinlian preparation with forsythoside A standard under detection wavelength of 330 nm
2.2.7 线性关系考察 分别配制质量浓度为连翘酯苷A 897.0 µg/mL、盐酸黄柏碱804.7 µg/mL、芍药内酯苷576.6 µg/mL、芍药苷739.9 µg/mL、甘草苷816.7 µg/mL、PGG 1 059.3 µg/mL、连翘苷982.4µg/mL、盐酸小檗碱982.5 µg/mL、巴马汀733.6µg/mL、甘草酸77.9 µg/mL、汉黄芩苷439.2 µg/mL的对照品溶液储备液,分别取各对照品储备液采用70%甲醇溶液稀释2、2.5、5、10、20、50、100、200 倍进样,配制质量浓度为287.1 µg/mL 黄芩苷对照品溶液分别进样0.2、0.6、0.8、1.0、1.4、1.8、2.2 μL,以进样量为横坐标(X),对照品峰面积为纵坐标(Y),绘制标准曲线。建立色谱峰峰面积对进样量的回归方程(表2),结果表明,各指标成分在检测的质量浓度范围内线性关系良好。
2.2.8 重复性考察 分别取芩连片、芩连胶囊、芩连丸样品各6 份,分别按样品处理方法制备样品溶液,在“2.2.1”项色谱条件下进样测定,记录芩连制剂特征图谱中38 个指标性成分色谱峰面积,得芩连制剂供试品溶液特征图谱中38 个特征峰峰面积和相对保留时间的重复性结果,各特征峰面积和相对保留时间RSD 值均小于5%,采用外标法计算样品中12 个指标性成分含量,结果见表3。
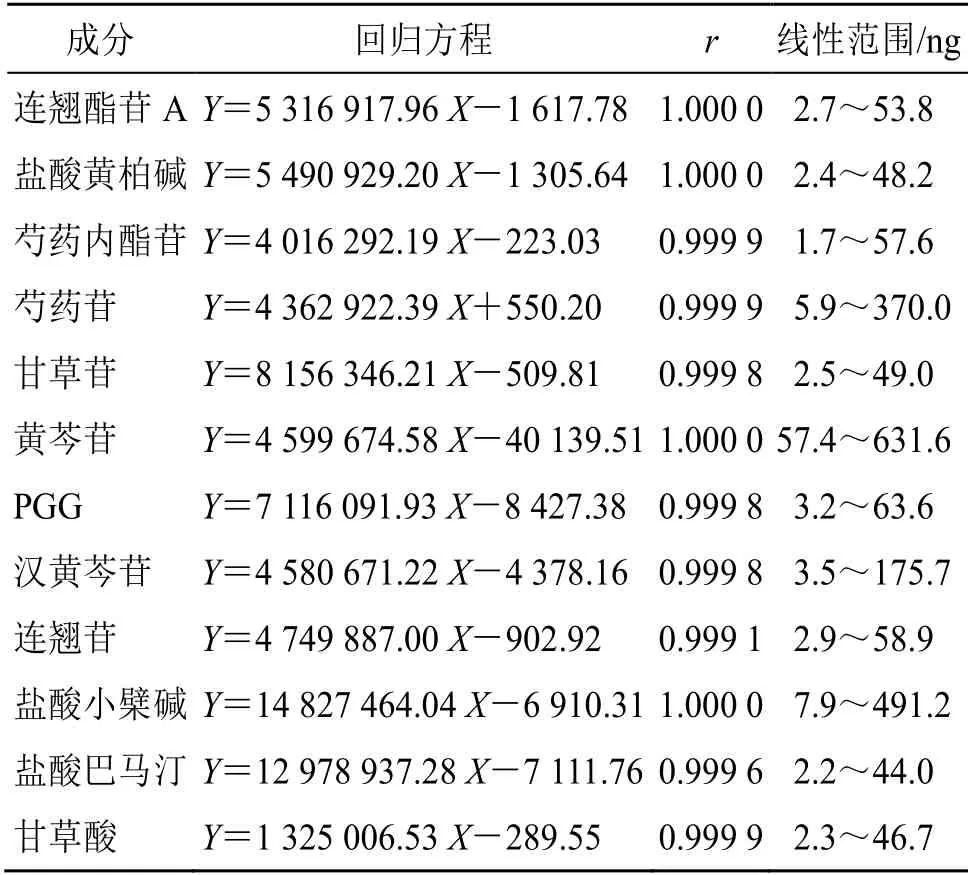
表2 12 个指标性成分线性回归方程Table 2 Linear regression equation of 12 exponential components
2.2.9 加样回收率考察 取已知指标性成分含量的3 种芩连制剂粉末各6 份,每份250.0 mg,参考“2.2.8”项下重复性含量测定结果,按照中间质量浓度加样回收率测定方法,分别加入25 mL 含有相应对照品质量浓度的70%甲醇,称定质量,加热回流处理90 min,放冷,用70%甲醇溶液补足减失的质量,用0.22 μm 微孔滤膜滤过,取续滤液,在“2.2.1”项色谱条件下进样测定。根据“2.2.8”项下重复性考察测得的各成分的量,计算各成分的加样回收率和RSD,结果见表4,12 个指标性成分回收率在83.58%~106.76%。
2.3 多批次芩连制剂质量测定结果
2.3.1 芩连制剂特征图谱质量表征结果 取11 批不同厂家生产芩连制剂样品,按照已建立的样品处理方法,在“2.2.1”项色谱条件下进样测定。各研究用样品均可检出38 个特征色谱法,各样品特征图谱结果见图5。记录峰面积值,以黄芩苷色谱峰(峰20)为参比峰(s),计算38 个色谱峰相对峰面积比值,见表5。
2.3.2 芩连制剂中12 个指标成分的含量测定结果采用已建立的分析方法,测定11 份芩连制剂中12个指标性成分质量分数,结果见表6。
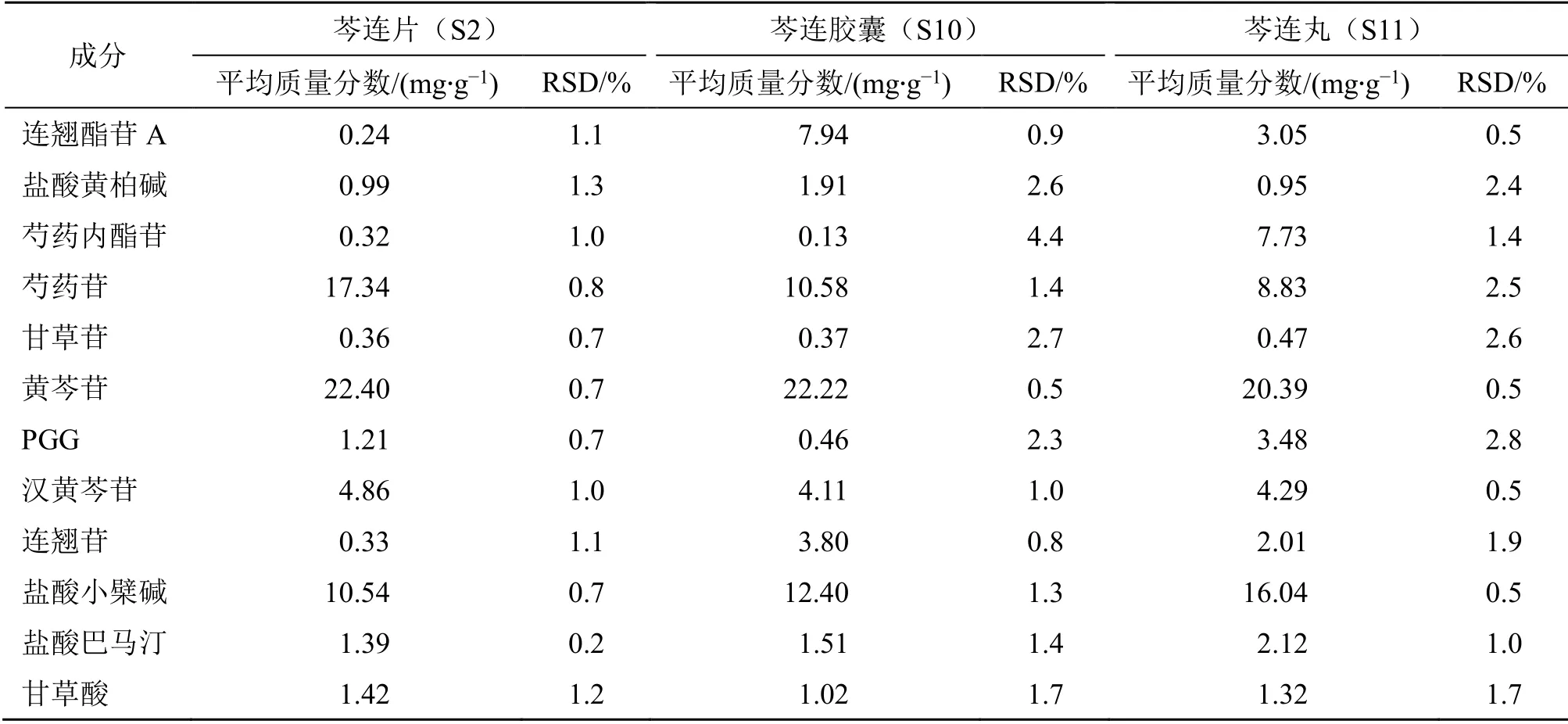
表3 芩连制剂指标性成分含量测定重复性结果Table 3 Repeatability results of determination of index components in Qinlian preparation
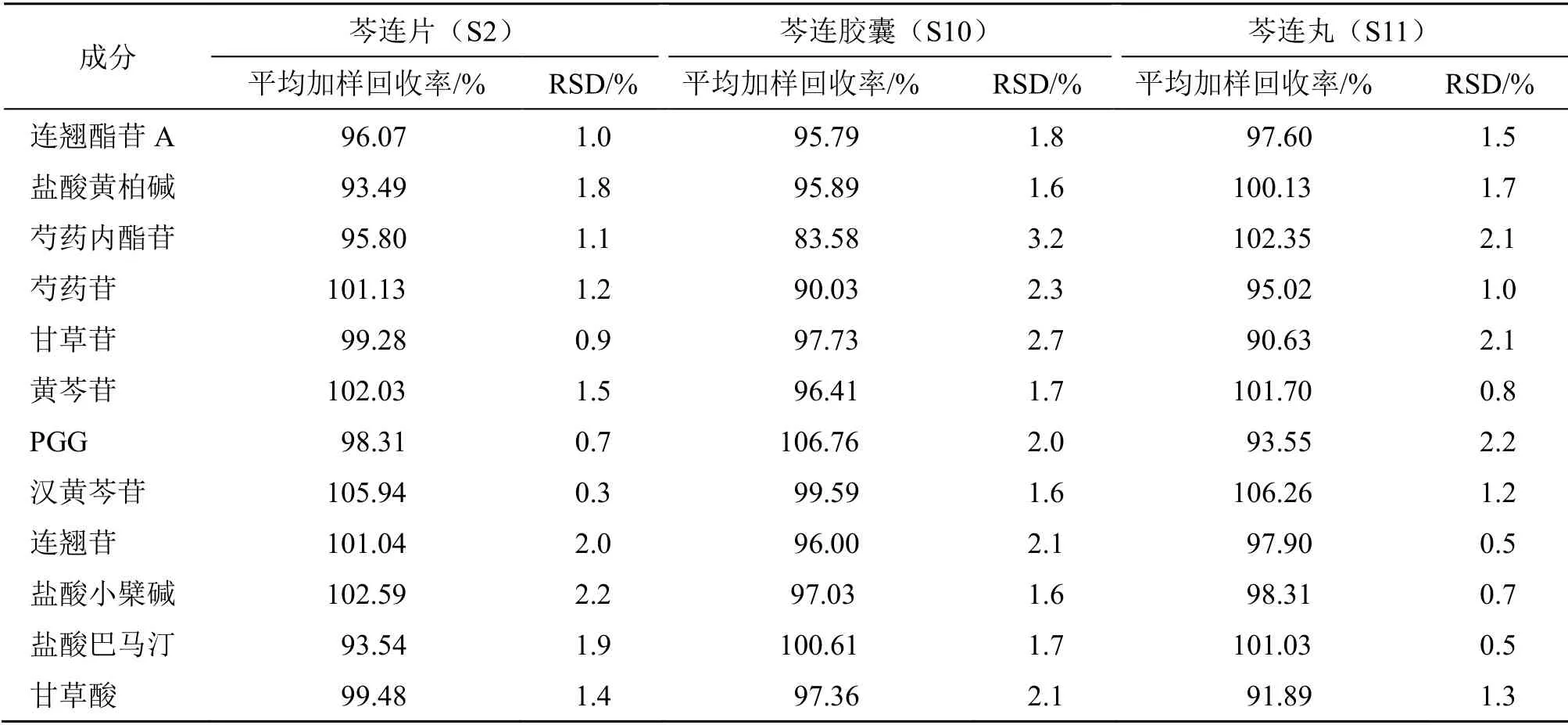
表4 芩连制剂指标性成分含量测定回收率考察结果Table 4 Test results of recoveries for determination of index compounds of Qinlian preparation
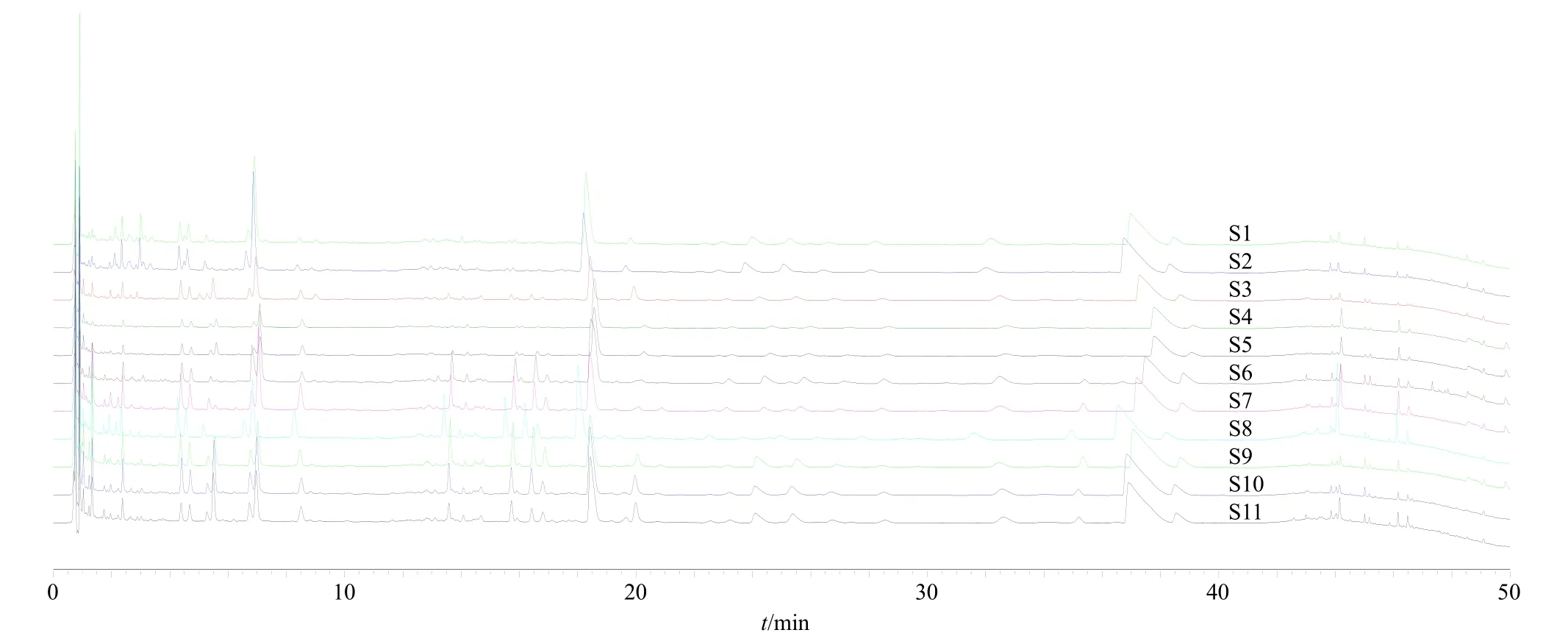
图5 11 批芩连制剂样品特征图谱Fig.5 Sample characteristics profiles of 11 batches of Qinlian preparation
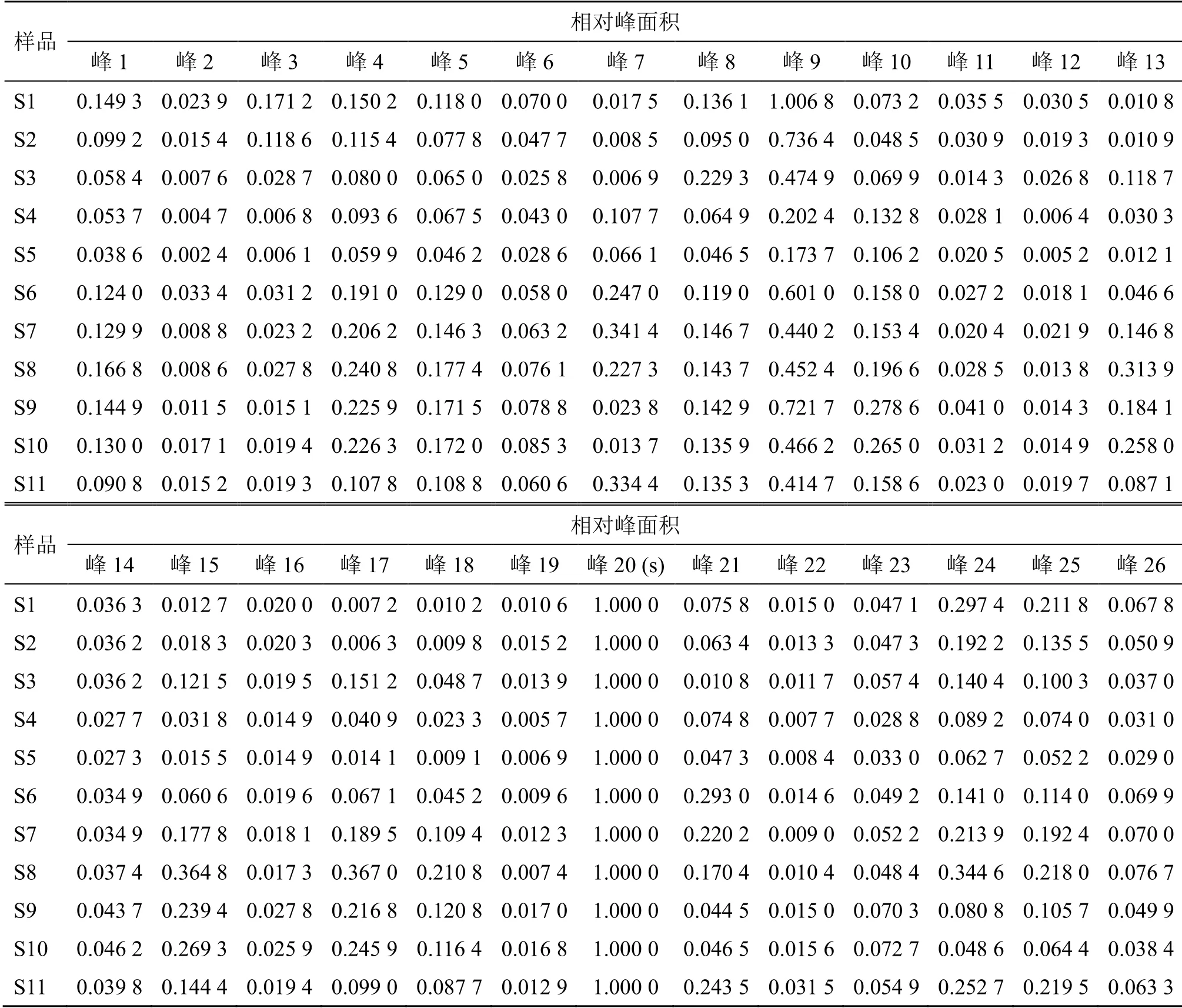
表5 11 批芩连制剂样品特征图谱相对峰面积测定结果Table 5 Determination of relative peak area of 11 batches of samples from Qinlian preparation
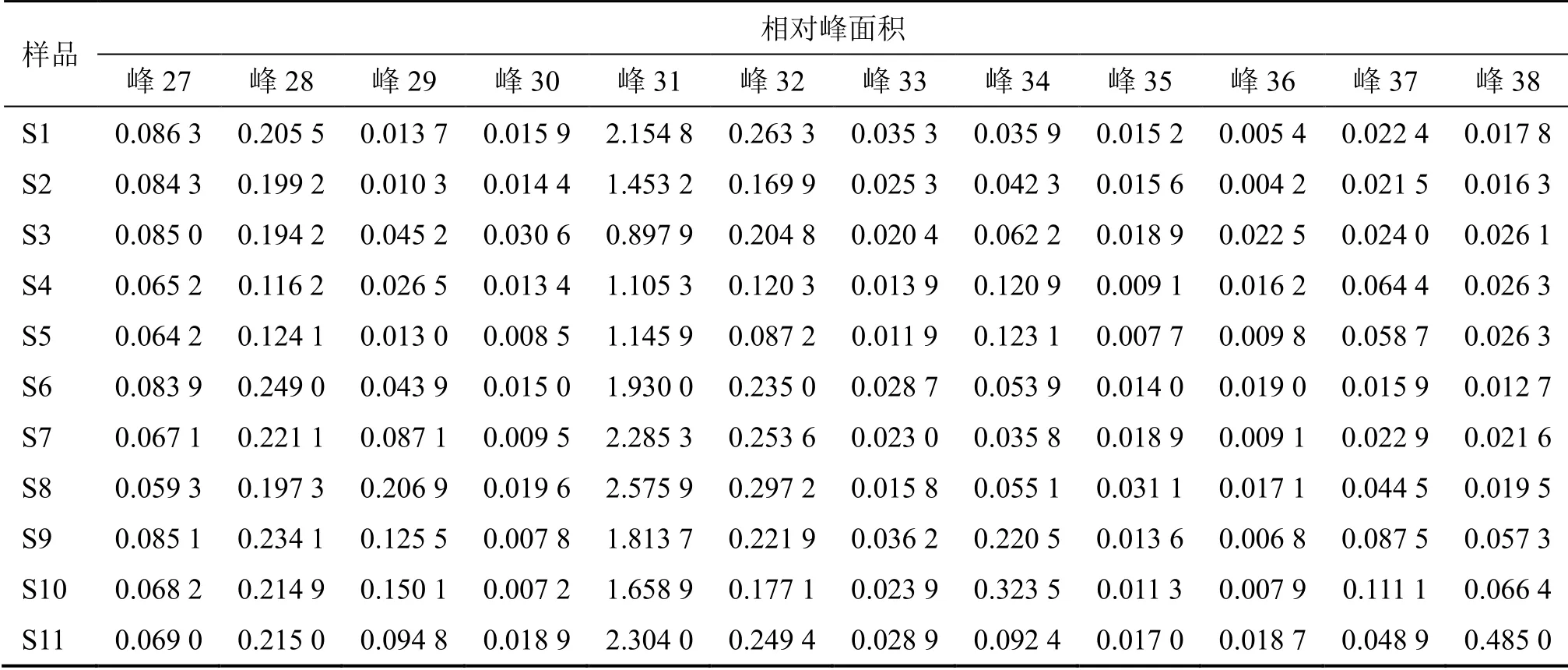
续表5
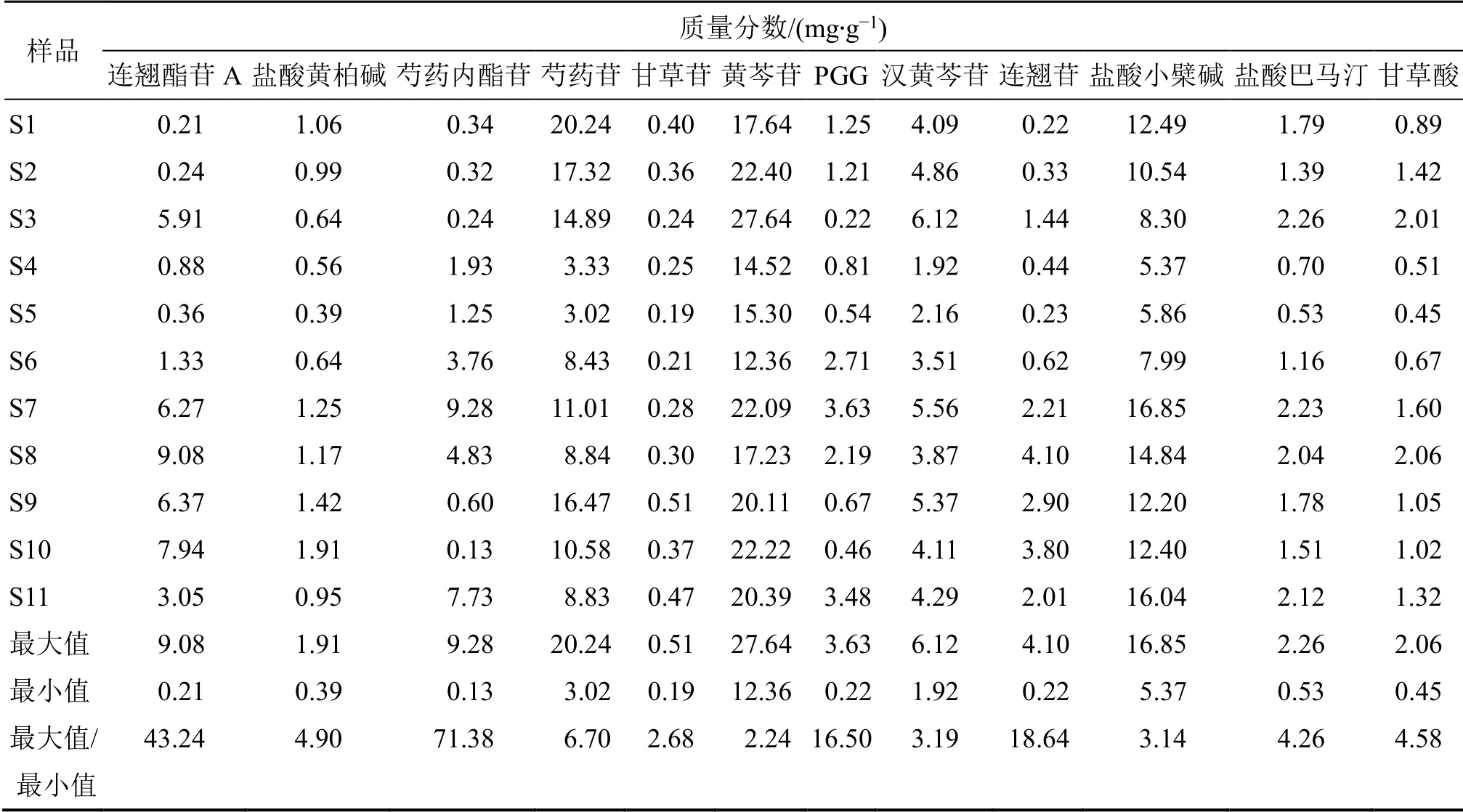
表6 11 份芩连制剂中12 个指标性成分含量测定结果Table 6 Determination of 12 index ingredients in 11 samples of Qinlian preparation
2.4 多批次芩连制剂样品质量分析
2.4.1 芩连制剂样品整体质量分析 采用SIMCA 13.0 统计分析软件PCA-X,OPLS-DA 分析方法,以芩连制剂特征图谱中38 个特征峰的相对峰面积比值及其12 个指标性成分含量为质量表征数据,分析11 份芩连制剂质量分布状况。
如图6所示,在无监督模型下(PCA-X),11批次芩连制剂整理质量分布按聚集程度分为3 类:第1 类包括S1~S3(片剂)、S6~S8(片剂、胶囊剂)、S11(丸剂);第2 类包括S4~S5(片剂);第3 类包括S9~S10(胶囊剂)。
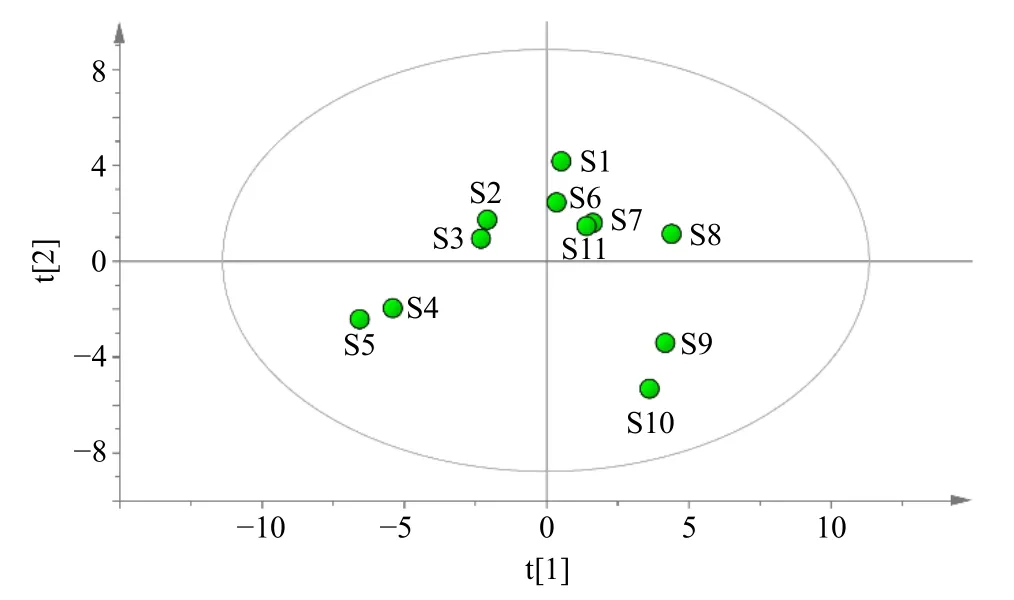
图6 无监督模型下11 批次芩连制剂特征图谱质量表征分布散点图Fig.6 Scatter plot of quality characterization profiles of 11 batches of Qinlian preparation under unsupervised model
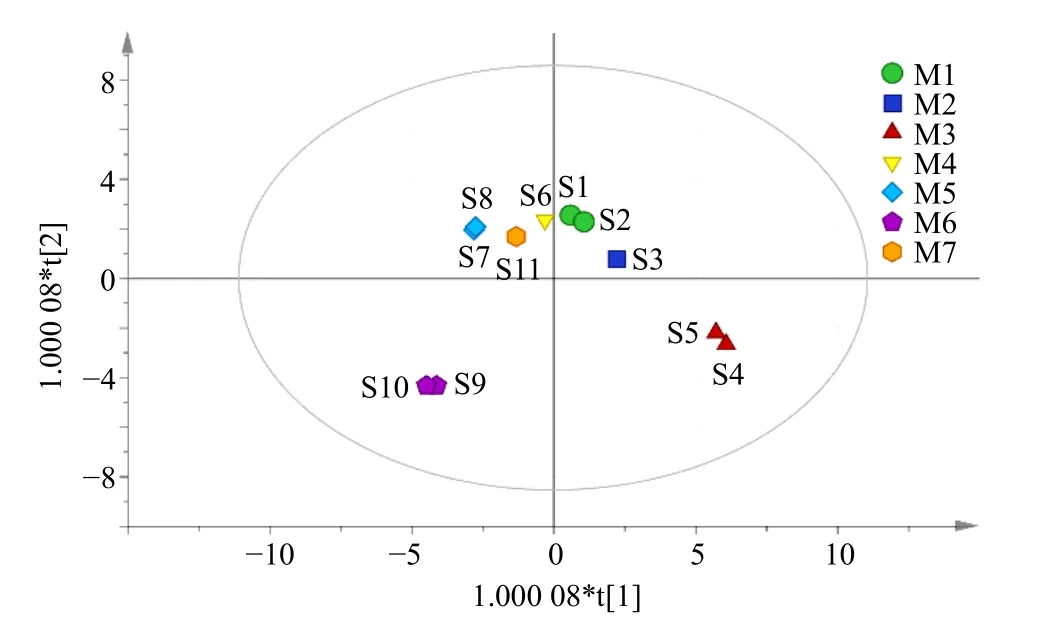
图7 以生产厂家为分类的有监督模型下11 批次芩连制剂特征图谱质量表征分布散点图Fig.7 Scatter plot of quality characterization distribution of 11 batches of Qinlian preparations under a supervised model classified by manufacturer
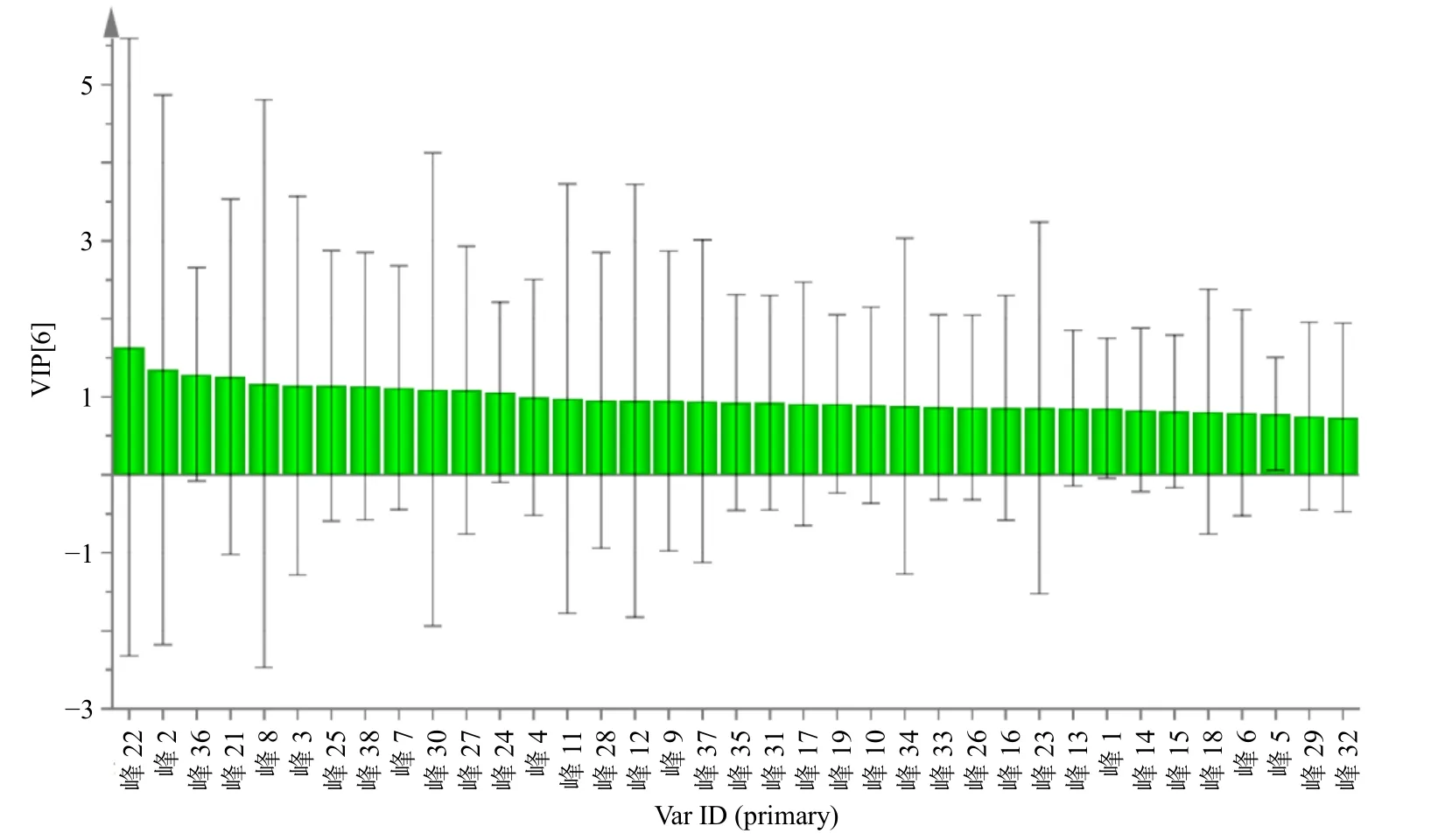
图8 以生产厂家为分类的有监督模型下11 批次芩连制剂特征成分VIP 得分图Fig.8 VIP score chart of characteristic components of 11 batches of Qinlian preparations under a supervised model classified by manufacturer
如图7所示,在以生产厂家为分类的监督模型下(OPLS-DA),11 批芩连制剂整体质量分布趋势,与无监督模型下一致(第1 类:S1~S2 厂家1,S3厂家2,S6 厂家4,S7~S8 厂家5,S11 厂家7;第2 类:S4~S5 厂家3;第3 类:S9~S10 厂家6);如图8所示,质量差异成分VIP 值得分高于1.0 的指标成分有13 个,依次为(VIP 值1.6~1.0 从大到小):峰22(黄芩)、2(赤芍)、36[连翘(连翘酯素)]、21[赤芍(PGG)]、8(黄连、川黄柏)、3(连翘)、25(黄连)、38(黄芩)、7[赤芍(芍药内酯苷)]、30(连翘)、27(黄芩)、24(黄连)、4(黄连、川黄柏);质量分类的相关成分主要来源于:黄芩(峰22、38、27),赤芍[峰2、21(PGG)、7(芍药内酯苷)],连翘[峰36(连翘酯素)、30)],黄连(峰24),黄连-川黄柏(峰8、4),连翘-赤芍(峰3)。
2.4.2 芩连制剂样品指标性成分的含量分析 根据指标性成分来源,分别对11 批芩连制剂中各药味指标性成分含量进行分析,统计11 批次芩连制剂中各指标性成分含量范围,计算最大含量和最小含量倍量关系,见表5;12 个指标成分含量差异范围为2~71 倍,根据各指标成分含量范围最大值与最小值的差量倍数依次从大到小排序为芍药内酯苷(71.38倍)>连翘酯苷A(43.24 倍)>连翘苷(18.64倍)>PGG(16.50 倍)>芍药苷(6.70 倍)>甘草酸(4.58 倍)>盐酸黄柏碱(4.90 倍)>盐酸巴马汀(4.26 倍)>汉黄芩苷(3.19 倍)>盐酸小檗碱(3.14 倍)>甘草苷(2.68 倍)>黄芩苷(2.24倍);指标性成分含量差异大于5 倍的药味来源主要是:连翘(连翘酯苷A 和连翘苷)、赤芍(芍药内酯苷、PGG 和芍药苷)。
3 讨论
3.1 芩连制剂质量差异表征分析
芩连片、芩连胶囊、芩连丸3 种制剂中成药处方组成相同,导致其质量差异的主要因素有:原料质量、提取次数、提取时间、提取溶剂量、干燥方式、辅料添加量等。因此,不同批次的芩连制剂特征图谱及其12 个指标性成分含量,都表现为以厂家为主的质量聚类分布。
从芩连制剂的整体质量分布分析结果看,以厂家为主的质量聚类分布相关因子,主要来源于黄芩(峰22、38、27)、赤芍[峰2、21(PGG)、7(芍药内酯苷)]、连翘[峰36(连翘酯素)、30)]、黄连(峰24)、黄连-川黄柏(峰8、4)、连翘-赤芍(峰3)。
从芩连制剂的指标性成分含量差异上看,不同厂家的生产工艺均由黄芩、川黄柏、甘草、连翘4味饮片同时提取制备,而黄芩、甘草、川黄柏指标性成分含量差异范围(2~5 倍)明显低于连翘指标性成分连翘酯苷A 含量差异(43.24 倍);同样,不同剂型的芩连制剂中赤芍和黄连均为粉碎后与提取物混合制备药物,而赤芍指标性成分芍药内酯苷含量差异(71.38 倍)明显高于其它黄芩、甘草、川黄柏、黄连的含量差异范围。结合连翘和赤芍原料饮片及其中药材的质量特征可知,青翘和老翘不同规格的连翘中连翘酯苷A 含量差异较大,赤芍和易混药材白芍中芍药内酯苷含量差异较大,芩连制剂中这两个成分含量的显著差异,应与原料中药材的质量差异相关。
3.2 芩连制剂特征图谱分析方法
在分析方法建立的过程中,通过甲酸、磷酸等不同流动相的对比考察,不同体积流量考察,发现赤芍成分与黄连、黄柏成分相互干扰严重,受流动相pH 值变化影响较大;小檗碱等生物碱成分拖尾较为严重,不易与连翘苷等成分分离检测;经实验选定了乙腈(含0.02%甲酸)-(10 mol/L 乙酸铵-0.09%甲酸缓冲液)为流动相,实现了目标测定成分较为稳定的分离效果。研究最终采用UHPLCDAD 法建立了芩连制剂特征图谱质量表征方法,在已有文献报道的基础上,提高了指标性成分定量范围的宽度和准确度,并首次建立了对芩连制剂组方6 味中药的12 个关键指标性成分含量的同时测定,为芩连制剂的质量评价提供的研究基础。
利益冲突所有作者均声明不存在利益冲突
