TKI耐药慢性髓系白血病患者ABL激酶区点突变的相关因素分析
2021-03-08陈东阳张砾丹张红宾
陈东阳,汪 晶,张砾丹,程 颖,张红宾
(重庆医科大学附属第一医院血液科,重庆 400016)
慢性髓系白血病(CML)是起源于骨髓造血干细胞的血液系统恶性肿瘤,约占成人白血病的15%[1]。其发病机制为t(9,22)(q34,q11)染色体易位,从而形成BCR/ABL融合基因,该基因编码的融合蛋白具有酪氨酸激酶活性,通过持续激活下游包括Ras、MAPK、PI3K、JAk-STAT、Src在内的多种信号通路,导致造血干细胞的恶性增殖及凋亡障碍,这也是伊马替尼(IM)等酪氨酸激酶抑制剂(TKI)治疗CML的分子基础[2]。TKI的出现极大地改善了CML患者的疗效,然而,随着其广泛应用于临床,耐药现象也随之出现,主要机制为ABL激酶区突变导致酶蛋白空间结构改变,阻碍TKI与之结合而影响疗效。据报道,约50%~90%的IM耐药患者存在激酶区突变[3]。本研究回顾性分析了37例TKI耐药CML患者激酶区点突变的相关因素,为预防激酶突变及制定最佳诊疗方案提供思路。
1 资料与方法
1.1一般资料 选择2014年1月至2017年12月于重庆医科大学附属第一医院诊断为CML且携带ABL激酶区点突变(包括7例E255K/V、3例T315I、3例Y253H、1例H396R、1例F359I、2例E255K/V/T315I、1例E255K/V/F359I突变)的耐药患者18例和无点突变的耐药患者19例作为研究对象,诊断标准参照张之南等[4]主编的《血液病诊断及疗效标准(第三版)》。突变组中男10例,女8例;年龄15~83岁,中位年龄47岁;处于慢性期(CP)10例,加速期(AP)2例,急变期(BP)6例。未突变组中男7例,女12例;年龄21~70岁,中位年龄49岁;处于CP 12例,AP 2例,BP 5例。两组一般资料比较,差异无统计学意义(P>0.05)。
1.2方法
1.2.1研究方法 患者入院后行骨髓穿刺及骨髓活检,收集骨髓标本送检细胞遗传学及分子生物学检查,检测Ph染色体、BCR/ABL融合基因及ABL激酶区耐药基因。同时抽取外周血行血常规、生化等检验。
1.2.2耐药诊断标准 接受IM治疗满3个月未获得完全血液学反应(CHR);满6个月未获得部分细胞遗传学反应(PCyR);满12个月未获得完全细胞遗传学反应(CCyR);任意时间丧失CHR或CCyR或主要分子学反应(MMR);任意时间出现TKI耐药性突变或Ph+细胞基础上的其他克隆性染色体异常。

2 结 果
2.1ABL激酶区点突变的单因素分析 以激酶区点突变为因变量,以性别、年龄、疾病分期等13个因素为自变量进行单因素分析,结果显示,Sokal积分(P=0.010)、染色体核型(P=0.003)、是否规律治疗(P=0.049)为影响激酶区点突变的危险因素。其余10个因素两组比较,差异无统计学意义(P>0.05),对激酶区点突变无影响。见表1。
2.2ABL激酶区点突变的多因素logistic回归分析 将单因素分析中有意义的3个因素纳入多因素logistic回归分析,结果显示,Sokal积分中、高危(P=0.049)、复杂染色体核型(P=0.029)、未规律治疗(P=0.022)均是ABL激酶区点突变的独立危险因素。对回归方程进行综合性检验,χ2=26.672,P<0.001,回归方程有意义。见表2。
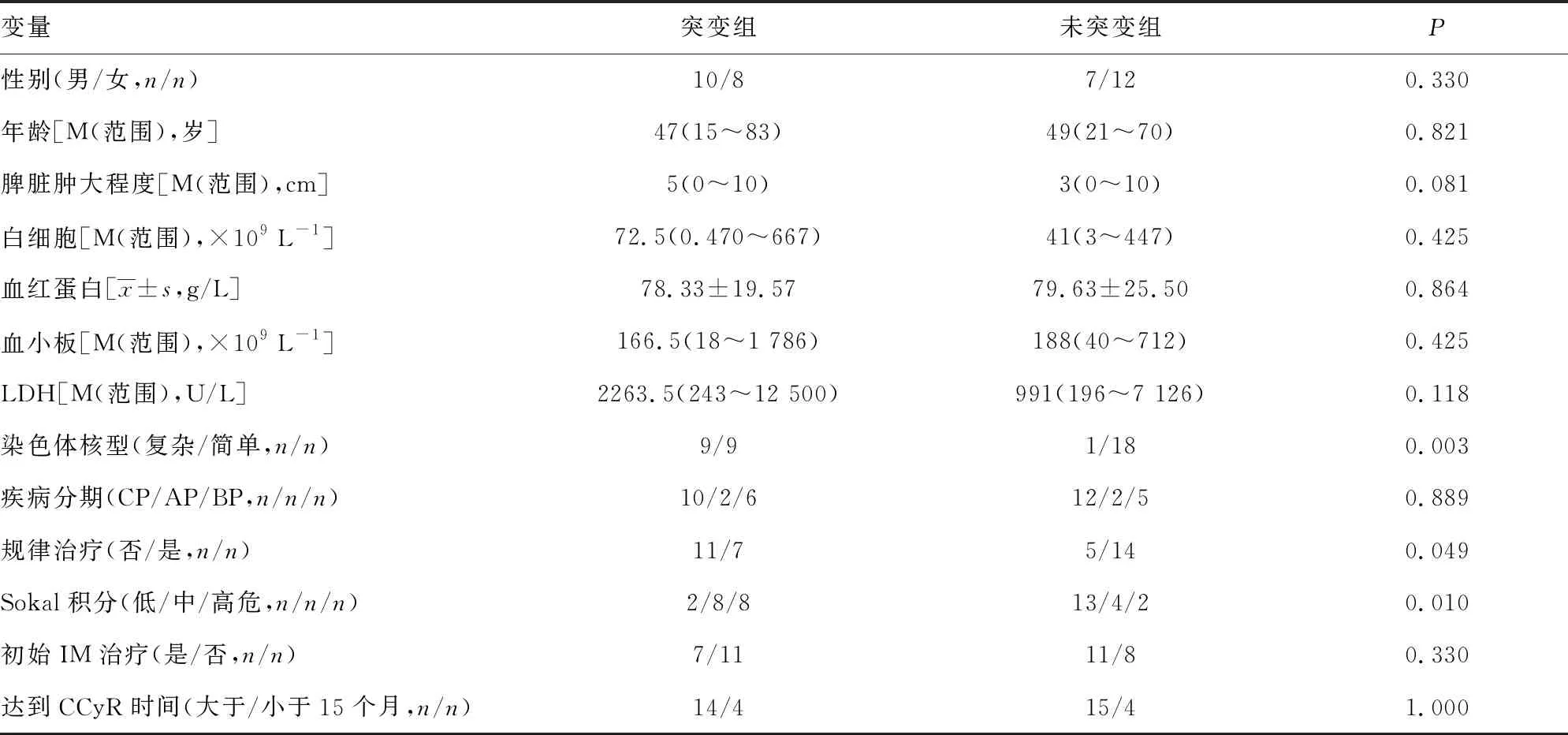
表1 突变组和未突变组基本资料的单因素分析结果
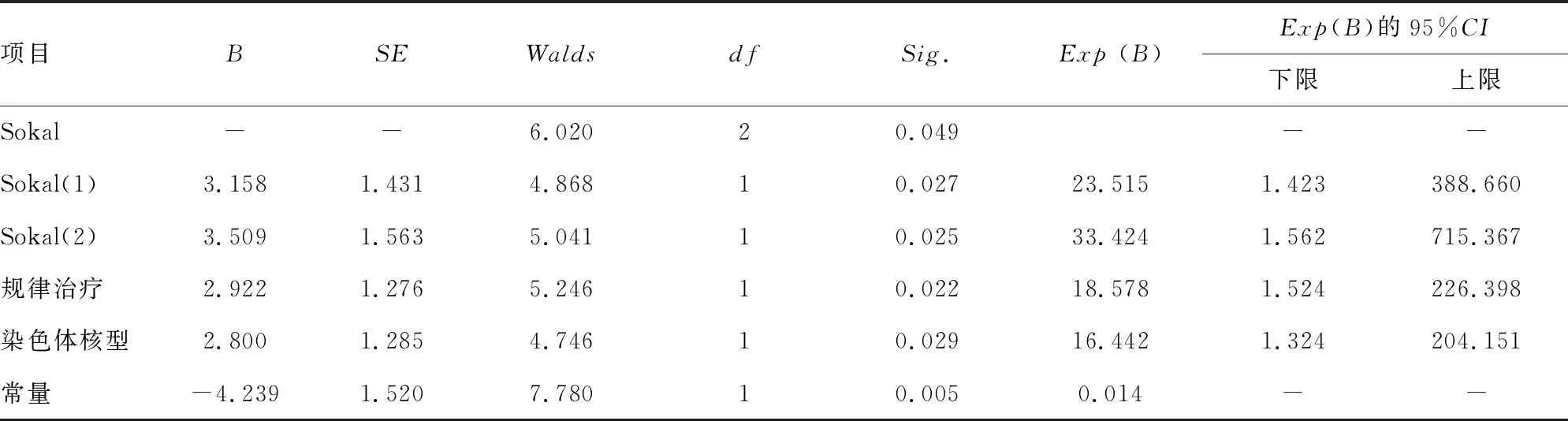
表2 ABL激酶区点突变的多因素logistic回归分析结果
3 讨 论
以IM为代表的相对分子质量小的TKI改变了羟基脲和干扰素对CML的传统疗法,为CML患者的治疗带来了新曙光,然而,激酶区突变带来的耐药问题仍有待解决。不同突变类型耐药程度各异,尤以T315I突变耐药程度最高,该类患者的BCR/ABL表达水平显著高于其他突变类型的患者[5-6]。不同突变类型推荐不同的治疗方案[1]。因此,及时识别导致激酶区突变的因素、更改为敏感方案治疗对改善患者预后至关重要。本研究对激酶区点突变的相关因素进行了回顾性分析。
本研究结果显示,复杂染色体核型和Sokal积分中、高危是激酶区点突变的独立危险因素,而性别、年龄、疾病分期不是危险因素。这与高冠论等[7]的研究结果相似,同时,本研究还对是否规律治疗进行了分析,发现未规律治疗也是激酶区突变的危险因素之一。
Ph染色体是CML的特征染色体,存在于约95%的CML患者中,在Ph染色体基础上出现附加染色体异常者在治疗过程中达CCyR和MMR的时间更长,无进展生存期(PFS)和总生存期(OS)更短,且通常更易进展至AP和BP,对患者预后存在负面影响[8]。本研究结果显示,具有复杂染色体核型的患者激酶区点突变风险约为单纯核型患者的16倍。 MARCÉ等[9]报道,细胞遗传学克隆演变与激酶区突变之间存在相关性,具有附加染色体异常的人群突变频率更高,与本研究结果相符。该研究同时指出虽未建立统计学联系,但进展至加速期的患者更具有激酶区突变的倾向。然而,在包括本研究在内的多项研究中,疾病分期与激酶区突变并无相关性,CP、AP、BP患者的突变频率无统计学差异[10-12],可能是由于目前研究的样本量相对较小,因此有待更大规模的研究进行深入探索。
Sokal积分在评估CML患者预后中扮演着重要角色,该评分纳入了年龄、脾脏肿大程度、血小板计数、血原始粒细胞比例进行积分,将CML患者分为低危、中危及高危组。NICOLINI等[13]报道,Sokal积分能有效预测CML患者预后,评分较低者通常具有较长的OS及PFS。本研究结果显示,Sokal积分中、高危是激酶区点突变的独立危险因素,中危患者的突变机会约为低危患者的23倍,高危患者的突变机会约为低危患者的33倍。CARELLA等[14]报道,高危组CML患者的激酶区突变率高达61.5%,中危组约为16.7%,而低危组中未发现突变,提示突变更可能与患者的基本生物学特征有关,而不是随机事件。KAGITA等[6]的研究也证实,Sokal积分中、高危患者的激酶区突变率显著高于低危患者,与本研究结果相符合。因此,临床上可对初诊CML患者及时进行Sokal积分分组,中高危组患者建议行ABL激酶区突变检测,对阳性患者及时更换敏感TKI治疗或考虑行造血干细胞移植。
另外,本研究对是否规律治疗也进行了分析,结果显示,其是激酶区点突变的另一独立危险因素,未规律治疗者突变风险增加了约17倍。有文献报道未规律治疗常导致IM耐药[11]。这一结果对临床治疗有一定的指导意义,自确诊CML后即进行规律治疗、提高患者依从性、定期随访可能可在一定程度上预防激酶区点突变,防止疾病进展。
PAGNANO等[15]报道,ABL激酶区突变组较未突变组有较高的脾脏肿大程度和较低的血红蛋白水平;然而,本研究中,突变组与未突变组比较,差异无统计学意义(P>0.05),可能是由于本研究样本量较小。此外,是否初始IM治疗、达到CCyR时间、白细胞计数、LDH水平、血小板计数也不是影响激酶区点突变的因素,但诸多临床生化指标有助于判断患者病情、评估疗效,因此也应给予密切关注。
综上所述,ABL激酶区点突变为CML患者耐药的主要原因,在众多临床因素中识别出激酶突变相关因素有助于指导临床决策。提高患者依从性、规律治疗、良好的患者教育可在一定程度上降低激酶突变风险,减少患者耐药。对于复杂染色体核型和Sokal积分中、高危的患者,及早行激酶区突变检测并调整治疗方案有助于改善患者预后。
