基于UPLC-Q-TOF-MS 技术的阿司匹林抵抗血清代谢组学研究*
2021-03-06蒋志涛吕玲燕
蒋志涛,吕玲燕,韩 怡,倪 磊
南京中医药大学附属张家港医院药学部,张家港 215600
阿司匹林抗血小板功效显著,常用于心血管疾病(cardiovascular disease,CVDs)的一级和二级预防。从20 世纪90 年代以来,临床上出现有部分患者使用阿司匹林后并没有达到预期治疗效果,称之为“阿司匹林抵抗”(aspirin resistance,AR)[1]。鉴于阿司匹林是改善患者CVD 结局干预措施的关键物质,有发生CVD 事件风险的患者如果出现AR 就是重要的临床问题。同时AR 患者的心血管事件发生率和死亡率显著增加,Gum PA 等[2]研究了326 例使用阿司匹林的稳定性CVD 患者,其中有17 例(5.2%)出现AR,平均随访1.9 年后,AR 患者的复合终点(死亡、心肌梗死或脑卒中)发生率为24%,显著高于其余患者的10%。目前尚不完全清楚AR产生的机制,研究显示,其主要的影响因素包括用药依从性差、阿司匹林药代动力学变化、与其他药物相互作用、血小板活性上调、非血小板COX-1 来源的血栓素A2 生成增多、药物治疗靶点变化等[3]。
现有的AR 治疗措施主要为调整药物剂量、服药时间、控制基础疾病等,临床效果并不显著。中医药干预AR 治疗具有独特的优势。马卫琴等[4]研究了87 例AR 患者的体质类型,其中以血瘀、气虚体质较为常见。陈光等[5]研究多项中医药临床干预AR,结果显示血瘀既是AR 的病因,也是AR 的病理产物,血瘀证与AR 紧密相关。还有研究表明,AR 最终将导致血瘀证的出现[6]。本研究运用超高效液相色谱-飞行时间质谱(UPLC-Q-TOF-MS)技术寻找AR相关的潜在生物标志物,为后期深入探讨“药物改善AR 的作用机理”打下基础。
1 仪器与材料
1.1 仪器
ACQUITY UPLC TM 型超高效液相色谱仪和Xevo G2-XS 型飞行时间质谱(美国Waters 公司);AE240 电子天平(上海梅特勒-托利多有限公司)。
1.2 药物与试剂
阿司匹林肠溶片(拜阿司匹林,批号BJ40031,拜耳医药保健公司);布洛芬缓释胶囊(芬必得,批号18010587,中美天津史克公司);硫糖铝咀嚼片(批号227004,重庆科瑞制药);乙腈、甲酸、甲醇为色谱纯;醋酸铵为分析纯;超纯水。
1.3 动物
雄性金黄地鼠(SPF 级)80 只,6~8 周龄,体重120~140 g,购于南京青龙山动物养殖场,动物许可证号:SCXK(苏)2017-0001。
2 方法与结果
2.1 金黄地鼠分组及AR 模型建立
参考唐世英等[7]金黄地鼠高脂血症动物模型研究,将金黄地鼠随机分为空白组(A 组,n=12)、阿司匹林抵抗模型组(B 组,n=12)。A 组自由餐食饮水;B 组给予饲料(高脂高盐高糖)喂养12 周。具体造模方式为:第9 周开始每天早上8 时给予B 组金黄地鼠硫糖铝(14.8 g·kg-1)灌胃一次,下午1 点给予B 组阿司匹林(0.74 g·kg-1)和布洛芬(2.22 g·kg-1)混合灌胃一次,药物剂量随金黄地鼠体重变化而每1 周调整一次。同时第9 周开始每天下午4 时将B 组金黄地鼠置于10 m2密闭实验室内,点燃香烟15 支,持续30 min。
模型判断标准:B 组金黄地鼠第12 周禁食12 h后,于腹主动脉取血进行检测,检测结果:甘油三酯>0.8 mmol·L-1、血清总胆固醇>1.6 mmol·L-1,表明高脂血症模型成功。该金黄地鼠再进行血小板聚集检测[8],其中血小板平均聚集率既符合腺苷二磷酸钠盐诱导下≥70%,又符合花生四烯酸诱导下≥20%,则认为其属于AR 造模成功。
2.2 血清样本采集与处理
采用腹主动脉取血法。为了减少采血对金黄地鼠体内内源性物质的干扰,采集空腹血样进行代谢组学分析。采血方法为:第12 周末,将所有金黄地鼠禁食12 h,10%水合氯醛(3 mL·kg-1)腹腔麻醉,仰卧位固定,开腹主动脉取血4 mL,以2 mL 全血供血小板聚集检测,2 mL 置于医用血清管中,3000 r·min-1离心20 min,取上层血清于-70 ℃保存,供UPLC-Q-TOF-MS 分析。
分析前于室温下解冻血清,涡旋30 s,取200 μL 样品加入1.5 mL EP 管中,而后加入800 μL 预冷的甲醇(4 ℃),涡旋30 s 后,4 ℃下12000 r·min-1离心10 min,吸取上清液,放置于离心浓缩仪35 ℃离心挥干,50%甲醇100 μL 复溶,4 ℃下12000 r·min-1离心10 min,吸取50 μL 于进样小瓶中待测。
为保证分析系统的稳定性,采用质量控制(quality control,QC)样品进行方法验证。QC 样品是由每个样品各取40 μL 复溶液混合而得,为降低误差,样品检测为随机进行。在对样品分析前,先运行5 次QC 样品以平衡系统,在检测过程中,每检测5个样品后运行1 次QC 样品,以衡量系统的稳定性。
2.3 色谱条件
采用Acquity UPLCTM BEH C18色谱柱(2.1mm×50 mm,1.7 μm);柱温:40℃;流速:0.4 mL·min-1,采用梯度洗脱的方式运行15 min。每次进样5μL,自动进样器温度设定4℃。正离子检测:A 流动相=99.9%乙腈、0.1%甲酸;B 流动相=99.9%水、0.1%甲酸。负离子检测:A 流动相=90%乙腈、10%水,10 mmol 醋酸铵,氨水调节pH 至9;B 流动相=5%乙腈、95%水,10 mmol 醋酸铵,氨水调节pH 至9。洗脱程序:0~0.5 min,3% B;0.5~1.5 min,3~20% B;1.5~6 min,20~60% B;6~9 min,60~95% B;9~12 min,95% B;12~12.1 min,95~3% B;12.1~15 min,3% B。
2.4 质谱条件
电喷雾离子源(ESI)采用正、负离子扫描模式,毛细管电压3.0kV,锥孔电压30V,碰撞能电压6eV,离子源温度120 ℃,除溶剂温度350 ℃,除溶剂气体流为700 L·h-1氮气,采集范围m/z 100~1000,碰撞气体为氦气。
质谱正离子扫描,全扫描范围m/z 70~1050。全扫描中选择离子强度TOP15 的母离子进行二级质谱鉴定。质谱负离子扫描,全扫描范围m/z 70~1050。全扫描中选择离子强度TOP15 的母离子进行二级质谱鉴定。
2.5 系统稳定性检测
运用UPLC-Q-TOF-MS 代谢组学研究,稳定的实验方法才能获得可靠的实验数据。每隔4 个样品分析QC 样品和空白样品,以检验分析方法的稳定性和色谱上样量。
2.6 数据处理和统计分析
获取UPLC-Q-TOF-MS 指纹图谱后,采用Analyst®TF 1.7 Software 导出原始数据,可以存储到与每份样品对应的独立的文件中,PeakView 将异常的峰去掉;Markview 进行峰对齐。最终获得包含质荷比、保留时间和峰面积三维数据表,利用QC 样品对所有峰进行校正,将校正后的数据导入Simca-P v13.0 和EZinfo 3.0 进行多维统计分析,以便筛选出变量。采用主成分分析(PCA)得分图,直观地表示组与组之间的差异,通过偏最小二乘法判别分析(PLS-DA)的变量投影重要性(variable importance in projection,VIP)值,筛选前后变化显著的差异代谢物,使用SPSS 16.0 软件进行统计学处理,两组间差异显著性比较采用t 检验,P<0.05 表示差异有统计学意义。将找到的潜在差异代谢物在HMDB(human metabolome databatabase)、METLIN 和KEGG(kyoto encyclopedia of genes and genomes)数据库进行检索与确认,得到最终匹配差异代谢物。
2.7 主成分分析
在正、负离子模式下,血清及QC 样品PCA 得分图见图1。将经过校正后的质谱数据,采用PCA法研究阿司匹林抵抗血清代谢物谱图模式变化,获得三组血清样本在空间上的分布情况。图1 同一颜色代表相同症状研究组,相同颜色越集中说明同一症状个体差异小,越分散表明个体差异大。PCA 结果表明,正、负离子模式下,QC 样品的聚集状况均良好,表明系统的稳定性良好。AR 组和对照组尽管有部分交叉重叠,但有一定的分离趋势。
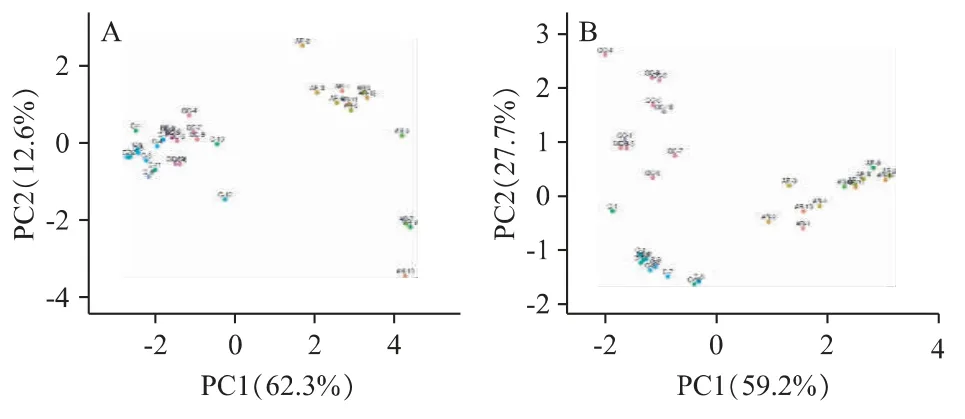
图1 血清及QC 样品正(A)、负(B)离子模式下的主成分分析得分图
2.8 偏最小二乘法及置换检验
为消除与研究目的无关的随机误差及组内误差,对UPLC-Q-TOF-MS 数据采用有监督的PLS-DA方法再次进行分析。PLS-DA 由PCA 演变而来的双线性回归模型,能够忽略次要因素对结果的不利影响,提高判别分析的能力,有助于确定两组间的差异成分,从而识别有效的标志物,不同颜色符号在此种建模中分散的越开,说明两组间的成分差异越显著。本研究PLS-DA 得分图见图2,其显示AR 组与对照组分离明显,说明两组间存在一定差异。PLS-DA 正、负离子模式的模型参数分别为R2Y=0.929,Q2=0.435;R2Y=0.978,Q2=0.673;表明模型有效。进一步对模型进行响应置换检验,100 次随机改变后建立对应数据的PLS-DA 模型,以获取模型的R2和Q2值。在两种模式下,R2=0.932,Q2=0.201;R2=0.954,Q2=0.137;说明建立的模型符合样本数据的真实情况,不存在过拟合现象,模型稳健性良好。
2.9 差异代谢物的筛选[9]
本研究使用PLS-DA 模型中VIP 值参数,结合t 检验进行组间比较,筛选潜在的差异代谢物,VIP值是两组中含量显著改变的代谢物值,VIP 值>1 并P<0.05 时,显示对应的代谢物是差异性代谢物。针对组间的比对情况,在金黄地鼠不同组血清样本中找到主要差异性代谢物,其中倍数变化(fold change,FC)代表不同组血清代谢物含量的比值,FC≥1.5 表明不同组血清中该代谢物质相比正常组含量上升,表达为上调代谢物,FC≤2/3 表明不同组血清中该代谢物质含量下降,表达为下调代谢物。通过搜索ChemSpide、MassBank、MetFrag 和Metlin等数据库,结合质谱数据鉴定差异代谢物。结果表明与对照组相比,AR 组有脱氧胆酸、硬脂酸、松香酸、谷氨酰胺、肌酸等11 个特异性代谢分子,其信息见表1。代谢物通路分析提示,与脂肪酸生物合成、二次胆汁酸生物合成、氨基酸代谢等密切相关。
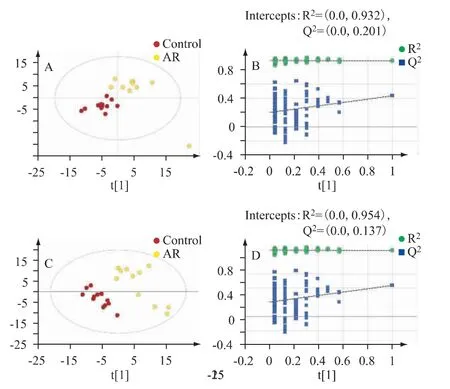
图2 对照组和AR 组正、负离子模式下最小二乘法判别分析
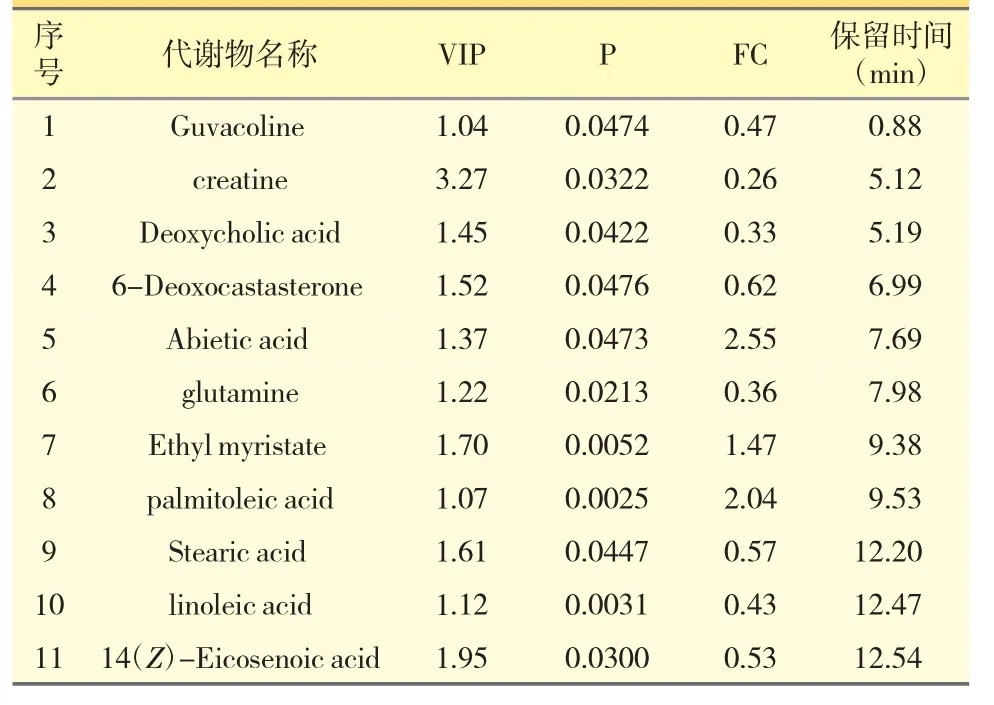
表1 主要差异代谢物信息
3 讨论
AR 的病理生理过程十分复杂,目前其机制尚未阐明。代谢组学技术的应用,为从代谢的视角揭示AR 病理生理学过程的变化,以及它们包含的生物学意义提供了新的工具和方法。本实验采用UPLC-Q-TOF-MS 技术比较了AR 大鼠与正常大鼠血清化学成分的变化。模型组大鼠血清中含有各类小分子代谢物,包括氨基酸、脂肪酸、胆汁酸等,且部分在含量上与对照组有明显差异,这些物质参与了多种生理生化过程,特别是脂代谢和胆汁酸代谢。
脱氧胆酸是胆酸失去一个氧原子衍生而得的一种游离胆汁酸,胆汁酸促进脂类物质的消化与吸收,是体内胆固醇的主要代谢去路,胆固醇转化为胆汁酸的代谢途径异常可导致高胆固醇血症,进而参与动脉粥样硬化的发生、发展。临床研究证明,胆汁酸与血脂代谢紊乱、冠心病及脑血管疾病关系密切,有可能是冠心病的独立危险因素[10]。
心肌在正常状态下,脂肪酸氧化是其能量代谢的主要形式,心肌缺血缺氧时,脂肪酸代谢异常,表现为脂肪酸氧化减弱,中间产物堆积,心肌内血清游离脂肪酸水平升高,其中硬脂酸是长链脂肪酸氧化的中间产物。模型组样本中硬脂酸含量升高,提示AR 导致脂肪酸氧化速率下降,心肌能量代谢异常。
目前中医药干预AR 的研究主要集中于临床研究,一些单味中药(银杏、丹参、三七等)及中成药(复方丹参滴丸、通心络胶囊、护心胶囊等)均报道对预防及治疗AR 效果显著,但机制研究较少。范英华等[11]研究发现,丹酚酸A 可有效抑制多种诱导剂(ADP、花生四烯酸等)诱导的大鼠血小板聚集,并能显著升高血小板中cAMP 的含量,其机制与cAMP多条GPCRs 信号通路有关。赖润民等[12]通过网络药理学研究发现,丹红注射液改善AR 机制涉及凝血过程、炎症反应、代谢调节的21 条通路。
本研究显示,AR 组有11 个差异代谢物:脱氧胆酸、硬脂酸、松香酸、谷氨酰胺、肌酸等,为AR 的潜在生物标志物,提示AR 致病机理可能与脂肪酸生物合成、二次胆汁酸生物合成、氨基酸代谢有关,这为今后深入探讨中药改善AR 的作用机理提供理论数据。
