高效液相色谱法测定人脑脊液中万古霉素浓度及临床应用*
2021-03-06黄晓会林志燕沈艳琳卜书红
黄晓会,林志燕,沈艳琳,卜书红,张 健
上海交通大学医学院附属新华医院,上海 200092
颅内感染是重型颅脑外伤开颅术后严重并发症,具有高致残、致死率,会延长住院时间、增加治疗费用,严重影响预后[1]。由于机体颅内血脑屏障的作用,使常规药物较难透过、较难进入,因此降低了颅内感染的治疗效果[2]。
万古霉素(vancomycin,VAN)属于三环糖肽类抗菌药物,被誉为抗生素最后一道防线。临床上是用于治疗严重的颅内感染的常用药,但其通过血脑屏障达到最小杀菌浓度的维持时间短,需要剂量大[2],其具有一定的抗生素后效应时间依赖性,并且有耳、肾毒性和血栓性静脉炎等严重不良反应。文献报道,脑室内或鞘内注射抗菌药物治疗颅内感染具有较好的临床疗效[3],此治疗方法逐渐普及,但缺乏相关基础研究,对药物的安全剂量、用药间隔时间、疗程没有统一的标准[4],因此对监测脑脊液中药物浓度至关重要。本研究采用内标法,建立脑脊液中的万古霉素含量测定方法,对本院患者脑脊液浓度进行监测,可及时调整给药方案,使其在安全有效浓度范围内。
1 材料与方法
1.1 仪器、药品及试剂
1260 高效液相色谱仪,包括G1367E 自动进样器,G1311B 四元泵,G4212B 二极管阵列检测器(美国Agilent 公司);Milli-Q 纯水器(Millipore);VORTEX KB3 型旋涡混悬器(海门市其林贝尔仪器制造有限公司);5424R 高速冷冻离心机(德国eppendorf 公司)。
万古霉素对照品(批号:130329-200501)、去甲万古霉素对照品(批号:130359-200503),均中国食品药品检定研究院;甲醇、乙腈(色谱纯,美国Fisher公司);高氯酸、磷酸、磷酸二氢钾均为分析纯;纯化水。
1.2 溶液配制
1.2.1 对照品溶液 精密称取万古霉素对照品20 mg,用水定容至5 mL 量瓶中,配制成质量浓度为4000 mg·L-1的对照品储备溶液,经水适当稀释成对照品溶液。
1.2.2 磷酸二氢钾缓冲液 精密称取磷酸二氢钾6.8045 g,用水溶解并定容至1000 mL,用磷酸调节pH 值至3.2,配制成0.05mol·L-1的磷酸二氢钾缓冲液。
1.2.3 内标溶液 精密称取去甲万古霉素对照品20 mg,用水定容至10 mL 的量瓶中,配制成质量浓度为2000mg·L-1的对照品储备液,再取该溶液125μL至25 mL 量瓶中,加水定容至刻度,稀释为10 mg·L-1的内标溶液,备用。
2 方法[5]与结果
2.1 色谱条件
色谱柱:Eclipse XDB C18(250mm×4.6mm,5μm);流动相:磷酸二氢钾缓冲液(pH3.2)-乙腈(梯度洗脱:0~20 min:98%~90%A;20~25 min:90%~90%A;25~25.1 min:90%~98%A;25.1~30 min:98%A);检测波长:236nm;柱温:30 ℃;流速:1 mL·min-1;进样量:20 μL。
2.2 样本前处理
精密取待测人脑脊液样品180 μL 于1.5 mL Eppendorf 管中,加入内标溶液20 μL(100 mg·L-1),加入乙腈:6%高氯酸(1∶1,v/v)溶液200 μL,涡旋振荡1 min,静置10 min,13000 r·min-1离心10 min,取上清液20 μL 进样分析。
2.3 专属性考察
取使用万古霉素的患者的人脑脊液样本(见图1A),再取空白脑脊液加入万古霉素及去甲万古霉素的对照品,经“2.2”项下样本前处理,按照“2.1”项下色谱条件进样分析,结果万古霉素与去甲万古霉素分离完全,其中内源性物质及流动相中的杂质对测定无干扰,色谱图见图1B。
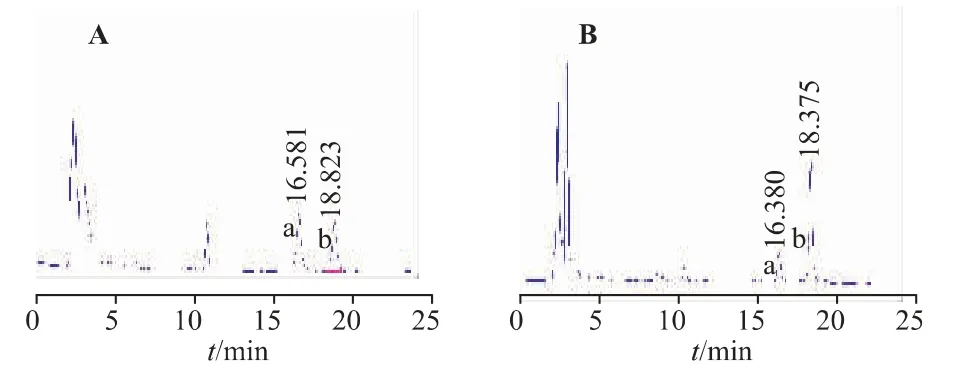
图1 万古霉素脑脊液样本(A)、万古霉素与去甲万古霉素加标脑脊液(B)色谱图
2.4 标准曲线及定量下限
精密量取空白脑脊液900 μL,加入4000 mg·L-1的万古霉素100 μL,配制成400 mg·L-1,依次用空白脑脊液稀释成1.5625、3.125、6.25、12.5、25、50、100、200 mg·L-1的脑脊液标本,同时稀释得低、中、高3种浓度的质控脑脊液标本,使其浓度分别为3.125、25、50 mg·L-1。经“2.2”项下样本预处理,每个浓度平行3 份及空白样本1 份,进样测定标准曲线,以万古霉素与去甲万古霉素峰面积比值为纵坐标,样本浓度(μg·mL-1)为横坐标进行线性回归。结果在1.5625~200 μg·mL-1浓度范围内万古霉素线性方程为:Y=8.41×10-2X+0.174,r=0.9990(n=3)。根据标准曲线,本方法的定量限为1.5625 μg·mL-1。
2.5 基质效应试验[5]
经“2.2”项下样本预处理的空白脑脊液,离心沉淀后用上清液分别配制成含万古霉素浓度为3.125、25、50 mg·L-1基质溶液,每个浓度配制3 份,待进样;另外,用水配制成相同含万古霉素浓度为3.125、25、50 mg·L-1的溶液,每个浓度配制5 份,按“2.1”项下色谱条件进样测定,分别比较3 个浓度的峰面积,空白脑脊液配制供试品比较水配制供试品,结果见表1。
2.6 准确度与精密度试验
取空白脑脊液作为基质,配制万古霉素低、中、高浓度为3.125、25.0、50.0mg·L-1的脑脊液样本,每个浓度平行配制5 份,经“2.2”项下前处理,按“2.1”项下色谱条件进样测定,分别测定低、中、高3 个浓度水平的样本各5 份,记录峰面积。取配制好的万古霉素对照品,依次稀释成为3.125、25.0、50.0mg·L-1对照品,每个浓度平行配制5 份,按“2.1”项下色谱条件进样测定,记录峰面积,两个峰面积比值计算绝对回收率,5 次进样峰面积计算日内精密度(RSD);每日按上述方法操作配制样本,连续3 日,计算日间精密度。结果显示,本方法测定脑脊液中万古霉素的准确度均符合血药浓度检测条件;日内、日间精密度均<6%。见表1。
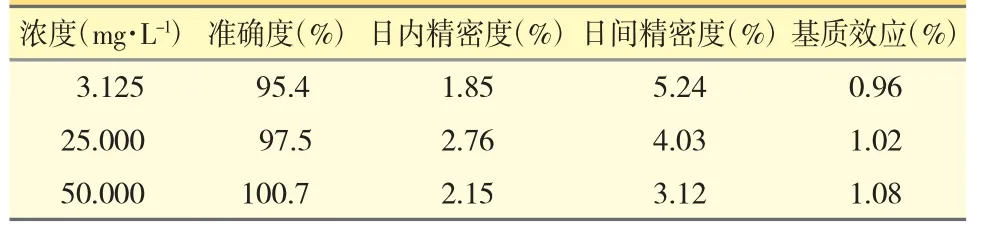
表1 测定脑脊液中万古霉素的准确度、精密度、基质效应(n=5)
2.7 稳定性试验
取低、中、高浓度各5 个平行样品,经“2.2”前处理后将上清液在室温下分别放置4、24、48 h,进样测定,计算变异系数(CV%);将配制好的质控样本置于4℃冰箱分装保存,每隔1 周复测1 次,3 个水平分别测定5 组平行样本,复测4 周,计算CV%。结果显示,去甲万古霉素和万古霉素的样本在上述试验情况下稳定性良好,CV%均<10%。
2.8 临床应用
采用本方法为本院重症颅内感染患者进行脑脊液中万古霉素浓度监测,采样为连续给药4 剂后、用药前0~30 min,采集谷浓度样本;给药结束后1~2 h 采集峰浓度样本。其中测定峰浓度的患者共6例,谷浓度的患者共8 例,结果见表2。

表2 测定患者脑脊液中万古霉素浓度结果
其中3 例患者脑脊液谷浓度低于10 μg·mL-1,4例患者谷浓度在10~20μg·mL-1,只有1 例大于20μg·mL-1,根据《桑福德抗微生物治疗指南》[6]和美国传染病学会[7]推荐:当治疗颅内感染时,万古霉素脑脊液谷浓度目标值范围为10~20μg·mL-1,至少要保持在10μg·mL-1以上,以免发生耐药。根据检测结果,并结合患者实际情况,对药物的用量做了适当调整。血药浓度监测结果说明万古霉素在患者中具有较大个体差异,对其进行脑脊液浓度监测非常重要。
3 讨论
样本处理方法的选择直接影响HPLC 法的分离效果,万古霉素与去甲万古霉素样本处理方法常用的有固相萃取法和直接沉淀法,其中直接沉淀法更为简便、省时。考虑万古霉素和去甲万古霉素性质等各方面的因素,初步选择乙腈、甲醇、6%高氯酸及乙腈:6%高氯酸(1∶1)作为沉淀提取剂、进行前处理优化,结果显示,单从外观方面,乙腈、甲醇、6%高氯酸沉淀反应较快;但使用乙腈、甲醇时回收率较低,6%高氯酸酸性较强,长时间使用致色谱柱柱效降低,缩短寿命;最终选择用乙腈:6%高氯酸(1∶1)做为沉淀提取剂,其净化反应较慢,需静置10 min,充分反应后,离心净化效果最佳,回收率高。
万古霉素和去甲万古霉素的最大吸收波长为220 nm,样本中此吸收波长干扰峰较多,参考有关文献,采用236 nm 作为检测波长[1]。流动相先后采用了水-甲醇、水-乙腈、pH3.2 磷酸二氢钾缓冲液-乙腈进行试验,在3 种流动相中,磷酸二氢钾缓冲液-乙腈分离的色谱峰型较好。又对磷酸二氢钾缓冲液与乙腈作梯度洗脱和等度洗脱的对比,结果显示,梯度洗脱分离度更好,且万古霉素与去甲万古霉素随着色谱柱柱效下降,两个峰分离会明显变差,而采用梯度洗脱色谱柱的寿命会延长,也可节约成本。本实验所建方法准确可靠,简单灵敏,检测限为0.5μg·mL-1,可满足临床脑脊液中万古霉素的药动学研究要求。后续可通过本方法对院内患者进行万古霉素脑脊液浓度测定,并收集病例进行分析,可对万古霉素静脉滴注联合鞘内注射的临床疗效及安全性进行评估研究。
