磁共振对超声阴性而乳腺X 线检出BI-RADS 4 类以上钙化灶的诊断价值分析
2021-03-06朱乃懿姜奕歆柴维敏
朱乃懿,姜奕歆,柴 丽,柴维敏
(上海交通大学医学院附属瑞金医院放射科,上海 200025)
可疑形态钙化灶是乳腺疾病在乳腺X 线摄影(mammography,MG)中常见的征象之一。乳腺影像报告及数据系统 (breast imaging-reporting and data system,BI-RADS) 4 类以上的可疑形态钙化灶可发生在各种良恶性乳腺疾病中,而可疑形态钙化灶可能是无肿块、无临床症状的早期乳腺癌的主要、甚至唯一征象[1-2]。MG 检查对钙化灶十分灵敏,可检出直径≥50 μm 的微小钙化灶[3]。美国放射学会的BIRADS 将MG 影像学表现分为0~6 类,分类越高,病灶为恶性的风险性越高。对于BI-RADS 4 类及以上的可疑形态钙化灶,BI-RADS 指南推荐做X 线引导下立体定位活检或钩针定位切除活检。但由于活检为有创性检查,会给患者带来较大的生理和心理负担。同时,在临床实践中,对于可疑形态的乳腺钙化灶,手术及活检的阳性率很低,多数病灶的病理结果为良性。既往研究显示,可疑乳微钙化灶的活检阳性率为10%~40%[2]。超声(ultrasound,US)检查对于不伴肿块的可疑形态钙化灶的诊断价值有限。
乳腺MRI 检查相较MG 具有较高的软组织分辨率,可进行多层面、多参数及多序列成像。虽不能直接显示钙化灶,但可显示钙化灶对应区域软组织病变的形态、分布、内部结构和血流动力学特征,对于MG 诊断困难的病灶,以往使用US 检查作为MG 诊断的补充,但遇到US 阴性的病变,则MRI 检查可为病灶的检出和定性诊断提供更为丰富的信息,大大提高了恶性病灶的检出率和诊断准确率。因此,本研究旨在分析US 阴性、MG 检出的BI-RADS 4 类以上可疑形态钙化灶的MRI 表现,探讨MRI 及MRI 联合MG 检查对于可疑形态乳腺钙化灶的诊断价值。
资料与方法
一、资料
本研究为回顾性研究,选取2020 年1 月至12 月在本院行乳腺钙化灶立体定位活检或钩针定位活检的126 个可疑形态乳腺钙化灶。患者平均年龄为(52.4±5.4)岁,均行MRI 检查。所有病灶均为MG BI-RADS 4 类以上,US 阴性定义为US 检查时未发现明显病灶或钙化,或US 检查诊断为BI-RADS 3类及以下的病灶。同时排除在行MRI 检查前6 个月内行乳腺穿刺或手术而病灶已经病理检查确诊的患者。
二、检查
MG使用Hologic Selenia Dimensions、Siemens Mammomat Inspiration 6118 全野数字化乳腺机,常规行双侧乳腺头尾位(CC 位)及内外侧斜位(MLO位) 摄片。MRI 的扫描设备是德国Siemens Aera 1.5T 超导型磁共振,采用4 通道乳腺专用相控阵线圈,均为横轴位扫描。患者采取俯卧位,双侧乳腺自然悬垂于乳腺线圈内。扫描范围从腋窝至双侧乳房下界。扫描序列为脂肪抑制T2W[快速反转恢复序列 (turbo inversion recovery magnitude,TIRM)];双b 值DWI (RS-EPI,50、800 s/mm2);T1 加权动态增强扫描(平扫一期+增强四期90 s×4)。
1.TIRM:采用TIRM,TR/TE=5 240/62 ms,层厚4 mm,视野(field of view,FOV)340×340 mm。
2.双b 值扩散加权成像(diffusion-weighted imaging,DWI)参数:TR/TE=9 500/72 ms,层厚4 mm,FOV 384 mm×384 mm,b 值选择50、800 s/mm2;激励次数为1 和3,扫描共计193 s。
3.T1 加权动态增强扫描:TR/TE=4.58 ms/1.89 ms,层厚1.5 mm,FOV 360×360 mm。本研究每个病例共扫描5 个时相(1 期平扫和4 期增强扫描),每个时相扫描时间为90 s,第1 序列进行平扫后,静脉注射对比剂钆喷替酸葡甲胺,流速为2.0 mL/s 的速度进行注射,其后以同样速率注入15 mL 生理盐水(0.9%氯化钠溶液)冲洗管腔内残留的对比剂。
动态增强扫描结束后,将数据传送至Siemens Aera 1.5T 后处理工作站,使用mean curve 软件,选取T1W 平扫和T1W 动态增强5 期图像,选取病灶强化最显著区并避开纤维腺体组织、导管及血管勾画感兴趣区(region of interest,ROI),获得时间信号强度曲线(time-signal intensity curve,TIC)。
可疑形态钙化灶定位活检方式包括乳腺X 线引导下钩针定位切除活检和乳腺X 线引导下真空辅助旋切活检。
三、MG 和MRI 图像分析
所有MG 图像分析均在高分辨率医用显示器上进行。依据美国2013 版MG BI-RADS 分类标准,分析钙化灶的形态、分布情况。所有MRI 图像的数据测量及后处理均在Siemens Aera 1.5T 工作站上完成。依据美国2013 版MRI BI-RADS 分类标准,将病变分为肿块强化和非肿块强化2 类;选取ROI,测量表观扩散系数(apparent diffusion coefficient,ADC)值;选取ROI,分析TIC(分为上升型、平台型、流出型3 型)。参考MG 钙化病变的位置,评价MRI 对应区域的表现。所有钙化灶形态学特点及MRI 强化特点由2 名乳腺影像工作年限10 年以上的影像科医师判定结果,若意见不同则通过讨论达成共识。MRI 呈无强化、点灶性强化、背景实质强化定义为无异常强化,而其余强化方式则为异常强化。
四、统计学处理
采用SPSS 22.0 对数据进行分析处理。对于计数资料,作χ2检验、Fisher 确切概率分析、耶茨连续性修正。计量资料采用t 检验,P<0.05 认为结果有统计学意义。
结 果
一、组织病理学结果
126 个乳腺病灶中,良性钙化灶100 个(79.37%),包括腺病64 个,纤维腺瘤形成19 个,导管上皮普通型增生1 个,导管内乳头状瘤10 个,导管扩张及囊肿形成9 个,硬化性腺病5 个,导管上皮不典型增生1 例,放射瘢痕2 例,其中部分病例为腺病合并纤维腺瘤或导管内乳头状瘤、导管扩张。恶性钙化灶26 个(20.63%),包括导管原位癌(ductal carcinoma in situ,DCIS)23 个,浸润性导管癌3 个。
二、影像学表现
MG 和MRI 检查的BI-RADS 分类均与乳腺钙化灶的良、恶性相关(见表1、2)。在MG 检查中,随着分类级别的提高,病灶的阳性率也逐步提高。BIRADS 4A、4B 类患者中,恶性钙化灶仅占18.49%,而4C 类及以上患者中恶性钙化灶所占比例达57.14%。MRI 检查中BI-RADS 2~3 类,恶性比例为3.08%;BI-RADS 4 类及以上,恶性比例达39.34%。
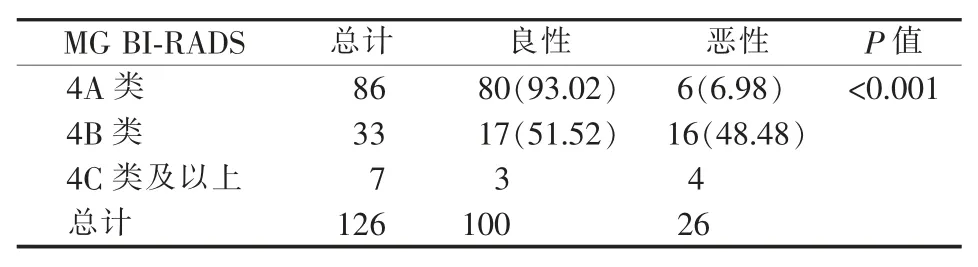
表1 良、恶性钙化灶MG 的BI-RADS 分类比较[n(%)]
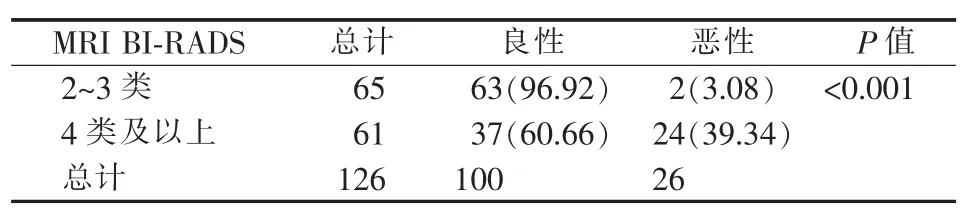
表2 良、恶性钙化灶乳腺MRI 的BI-RADS分类比较[n(%)]
乳腺良、恶性钙化灶的MG 形态表现不同(见表3),良性钙化灶以模糊无定形钙化为主,占68.00%(68/100),其次为粗糙不均质钙化[30.00%(30/100)]及细小多形性钙化[2.00%(2/100)]。恶性钙化灶则以粗糙不均质钙化[53.85%(14/26)]为主,其次为模糊无定形钙化[30.77%(8/26)],随后为细小多形性钙化 [7.69%(2/26)]、线状分支状钙化[7.69%(2/26)]。良、恶性钙化灶均以集群样分布多见(见表3),良性钙化中集群样分布钙化占89.00%(89/100),恶性钙化中集群样分布钙化占65.38%(17/26)。良、恶性钙化灶的伴随征象表现不同(见表3),良性钙化灶在MG 图像上多仅表现为钙化灶95.00%(95/100),仅5.00%(5/100)表现为钙化伴肿块、不对称或结构扭曲,而19.23%(5/26)的恶性钙化灶表现为钙化伴肿块、不对称及结构扭曲。
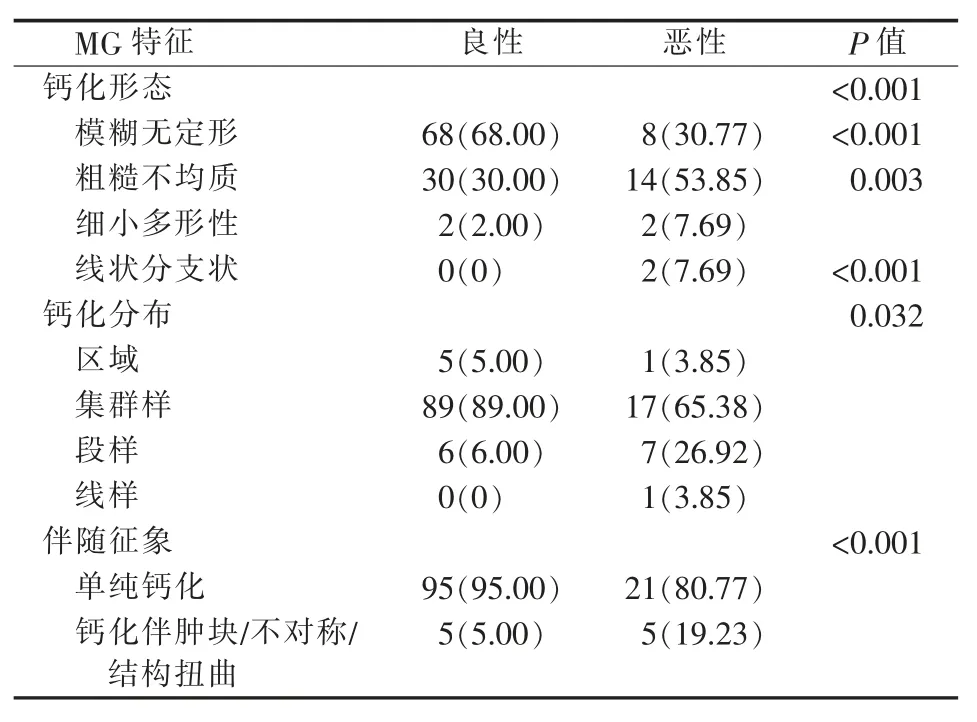
表3 良、恶性钙化性病变的MG 表现比较
乳腺良、恶性钙化灶MRI 表现不同(见表4)。良性钙化灶以无异常强化表现为主,占67.00%(67/100);恶性钙化灶在MRI 图像上均可见异常强化,以肿块强化表现为主,占61.54%(16/26)。良、恶性钙化灶在MRI 图像上强化方式不同(见表4)。良性钙化灶强化的TIC 以上升型为主 (63.6%,21/33),良性钙化灶中TIC 呈上升型的百分比多于恶性钙化灶 (恶性11.54%)(P<0.001);恶性钙化强化的TIC 以流出型为主(73.08%,19/26),恶性钙化灶中TIC 呈流出型的百分比多于良性钙化灶(P<0.001)。
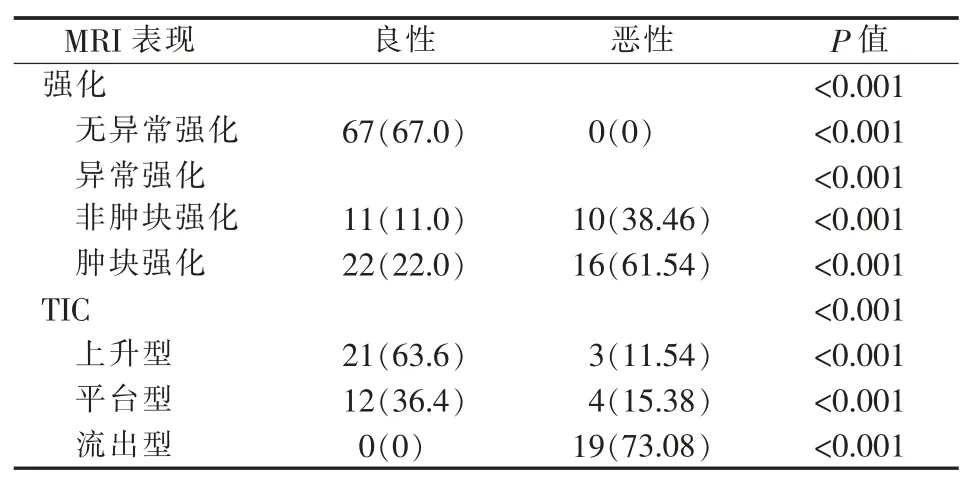
表4 良、恶性钙化灶乳腺MRI 表现的比较[n(%)]
以病理结果为金标准,MG 以≥BI-RADS 4C类、MRI 以≥BI-RADS 4 类评估为恶性,计算MG、MG+MRI 检查对于乳腺钙化病灶良恶性诊断的灵敏度、特异度、准确率、阳性预测值、阴性预测值(见表5)。对于US 阴性的乳腺良、恶性钙化灶,乳腺MG 联合MRI 检查的灵敏度优于MG(P<0.001),乳腺MG 联合MRI 检查诊断恶性病灶的准确率优于MG(P<0.001),乳腺MG 联合MRI 检查的阴性预测值优于MG(P<0.001)。
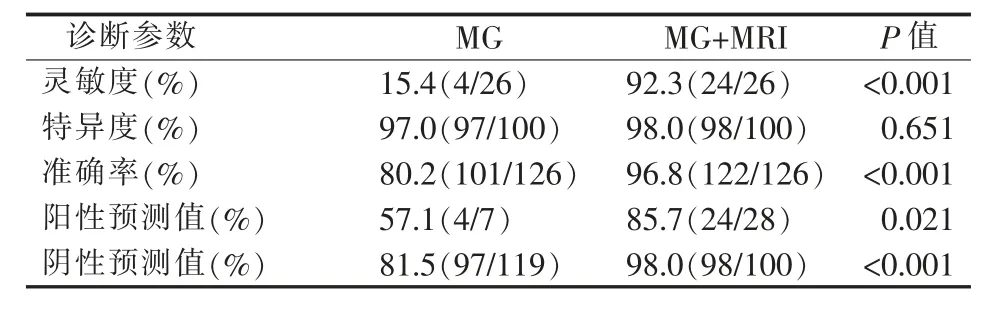
表5 2 种影像学方法诊断价值比较[n(%)]
讨 论
乳腺良、恶性病变均可发生钙化,根据美国放射学会BI-RADS 标准,乳腺钙化灶分为典型良性钙化、可疑形态钙化。MG 对钙化较敏感,可显示钙化灶的形态、分布等细节信息,因此MG 是评估乳腺钙化灶最佳的检查方法。US 无电离辐射、耐受性良好,无需静脉注射对比剂,方便引导穿刺活检[4]。US 对于伴有肿块的乳腺钙化灶诊断较准确,对于不伴肿块的单纯乳腺钙化灶的诊断价值有限[5]。MRI 检查软组织分辨率较高,虽然不能直接显示钙化灶,但可以通过显示钙化灶所在区域血流动力学特征,提供良、恶性钙化灶周围微血管生成的信息。既往研究显示,MG 检出的可疑乳腺恶性钙化的阳性预测值为23.0%~32.6%,而US 的阳性预测值为8.8%~8.9%[5-7],MRI 检查对于可疑形态乳腺钙化灶的诊断价值,尤其是US 阴性的可疑形态乳腺钙化灶,既往研究较少。
一、MG 上乳腺良恶性钙化的表现差异及MG的诊断效能
由于本研究入组标准为US 阴性的可疑形态钙化,即US 未发现病灶,或仅为BI-RADS 3 类及以下病灶,故本研究入组病例的典型恶性征象较少,钙化灶集中于BI-RADS 4A、4B 类 (119/126 例),BI-RADS 4C 类的钙化灶比较少(7/126 例)。
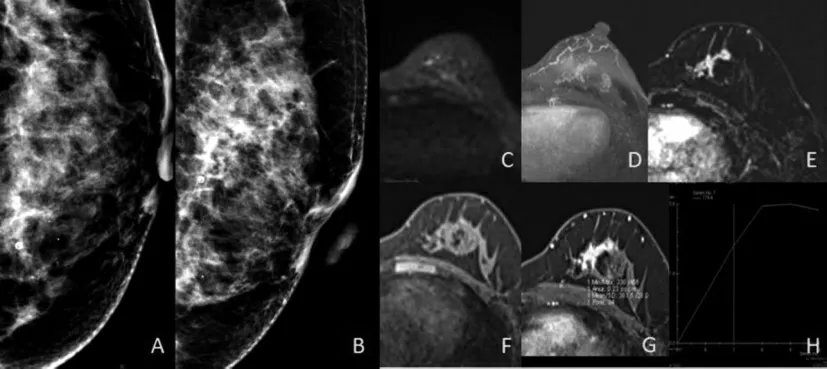
图1 左乳高级别导管原位癌伴少量经典型小叶原位癌及粉刺样坏死
本研究结果显示,可疑形态乳腺钙化灶活检的阳性率仅为20.6%,与既往的研究报道[2]结果(10%~40%)相仿。可见,在活检前明确病灶性质以减少不必要的穿刺活检十分重要。本研究中,乳腺良、恶性钙化灶的形态差异有统计学意义(P<0.001),良性钙化灶以模糊无定形钙化为主,恶性钙化灶以粗糙不均质钙化为主。本研究中,模糊无定形钙化灶的恶性率为10.5%(8/76)。Uematsu 等[8]的研究结果显示,25%的模糊无定形钙化灶结果为恶性。本研究8 例恶性模糊无定形钙化灶行MRI 检查,MRI检出了8 例。因此,对于模糊无定形钙化灶,其恶性概率不超过10%,在MRI 同时表现为阴性的情况下,可考虑暂不予活检、短期随访。本研究显示,粗糙不均质钙化的表现对于良、恶性乳腺病灶的鉴别无意义(P=0.073)。有研究[2]报道,这种形态的钙化可出现在乳腺恶性病变中,亦可出现在纤维腺瘤以及外伤、手术、放疗造成缺血坏死等良性乳腺病变中。本研究的14 例粗糙不均质恶性钙化灶中,12 例经MRI 检查诊断为恶性。因此,对于粗糙不均质钙化灶的诊断更依赖于MRI 检查。细小多形性及线状分支状钙化多出现在恶性病灶中。本研究结果显示,线状分支状钙化灶在乳腺恶性病灶中的百分比高于良性病灶(P<0.001),而细小多形性钙化灶在良性及恶性组中均为2 例,这可能由于本研究入组病例数量少有关。Uematsu 等[8]的研究结果显示,乳腺细小多形性钙化灶中64%为恶性,线状分支状钙化灶中92%为恶性。本研究中,50.00%(2/4)的乳腺细小多形性钙化灶和100%(2/2) 的线状分支状钙化灶为恶性,前者恶性比例略低于文献,后者数据与文献数据大致相仿。对这2 种形态的乳腺钙化病灶,应积极行活检。Uematsu 等[8]的研究结果显示,乳腺钙化灶中,28%的集群样分布钙化灶、40%的段样分布钙化灶、67%的线样分布钙化灶为恶性。但本研究结果显示,良、恶性乳腺钙化灶的分布方式差异无统计学意义(P=0.002),均以集群样钙化分布为主,这可能与本研究入组标准为US 阴性钙化灶有关,本研究入组病例大多为MG BI-RADS 4A-4B 类的钙化,这也是本研究的局限性之一。本研究中95.00%的良性乳腺钙化灶表现为单纯钙化,19.23%的恶性钙化病灶则有伴随征象 (P<0.001),如局部可伴结构扭曲、不对称及肿块。但这些病灶在US 检查中尚未发现肿块性病变,其病理基础可能是早期恶性肿瘤周围正常组织的反应性增生,使脂肪和正常乳腺实质间的界面发生扭曲、紊乱,为恶性病变早期征象之一[9]。
二、MRI 图像上良恶性乳腺钙化灶的表现差异及诊断效能
良性乳腺钙化灶的MRI 表现一般为血供不丰富,无异常强化。本研究中BI-RADS 4 类及以上的US 阴性的可疑形态乳腺钙化灶,在MRI 图像上多表现为无异常强化(53.17%,67/126),点灶性强化、背景实质强化亦归入无异常强化。文献报道,良性乳腺钙化灶在DCE-MRI 上多表现为无异常强化或轻度异常强化,以上升型多见;而恶性钙化灶在DCE-MRI 上表现为钙化灶对应区域的早期强化,以平台型和流出型曲线多见[10-13]。本研究中恶性乳腺钙化灶38.46%(10/26) 表现为非肿块强化,64.54%(16/26)表现为肿块强化。Tozaki 等[14]对61 例MRI 表现为非肿块强化的病灶进行研究,结果发现成簇小环样强化在恶性病灶中的百分比为63%,而在良性病灶中的百分比仅为4%。因此,成簇小环状强化是鉴别良、恶性钙化灶的重要征象。
三、MG 联合MRI 的诊断价值
本研究显示,对于US 阴性的可疑形态乳腺钙化灶,MG 联合MRI 的诊断灵敏度高于MG(92.3%比15.4%)。既往研究认为,MRI 检查对于乳腺癌的灵敏度高于MG,无论病灶是否含有钙化[15]。本研究中乳腺导管内原位癌占恶性钙化灶的88.46%(23/26),Kuhl 等[13]、Yu 等[16]研究发现,MRI 对于乳腺导管内原位癌的诊断灵敏度明显高于MG。本研究中两者的诊断特异度相当,MG 为97.4%,MG 联合MRI 为98.3%。而文献也认为,MRI 的诊断特异度结果变化较大[8,23]。MG 联合MRI 鉴别良、恶性乳腺钙化灶的阳性预测值、阴性预测值均高于MG,差异有统计学意义。
然而,本研究还有以下不足之处。本研究的入组标准为US 阴性的病例,此类病例的MG 及MRI检查结果大多为BI-RADS 4A、4B 类,较少有BIRADS 4C 类,因此纳入的阳性病例数较少,客观造成了统计分析上的偏倚。
本研究结果表明,①对于US 阴性的可疑形态乳腺钙化灶,MG 图像上表现为模糊无定形钙化,而MRI 图像上无异常强化的病灶,良性可能性较大;MG 图像上表现为细小多形性、分支线状钙化,而MRI 图像上肿块强化、TIC 呈流出型的病灶,恶性可能性大。②MG 联合MRI 检查对于US 阴性的可疑形态乳腺钙化灶具有更高的诊断灵敏度、准确率和阴性预测值,可以提高诊断效能,以减少不必要的穿刺活检。
