肾移植前后丙型肝炎病毒感染的管理
2021-03-01黄霞吉英杰程勇前南方医科大学第二临床医学院广东广州510515中国人民解放军总医院第五医学中心老年医学科北京100039
黄霞,吉英杰,程勇前 (1.南方医科大学第二临床医学院, 广东 广州 510515;.中国人民解放军总医院第五医学中心老年医学科,北京 100039)
丙型肝炎病毒(hepatitis C virus, HCV)除导致肝功能损伤外,约43%~85%的慢性丙型肝炎(chronic hepatitis C,CHC)患者可伴有多种肝外表现(extrahepatic manifestations,EHM)[1-4],包括多种 HCV 感染相关肾脏疾病[5-6]。Ferri 等[2]研究表明,CHC 患者出现尿蛋白的风险增高51%,慢性肾脏病(chronic kidney disease,CKD)发生率增高43%。Park 等[7]通过回顾性队列纳入美国Truven Health MarketScan 数据库(2008 — 2015 年)的56 448 例HCV 感染者和倾向评分(1:3)匹配的169 344 例非HCV 感染患者进行多变量Cox 回归模型分析,结果显示,HCV 感染患者发生CKD 的风险比增加27%(危险比为1.27;95%置信区间为1.18 ~ 1.37)。
CKD 患者如进展至终末肾脏疾病(end stage renal disease, ESRD)则不可避免地接受规律性血液透析或肾移植治疗。然而,ESRD 患者也可能因在治疗过程中感染HCV 导致肾损伤进一步加重。相比透析治疗,肾移植治疗费用更低、生存质量更高和预期寿命更长,是ESRD 患者首选治疗方式[8]。
直接抗病毒治疗药物(direct antiviral agents,DAA)的出现,使干扰素时代无法进行抗病毒治疗的CKD 合并HCV 感染者及肾移植术后患者的抗病毒治疗成为可能[9],可在短期内(通常为12 周)获得95%以上持续病毒学应答(sustained virologic response,SVR)。根据慢性肾脏病:改善全球预后工 作 组 (Kidney disease: Improving Global Outcome,KDIGO)发布的最新2018 《慢性肾脏病中丙型肝炎预防、诊断、评价和治疗指南》[10-11],所有HCV 感染患者,均应进行抗病毒治疗。因此,肾移植前后HCV 感染的管理尤为重要,本文就此方面进展进行介绍。
1 HCV 感染者肾移植前管理
对拟行肾移植的合并HCV 感染患者应对肝、肾功能进行全面评估以确定抗病毒治疗时机以及抗病毒治疗药物的选择。
1.1 肝功能评估与抗病毒治疗时机:目前常用肝功能评估方法是根据肝功能CHILD PUGH 分级、内镜检查、无创放射学评估或直接门静脉压力测量等监测门静脉高压[12]〔门静脉压力梯度<10 mmHg(1 mmHg =0.133 kPa)提示肝硬化处于代偿期〕。当肝脏疾病的病因不明确或与非侵入性检测结果不一致时,也可考虑进行肝活检来评估是否存在肝硬化[10,13]。
对于肝脏疾病尚未进展至肝硬化阶段,或处于肝硬化代偿期且门静脉压力<10 mmHg 的患者,应选择单纯肾移植治疗[10]。对于可择期进行肾移植的患者,应在肾移植前首先进行抗病毒治疗。有研究表明,HCV 治愈可以阻止肝脏疾病发展,获得SVR后肝脏炎症显著消退,肝纤维化进程减慢[12],同时降低肝硬化、肝衰竭、肝癌等相关并发症的发生率[13]。D’Ambrosio 等[14]对 38 例肝硬化达到 SVR的患者进行治疗前后的肝活检,结果提示肝硬化及纤维化减轻较常见,推测HCV 消除后门脉炎症及窦周纤维化可减轻。
关于HCV 感染是否导致肾移植受者生存率及移植肾存活率明显下降存在争议[14-17]。Okino 等[16]对1974 年— 2013 年间在同一医院接受了同种异体肾移植的187 例HCV 感染成年患者及145 例非HCV 感染肾移植患者的远期生存率及移植肾的存活率的统计分析,发现HCV 感染组肾移植患者生存率及移植肾的存活率显著降低,其中 HCV-Ag 阳性是影响肾移植术后生存和移植物功能最重要的独立危险因素。葡萄牙单中心回顾性研究从1985 年1 月— 2013 年12 月的1 239 例肾移植患者,肾移植患者感染HCV 的患病率为2.7%(n =34),对照组(n =80)[17]。通过平均11 年的随访,发现在 1、5 和10 年后,HCV 阳性患者的移植物的存活率分别为94.1%、78.1%和66.9%;HCV 阴性患者的移植物存活率分别为94.9%、89.1%和80.4%。各组间移植物存活率并无显著差异 (P <0.154 和P <0.159)。研究者认为HCV 感染并非导致移植物失活的重要危险因素,HCV 感染对肾移植后移植物存活的长期影响并不显著。
尽管存在上述争议,由于目前DAAs 抗病毒治疗的高SVR,多数学者认为,对于可择期肾移植的合并HCV 感染患者可选择在抗病毒治疗获得SVR 后再进行肾移植治疗。但是,当处于肝硬化失代偿期或门静脉压力≥10 mmHg 时,无论是否已经获得SVR 均应首先考虑肝肾联合移植[10,18],未达SVR 的患者建议术后再给予抗病毒治疗[10]。
同时,由于DAAs 抗病毒治疗对HCV 的高清除率,肾移植前后DAAs 治疗的最佳时机也应以捐肾者类型(尸体捐肾或活体捐肾)、等待肾源时间、肾脏移植中心特定政策等为基础,结合患者实际情况进行选择。对于短期内可获得供体肾源的患者,可将针对HCV 的抗病毒治疗延迟至器官移植术后。如等待肾移植时间≥24 周、预期寿命评估先进行DAAs 治疗获益更大时、患者主观因素要求等情况下均应考虑先接受DAAs 治疗[10-11]
1.2 DAAs 药物的选择:尽管DAAs 药物使大多数既往无法进行抗病毒治疗的CKD 患者获得了治疗机会,并达到很高的SVR。但由于DAAs 主要经肝脏或肾脏进行代谢(表1),对于合并HCV 感染的CKD 患者,尤其是存在肝硬化的CKD 患者仍需全面评估肝、肾功能谨慎选择。避免药物相关的肝功能失代偿或肾移植等待期AKI 的发生。
1.2.1 根据肝功能选择DAAs 治疗方案:经肝功能评估未达到肝硬化的患者,可根据HCV 基因型进行选择任何已经获批上市的DAAs 治疗方案。由于NS3/4A 蛋白酶抑制剂主要经肝脏代谢,具有潜在肝毒性,对肝功能Child-Pugh A 级患者,应进行密切临床或实验室监测,否则不推荐使用含NS3/4A蛋白酶抑制剂的方案[19],伴有肝功能失代偿或既往曾有肝功能失代偿病史或肝功能达Child-Pugh B或C 的患者不推荐使用含NS3/4A 蛋白酶抑制剂的DAAs。当肝功能达到Child-Pugh C 时,需综合评估患者预期寿命及进行肝肾联合移植的可能性,选择是否进行DAAs 治疗。
1.2.2 根据肾功能选择DAAs 治疗方案:CKDG1-G3b 期(eGFR ≥ 30 ml/min·1.73 m2):患者可根据HCV 基因型进行选择任何已经获批上市的DAAs 治疗 方 案。CKD G4 期、 G5 期、CKD G5D(eGFR <30 ml/min·1.73 m2),患者肾功能较差,由于DAAs经肾脏清除率发生变化,临床医生应根据DAAs 代谢途径、HCV 基因型、药物-药物相互作用(drugdrug interaction, DDI)及国家上市药物政策等选择不含 RBV 的 DAAs 方案。
前期大部分研究包括 2018 KDIGO 指南[10,20]认为,索磷布韦80%经肾脏进行消除,仅可用于CKD G1-G3b(GFR > 30 ml/min·1.73 m2) 的 患 者。 因此,对于等待肾移植的患者,如果既往曾有肝功能失代偿病史或肝功能达Child-Pugh B 或C,则既不推荐应用主要经肾脏代谢的含索磷布韦的DAAs,又不推荐含NS3/4A 蛋白酶抑制剂的方案,这部分患者的抗病毒治疗成为了DAAs 时代抗病毒治疗的盲点。
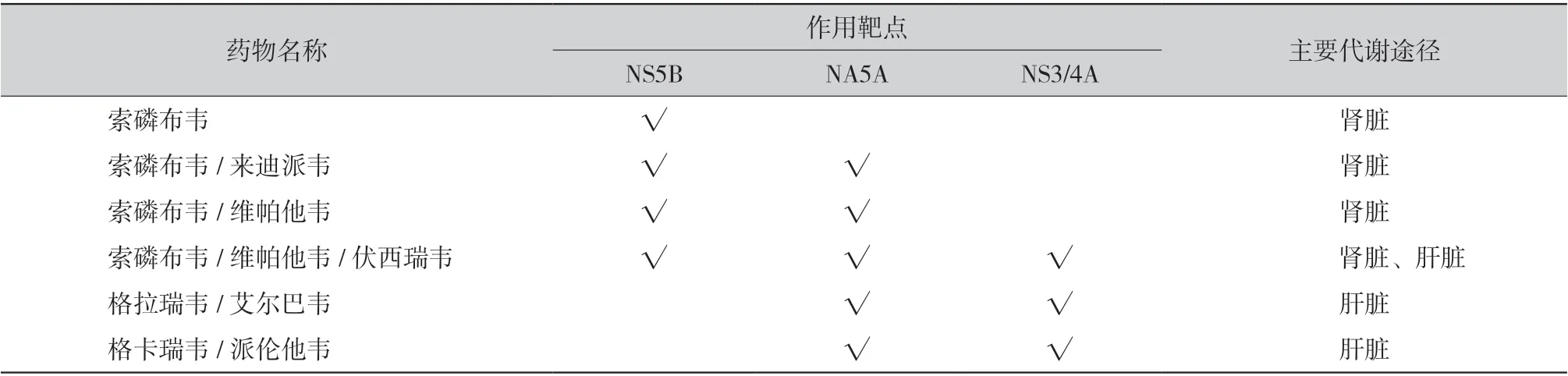
表1 目前DAAs 药物作用靶点及主要代谢途径
针对这一问题,最新研究表明,虽然在ESRD患者肾脏中可检测出浓度较高的索磷布韦代谢产物GS-331007,但是有临床回顾分析发现含SOF的DAAs 并非导致急性肾损伤(acute kidney injury,AKI)的独立危险因素。Borgia 等[21]及 Aude 等[22]研究表明,对于正在透析的ESRD 患者,使用索磷布韦/维拉帕韦治疗12 周也是安全有效的。Telep等[23]通 过 对 比 分 析 2006 年 1 月 1 日 到 2015 年9 月30 日HCV 感染患者发生急性肾损伤风险及使用含索磷布韦的DAAs 治疗方案后发生AKI 风险(n =741998,对照组n =311779),结果表明,在控制人口统计学特征、基线水平、药物使用情况后,HCV 感染患者发生AKI 风险比对照组增高4.3 倍,但是使用含有索磷布韦的DAAs 方案并不是发生AKI 的独立危险因素。基于上述研究结果,2020 年7 月在索磷布韦/来迪派韦、索磷布韦/维帕他韦药品说明书中对肾功能不全患者的用法用量已更新为“对于任何程度的肾功能损害患者(包括需要透析的患者),建议无需调整剂量。”
1.2.3 共病患者的合并用药选择:合并HCV 感染的CKD 患者,常因治疗肾脏疾病,以及存在糖尿病、高血压、高血脂等共病而服用多种药物,王琴等[24]通过分析2013 年至2015 年中国城镇医疗保险慢性丙型肝炎患者合并其他疾病及合并其他疾病用药情况,发现我国排名前三位的分别是:糖尿病(约占28.9%)、高血压(约占28.2%),冠心病(约占21.9%)。因此在应用DAAs 进行抗病毒治疗时还需关注药物间相互作用。
为避免因DDI 合并用药不良反应造成严重后果,临床医生在使用DAAs 方案前应详细询问患者用药史并查询利物浦大学的肝炎药物相互作用 网 站(http://www.hep-druginteractions.org), 合 理选择[10,24]。
2 肾移植术后HCV 感染管理
2.1 移植后出现HCV RNA 阳性情况:由于HCV感染不产生保护性免疫,因此,移植术后患者应定期监测血清抗-HCV,或有条件情况下应监测HCV RNA,以及时发现HCV 感染状况。HCV 感染的肾移植受者应至少每6 个月检测一次蛋白尿[10]。对HCV RNA 阳性患者接受肾移植术后,应定期筛查蛋白尿及血尿[10]。器官移植术后再次检测出HCV RNA 阳性有多种可能,包括HCV 感染患者术前未进行抗病毒治疗或未达到SVR、接受了HCV RNA阳性器官移植[25]、甚至是器官移植术后再次肾功能衰竭而行透析治疗、输血治疗过程中新发HCV 感染等。对于术前感染HCV 但未治疗患者、经治疗后未达SVR 患者、紧急接受了HCV RNA 阳性器官患者及再度新发HCV 感染患者均应在移植术后及时开始DAAs 治疗,以尽快达到 SVR[26]。移植前达 SVR 的HCV 感染患者在移植术后3 个月或出现肝功能损害时,应进行 HCV RNA 检测[10]。
2.2 移植术后抗病毒方案选择:肾移植或肝肾联合移植术后DAAs 治疗方案的选择,原则上与移植术前相同,同样需要综合评估肝肾功能。需要注意的是,移植术后患者需服用抗排斥药物,因此,除移植术前的共病药物外,还需充分评估DAAs 药物与抗排斥药物之间的DDI,并密切监测血药浓度,综合分析抗排斥药物血药浓度变化的原因,及时调整药物剂量。
HCV 感染患者接受肾移植或肝肾联合移植术后需常规使用免疫抑制剂,虽然2018 KDIGO 指南推荐常规诱导和维持免疫抑制剂均可用于HCV 感染的肾移植患者,但是由于大部分免疫抑制剂经细胞色素P450 在肝脏进行代谢,同时部分DAAs 也经肝脏进行代谢,因此存在底物竞争,这将影响血药浓度。另外临床医生还需结合患者术后其他基础疾病用药情况再选择采取何种DAAs 治疗方案,同样可通过查询利物浦大学的肝炎药物相互作用网站(http://www.hep-druginteractions.org)了解最新合理用药配伍[10]。(表 2,表 3)
3 肾源管理
3.1 HCV 感染肾供体的利用 :截至2013 年我国CKD 患者约为 1.195 亿[27],总体患病率为 10.8%,肾源供应明显缺乏,因此,提高肾移植成功率及肾脏长期存活率尤为重要。并且,如果剔除HCV 感染的供体肾,将造成高达4.2%的抗-HCV 阳性的肾脏丢失[28]。
HCV 感染肾供体可扩大肾脏供体库,让更多患者获得肾移植机会。Kling 等[29]通过对9 290 例同时检测了抗HCV 及 HCV RNA 的器官捐献者进行回顾性研究,发现接受抗-HCV 阴性、HCV RNA 阴性肾源与抗-HCV 阳性、HCV RNA 阴性肾源的速率分别为(81.2%比73.2%,P =0.03),应用倾向评分匹配模型研究发现,若以相同的速率采用抗-HCV阳性、HCV RNA 阴性捐献者的肾源,将增加48 例肾源。

表2 移植术后常用免疫抑制剂
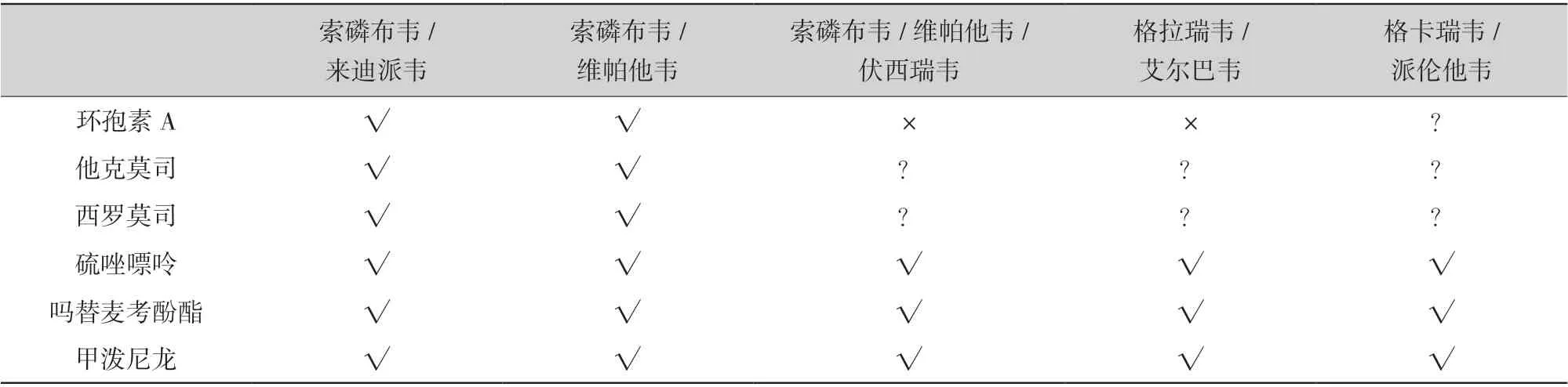
表3 移植术后常用免疫抑制剂与DAAs 的配伍选择
3.2 如何分配HCV 感染肾供体的器官:2018 KDIGO指南推荐所有供体肾源均应进行抗-HCV 检测,有条件时应进行HCV RNA 检测,以筛查HCV 感染[11]。同时应根据HCV 基因型进行器官的匹配[30]。一般而言,HCV RNA 阴性供体的肾脏可以捐献给抗-HCV 阴性患者。HCV RNA 阳性供体的肾脏定向分配给HCV RNA 阳性患者[30-31]。将抗-HCV 阳性供体肾定向分配给抗-HCV 阳性患者,既可避免这类供体传播HCV 的风险,也有助于扩大肾脏供体库。将抗-HCV 阳性供体肾脏移植给抗-HCV 阴性肾脏受者方面的临床数据较少,应慎重考虑。Joseph 等[32]回顾性分析在 2000 年到2012 年间1 679 例接受尸体供肾的抗-HCV 阳性受者,发现接受抗-HCV 阳性供体的患者等待时间(318 d) 比接受抗-HCV 阴性供体的等待时间(613 d) 更短;患者等待肾移植时间越短,则越有助于改善尸体移植物术后的存活率。
3.3 HCV 感染的潜在活体器官供体患者的管理:HCV 感染的潜在器官供体,应积极进行抗病毒治疗,并定期检测肝纤维化程度,确定DAAs 治疗方案,在抗病毒治疗期间及治疗后均应监测肾功能及有无出现蛋白尿[2,10]。当潜在器官供体HCV 感染患者达到SVR 后可进行正常活体器官捐献。
总之,随着肾脏移植技术及DAAs 药物的进展,为合并HCV 感染的ESRD 患者带来了更多治愈的希望,但在此类患者的治疗仍需谨慎、全面地评估,包括肝肾功能、潜在药物间相互作用、肾源种类及可获得时间等多种因素。尤其对于合并HCV 感染后肝硬化的ESRD 患者DAAs 药物选择尚需进一步的临床研究积累。
