复方黄连灌肠液总生物碱含量测定研究
2021-02-27倪晓霞刘晓玲杨育儒王庆芬
倪晓霞,刘晓玲,杨育儒,王庆芬
0 引 言
复方黄连灌肠液是我院消化内科协定处方制成的复方中药灌肠液,临床上用于治疗溃疡性结肠炎,效果显著。组方由黄连、白头翁、黄芪、甘草、山药等13味中药组成,方中君药黄连、白头翁及其他多味中药均含有生物碱类物质。现代药理学研究表明,生物碱类物质具有多种生物活性[1-4],是重要有效成分,且生物碱含量与其作用功效之间存在正相关的量效关系。目前,总生物碱含量测定常用酸性染料比色法[5-6]与紫外分光光度法,但酸性染料比色法,操作繁琐,干扰因素多,重现性与结果准确性有待考量[7]。复方黄连灌肠液中总生物碱测定方法未见报道,为加强制剂质量控制,确保临床用药安全,本文参考有关文献[5-11],建立柱色谱-紫外可见分光光度法测定复方黄连灌肠液中总生物碱含量,现报道如下。
1 仪器与试药
紫外可见分光光度计(UV-2550,岛津-苏州),电子分析天平(AUW120D,岛津-日本),华美冷柜(SY-176,杭州华美电冰箱厂),数控超声波清洗器(KQ-250DB型,昆山市超声仪器有限公司)。
盐酸小糪碱对照品(贵州迪大生物科技有限责任公司,批号:633-65-8);盐酸、甲醇、无水乙醇、乙腈、95%乙醇等均购自西陇化工股份有限公司,试剂均为分析纯;水为纯化水;复方黄连灌肠液(本院自制,批号:20190828、20190829、20190830)。
2 方法与结果
2.1 对照品溶液的配制精密称取盐酸小糪碱对照品0.0101 g,置于25 mL量瓶中,加适量盐酸-甲醇(1∶100)溶液溶解并稀释至刻度,摇匀,即得0.404 mg/mL的对照品储备液。精密量取对照品储备液5.0 mL,置于25 mL量瓶中,加0.05 mol/L硫酸溶液溶解并稀释至刻度,即得80.8 μg/mL的盐酸小糪碱对照品溶液。
2.2 提取方法考察
2.2.1 直接提取法精密称取复方黄连灌肠液5.0 mL(批号:20190828、20190829、20190830),每批次平行3份,置于50 mL量瓶中,加盐酸-甲醇(1∶100)溶液定容,摇匀,静置1.0 h,过滤,精密量取上述滤液5.0 mL,置中性氧化铝柱上,用0.05 mol/L硫酸溶液洗脱并定容至25 mL,摇匀,即得直接提取法供试液,精密量取供试液3.0 mL于25 mL量瓶中,用0.05 mol/L硫酸溶液稀释至刻度,摇匀,以0.05 mol/L硫酸溶液为参比,于345 nm测定吸光度,见表1。
2.2.2 超声提取法精密称取复方黄连灌肠液5.0 mL(批号:20190828、20190829、20190830),每批次平行3份,置于100 mL烧杯中,加盐酸-甲醇(1∶100)溶液40 mL,超声1 h(超声功率250 W),过滤,滤液转移至50 mL量瓶中,用盐酸-甲醇(1∶100)溶液定容,精密量取上述滤液5.0 mL,置中性氧化铝柱上,用0.05 mol/L硫酸溶液洗脱并定容至25 mL,摇匀,即得超声提取法供试液,供试液按“2.2.1”项下方法测定吸光度,见表1。
2.2.3 水浴加热回流提取法精密称取复方黄连灌肠液5.0 mL(批号:20190828、20190829、20190830),每批次平行3份,置于250 mL圆底烧瓶中,加盐酸-甲醇(1∶100)溶液40 mL,水浴加热回流1 h,冷却至室温,过滤,滤液用盐酸-甲醇(1∶100)溶液定容至50 mL,精密量取上述滤液5 mL,置中性氧化铝柱上,用0.05 mol/L硫酸溶液洗脱并定容至25 mL,摇匀,即得水浴加热提取法供试液,供试液按“2.2.1”项下方法测定吸光度,见表1。
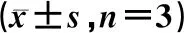
表1 复方黄连灌肠液总生物碱提取方法考察结果
结果表明,3批复方黄连灌肠液的供试液,超声提取法与水浴加热回流提取法的吸光度值明显高于直接提取法,且与超声提取法比较,水浴加热回流提取法供试液的吸光度差异具有统计学意义(P<0.05)。综合考虑选择水浴加热回流提取法作为供试液总生物碱的提取方法。
2.3 提取方法优化
2.3.1 提取溶剂考察精密称取复方黄连灌肠液5.0 mL(批号:20190828),置于250 mL圆底烧瓶中,分别加入1%盐酸溶液、乙腈-1%乙酸溶液(80∶20)、65%乙醇溶液、85%乙醇溶液及盐酸-甲醇(1∶100)溶液40 mL,编号1至5组,每组平行3份,水浴加热回流1 h,冷却至室温,过滤,滤液用相应溶剂容至50 mL,分别精密量取上述滤液5 mL,置中性氧化铝柱上,用0.05 mol/L硫酸溶液洗脱并定容至25 mL,摇匀,即得各组供试液,供试液按“2.2.1”项下方法测定吸光度,平行测定3次,以平均吸光度为纵轴做图,见图1a。图谱提示,第1组、第5组供试液的吸光度大于其他溶剂提取组,且第5组(盐酸-甲醇(1∶100)溶液)显著高于第1组。
2.3.2 提取时间考察精密称取复方黄连灌肠液5.0 mL(批号:20190828),置于250 mL圆底烧瓶中,分别加入盐酸-甲醇(1∶100)溶液40 mL,分别水浴加热回流0.5、1.0、1.5、2.0、2.5 h,每组平行3份,冷却至室温,过滤,滤液用盐酸-甲醇(1∶100)溶液定容至50 mL,分别精密量取上述滤液5 mL,置中性氧化铝柱上,用0.05 mol/L硫酸溶液洗脱并定容至25 mL,摇匀,即得各组供试液,供试液按“2.2.1”项下方法测定吸光度,平行测定3次,以平均吸光度为纵轴做图,见图1b。图谱提示,提取时间为1.5 h时,供试液吸光度值最大。
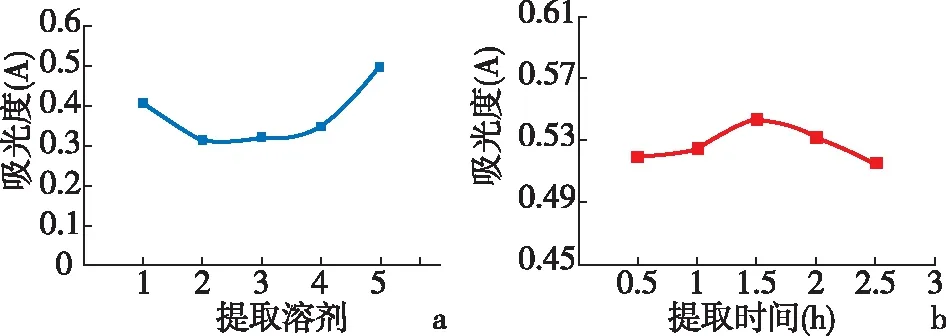
1:1%盐酸溶液;2:乙腈-1%乙酸溶液(80∶20);3:65%乙醇溶液;4:85%乙醇溶液;5:盐酸-甲醇(1∶100)溶液
2.4 供试品溶液制备方法结合上述实验结果,综合考虑实验过程的高效性与经济效益,最终确定供试品溶液的制备方法:精密称取复方黄连灌肠液5.0 mL,置于250 mL圆底烧瓶中,加盐酸-甲醇(1∶100)溶液40 mL,水浴加热回流1.5 h,冷却至室温,过滤,滤液用盐酸-甲醇(1∶100)溶液定容至50 mL,精密量取上述滤液5 mL,置中性氧化铝柱上,用0.05 mol/L硫酸溶液洗脱并定容至25 mL,摇匀,即得。
2.5 含量测定方法建立与方法学验证
2.5.1 最佳吸收波长选择分别精密量取对照品溶液3.0 mL、供试品溶液5.0 mL(批号:20190828),置于25 mL量瓶中,用0.05 mol/L硫酸溶液溶解并稀释至刻度,摇匀,以0.05 mol/L硫酸溶液为空白,于200~600 nm范围内扫描,见图2。图示盐酸小糪碱对照品溶液在345 nm处有吸收峰;而供试品溶液的吸收峰略微红移在335 nm处,综合考虑,最后确定以345 nm为测定波长。
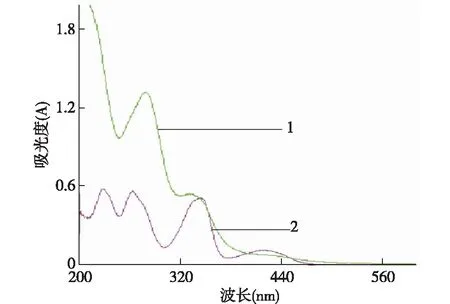
1:供试品溶液;2:盐酸小糪碱对照品溶液图2 复方黄连灌肠液紫外吸收光谱图
2.5.2 线性与回归方程分别精密量取盐酸小糪碱对照溶液0.5、1.0、2.0、3.0、4.0、5.0、6.0 mL,置于25 mL量瓶中,用0.05 mol/L硫酸溶液定容至刻度,制备系列浓度对照品溶液;以0.05 mol/L硫酸溶液为参比溶液,于345 nm处波长处测定吸光度,以浓度(μg/mL)为横坐标、吸光度(A)为纵坐标绘制标准曲线。计算得回归方程为:Y=0.17902X+0.0071(r=0.999 98),表明盐酸小糪碱对照品浓度在1.616~19.392 μg/mL范围内与吸光度之间呈现良好的线性关系。
2.5.3 精密度试验精密称取盐酸小糪碱对照品溶液3.0 mL,置于25 mL量瓶中,平行6份,用0.05 mol/L硫酸溶液定容至刻度,并以0.05 mol/L硫酸溶液为参比,于345 nm处测定吸光度,以吸光度计算相对标准差(RSD),结果RSD为0.364%(n=6),表明精密度良好,见表2。
2.5.4 重复性试验取同一批复方黄连灌肠液(批号:20190828),按“2.4”项下方法制备供试品溶液6份,分别精密称取供试品溶液3.0 mL,置于25 mL量瓶中,用0.05 mol/L硫酸溶液定容,并以0.05 mol/L硫酸溶液为参比,于345 nm处测定吸光度,以吸光度计算RSD%,结果RSD为0.389%(n=6),表明供试品重复性良好,见表2。
2.5.5 稳定性试验精密量取供试品溶液(批号:20190828)3.0 mL,置于25 mL量瓶中,按“2.5.4”项下方法测定,每隔10 min测定1次,以吸光度计算RSD为1.044%(n=6),供试品溶液在60 min内稳定,见表2。
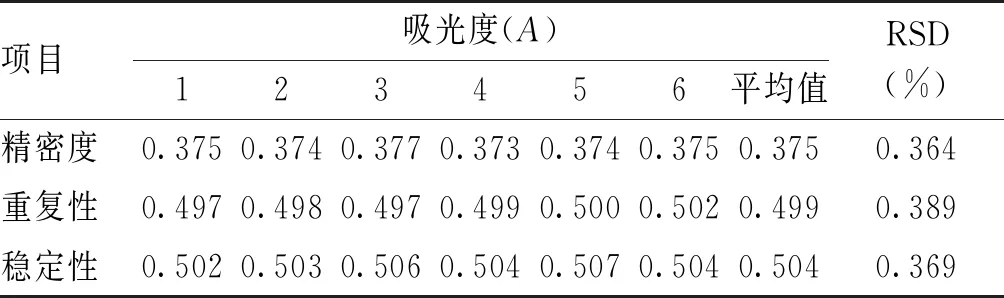
表2 复方黄连灌肠液中总生物碱含量测定方法精密度、重复性、稳定性试验结果(n=6)
2.5.6 加样回收率试验取同一批复方黄连灌肠液(批号:20190828,总生物碱含量为3.554 4 mg/mL)3.0 mL,置于250 mL圆底烧瓶中,分别加入盐酸小糪碱对照品溶液(0.948 mg/mL)9.0 mL,按“2.4”项下方法制备加样回收试验供试品溶液,平行制备6份,分别精密量取上述加样回收试验供试品溶液3.0 mL,按“2.5.4”项下方法测定,结果得平均回收率为100.86%,RSD为1.852%(n=6),见表3。
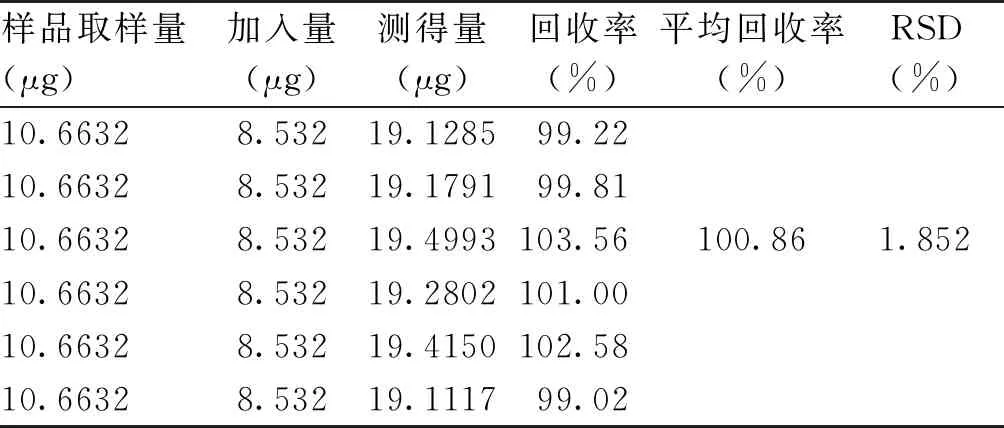
表3 总生物碱含量测定方法加样回收率实验结果(n=6)
2.6 复方黄连灌肠液总生物碱含量测定取复方黄连灌肠液按“2.4”项下方法制备供试品溶液3批(批号:20190828、20190829、20190830),分别精密量取供试品溶液3.0 mL,分别置于25 mL量瓶中,0.05 mol/L硫酸溶液稀释至刻度,摇匀,以0.05 mol/L硫酸溶液为参比,于345 nm测定吸光度,外标法计算总生物碱含量,见表4。
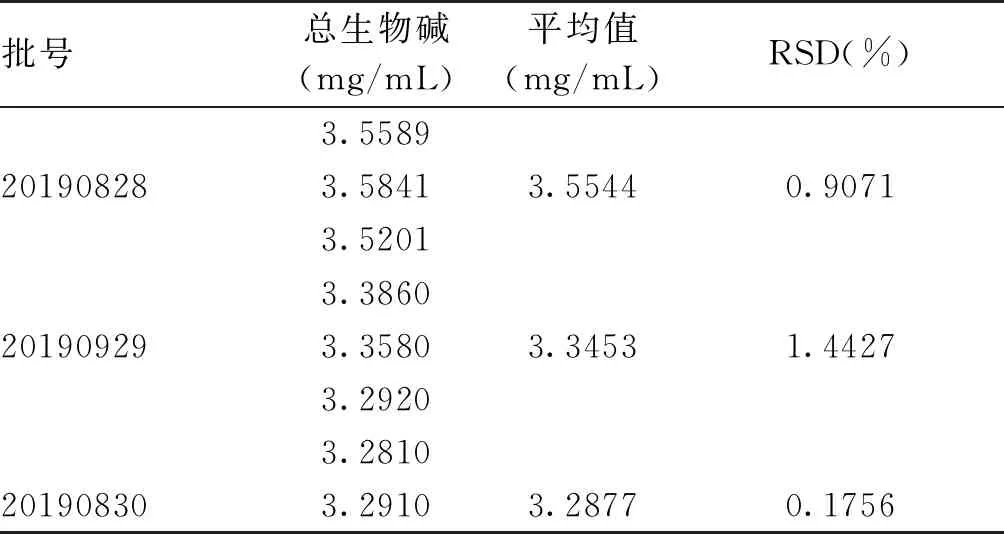
表4 复方黄连灌肠液中总生物碱含量测定结果(n=3)
3 讨 论
生物碱是存在于植物中具有最为显著活性的效部位成分具有抗肿瘤、抗炎、抗病毒、抗心血管疾病等作用[16]。目前的文献报道多是研究植物药材中总生物碱的提取与质量控制[7-9,12-15],对于富含生物碱的制剂成品研究报道较少[16-17],本研究建立柱色谱-紫外分光光度法测定复方黄连灌肠液中总生物碱含量的方法,并根据2015版《中国药典》对所建立的方法进行方法学验证,该方法具有简便快速、准确可靠等优点,可以作为复方黄连灌肠液中总生物碱含量测定及质量控制提供依据。
本研究参考有关文献,考察采用总生物碱提取常用的直接静置、超声以及水浴回流等方法提取复方黄连灌肠液中总生物碱,结果表明水浴回流提取法,提取比较完全,紫外吸收度值高于其他两种方法;再经过预实验确定进一步优化考察5种提取溶剂和5个回流时间后,综合考虑提取效果,最终确定提取方法为以盐酸-甲醇(1∶100)溶液为溶剂水浴加热回流1.5 h。
本研究考察最佳吸收波长时,盐酸小糪碱对照品溶液在228、263、345 nm处有吸收峰,而供试品溶液在279、335 nm处有强吸收,考虑是供试品溶液中其他成分对吸收峰位移的影响,并且在345 nm处供试品的吸收处于肩峰的位置,且波峰基线较平稳,峰形较好,最后确定345 nm 为测定波长。
