系统性红斑狼疮患儿霉酚酸酯血药浓度与疾病活动、疾病复发及不良反应的关系
2021-02-26李一帆刘海梅李国民管皖珍
李一帆 刘海梅 张 涛 李国民 管皖珍 姚 文 孙 利
复旦大学附属儿科医院风湿科(上海 201102)
系统性红斑狼疮(systemic lupus erythematosus,SLE)是一种临床表现多样、可全身多脏器受累的自身免疫性疾病[1]。目前多种免疫抑制剂用于SLE的治疗,包括糖皮质激素、羟氯喹、甲氨蝶呤、环磷酰胺、环孢素及霉酚酸酯等。其中霉酚酸酯由于其治疗效果好、不良反应少等优点,近年来广泛用于SLE 的诱导缓解及维持治疗阶段。
吗替麦考酚酯(mycophenolate mofetil,MMF)是一种前体药物,口服后在体内通过小肠、肝脏及血浆中的酯酶迅速水解为具有免疫抑制活性的药物霉酚酸(mycophenolic acid,MPA)。霉酚酸最早在1893年自青霉菌中分离出来,1969 年发现霉酚酸具有免疫抑制作用[2]。MPA 可选择性抑制T 和B 淋巴细胞中次黄嘌呤单核苷酸脱氢酶(inosine 5'-monophosphate dehydrogenase,ⅠMPDH)的活性,抑制鸟嘌呤合成,从而选择性抑制T和B淋巴细胞的增殖[3]。MPA还可以通过抑制淋巴细胞黏附分子的形成,降低淋巴细胞在慢性炎症部位的聚集,抑制自身抗体产生、抑制血管平滑肌增殖、诱导淋巴细胞凋亡等机制,发挥免疫抑制作用[4]。
MMF 最初用于器官移植的抗排斥治疗,关于MPA 血药浓度与治疗效果及不良反应的研究多来自于实体器官移植后的患者资料。为更好地控制免疫排斥反应、减少不良反应的发生,临床推荐MPA 0-12h时间曲线下面积(area under the curve,AUC0-12h)作为MMF的治疗药物检测指标。MPA AUC0-12h不仅与临床排斥反应的发生密切相关,与不良反应的发生亦有一定的关系[5]。目前认为在肾移植患者中,AUC0-12h是可以反映MPA 在体内暴露情况的最佳指标,AUC0-12h推荐目标水平为30~60mg/(h·L)[6]。MMF应用于儿童SLE等自身免疫性疾病的治疗中,其药物浓度检测及推荐范围多参考器官移植患者,目前尚无统一的标准。本研究回顾性分析2017年1月—2019年6月收治使用MMF 的SLE 患儿的临床资料,分析患儿MPA AUC0-12h与疾病活动度、疾病复发及不良反应之间的关系,以探讨MMF治疗儿童SLE的适宜浓度,帮助临床治疗。
1 对象与方法
1.1 研究对象
以2017 年1 月—2019 年6 月住院的81 例SLE 患儿为研究对象。研究对象纳入标准:①确诊时年龄≤18岁;②估算肾小球滤过率(estimated glomerular filtration rate,eGFR)≥60 mL/(min·1.73m2);③符合SLE分类标准,在本中心就诊的SLE患儿;④口服MMF维持该剂量≥5天,且在近半年MMF用药剂量无调整;⑤每1~3个月规律随访,且检测MPA血药浓度,并能成功拟合AUC代谢曲线。排除标准:①未规律随访,病历资料不完整者;②近半年应用其他免疫抑制剂,如环孢素、他克莫司,或生物制剂,如利妥昔单抗。
纳入患儿近半年的治疗方案为激素联合MMF、羟氯喹,MMF使用剂量为20~40 mg/(kg·d),且近半年未使用其他免疫抑制剂,其中11例检测血药浓度时处于诱导缓解治疗阶段,70例处于维持治疗阶段。诱导缓解治疗阶段患儿每1~2个月随访1次,维持治疗阶段每3~6个月随访1次。
1.2 方法
1.2.1 临床资料收集 通过病史系统、随访单等途径,获取患儿的临床资料,包括①一般资料:姓名、性别、出生日期、发病年龄、身高、体质量、诊断、血白蛋白(albumin,Alb)、肌酐等;②用药情况:MMF种类、剂量、加用时间以及激素使用情况。
1.2.2 治疗有效性评价 收集检测MPA AUC 当时及其后3 个月、6 个月患儿的SLE 疾病活动度评分(systemic lupus erythematosus activity disease index,SLEDAⅠ)及近1 年内有无疾病复发情况(复发定义为SLEDAⅠ由≤4 分增加至≥5 分,或两次随访之间SLEDAⅠ增加≥3分)。
1.2.3 MMF 药物不良反应 近1年有无感染、血常规三系降低及消化道症状等不良反应。
1.2.4 MMF 血药浓度 采集患儿在维持使用药物或调整用药5 天后达到稳态的血药浓度,利用有限采样法在 4 个时间点采集血样,分别在服药前 30 min,服药后 20 min、1 h、3 h 采集静脉血,乙二胺四乙酸(EDTA) 抗凝,检测对应时间点的药物浓度值。采血由本院采血小组专门执行,并在每次采血前用扫描仪记录采血时间,以确保采血时间的准确性。MMF服药前30 min(C0)、服药后20 min(C0.33)、服药后1 h(C1)、服药后3 h(C3)、采用 Mwphar+软件模拟 MPA 在儿童体内代谢曲线,并计算 AUC0-12h。
1.2.5 分组 ①根据患儿MPA AUC0-12h检测后3个月及6个月的SLEDAⅠ分为2组:SLEDAⅠ≥5分为疾病活动组,SLEDAⅠ≤4分为疾病非活动组。比较疾病活动组与非活动组间MPA AUC0-12h的差异。②根据MPA AUC0-12h的水平将患儿分为3组:<40 mg/(h·L)为低AUC组,40~60 mg/(h·L)为中AUC组,>60 mg/(h·L)为高AUC 组,比较MPA AUC0-12h检测后3 个月及6 个月的SLEDAⅠ在三组间的差异。③根据在维持期治疗中进行MPA AUC0-12h检测的患儿在检测后1 年内有无复发分为复发组及未复发组,比较两组间MPA AUC0-12h的差异。④根据MPA AUC0-12h检测后1年内有无出现药物相关不良反应分为不良反应组及无不良反应组,比较两组间MPA AUC0-12h的差异。
1.3 统计学分析
所有数据使用SPSS 17.0 进行统计分析。符合正态分布的计量资料以均数±标准差表示,多组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验,两组间比较采用两独立样本t检验;非正态分布计量资料以中位数(四分位数范围)表示,组间比较采用秩和检验。绘制ROC曲线,评估MPA AUC对于随访3个月与6个月的SLEDAⅠ评分以及复发的预测价值。以P<0.05为差异有统计学意义。
2 结果
2.1 一般资料
共纳入81例患儿,男20例、女61例,年龄4.5~17岁,中位年龄为13.1(11.0~14.4)岁。81 例患儿中有11 例处于诱导缓解治疗阶段,70 例处于维持治疗阶段。
2.2 MPA AUC0-12h与SLE患儿疾病活动度的关系
根据SLEDAⅠ评价患儿的疾病活动度,收集MPA AUC0-12h检测后随访3个月患儿的SLEDAⅠ评分情况。根据SLEDAⅠ-3个月分组,非活动组67例,活动组14例。与非活动组相比,活动组患儿起病年龄偏小,白蛋白和肌酐水平较低,eGFR较高,差异均有统计学意义(P<0.05)。见表1。
2.3 活动组与非活动组患儿间MPA AUC0-12h差异
随访3个月,非活动组(3个月)的MPA AUC0-12h高于活动组(3个月),差异有统计学意义(P<0.05)。随访6个月,非活动组(6个月)74例、活动组(6个月)7 例。非活动组(6 个月)MPA AUC0-12h高于活动组(6个月),差异有统计学意义(P<0.05)。见表2。
2.4 患儿无活动时MPA AUC0-12h截断值
绘制ROC 曲线,发现根据SLEDAⅠ-3 个月评分为非活动组的患儿,MPA AUC0-12h的截断值为40.13 mg/ (h·L),曲线下面积为0.73(P=0.008,95%CI:0.59~0.87),灵敏度64.3%,特异度80.3%。6个月SLEDAⅠ评分为非活动组的患儿,MPA AUC0-12h的截断值亦为40.13 mg/(h·L),曲线下面积为0.73(P=0.042,95%CI:0.52~0.95),灵敏度78.4%,特异度71.4%。见图1。

表1 SLE患儿非活动组与疾病活动组临床资料比较

表2 随访3个月及6个月非活动组及活动组患儿的MPA AUC比较[M(P25~P75),mg·(h·L)-1]
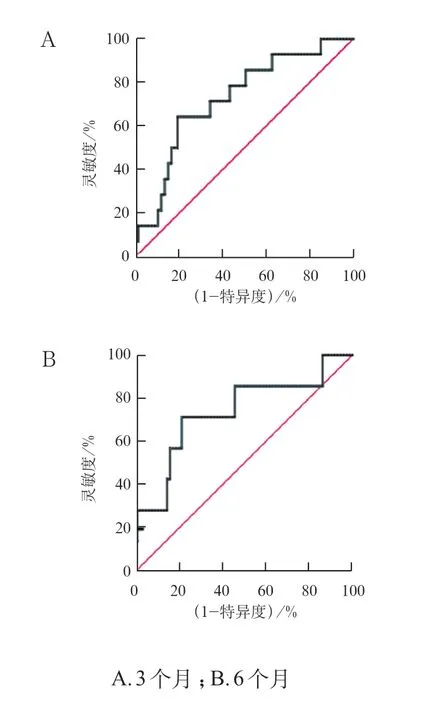
图1 MPA AUC 预测SLEDAI 评分的ROC 曲线
2.5 不同MPA AUC水平组间比较
根据MPA AUC 水平将患儿分为3 组,包括低AUC组22例,中AUC组44例,及高AUC组18例。低、中、高三组之间随访3 个月以及6 个月后的SLEDAⅠ评分差异均有统计学意义(P<0.05),均以低AUC组SLEDAⅠ评分较高。见表3。
2.6 疾病未复发组与复发组患儿MPA AUC0-12h比较
81例患儿中包含维持期治疗70例,根据维持期治疗患儿检测MPA AUC0-12h后1 年内有无复发将其分为未复发组及复发组,其中复发组7 例,未复发组63例。复发组MPA AUC 水平显著低于未复发组,差异有统计学意义(P=0.001)。利用ROC曲线,预测患儿复发时MPA AUC的截断值为43.03 mg/(h·L),曲线下面积为0.89(P=0.001,95%CI:0.79~0.98),灵敏度100%,特异度69.8%。见表4、图2。
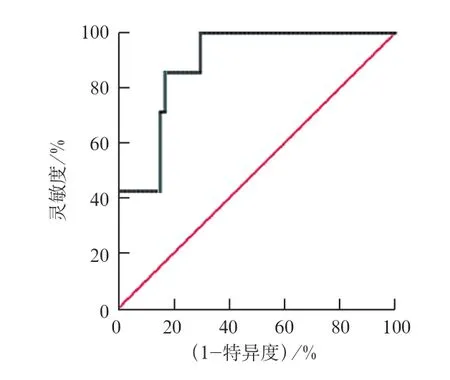
图2 MPA AUC 水平预测患儿疾病复发的ROC 曲线
2.7 MMF在SLE患儿中不良反应情况比较
根据患儿检测MPA AUC后1年有无出现不良反应将患儿分为2组,其中出现不良反应组患儿有13例(16.0%),其中3例为胃肠道反应包括腹痛、恶心、呕吐,有10 例表现为感染,最常见为水痘-带状疱疹病毒感染(3例);无不良反应组68例。
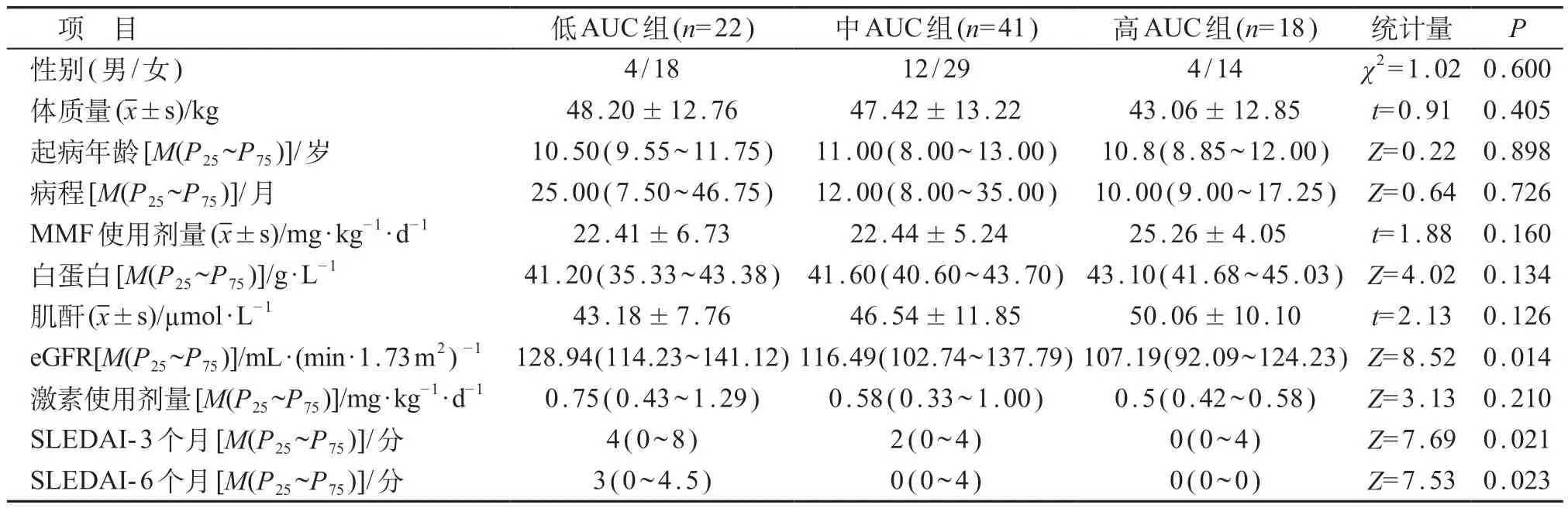
表3 低、中、高MPA AUC三组临床资料比较
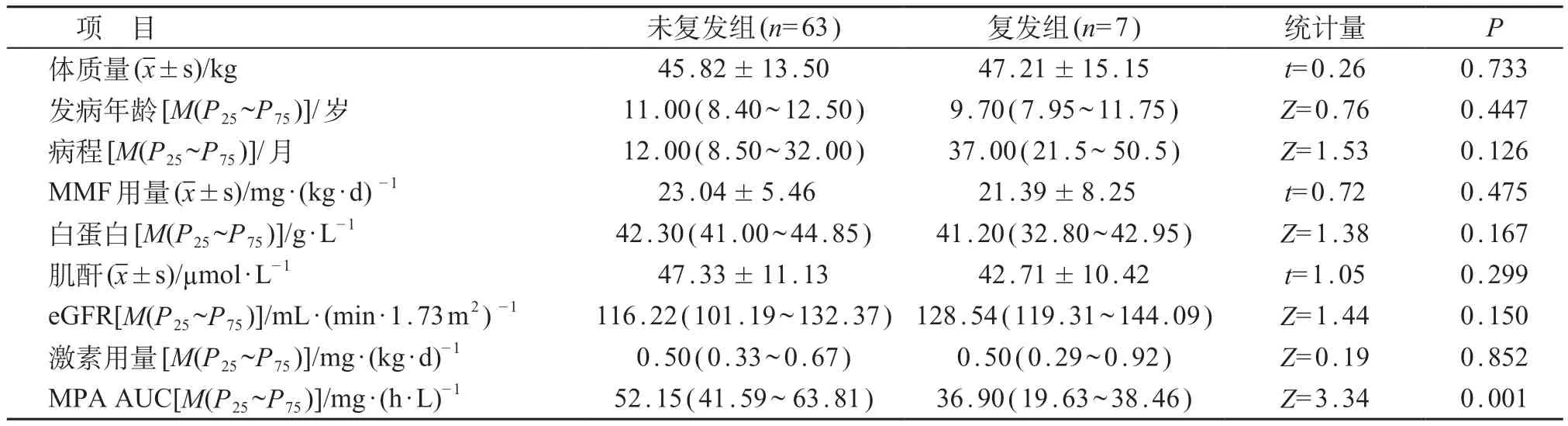
表4 SLE患儿疾病未复发组及复发组临床资料比较
无不良反应组MPA AUC 中位水平为46.24(39.46~56.36),与不良反应组56.75(42.15~66.65)相比,差异无统计学意义(Z=1.40,P=0.162)。13 例出现不良反应的患儿均未因不良反应而进行减量,感染急性期控制后均可恢复既往剂量维持。
3 讨论
MMF 目前广泛用于SLE 的治疗。2018 年我国颁布的儿童狼疮性肾炎的指南推荐,MMF 可用于狼疮性肾炎Ⅲ型及Ⅳ型的诱导缓解及维持治疗阶段。2019年欧洲抗风湿病联盟(EULAR)更新的对SLE 治疗的推荐指南中,建议MMF 用于中重度非肾脏受累的SLE患者的治疗[7]。MPA AUC水平检测已广泛推荐用于肾脏移植后的评估,MMF 是MPA 的前体物质,其药代动力学复杂,多项研究提示SLE患儿之间及患儿本身不同时期体内MPA 的水平差异较大,因此MPA AUC 水平检测越来越多地应用于SLE 患儿以指导临床治疗[8-9]。
本研究回顾性分析了2017 年1 月—2019 年6 月共81例SLE患儿的MPA AUC数据,分别分析了MPA AUC 与疾病活动、疾病复发及不良反应的关系,结果发现,SLE 患儿疾病活动组的MPA AUC 水平显著低于非活动组。MPA AUC低水平组的疾病活动度SLEDAⅠ评分高于中高水平组,提示MPA AUC 水平与SLE患儿疾病活动度呈负相关。
在一些既往的成人及儿童SLE 研究中,也有相似的结论产生。相关研究发现肾病综合征及狼疮性肾炎的复发很有可能与治疗过程中MPA 的浓度过低有关,当其谷浓度>3 μg/mL 则可有效避免蛋白尿的复发[10]。一项纳入36 例儿童SLE 的回顾性研究发现,疾病活动组(SLEDAⅠ>6 分)的MPA AUC 显著低于非活动组;通过多元回归分析及ROC 曲线得出MPA AUC<44 mg/(h·L)时,出现疾病活动的可能性大[11]。在另一项纳入19 例SLE 患儿的研究中发现,AUC ≥30 mg/(h·L)时可明显减少SLE 的疾病活动[12]。本研究通过ROC 曲线得出MPA AUC<40.13 mg/(h·L)时,根据3个月后的SLEDAⅠ评分计算其曲线下面积为0.726(P=0.008),灵敏度64.3%,特异度80.3%;根据6个月后的SLEDAⅠ评分计算其曲线下面积为0.734(P=0.042),灵敏度78.4%,特异度71.4%;均说明MPA AUC<40.13 mg/(h·L)时,可能出现疾病活动。
SLE属于慢性病程,在病程中可能有疾病活动或疾病反复,可能需长期使用免疫抑制剂治疗。在一项关于非肾脏受累SLE成人患者的回顾性分析研究中,纳入20例使用MMF进行维持治疗的患者,分析MPA AUC 后半年内疾病的复发率,结果显示MPA C12h<3 mg/L时,92%可能在半年内出现疾病复发[13]。而目前尚未见儿童MPA AUC 与疾病复发之间关系的研究。本研究回顾性分析了以MMF 用于维持期治疗的70例患儿,发现MPA AUC预测1年内疾病复发的ROC曲线下面积为0.886(P=0.001),灵敏度100%,特异度69.8%;在MPA AUC<43.03 mg/(h·L)时,疾病复发可能性大。
一项关于肾移植后MMF 的meta 分析显示,血液系统不良反应、感染及胃肠道反应是导致MMF 减量的最为常见的三大原因[14]。多项研究表明,MMF 在SLE患儿中使用安全性较好,常见的不良反应包括胃肠道反应(腹痛、呕吐、腹泻)、感染及血液系统不良反应(白细胞降低、血小板减少),大多可耐受,不需减量[15]。在日本一项纳入115 例儿童SLE 的回顾性研究中,最为常见的不良反应为带状疱疹病毒感染(8/115),其次为胃肠道反应(7/115)[16]。本研究纳入的81例患儿中,最为常见的不良反应为水痘-带状疱疹病毒感染和胃肠道反应,与既往研究结果相符。本研究中不良反应组与无不良反应组的MPA AUC差异并不显著。
本研究的局限性在于:①本研究为回顾性分析,检验效能有限;②样本量有限,结果可能产生偏倚;③本研究中未包含使用其他免疫抑制剂及生物制剂患儿,可能未包含部分重症SLE 及难治性SLE 患儿,会造成样本选择的偏倚。因此,如需进一步明确SLE患儿MMF 与疾病活动及复发的关系,需进一步开展随机对照试验。
综上所述,本研究回顾性分析了使用MMF的SLE患儿MPA AUC与疾病活动、复发之间的关系及MMF不良反应情况,结果发现MPA AUC0-12h水平与疾病活动呈负相关,MPA AUC0-12h<40.13 mg/(h·L)时疾病活动可能性大;使用MMF 进行维持期治疗时,MPA AUC0-12h水平<43.03 mg/(h·L)时,疾病复发的可能性大。提示在使用MMF 治疗SLE 时,MPA AUC0-12h目标维持在43.03 mg/(h·L)以上,可减少疾病的活动及复发情况。MMF安全性较好,最为常见的不良反应为水痘-带状疱疹病毒感染及胃肠道反应,患儿均可耐受,未出现因不良反应而导致药物减量的情况。对于MPA AUC 的治疗上限,本研究未得出结果;但在MPA AUC0-12h>60 mg/(h·L)时,与MPA AUC0-12h处于40~60 mg/(h·L)的患儿相比,疾病活动度并无改善,提示更高浓度的MPA AUC可能并不能更好的控制疾病活动。
