人参皂苷Rg1抑制小鼠实验性自身免疫性脑脊髓炎的作用及免疫机制
2021-02-24朱国旗
徐 文,周 妍,朱国旗
(1.中国科学技术大学附属第一医院神经内科,安徽 合肥 230000;2.安徽省儿童医院儿保科,安徽 合肥 230051;3.安徽中医药大学新安医学教育部重点实验室,安徽 合肥 230038)
多发性硬化是一种常见的神经系统脱髓鞘疾病,以青少年发病为主。多发性硬化的主要特征是中枢神经系统脱髓鞘病变的时间和空间多发性,临床以复发-缓解病程为主。多发性硬化目前病因并不十分明确,环境因素、遗传、T细胞介导的免疫失衡均参与多发性硬化的发病。特别是CD4T细胞和CD8T细胞介导的免疫应答、辅助性T细胞17/调节性T细胞(T helper cell 17/regulatory cell,Th17/Treg)失衡等在多发性硬化的发病中有重要作用。
中医药在多发性硬化的治疗中具有一定优势,中药人参具有升阳举陷、益气固表的作用,其单药提取物人参皂苷Rg1具有调节免疫功能、抗炎、保护中枢神经系统的作用。本研究利用实验性自身免疫性脑脊髓炎(experimental autoimmune encephalomyelitis, EAE)模型,观察人参皂苷Rg1对EAE小鼠外周血CD4、CD8、辅助性T细胞1(T helper cell 1,Th1)、Th17、Treg等细胞亚群的影响,探讨人参皂苷Rg1改善EAE的可能机制。
1 材料
1.1 实验动物 SPF级C57BL/6雌性小鼠购买自上海斯莱克实验动物有限公司,共30只,6周龄,体质量为16~18 g,饲养于室内温度为23~26 ℃,相对湿度为40%~60%的环境中,标准饲料喂养,自由饮水,明暗节律为12 h交替。适应性饲养2周后用于实验。
1.2 药物及试剂 人参皂苷Rg1(批号 22427-39-0,纯度≥98%):上海源叶生物科技有限公司;小鼠髓鞘少突胶质糖蛋白33-35(myelin oligodendrocyte glycoprotein 33-35,MOG33-35):上海强耀生物科技有限公司;弗氏完全佐剂:Sigma公司;百日咳毒素:Merk公司;灭活H37RA结核分枝杆菌(TB)、FITC-抗小鼠CD4抗体(553651,0.5 mg)、APC-Cy7抗小鼠CD25抗体(557658,0.1 mg)、PerCP-Cy5.5抗小鼠CD4抗体(561115,25 μg)、BV510-抗小鼠CD45抗体(563891,50 μg)、PE-抗小鼠干扰素-γ(interferon gamma, IFN-γ)抗体(554412,0.1 mg):美国BD生物公司。PECy7-抗小鼠IL-17A抗体(25-7177-82,100 μg)、APC-Foxp3抗体(17-5773-82,100 μg)、FITC-抗小鼠CD8抗体(11-0081-82,100 μg):Ebioscience公司。
2 方法
2.1 EAE模型复制方法 利用异戊巴比妥麻醉小鼠后,每只小鼠皮下注射含H37Ra TB 400 μg和MOG35-55 300 μg的100 μL弗氏完全佐剂,分2点背部皮下注射。模型复制当日,每只小鼠同时腹腔注射百日咳毒素300 ng。48 h后每只小鼠腹腔再次注射百日咳毒素 300 ng。模型复制后观察小鼠发病情况,神经功能评分如下:
0分:不发病;1分:小鼠尾部张力降低或麻痹;2分:尾部麻痹,后肢无力;3分:小鼠后肢瘫痪;4分:小鼠四肢瘫痪,人为翻身后不能复位;5分:濒死状态或发病后死亡。EAE临床评分≥1分即为模型复制成功,模型复制成功率>95%。
2.2 分组及给药 将小鼠随机分为5组(n
=6):正常对照组,模型组,Rg1低剂量(20 mg/kg)、中剂量(40 mg/kg)、高剂量(80 mg/kg)组。EAE模型复制后第10天,开始进行不同剂量Rg1腹腔注射(调整容积为100 μL),每日1次,连续给药14 d,模型组和正常对照组小鼠给予同容积生理盐水。2.3 样本收集及组织病理评分 模型复制后第35天处死小鼠,眼球摘除后取眼眶外周血,离心后用于ELISA检测。颈椎脱臼处死后,4%多聚甲醛心脏灌流,取颈胸段脊髓约5 mm,于4%多聚甲醛中4 ℃固定2 d,蔗糖梯度脱水后进行石蜡包埋,组织连续切片后,分别进行苏木精-伊红(hematoxylin-eosin, HE)染色和神经髓鞘固蓝(luxol fast blue staining, LFB)染色,光学显微镜下分别观察脊髓炎症细胞浸润情况和脱髓鞘变化并进行评分:
①HE染色下炎症细胞浸润评分标准:0分,无炎症细胞;1分,少量炎症细胞;2分,血管周围组织炎症细胞浸润;3分,大量炎症细胞浸润。②LFB染色下脱髓鞘评分标准:0分,无脱髓鞘;1分:罕见脱髓鞘;2分:少数脱髓鞘;3分:大面积脱髓鞘。
2.4 流式细胞仪检测脾淋巴细胞中CD4、CD8T细胞占CD45T细胞百分比及Th17(CD4IL-17A)、Th1(CD4IFN-γ)、Treg(CD4CD25Foxp3)的百分比 将小鼠处死后,分离脾脏,在超净工作台下用150目细胞筛将脾细胞磨碎,反复冲洗、离心、分离脾细胞后加入1640培养液,调整细胞密度为2×10/mL,将样品分为2份,每管500 μL,其中一管直接在细胞表面标记FITC-CD4、APC-Cy7-CD25,4 ℃孵育30 min,固定破膜后再标记APC-Foxp3,室温孵育40 min,洗涤细胞后用300 μL PBS重悬细胞。另一管加入50 ng/mL PMA、1 μg/mL离子霉素和3 μg/mL莫能霉素,37 ℃温箱孵育5 h,洗涤后分别加入FITC-CD8、PerCP-Cy5.5-CD4、APC-Cy7-Dye、BV510-CD45,进行细胞表面染色,4 ℃孵育30 min,固定破膜后再标记PE-IFN-γ、PECy7-IL-17A,室温孵育40 min,洗涤细胞后用200 μL PBS重悬细胞,流式细胞仪检测各细胞亚群百分比。
2.5 ELISA法检测外周血清中细胞因子水平 取小鼠眼眶外周血后,3 000 r/min离心10 min,吸取上层血清,液氮快速淬取,-80 ℃保存,稀释1倍后检测血清IFN-γ、IL-17A、IL-6、IL-10水平。

3 结果
3.1 人参皂苷Rg1对EAE小鼠神经症状的影响 第12~14天小鼠开始出现EAE症状,小鼠饮食活动减少,精神萎靡,并逐渐出现尾尖拖地或单侧后肢或双后肢瘫痪,部分出现全肢瘫痪。含有一个重复测量变量的两因素方差分析结果(见表1)显示,组别因素、时间因素的主效应及两者的交互作用均具有统计学意义(P
<0.05)。简单效应分析结果显示,从第15天至实验结束,40、80 mg/kg人参皂苷Rg1干预的EAE小鼠神经功能评分均较模型组显著下降(P
<0.05)。见图1。
图1 不同时点5组小鼠临床神经功能评分比较
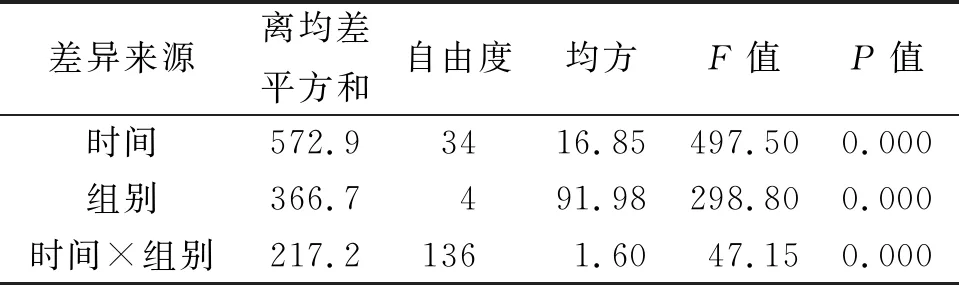
表1 含有一个重复测量数据的两因素方差分析结果
3.2 人参皂苷Rg1对EAE小鼠脊髓病理变化的影响 HE染色及LFB染色后显微镜下观察,可见EAE小鼠出现明显的炎症细胞浸润及大面积的髓鞘脱失,而给予不同剂量人参皂苷Rg1干预后,小鼠炎症细胞浸润和髓鞘脱失减轻,见图2。与模型组比较,Rg1低、中、高剂量组小鼠炎症细胞浸润评分和脱髓鞘评分显著降低(P
<0.05),Rg1高剂量组炎症细胞浸润评分和脱髓鞘评分显著低于Rg1低剂量组(P
<0.05)。见表2。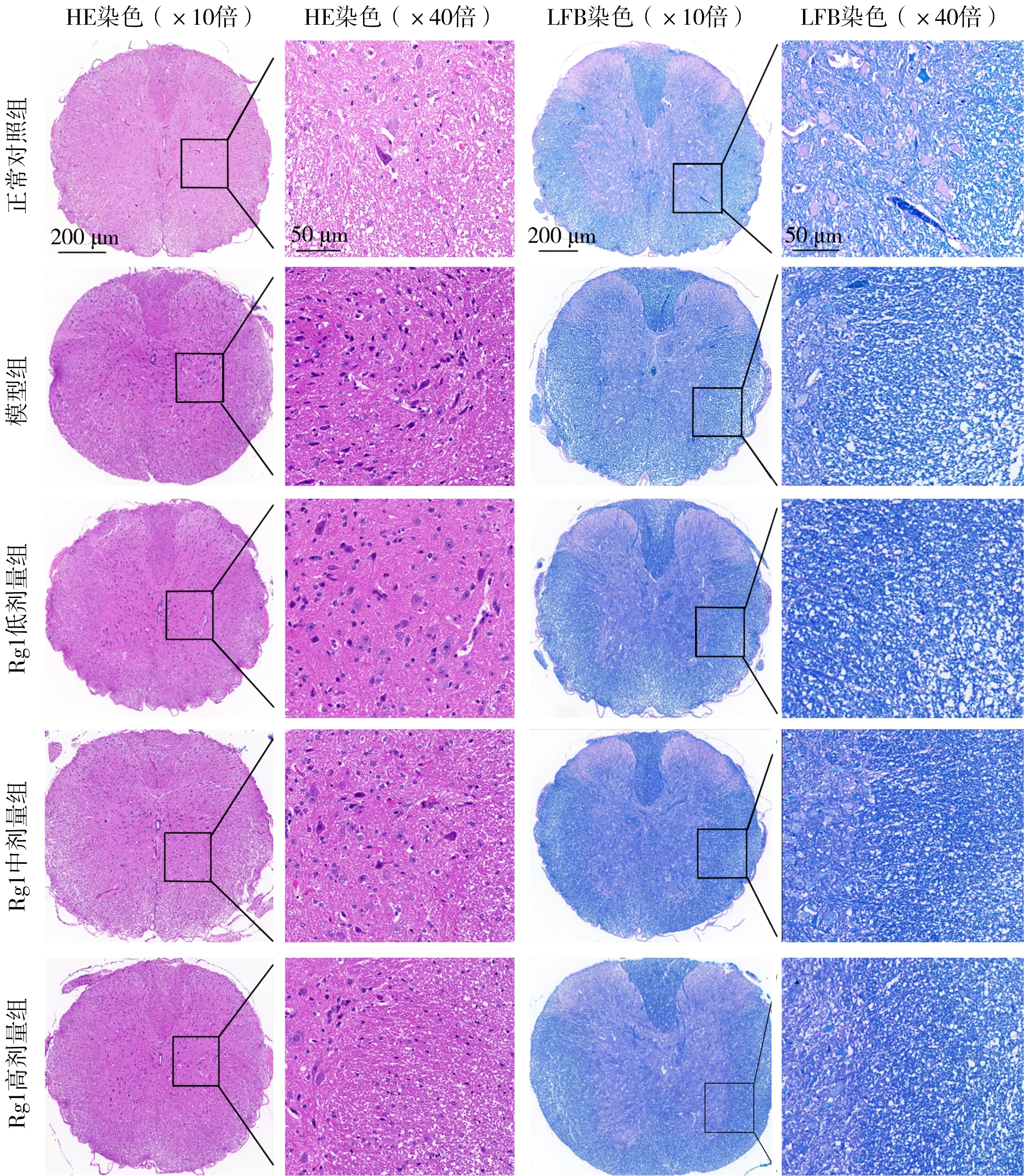
图2 5组小鼠脊髓的组织形态学变化(HE染色下显示炎症细胞浸润情况,LFB染色下显示脱髓鞘情况)

表2 5组小鼠炎症细胞浸润和脱髓鞘评分比较
3.3 人参皂苷Rg1对EAE小鼠脾淋巴细胞亚群的影响 与模型组比较,人参皂苷Rg1低、中、高剂量组小鼠脾淋巴细胞CD4、CD8占CD45T细胞百分比,以及Th1、Th17细胞亚群占CD4T细胞比例显著减低(P
<0.05),而Treg(CD4CD25FoxP3)比例明显增加(P
<0.05),且人参皂苷Rg1的作用呈剂量依赖性。见表3。3.4 人参皂苷Rg1对EAE小鼠外周血IFN-γ、IL-17A、IL-6、IL-10水平的影响 与正常对照组比较,模型组小鼠外周血IFN-γ、IL-17A、IL-6水平显著升高(P
<0.05),IL-10水平显著降低(P
<0.05);与模型组比较,人参皂苷Rg1低、中、高剂量组IFN-γ、IL-17A、IL-16水平显著下降(P
<0.05),而IL-10水平显著升高(P
<0.05)。人参皂苷Rg1的作用呈剂量依赖性。见表4。4 讨论
多发性硬化可导致肢体无力、肢体瘫痪,本病属中医学“痿证”“痹证”范畴。《素问·痿论》指出:“脾气热,则胃干而渴,肌肉不仁,发为肉痿;肾气热,则腰脊不举,骨枯髓减,发为骨痿。”《景岳全书》认为“补中益气、健脾升清”是治疗痿证的重要方法。人参作为传统中药,是刺五加科多年生草本植物的干燥根,具有补气固脱、健脾益肺、宁心益智、养血生津之功效。而人参皂苷Rg1作为人参的主要活性药理成分,具有明显的抗炎、调节免疫作用。前期研究显示,人参皂苷Rg1可以通过调控PI3K/AKT通路改善小鼠认知及记忆功能。有研究显示,人参皂苷Rd可缓解EAE。韩国学者Lee等发现,韩国红参和人参中有效成分Rb1和Rg1联用可有效抑制Th1、Th17,从而改善EAE,但尚未明确发挥作用的药物有效成分。人参皂苷Rg1对EAE的作用尚未见报道。
表3 5组小鼠脾淋巴细胞亚群比较

表4 5组小鼠外周血IFN-γ、IL-17A、IL-6、IL-10水平比较
本研究显示,人参皂苷Rg1可显著减轻EAE小鼠的症状,有效改善EAE小鼠脊髓的炎症细胞浸润和髓鞘脱失,尤其是人参皂苷Rg1中、高剂量组小鼠的髓鞘脱失和炎症细胞浸润程度明显减轻。结果提示人参皂苷Rg1可有效改善EAE的临床症状,抑制EAE的中枢神经系统损伤。
CD4T细胞在多发性硬化的发病机制中具有重要作用,特别是Th1、Th17细胞可能是多发性硬化治疗的重要靶点。Th17细胞最早发现于2005年,Th17细胞可以穿过血脑屏障,浸润中枢神经系统。Th17细胞介导发病主要依赖细胞因子IL-17A。研究表明,IL-17A可增强各种炎症递质的分泌,包括IL-6、TNF-1、MIP-2、CXCL-1等,IL-17A是中性粒细胞浸润和炎症细胞因子的有效诱导剂,在多发性硬化患者的斑块和脑脊液中均可以检测到IL-17A高表达。Treg细胞被认为是维持外周对自身抗原耐受的关键因素,可通过各种可溶性递质如IL-10、TGF-β发挥其免疫抑制作用,Fop3为其关键转录因子。多发性硬化可能与Treg细胞失衡,Th1、Th17反应增强相关,这种失衡可能由于Treg细胞的抑制功能缺失导致髓鞘破坏,引起神经损伤和神经炎症。本研究显示,人参皂苷Rg1可明显抑制CD4T细胞及CD8T细胞亚群的表达,特别是人参皂苷Rg1高剂量可显著抑制CD4T细胞表达。同时人参皂苷Rg1也可以抑制Th1、Th17细胞表达,而与之对应,人参皂苷Rg1的应用可引起Treg细胞水平上调。在细胞因子水平,人参皂苷Rg1可抑制IFN-γ、IL-17A、IL-6等炎症细胞因子表达,而作为抑制性因子的IL-10表达则上调。这提示人参皂苷Rg1可通过抑制Th17、Th1细胞及其分泌的炎症细胞因子而调控Treg细胞失衡,抑制中枢神经系统炎症过度激活,从而改善EAE的临床症状。
综上所述,人参皂苷Rg1可有效缓解EAE小鼠模型的临床症状,减轻其中枢神经系统的炎症细胞浸润和髓鞘脱失,其作用机制可能与调控Th17/Treg细胞亚群平衡,抑制炎症因子水平有关。
