Ru-Ir/Ti阳极的制备及性能
2021-02-19王冰冰田林庄晓东林琳俞小花谢刚凡杰
王冰冰,田林,庄晓东,林琳, 俞小花,谢刚,2,3,凡杰
(1.昆明理工大学 冶金与能源工程学院,云南 昆明 650093;2.昆明冶金研究院有限公司,云南 昆明 650503; 3.共伴生有色金属资源加压湿法冶金技术国家重点实验室,云南 昆明 650503)
20世纪60年代,研究者们研制出了以钛为基体,表面涂覆金属氧化物的钛基涂层电极,其涂层氧化物主要包括 RuO2、IrO2、MnO2、Ta2O5、SnO2和 TiO2等[1-8]。Liu Bao等[9]采用溶胶-凝胶法制备了Ti/IrO2-RuO2-SiO2阳极涂层,探究了该阳极涂层在酸性溶液中的腐蚀机理和失效原因。Mazhari H等[10]采用热分解法制备了Ti/IrO2-Ta2O5和Ti/IrO2-RuO2-Ta2O5钛阳极涂层,研究得到含量为30%的RuO2有利于增加涂层表面活性面积,提高阳极性能和寿命。铱系涂层和钌系涂层钛阳极依旧是目前贵金属涂层钛阳极最主要的两种电极材料,其主要以RuO2和IrO2为主要活性物质。本实验分别采用热分解法和溶胶-凝胶法制备了Ru-Ir/Ti阳极,比较了两种方法所制备Ru-Ir/Ti阳极涂层的组织结构,并探究了其在酸性溶液中的电化学性能,对钛阳极的制备与测试具有一定的补充与指导意义。
1 实验部分
1.1 试剂与仪器
氯铱酸(H2IrCl6·6H2O)、三氯化钌、无水乙醇、草酸、硫酸、碳酸钠、柠檬酸、乙二醇、聚丙烯酰胺均为分析纯;工业用TA2钛板。
DS8-13箱式电阻炉;DHG-9023A电热鼓风干燥箱;DL-1000E数控超声波清洗器;FA2204B电子分析天平;Empyrean X射线衍射仪;TM-3000扫描电子显微镜;OUTLAB302电化学工作站。
1.2 涂层阳极的制备
1.2.1 基体预处理 将钛板切割成尺寸3 cm×1 cm×1 cm的样板,先用砂纸打磨去除钛板表面的氧化层,再将其放入10%(质量分数的)Na2CO3溶液(微沸状态)中除油1 h,然后放在10%草酸溶液(微沸状态)中酸洗刻蚀2 h,表面出现均匀灰色麻面时,取出钛板放入去离子水中超声处理10 min,用去离子水冲洗干净,干燥后浸泡在无水乙醇中备用[13]。
1.2.2 阳极涂液的制备
1.2.2.1 热分解法 按摩尔比Ir∶Ru=7∶3称取RuCl3、H2IrCl6,溶于聚丙烯酰胺中,在超声波清洗器中超声分散处理20 min使之均匀混合后待用。
1.2.2.2 溶胶-凝胶法 按摩尔比Ir∶Ru=7∶3称取RuCl3、H2IrCl6溶于无水乙醇,超声振荡使之均匀混合;按摩尔比M(RuCl3、H2IrCl6)∶柠檬酸∶乙二醇=1∶3∶14称取柠檬酸和乙二醇溶于无水乙醇,超声振荡使之均匀混合,然后以1滴/s的速度滴入到RuCl3、H2IrCl6混合溶液中,振动4 h,得到棕红色胶体溶液,室温下静置24 h后待用。
1.2.3 涂层阳极的制备 移取适量的涂液到处理好的钛板上,用软毛刷均匀的涂刷在钛板表面,转移至干燥箱中,100 ℃下干燥15 min。放入电炉中500 ℃ 烧结10 min。取出,空冷至室温。重复以上操作,多次涂刷,直到达到所需涂层厚度或质量,最后一次在500 ℃下烧结1 h,并随炉冷却至室温,制得金属氧化物涂层阳极。
1.3 微观结构及物相分析
采用Empyrean锐影X射线衍射仪(XRD)对涂层进行衍射分析,测试条件为:Cu靶Kα射线λ=0.154 06 nm,扫描速度10 (°)/min,扫描范围5~80°,测试结果采用Jade6.5软件进行分析处理。采用TM3000扫描电镜(SEM)观察样品形貌。
1.4 电化学性能测试
电化学测试使用Autolab-302N电化学工作站,采用三电极体系,工作电极为金属氧化物涂层阳极,测试面积为 1 cm2,辅助电极为1.5 cm×1.5 cm的铂片电极,参比电极为饱和硫酸亚汞电极,电解液为1 mol/L H2SO4溶液,测试温度为(25±0.5) ℃。Tafel 曲线测试的扫描速率为 5 mV/s;循环伏安曲线测试的扫描速率为 5 mV/s;交流阻抗谱测试的频率范围为1×10-5~0.1 Hz,动电位为10 mV,采样点位为10,测试结果采用NOVA软件和ZSimpWin软件进行分析处理。
2 结果与讨论
2.1 涂层的形貌与结构
2.1.1 物相分析 图1为两种不同方法制备钛阳极的XRD图谱。

图1 热分解法和溶胶-凝胶法 制备Ru-Ir/Ti阳极的XRD图谱Fig.1 XRD spectra of Ru-Ir/Ti anode prepared by thermal decomposition and sol-gel method
由图1可知,不同方法制备钛阳极的 XRD 谱线虽然有所不同,但都主要呈现 IrO2、RuO2和Ti的衍射峰,并且其峰位置均与标准卡片有一定程度的偏离,说明涂层不只是简单金红石相的IrO2和RuO2,也存在金红石相(Ir-Ru)O2固溶体。根据谢乐公式计算得到热分解法制备的Ru-Ir/Ti阳极氧化物晶粒平均尺寸为12.1~15.8 nm,溶胶-凝胶法制备的Ru-Ir/Ti阳极涂层氧化物晶粒平均尺寸为7.5~10.9 nm,说明溶胶-凝胶法制备涂层具有细化涂层氧化物晶粒的效果,而涂层表面氧化物晶粒越小,比表面积越大,这样有利于阳极的电催化活性。
2.1.2 表面形貌分析 图2为不同方法制备的Ru-Ir氧化物涂层的SEM图。

图2 热分解法和溶胶-凝胶法制备 Ru-Ir氧化物涂层的SEM图Fig.2 SEM diagram of Ru-Ir oxide coating prepared by thermal decomposition and sol-gel method a.热分解法制备Ru-Ir氧化物涂层; b.热分解法制备Ru-Ir氧化物涂层局部图; c.溶胶-凝胶法制备Ru-Ir氧化物涂层; d.溶胶-凝胶法制备Ru-Ir氧化物涂层局部图
由图2可知,采用热分解法和溶胶-凝胶法所制备的Ru-Ir氧化物涂层表面均产生了明显的泥裂纹形貌,但不同方法制备的Ru-Ir氧化物涂层形貌差别较大。采用热分解法制备的Ru-Ir氧化物涂层表面裂纹明显且较宽,涂层呈多层裂纹结构,裂纹块状大小不等,裂纹呈无规则走向,裂缝平均宽度约为2.014 μm,通过局部放大图还可看出,裂纹边缘及表面粗糙,裂块表面和裂缝中有明显的蜂窝状结构存在,且有少量晶体析出,这可能是热分解法涂液中Ir4+和Ru4+结合不充分,导致较易产生偏析的IrO2析出。采用溶胶-凝胶法制备的Ru-Ir氧化物涂层表面裂纹细密且分布均匀,无多层裂纹结构,裂缝较窄,平均宽度小于293 nm,涂层表面较为平整和光滑,无明显的晶体析出。这可能是因为,溶胶-凝胶能够使得Ru4+和Ir4+均匀的分散并结合,而Ru4+和Ir4+的相互协调可避免晶格发生严重畸变,所以表现出涂层表面较为平整,裂纹较窄且均匀。可知,不同方法制备Ru-Ir氧化物涂层形貌结构的不同将直接影响Ru-Ir/Ti阳极的电化学活性点数目和活性面积,进而影响Ru-Ir/Ti阳极的电化学性能。
2.2 电化学性能
2.2.1 极化曲线 极化曲线显示涂层阳极在一定电流密度下的析氧或析氢电位,是判断涂层阳极电流效率的重要方法。对于主要为析氧的电解体系,涂层阳极的析氧电位越低,电流效率越高,电耗也越低[11-12]。图3为两种方法制备的Ru-Ir/Ti阳极在1 mol/L H2SO4溶液中,扫速为5 mV/s条件下测试的极化曲线。
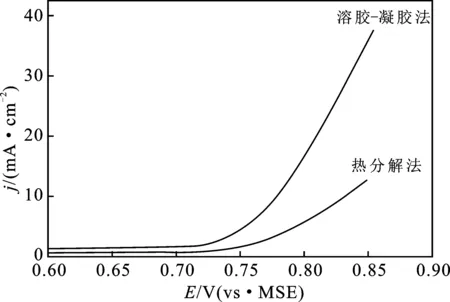
图3 热分解法和溶胶-凝胶法制备 Ru-Ir/Ti阳极的极化曲线Fig.3 Polarization curves of Ru-Ir/Ti anode prepared by thermal decomposition and sol-gel method
由图3可知,在E<0.73 V时,两种方法所制备的Ru-Ir/Ti阳极表面电流密度变化不大;E>0.73 V时,电流密度变化较为明显,并且在同一电位下,溶胶-凝胶法制备Ru-Ir/Ti阳极的电流密度明显比热分解法制备Ru-Ir/Ti阳极的电流密度大得多,说明溶胶-凝胶法制备的钛阳极具有更好的导电性和电催化活性,在实际生产中有利于提高电流效率、降低槽电压,具有节能降耗的效果。阳极涂层的外表形貌和内部结构能够影响阳极的电催化活性,通过检测可以看出,热分解法制备的阳极表面会出现典型的“龟裂纹”,表面析出物较多且晶粒尺寸较大,而溶胶-凝胶法制备的阳极涂层分散均匀,裂纹较小且均匀,晶粒尺寸更小,涂层比表面积更大,因此在阳极发生析氧反应时,溶胶-凝胶法制备的阳极涂层表面活性点更多,从而表现出较好的电催化活性。
图4为两种不同方法钛阳极在1 mol/L H2SO4溶液中扫描速率为5 mV/s所测得的 Tafel 曲线。不同方法所制备Ru-Ir/Ti阳极腐蚀性能数据表见表1。

图4 热分解法和溶胶-凝胶法制备 Ru-Ir/Ti阳极涂层的Tafel曲线Fig.4 Tafel curve of Ru-Ir/Ti anode coating prepared by thermal decomposition and sol-gel process

表1 不同方法制备Ru-Ir/Ti 阳极涂层的腐蚀性能数据表Table 1 Corrosion performance data of Ru-Ir/Ti anode coating prepared by different methods
由表1可知,采用溶胶-凝胶法制备的Ru-Ir/Ti阳极的腐蚀电位大于热分解法制备的Ru-Ir/Ti阳极的腐蚀电位,而腐蚀电流却较小。腐蚀电位越大,腐蚀电流密度越小,说明该阳极的耐腐蚀性越好。相比于热分解法,溶胶-凝胶法制备的钛基铱钌阳极具有更优越的耐腐蚀性。
2.2.2 循环伏安曲线 图5为热分解法和溶胶-凝胶法所制备的Ru-Ir/Ti阳极在1 mol/L H2SO4溶液中,扫速为5 mV/s条件下测试的循环伏安曲线。
由图5可知,采用溶胶-凝胶法制备Ru-Ir/Ti阳极的循环伏安曲线在-0.35~1.15 V(vs·MSE)电位区间内,阳极基本未发生明显的析氢或析氧反应,反应主要发生在双电层区域,电流为双电层充电电流,在此电位区间内具有明显的氧化还原峰,主要是由涂层表面活性组元Ir3+/Ir4+、Ru4+/Ru8+相互转化引起,可由式(1)、(2)表示。各循环伏安曲线基本对称,说明Ru-Ir/Ti阳极表面的反应是可逆的。Ru-Ir/Ti阳极涂层表面电荷容量Q*值的大小与循环伏安曲线所包围的面积成正比关系,可以直接反映阳极的电催化活性,曲线包围的面积越大,则阳极表面活性点的数量越多,阳极的电催化活性越好[13-14]。

图5 热分解法和溶胶-凝胶法制备 Ru-Ir/Ti阳极的循环伏安曲线Fig.5 Cyclic voltammetry of Ru-Ir/Ti anode prepared by thermal decomposition and sol-gel method
由图5可知,溶胶-凝胶法制备的Ru-Ir/Ti阳极的循环伏安曲线面积较大,通过积分计算得到,热分解法法制备的Ru-Ir/Ti阳极板的伏安电量为286.94 mC/cm2,溶胶-凝胶法制备的Ru-Ir/Ti阳极板的伏安电量为596.99 mC/cm2。说明相比于热分解法,溶胶-凝胶法制备的钛阳极具有更好的电催化活性,与极化曲线分析结果相吻合。

(1)

(2)
该反应为可逆反应,反应中IrO2、RuO2作为涂层的活性组元起着催化的作用。
2.2.3 交流阻抗谱分析 由图6可知,样品的交流阻抗曲线为圆弧形。其中,Rs是欧姆电阻,表示工作电极和参比电极之间的溶液电阻;Rct表示电荷转移电阻;CPE表示电解液与电极表面所形成的电容[15-17]。通过Zsim Demo 3.30d软件的拟合分析,Rs、Rct和CPE的值见表2。
由表2可知,采用溶胶-凝胶法制备的Ru-Ir/Ti阳极的Rct值较小,说明采用溶胶-凝胶法制备的Ru-Ir/Ti阳极容易进行析氧反应,这可能是由于该方法制备的Ru-Ir涂层表面裂纹较小,且分布均匀,Ru-Ir涂层能够很好的在表面形成均匀的(Ir,Ru)O2固溶体活性层;而采用热分解法制备的Ru-Ir涂层表面裂纹较大,且不均匀,无法在表面形成均匀的(Ir,Ru)O2固溶体活性层,大裂纹也易导致电解液渗透涂层与钛基体接触而失效。

图6 热分解法和溶胶-凝胶法制备 Ru-Ir/Ti阳极的交流阻抗图及拟合电路图Fig.6 Impedance diagram and fitting circuit diagram of Ru-Ir/Ti anode prepared by thermal decomposition and sol-gel method

表2 交流阻抗图谱数据Table 2 AC impedance map data
3 结论
(1)采用热分解法和溶胶-凝胶法制备涂层的相成分都以金红石相(Ir,Ru)O2固溶体相为主,涂层表面均有裂纹出现。与热分解法制备钛阳极的晶粒尺寸相比,溶胶-凝胶法具有细化晶粒的效果,表面形成的(Ir,Ru)O2固溶体活性层裂纹较小且均匀。
(2)采用溶胶-凝胶法制备的Ru-Ir/Ti阳极在1 mol/L H2SO4溶液中具有较大的腐蚀电位和较小的腐蚀电流,具有较好的耐腐蚀性。
(3)采用溶胶-凝胶法制备的Ru-Ir/Ti阳极在1 mol/L H2SO4溶液中相同电位下电流密度更高,(Ir,Ru)O2固溶体活性层有效面积更大,析氧电位较低,有利于析氧反应,具有更优越的导电性和电催化活性。
