生物炭复合高吸水树脂吸附亚甲基蓝性能研究
2021-02-19揭伟伟林鑫晨邓文勇刘倩刘光斌胡秀霞龚磊
揭伟伟,林鑫晨,邓文勇,刘倩,刘光斌,胡秀霞,龚磊,
(1.江西农业大学 化学系,江西 南昌 330045;2.南昌市植物资源化学利用重点实验室,江西 南昌 330045)
染料在纺织、造纸等领域有广泛应用[1-2]。染料废水未经处理排放,会对人体健康和生存环境造成危害[3-4]。生物炭是一种原料来源广、价格低廉的生物质材料,因其具有高比表面积和丰富的孔隙结构等特性,被广泛用作废水处理吸附剂[5-6]。但生物炭颗粒细小,吸附后难以从染料废水中分离出来[7-8],可通过制备成生物炭复合材料解决[9-10]。高吸水树脂在溶液中呈凝胶状,且含有大量活性基团,常被用于吸附和分离染料[11-12]。本文制备了生物炭与AA、AM接枝共聚的复合高吸水树脂,并研究其对亚甲基蓝吸附性能,可为染料废水处理提供参考。
1 实验部分
1.1 试剂与仪器
生物炭,自制(75%锯木屑、25%竹屑于700 ℃氮气氛围中炭化);丙烯酸(AA)、丙烯酰胺(AM)、N,N’-亚甲基双丙烯酰胺、(NH4)2S2O8、氢氧化钠、无水乙醇、盐酸、亚甲基蓝均为分析纯。
WHY-2水浴恒温振荡器;Spectrum Two红外光谱仪;SU-8100扫描电子显微镜;V-5000可见分光光度计。
1.2 BC-SA的制备
BC-SA的制备方法参考文献[13]。
1.3 吸附性能测试
1.3.1 不同pH对吸附性能的影响 在150 mL的锥形瓶中加入100 mL浓度为400 mg/L的MB 溶液,用HCl和NaOH溶液调节pH值(2~10),加入0.1 g BC-SA,于30 ℃下振荡24 h,用V-5000可见分光光度计在665 nm波长下测定MB浓度。MB吸附量计算公式如下:
Qe= (ρ0-ρe)V/W
(1)
式中Qe——MB吸附量,mg/g;
ρ0和ρe——吸附前后MB浓度,mg/L;
V——MB溶液的体积,L;
W——BC-SA的质量,g。
1.3.2 吸附温度和时间对吸附性能的影响 在100 mL浓度为400 mg/L的MB溶液中加入0.1 g BC-SA,于30,40,50 ℃下振荡,在预定时间取滤液,测定MB的浓度。
1.3.3 初始浓度对吸附性能的影响 在100 mL不同初始浓度的MB溶液中加入0.1 g BC-SA,于30 ℃下振荡24 h,测定吸附后溶液中MB浓度。
2 结果与讨论
2.1 pH值对吸附量的影响
溶液pH对吸附量的影响见图1。

图1 溶液pH对吸附量的影响Fig.1 Influence of pH on adsorption capacity

2.2 MB初始浓度对吸附量的影响
MB初始浓度对吸附量的影响见图2。

图2 MB初始浓度对吸附量的影响Fig.2 Influence of MB initial concentration on adsorption capacity
由图2可知,当MB初始浓度从100 mg/L增加至1 500 mg/L,BC-SA对MB的吸附量从99.3 mg/g增加至1 363.3 mg/g。MB浓度继续增大时,MB的吸附量增幅趋缓,在MB初始浓度为2 500 mg/g达到饱和,此时的吸附量高达1 748.5 mg/g。这是因为MB初始浓度较低时,BC-SA有较多的吸附位点,MB浓度增大使吸附量增加。随着MB浓度继续增大,BC-SA的吸附位点被MB占据,因而吸附量增加缓慢。当BC-SA的吸附位点被完全占据,吸附量不再增加。
2.3 吸附温度和时间对吸附量的影响
图3为30,40,50 ℃下BC-SA对MB的吸附量。

图3 吸附温度和时间对吸附量的影响Fig.3 Influence of temperature and time on adsorption capacity
由图3可知,吸附时间为0~40 min时,BC-SA对MB的吸附量迅速提高,吸附量分别增加至343.8,329.6,343.7 mg/g;而40~120 min,其对MB的吸附量呈缓慢上升趋势。120 min之后,吸附量基本保持不变,吸附量分别为392.3,389.3,391.1 mg/g。 提高吸附温度对MB的吸附量影响不大。
2.4 吸附等温线
分别采用Langmuir和Freundlich吸附等温式对实验数据拟合,表达式分别如(2)和(3)。
ρe/Qe=1/Q0Kb+ρe/Q0
(2)
lnQe=lnKf+(1/n)lnρe
(3)
式中Q0——理论吸附量,mg/g;
Kb和Kf——吸附平衡和吸附能力常数;
n——无量纲常数。
表1列出了BC-SA吸附MB的Langmuir和Freundlich拟合参数。

表1 BC-SA对MB吸附等温线参数Table 1 Adsorption isotherm parameters of MB for BC-SA
由表1可知,BC-SA吸附MB的Langmuir吸附等温式相关系数(R2=0.999 2)高于Freundlich吸附等温式,由Langmuir吸附模型计算得到的理论吸附量Q0为1 781.18 mg/g,与实验值很接近,表明 BC-SA吸附MB的吸附符合Langmuir吸附模型,为单分子层吸附。
2.5 吸附动力学
分别采用准一级动力学方程(4)和准二级动力学方程(5)对BC-SA吸附MB实验数据进行拟合分析:
ln(Qe-Qt)=lnQe-k1t
(4)
(5)
式中Qt——时间为t时的吸附量,mg/g;
k1和k2——准一级和准二级动力学方程速率常数。
表2为BC-SA吸附MB的动力学参数。

表2 BC-SA对MB吸附动力学参数Table 2 Kinetic parameters of MB for BC-SA
由表2可知,不同吸附温度下(30,40,50 ℃)BC-SA吸附MB的准二级动力学方程拟合的相关性系数(R2>0.999 0)远高于准一级动力学方程,且理论平衡吸附量Qe与实验值非常接近,表明BC-SA对MB的吸附过程用准二级动力学方程描述更为准确。
2.6 SEM分析
图4为BC-SA吸附MB前(A)后(B)的SEM图。

图4 BC-SA吸附MB前(A)后(B)的SEM图Fig.4 SEM images of BC-SA (A) and BC-SA saturated with MB solution (B)
由图4(A)可知,BC-SA表面为凹凸褶皱状,且具有很多大微孔和小毛细孔,有效增大BC-SA与MB的接触面积,从而提高了BC-SA对MB的吸附速率和吸附容量。由4(B)可知,BC-SA吸附MB后表面光滑、平整,孔隙结构消失,这表明BC-SA在MB溶液中完全溶胀,有利于对溶液中MB的吸附。
2.7 FTIR分析

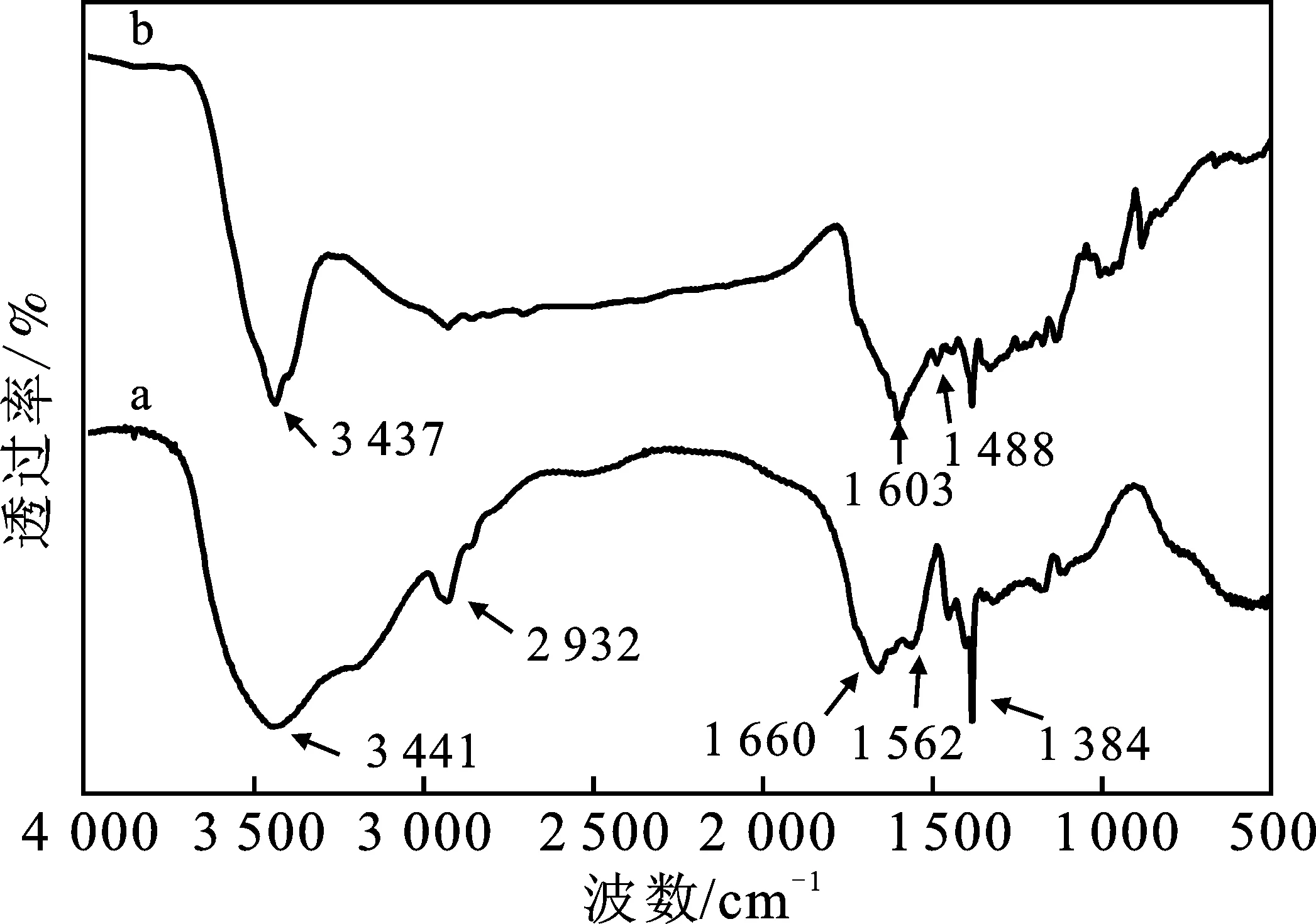
图5 BC-SA吸附MB前(a)后(b)的红外光谱图Fig.5 Infrared spectra of BC-SA before (a) and after (b) absorbing MB
2.8 BC-SA吸附MB的机理
图6为BC-SA吸附MB的机理。BC-SA对MB吸附机制主要是氢键、静电作用和离子交换等方式[16-18]。 BC-SA分子链有大量的—COONa基团,溶液中MB+与Na+进行交换,对MB进行吸附。也可能是BC-SA的—COOH与 MB分子中的S原子之间存在静电作用。BC-SA含有大量的羟基,可与MB分子中的N原子产生氢键。BC-SA分子链有大量的—CONH2,通过静电作用对MB形成吸附。
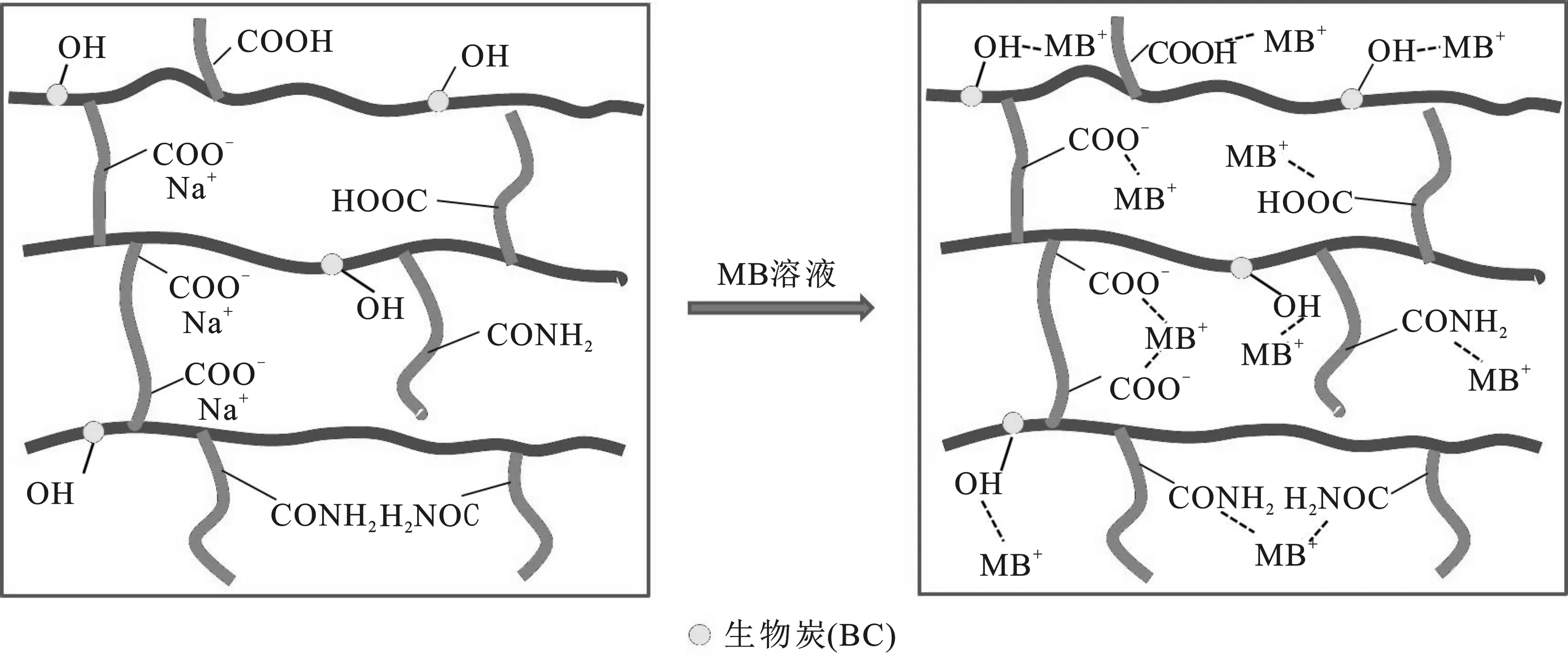
图6 BC-SA对MB的吸附机理Fig.6 Adsorption mechanisms of MB on BC-SA
3 结论
(1)BC-SA对MB的吸附受pH值、初始浓度、吸附时间和温度条件的影响。BC-SA吸附MB的适用pH为3~10。BC-SA吸附量随MB初始浓度的增加而增大,2 500 mg/L时达到最大,为1 748.5 mg/g。BC-SA对MB的吸附在120 min达到平衡。30~50 ℃ 范围内,温度对吸附量影响不大。
(2)BC-SA吸附MB符合Langmuir方程和准二级动力学方程。
(3)采用SEM和FTIR对吸附MB前后的BC-SA进行了表征,BC-SA表面褶皱,具有多孔结构,—OH,—COOH及—CONH2对MB吸附起主要作用。其通过氢键、静电作用和离子交换等方式吸附MB。
