老年血液透析患者认知衰弱现状及其影响因素分析
2021-02-08
(南华大学护理学院,湖南 衡阳 421000)
血液透析(HD)是目前终末期肾脏病患者重要的治疗方式之一。研究显示[1],至2014 年12 月31 日全国血液净化病例信息登记系统数据显示,在透患者为339748 例(年增长率为9.7%)。尿毒症、炎症、合并症、药物、饮食限制及抑郁引起的厌食症等原因,使维持性血液透析(MHD)患者能量摄入减少,骨骼肌质量、力量及功能降低,引起衰弱[2]。衰弱是一项复杂的老年综合征,严重影响老年人群的健康水平和生存质量。MHD 患者衰弱与认知功能障碍往往同时存在,且发生率较高[3]。认知衰弱即同时存在身体衰弱和认知损害的一种异质性临床表现[4]。认知衰弱人群跌倒发生率、失能率、入院、住院总费用及死亡率均较高,给社会和家庭带来了沉重的经济负担[5-7]。目前,社区老年人群及糖尿病患者认知衰弱研究较多,而针对老年MHD 人群的研究较少。本研究旨在探讨老年MHD 患者认知衰弱现状,分析其可能影响因素,为老年MHD 患者认知衰弱的防治提供依据。
1 对象与方法
1.1 研究对象 于2020 年5 月~7 月,对衡阳市3 所三级甲等医院的204 例老年血透患者进行问卷调查。患者知情同意。纳入标准:①年龄≥65 周岁;②血液透析≥3 个月,每次透析治疗时间3~4 h 患者;③意识清楚,无视力、听力障碍,能正确表达自己的意愿;④日常生活能力不受影响者。排除标准:①合并有阿尔兹海默症或其它神经系统疾病患者;②严重躯体功能障碍者。
1.2 方法 在血液净化中心医生和护士的协助下进行调查。医生主要负责评估认知功能,研究者负责问卷的发放。调查时征求患者同意后由调查员一对一询问和填写。
1.2.1 调查工具 ①一般情况调查表:自行设计,包括性别、年龄、受教育程度、婚姻状况、居住状态、付费方式、血透期、合并症个数、脑卒中病史等;②Fried衰弱表型量表:由Fried LP 等[8]于2001 年提出,包括体重下降、步速减慢、握力低、身体活动量低和疲乏5 项,每项1 分,得分范围为0~5 分,0 分为非衰弱,1~2 分为衰弱前期,≥3 分为衰弱。内容效度指数为0.98,克朗巴赫系数(Cronbach's α)为0.93[9]。③长沙版蒙特利尔认知评估量表(MoCA):靳慧[10]于2011 年修订形成,包括视空间/执行功能、命名、记忆、注意、语言、抽象、延迟回忆及定向8 个认知功能域,共28 个条目,总分为30 分,受教育年限≤6 年者加1 分,<26 分提示认知功能障碍,得分越高,认知功能越好。灵敏度和特异度分别为90.6%和70.9%,克朗巴赫系数(Cronbach's α)为0.846[11];④抑郁自评量表(SDS):W.K.Zung 等于1965 年编制,由20 个条目组成,每个条目为1~4 分,抑郁严重程度指数=题目累计分/80,抑郁严重程度指数在0.50以下者为无抑郁,0.50~0.59 为轻度抑郁,0.60~0.69为中度抑郁,0.70 及以上为重度抑郁;⑤临床痴呆评定量表(CDR):由临床专业人员对可疑患者进行痴呆诊断与痴呆程度的评估,量表内容包括记忆力、定向力、判断与解决能力、社会事务能力、家务与业余爱好、个人自理能力6 项,划分标准为:认知正常0分、可能痴呆0.5 分、轻度痴呆1 分、中度痴呆2 分、重度痴呆3 分,指南推荐,0.5 分是MCI 的主要诊断标准之一[12]。
1.2.2 认知衰弱界定标准 参考国际协会共识[12],本研究中认知衰弱的筛查方法为:①Fried 衰弱表型量表得分≥3 分;②MoCA 得分<26 分;③主观感觉或家属诉说老年人认知功能减退;④CDR=0.5 分。
1.3 统计学方法 应用SPSS 22.0 软件对资料进行统计分析,计量资料采用()表示,计数资料采用(%)表述,单因素分析采用χ2检验。采用二元Logistic 回归分析老年MHD 患者认知衰弱发生的危险因素,检验水准α=0.05。
2 结果
2.1 老年MHD 患者认知衰弱发生情况 本研究共调查215 例患者,204 例调查问卷合格有效,有效率94.88%。204 例MHD 患者中,有42 例发生认知衰弱,认知衰弱发生率为20.58%。
2.2 老年MHD 患者认知衰弱单因素分析 结果显示,不同年龄、脑卒中病史、合并症数量及抑郁严重程度的老年维持性血液透析患者认知衰弱比较,差异有统计学意义(P<0.05),见表1。
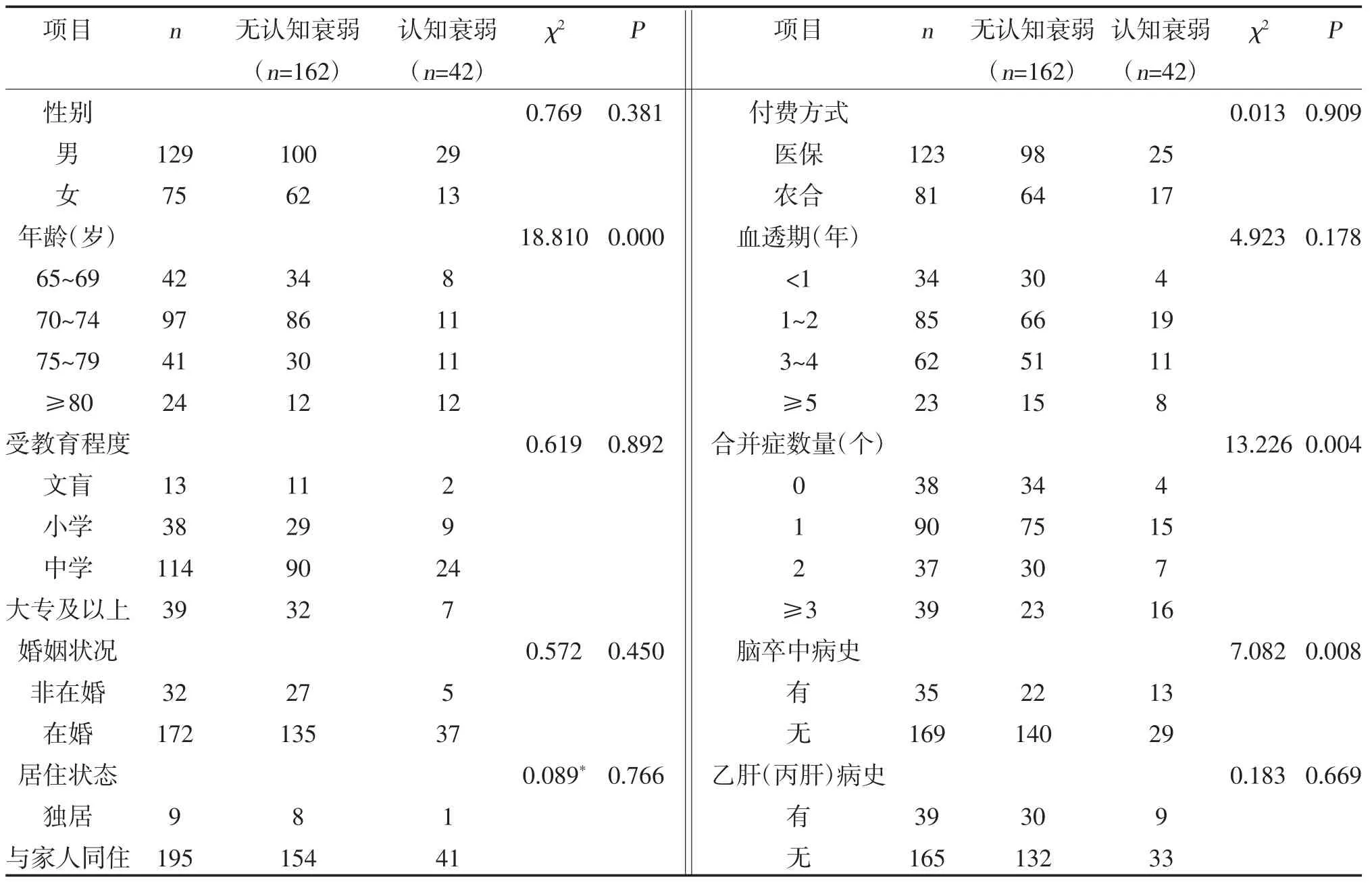
表1 老年维持性血液透析患者认知衰弱单因素分析(n)

表1 (续)
2.3 老年MHD 患者认知衰弱多因素分析 以是否发生认知衰弱为因变量,将单因素分析中差异有统计学意义的变量为自变量,进行Logistic 回归分析,α入=0.05,α出=0.10,对各变量进行赋值,年龄(0=65~69 岁,1=70~74 岁,2=75~79 岁,3=≥80 岁),合并症个数(0=0 个,1=1 个,2=2 个,3=≥3 个以上),脑卒中病史(0=无,1=有),抑郁(0=无,1=轻度抑郁,2=中度抑郁,3=重度抑郁),所有参照组均为最低赋值组。结果表明,高龄、合并症个数多、有脑卒中病史及抑郁是认知衰弱发生的独立危险因素,见表2。

表2 老年维持性血液透析患者认知衰弱多因素分析
3 讨论
3.1 老年MHD 患者认知衰弱发生率较高 本研究结果显示,老年MHD 患者认知衰弱发生率为20.58%,与蒋婷婷等[13]结果相似,而高于潘利妞等[14]研究,可能与纳入研究对象及样本量不同有关,本研究对象为老年MHD 患者,长期炎症状态、毒素累积、血管系统损害、磷酸盐的摄入减少、代谢性酸中毒导致蛋白质分解代谢及系列并发症等,导致血透患者身体机能减退,衰弱及认知功能障碍发生率更高。慢性肾脏病患者生长激素缺乏及活性降低,容易诱发肌肉萎缩,肌肉质量减少,影响步行能力,导致增加了患者衰弱的风险。研究显示[15],与非衰弱且不患有认知障碍的人群相比,有衰弱且患有认知障碍的人群,其生存率更低。认知衰弱对失能、再入院、死亡有重要预测作用,因此,透析中心医务人员应重视老年MHD 患者认知衰弱的早期识别,控制可能危险因素,避免认知衰弱的发生。
3.2 老年MHD 患者认知衰弱影响因素分析
3.2.1 高龄 本研究结果显示,高龄是MHD 患者认知衰弱发生的独立预测因子,年龄≥80 岁患者认知衰弱发生率是年龄65~70 岁患者的3.873 倍,与张爽等[16]研究结果相似。随着年龄增长,大脑重量下降速度不断增加,脑组织逐渐萎缩[16],而衰弱及认知功能都与年龄相关的衰退周期存在相互作用[17],身体衰退及脑老化常常同时进行,促进认知衰弱的发生。随着年龄层级的增长,认知衰弱的患病率也呈现出递增趋势。马来西亚一项研究也指出,年龄每增加1岁,成年人中认知衰弱的发生几率就会增加[17]。这提示医务人员应重视高龄MHD 患者认知衰弱的发生,及时采取预防措施,如加强营养、适当体育锻炼及丰富社交生活等。
3.2.2 脑卒中史 本研究结果显示,有脑卒中病史是老年MHD 患者认知衰弱发生的独立风险因素,且有脑卒中病史患者认知衰弱发生率是没有脑卒中病史患者的2.949 倍。分析原因,一方面可能是因为脑卒中发生后,脑血管的急性改变,导致脑细胞部分死亡、内皮功能障碍、脑白质损害等常常影响患者执行能力,另一方面,可能是因为疾病后期,部分患者伴随肢体不协调、言语不清等后遗症,使得患者认知衰弱发生率增加[18]。
3.2.3 合并症多 本研究结果显示,不同合并症个数老年MHD 患者认知衰弱患病率之间有差别(P<0.05),合并3 种及3 种以上的老年血透患者认知衰弱患病率是无合并症患者的4.207 倍,提示合并症数目越多,越容易患认知衰弱,与王凌霄等[19]研究一致。慢性肾脏病患者多病共存现象较为常见,心血管系统疾病、水钠储留、睡眠障碍等长期慢性并发症导致血透患者躯体不适、营养缺乏,使得骨骼肌质量及数量下降,诱发认知衰弱的发生。此外,并发症可能会使机体生理储备下降和抗应激能力减退,导致稳态失衡或衰弱[20]。
3.2.4 抑郁 本研究结果显示,中度及重度抑郁的老年MHD 患者认知衰弱患病率分别是无抑郁血透患者的2.936、4.540 倍,提示抑郁水平与老年MHD 患者认知衰弱发生相关,与孔令磷等[21]研究结果一致。抑郁情绪可能降低个人参与社会活动的愿望,无法建立必要的社会支持系统,从而增加老年人认知衰弱的风险[22]。相比于长期处在抑郁状态的患者,通过增加社会活动、积极治疗而改善的衰弱患者其死亡率较低[23]。长期抑郁不仅带给患者精神上的痛苦,更会使他们产生极大的疲劳感。抑郁症状与衰弱存在梯度效应,不同程度抑郁症状均与衰弱相关,所以医务工作者,不仅要针对有明显抑郁症的老年人采取干预措施,而且还要以整个人群为基础改善老年人抑郁症状,从总体上显著减低衰弱的发生风险[24]。
综上所述,老年维持性血液透析患者认知衰弱发生率较高,高龄、有脑卒中病史、存在3 种及3 种以上并发症及抑郁是其发生的独立危险因素。因此,医务人员应重视老年血液透析患者认知衰弱的早期筛查,可针对相关危险因素采取干预措施,从而减少或延缓认知衰弱。本研究纳入的影响因素有限,可能低估了其他因素对认知衰弱的影响,且需要开展大样本前瞻性研究以进一步探讨其影响因素,为制定有效的干预方案提供更科学的证据。
