基于UPLC-Q-TOF-MS技术的芪风固表颗粒血清药物化学研究
2021-02-03郑单单魏文峰霍金海王伟明
郑单单,魏文峰,霍金海,王伟明
黑龙江省中医药科学院,黑龙江 哈尔滨 150036
芪风固表颗粒是黑龙江省中医药科学院自主研发的中药新药(发明专利号:CN1325098C,批准文号:国药准字B20020410),该药由黄芪、麦冬、防风、刺五加、炒白术、五味子6 味中药组成,具有益肺、健脾、补肾、益卫固表、补气生津的功效,是治疗表虚不固易感病症有效方剂。文献报道表明,芪风固表颗粒能止咳化痰,延长咳嗽潜伏期,又能缓解气管炎症,抑制肺组织病变,改善和治疗支气管炎和肺炎,减少肺部炎症发作,能调节免疫功能,使机体免疫系统恢复到平衡状态[1-4]。芪风固表颗粒的药理作用已有初步研究,然而其药效物质基础尚未完全阐明。
中药方剂成分复杂,口服给药后,有效成分被直接吸收入血,或转化为代谢产物被吸收入血。通过中药血清药物化学研究可以确立中药中的有效成分,以此为指标建立定性、定量方法,从而使中药及中药复方质量标准化[5]。本研究利用中药血清药物化学方法初步研究芪风固表颗粒的入血成分,旨在明确其药效物质基础,进一步锁定建立芪风固表颗粒质量标准化相关指标。
1 仪器与材料
1.1 仪器
Waters ACQUITYTMUPLC 液相色谱仪(美国Waters 公司);AB Sciex 5600+型质谱仪、Analyst TF1.6 工作站(美国Sciex 公司);PeakView 2.0 软件、Metabolite pilot 2.0.2 软件(美国Sciex 公司);IKAMS3 digital 涡旋振荡器(广州仪科实验室技术有限公司);ST16R 型低温高速离心机(美国Thermofisher Scientific 公司);MTN-2800W 氮吹浓缩装置(天津奥特赛恩斯仪器有限公司)。
1.2 试剂与药品
黄芪(批号20180909)、防风(批号DC1111)、麸炒白术(批号180602)、麦冬(批号180501)、五味子(批号20180325)、刺五加(批号20171121)以上6 味饮片均购于北京同仁堂(亳州)饮片有限责任公司,经黑龙江省中医药科学院霍金海副研究员鉴定,黄芪为豆科植物蒙古黄芪Astragalus membranaceus(Fisch.) Bge.var.mongholicus(Bge.)Hsiao 的干燥根;防风为伞形科植物防风Saposhnikovia di varicate(Turcz.) Schischk.的干燥根;麸炒白术为菊科植物白术Atractylodes macrocephalaKoidz.的干燥根茎蜜制麸皮炒制品;麦冬为百合科植物麦冬Ophiopogon j aponicus(L.f)Ker-GawL 的干燥块根;五味子为木兰科植物五味子Schisandra chinensis(Turcz.) Baill.的干燥成熟果实;刺五加为五加科植物刺五加Acanthopanax s enticosus(Rupr.et Maxim.) Harms 的干燥根和根茎或茎。
对照品升麻素苷(批号S-004-150421)、升麻素(批号 S-007-170426)、鲁斯可皂苷元(批号L-009-171026)、芒柄花素(批号C-018-140128)均购于成都瑞芬思生物科技有限公司,质量分数>98%。刺五加按《中国药典》2015年版“刺五加水浸膏制备方法”制成刺五加浸膏。甲醇和乙腈(色谱级,Merck 公司);甲酸(色谱级,Fisher 公司);蒸馏水(广州屈臣氏食品饮料有限公司)。
1.3 实验动物
健康SD 雄性大鼠,体质量(240±20)g,SPF级,许可证号SCXK(黑)2019-001,由哈尔滨医科大学动物实验中心提供。该实验由黑龙江省中医药科学院动物伦理委员会批准,批准号:201903001。
2 实验方法
2.1 芪风固表颗粒供试品的制备
按照2020 版《中国药典》[6]规定,取黄芪3000 g、白术(炒)1000 g、五味子500 g,防风1000 g、麦冬1000 g,加水煎煮2 次,煮沸起开始计时,每次1 h,合并煎液,离心,滤过,静置24 h,倾取上清液,加入刺五加浸膏75 g,浓缩至相对密度1.20~1.22(60 ℃)的清膏,趁热加入糊精适量,混匀,60 ℃干燥,粉碎成细粉,加乙醇适量制粒,干燥。按《标准》的1/20 用药量以上述方法,制备芪风固表颗粒供试品。
2.2 供试品溶液的制备
取供试品芪风固表颗粒粉末约3 g,精密称定,置具塞锥形瓶中,加入50%甲醇水30 mL,密塞,称定重量,超声处理50 min,放冷至室温,用50%甲醇水补足减失的质量后摇匀,5000 r/min 离心10 min,取上清液,过0.22 μm 微孔滤膜,即得。
2.3 药液的制备
取芪风固表颗粒供试品,加适量蒸馏水超声溶解,配制成质量浓度1.08 g/mL 的芪风固表颗粒大鼠ig 药液,储存至4 ℃冰箱中,备用。
2.4 体内分析样品的制备
取SD 大鼠,禁食12 h(自由饮水),给药组按照9.0 g/kg(相当于人体临床每日10 倍剂量)ig 给予芪风固表颗粒ig 药液,空白组按照20.0 mL/kg ig给予蒸馏水。给药1 h 后,ip 10%水合氯醛进行麻醉,腹主动脉取血,3000 r/min 离心10 min,取上清液,-80 ℃冻存备用。
取大鼠空白血清及给药血清各1.2 mL,各加4.8 mL 甲醇,3000 r/min 涡旋震荡90 s,4 ℃、13 000 r/min 离心10 min,取上清液,氮气挥干,残渣用150 μL 70%甲醇复溶,3000 r/min 涡旋震荡90 s,4 ℃、13 000 r/min 离心10 min,取上清液,进样3 μL 供UPLC-Q-TOF-MS 分析。
2.5 质谱条件
电喷雾正、负离子模式,正、负离子源电压分别为5500 V、-4500 V,离子源温度为550 ℃,雾化气体为N2,雾化气、辅助气压力均为379.2 kPa,气帘气压力为241.3 kPa,裂解电压为±80 V,碰撞能量为±35 eV,碰撞能量扩展均为15 eV。TOF/MS 扫描范围为m/z100~1500,IDA 设置响应值超过100 cps的8个最高峰进行二级质谱扫描,Product Ion 扫描范围为m/z50~1500,开启动态背景扣除(DBS)。数据采集所用软件为Analyst TF 1.6 software,数据处理软件为Peakview 2.0-masterview 1.0。
2.6 色谱条件
Waters ACQUITYTMUPLC 液相色谱仪;ACQUITYTMBEH C18色谱柱(100 mm×2.1 mm,1.7 μm);ACQUITYTMUPLC BEH C18预柱(5 mm×2.1 mm,1.7 μm);柱温35 ℃;流动相0.1%甲酸水溶液(A)-0.1%甲酸乙腈(B);梯度洗脱:0→15 min,95%→50% A;15→18 min,50%→0 A;18→18.1 min,0→95% A;18.1→20 min,95% A。体积流量0.3 mL/min;样品仓温度4 ℃;进样量8 μL;色谱仪流出液不分流直接进行正、负离子扫描检测。
2.7 数据分析方法
利用Peakview 软件通过对比给药后血清和空白血清的质谱图,扣除血清中的内源性成分,将剩余离子峰与体外药材提取液离子峰的保留时间、质荷比及二级质谱图进行对比,如果一致则确认为芪风固表颗粒中的原型成分;利用MetabolitePilot 数据处理软件,导入化合物信息建立 Compound library,设置Biotransformation parameters,选择I和II 相代谢途径,设置Processing parameter,将空白血清及给药血清样品导入,筛选代谢产物,根据软件数据结果和参考文献资料推测其代谢产物。

图1 正离子和负离子模式下的总离子流图Fig.1 Total ion current chormatograms in positive and negative ion mode
3 结果
3.1 UPLC-Q-TOF-MS 色谱图的采集
依据“2.5”项质谱条件及“2.6”项色谱条件分析样本,在正、负离子模式下采集以上样品的色谱图,见图1。
3.2 入血成分分析
本课题组前期已经应用UPLC-Q-TOF-MS 技术对芪风固表颗粒的化学成分进行了分析,在分析过程中根据精确相对分子质量、同位素丰度比、分子碎片峰,参考相关文献、对照品色谱保留时间及二级谱图,共推断了110 个化合物,其中22 个来自黄芪,13 个来自防风,6 个来自白术,10 个来自麦冬,21 个来自五味子,14 个来自刺五加。本实验在此基础上根据“2.7”项下方法,结合以往文献报道[7-11],并参照对照品二级色谱图,鉴定了大鼠口服芪风固表颗粒后血清中的37 个入血成分,其中17 个为原型成分,20 个为代谢产物,并对其来源进行了归属,结果见表1。
3.3 主要色谱峰的质谱分析
3.3.1 原型成分 共鉴定和表征出17 个原型成分,分别以化合物3、9 为例说明推测过程。
化合物3:正离子模式下,其在含药血清总离子图与芪风固表颗粒总离子流图中升麻素的保留时间基本一致,二级质谱碎片一致,准分子离子峰m/z307 [M+H]+相对丰度最强,拥有共同二级碎片m/z289、259、235 等,见图2,参考文献报道[7],对比升麻素对照品的二级质谱图,故推测其结构为升麻素,可能的裂解途径见图3。
化合物9:正离子模式下,其与芪风固表颗粒总离子流图中鲁斯可皂苷元的保留时间基本一致,二级质谱碎片一致,准分子离子峰m/z431 [M+H]+相对丰度较强,拥有共同二级碎片m/z395、269 等,见图4,参考文献报道[8],对比鲁斯可皂苷元对照品的二级质谱图,故推测其结构为鲁斯可皂苷元,可能的裂解途径见图5。
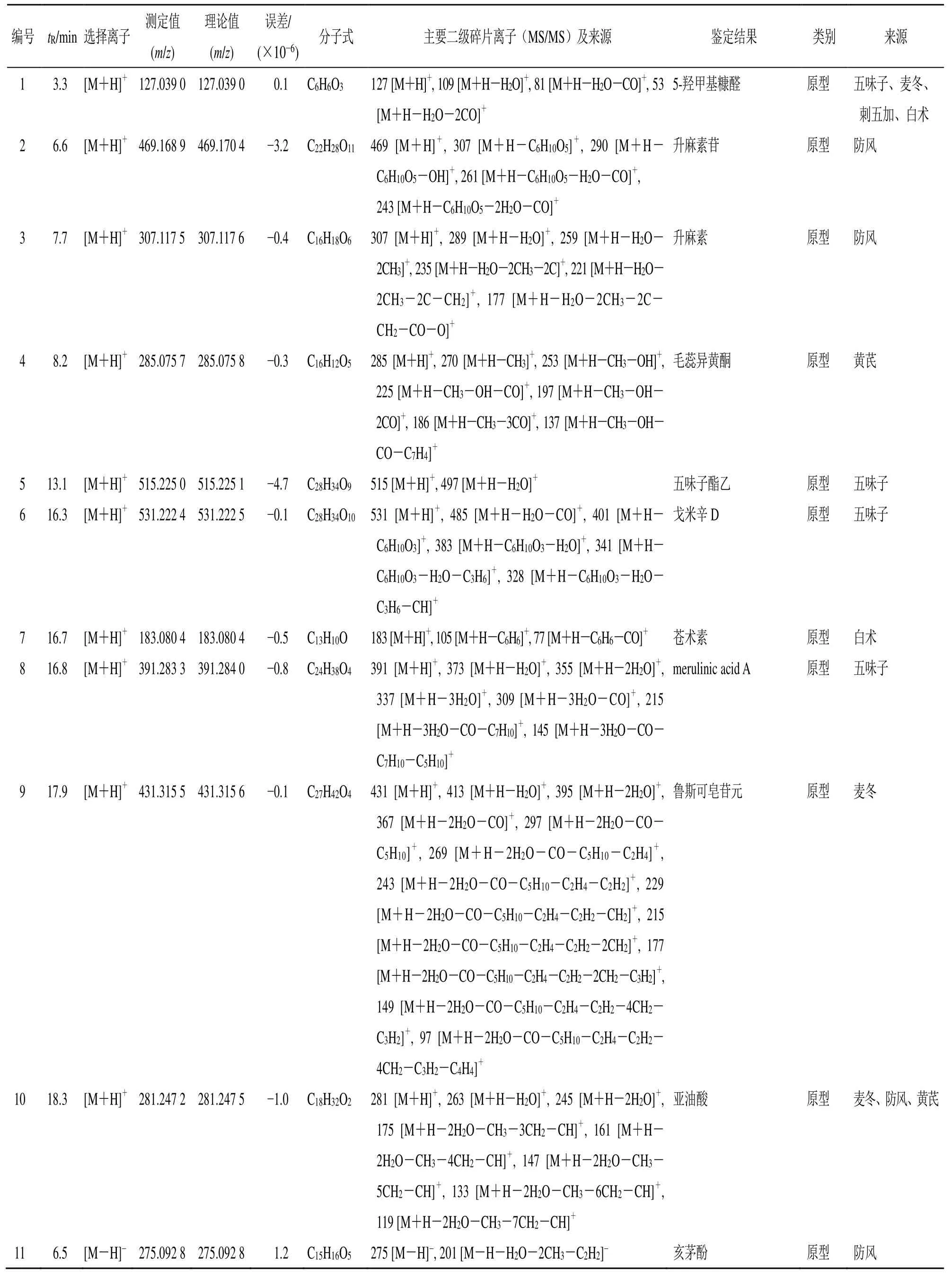
表1 芪风固表颗粒入血成分分析结果Table 1 Chemical composition analysis results of Qifeng Gubiao Granules
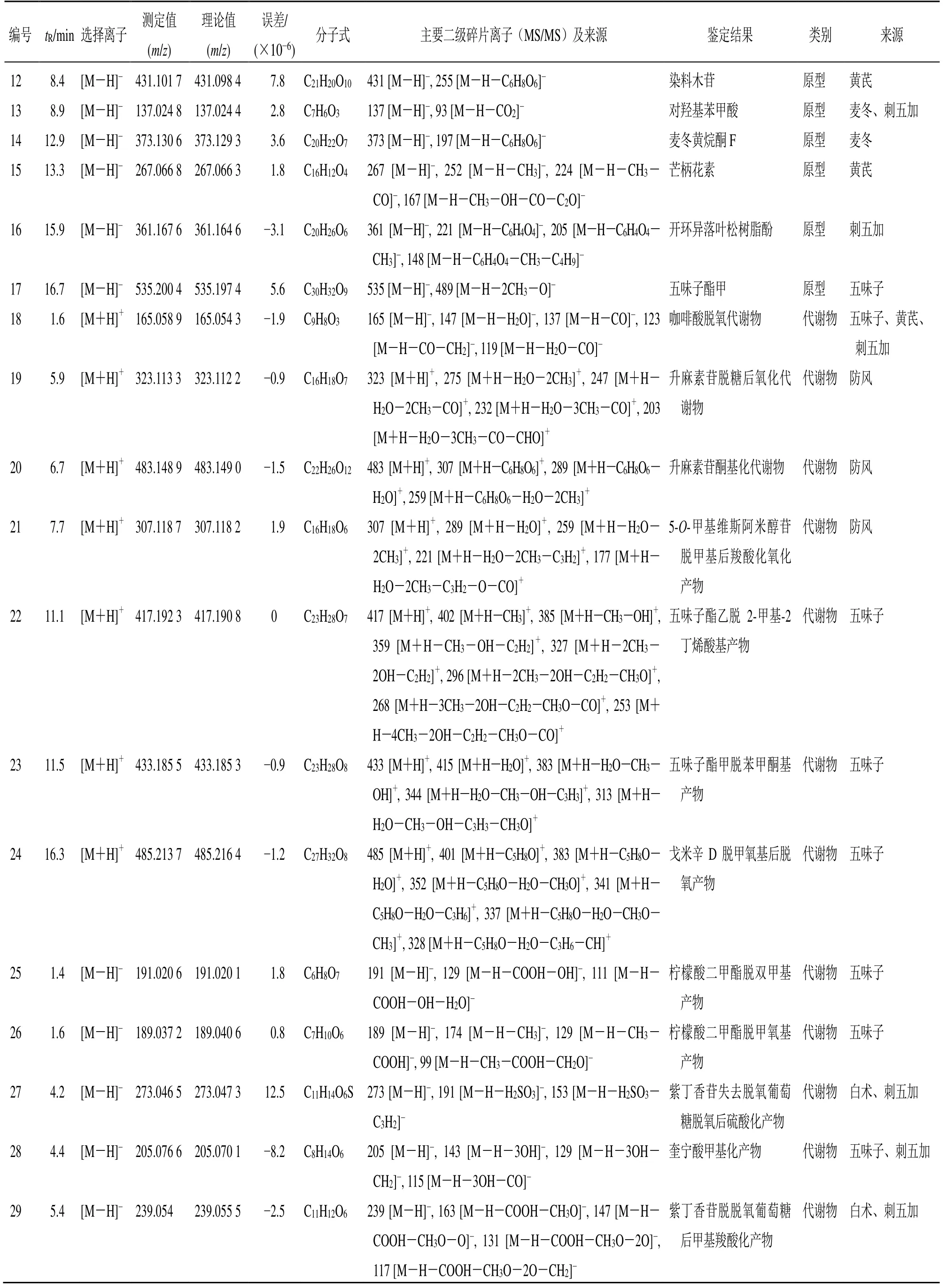
续表1
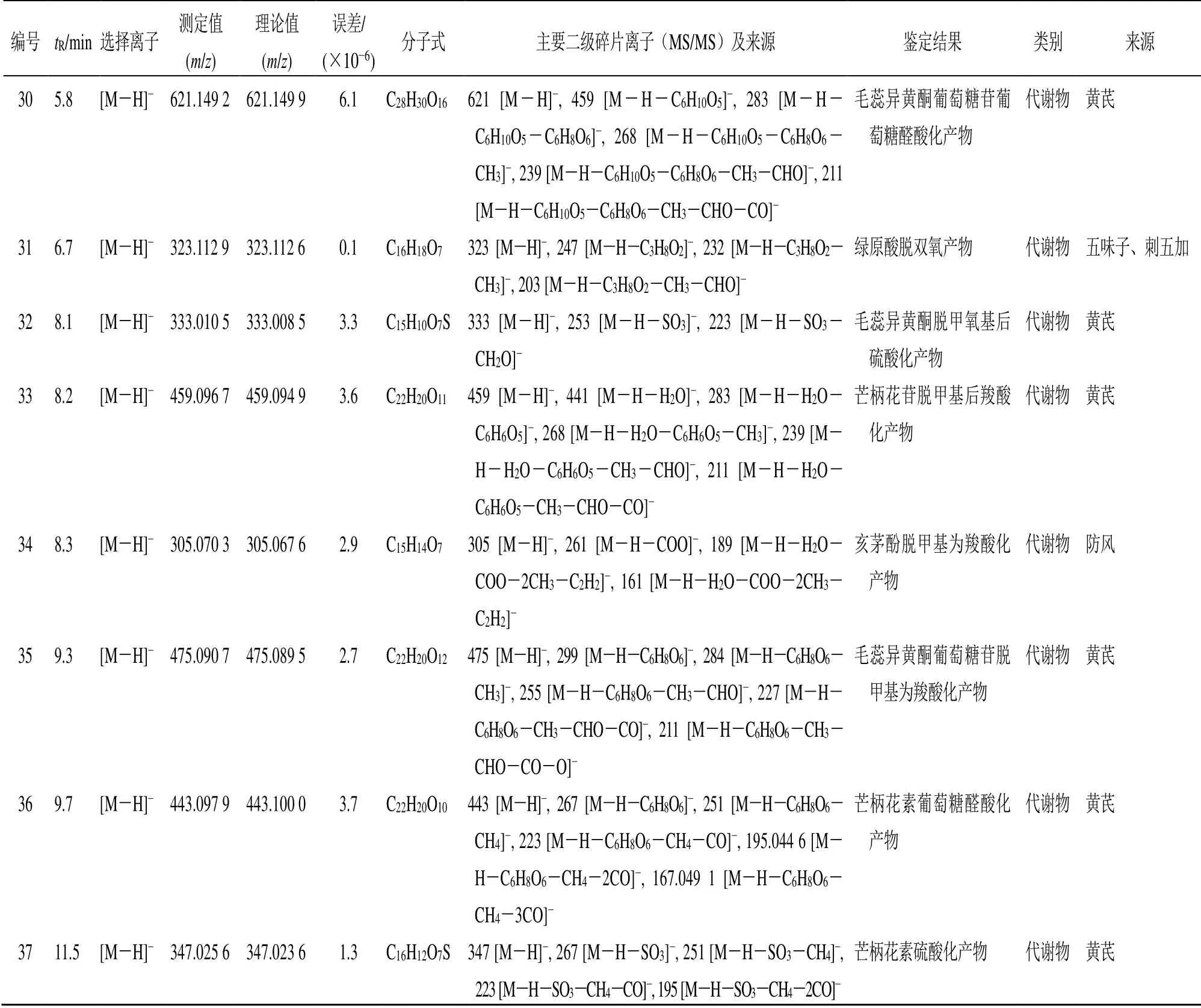
续表1
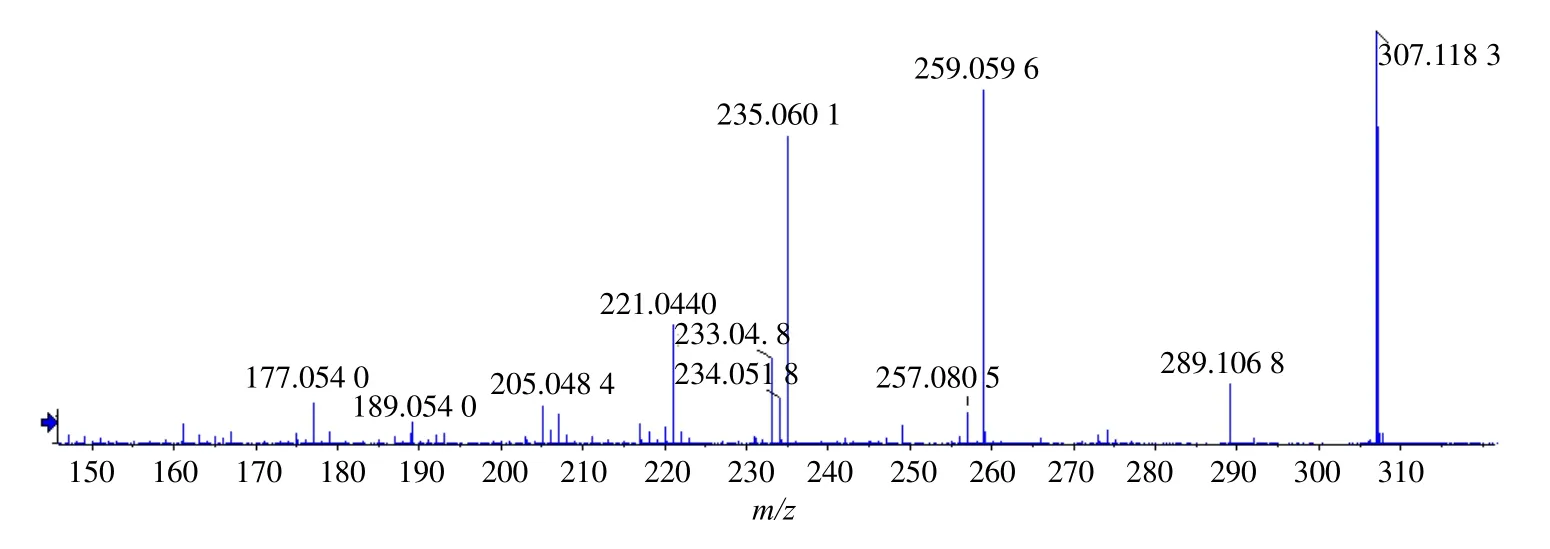
图2 升麻素正离子模式下的MS/MS 质谱图Fig.2 MS/MS mass spectrum of atractylodin in a positive mode
3.3.2 代谢产物 根据“2.7”项下方法结合Metabolite Pilot 代谢物数据处理软件给出的代谢物最优化峰匹配,最终推测20 个代谢产物,以化合物27、36 为例说明鉴定过程。
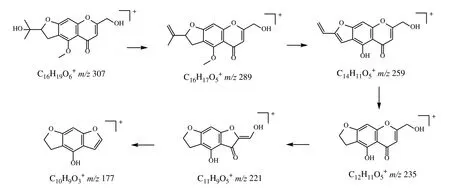
图3 推测的升麻素裂解途径Fig.3 Speculative cleavage pathway of atractylodin

图4 鲁斯可皂苷元正离子模式下的MS/MS 质谱图Fig.4 MS/MS mass spectrum of ruscogen in positive mode
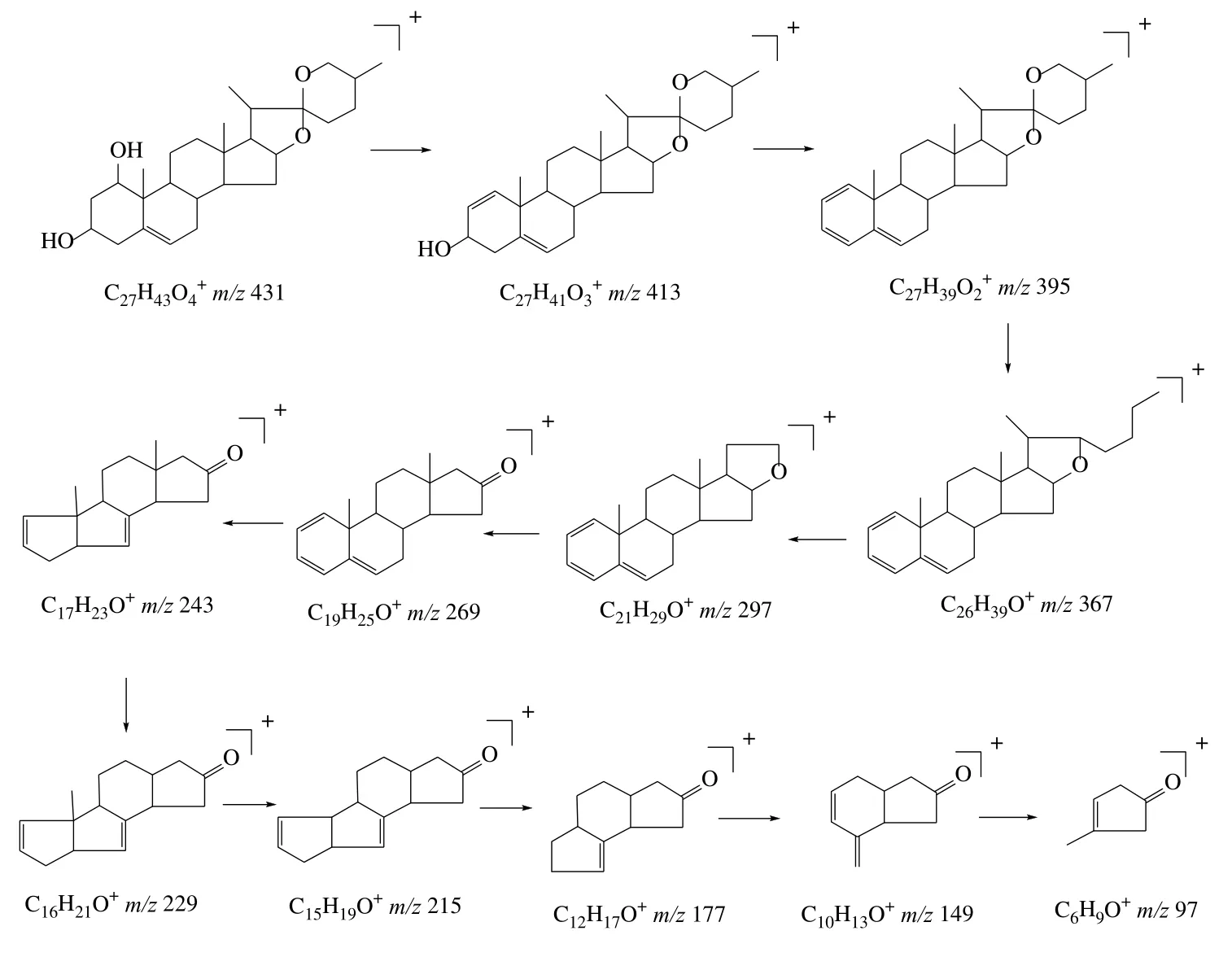
图5 推测的鲁斯可皂苷元裂解途径Fig.5 Speculative cleavage pathway of ruscogen
化合物27:刺五加中的刺五加苷类成分是其主要活性部位,紫丁香苷是主要成分之一。紫丁香苷是苯丙醇的苷类化合物,该化合物在体内发生I 相水解反应,失去脱氧葡萄糖水解为苷元,其苷元脱氧后苯环上的羟基发生硫酸酯化,形成硫酸酯化代谢产物。代谢物在负离子模式下,准分子离子峰m/z273 [M-H]-,比紫丁香苷准分子离子峰m/z371 [MH]-少98,提示其失去脱氧葡萄糖脱氧后硫酸酯化,结合碎片m/z191、153 等,与紫丁香苷二级碎片比较,符合其裂解过程,结合文献报道[9],紫丁香苷苷元苯环上的羟基可能发生硫酸酯化。紫丁香苷失去脱氧葡萄糖脱氧后硫酸酯化产物和紫丁香苷在负离子模式下的质谱匹配度见图6,可能的裂解途径见图7。
化合物36:芒柄花素是来自黄芪的黄酮类化合物,易发生II 相代谢反应,A 环7 位羟基发生葡萄糖醛酸化,生成芒柄花素葡萄糖醛酸化产物。该产物在负离子模式下,准分子离子峰m/z443 [MH]-,比异微凸剑叶莎醇准分子离子峰m/z301 [MH]-多142,表明化合物发生葡萄糖醛酸化,结合其特征碎片m/z267、251、223 等,与芒柄花素二级碎片比较,符合其葡萄糖醛酸化过程,参考文献报道[10-11],芒柄花素A 环7 位羟基易发生葡萄糖醛酸化,同时芒柄花苷在大鼠体内发生I 相代谢水解后,生成芒柄花素,亦可能有相同代谢产物。芒柄花素葡萄糖醛酸化产物和芒柄花素在负离子模式下的质谱匹配度见图8,推测的裂解途径见图9。
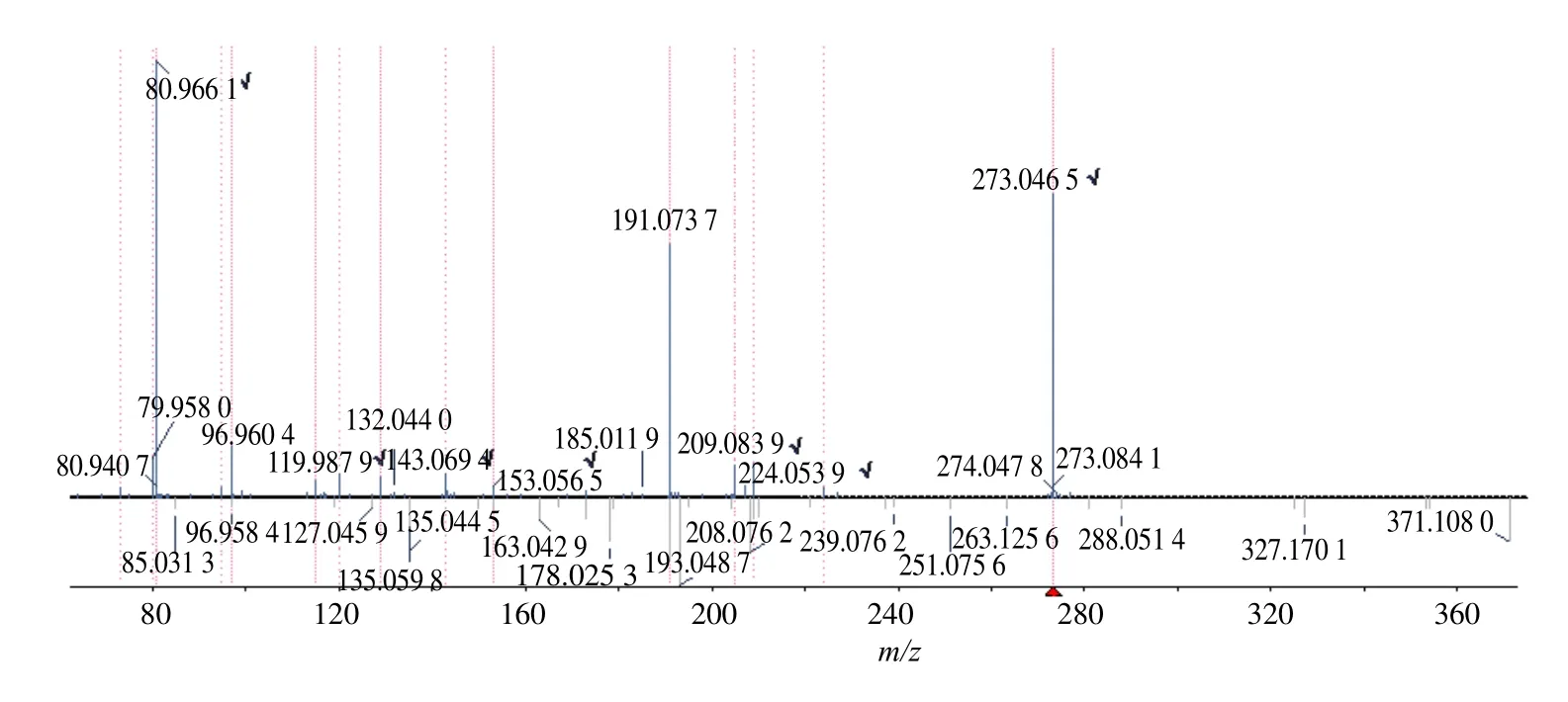
图6 紫丁香苷失去脱氧葡萄糖脱氧后硫酸酯化产物和紫丁香苷负离子模式下的质谱图Fig.6 Mass spectra of sulphate conjugation after lost deoxyglucose and oxygen of syringin in negative mode
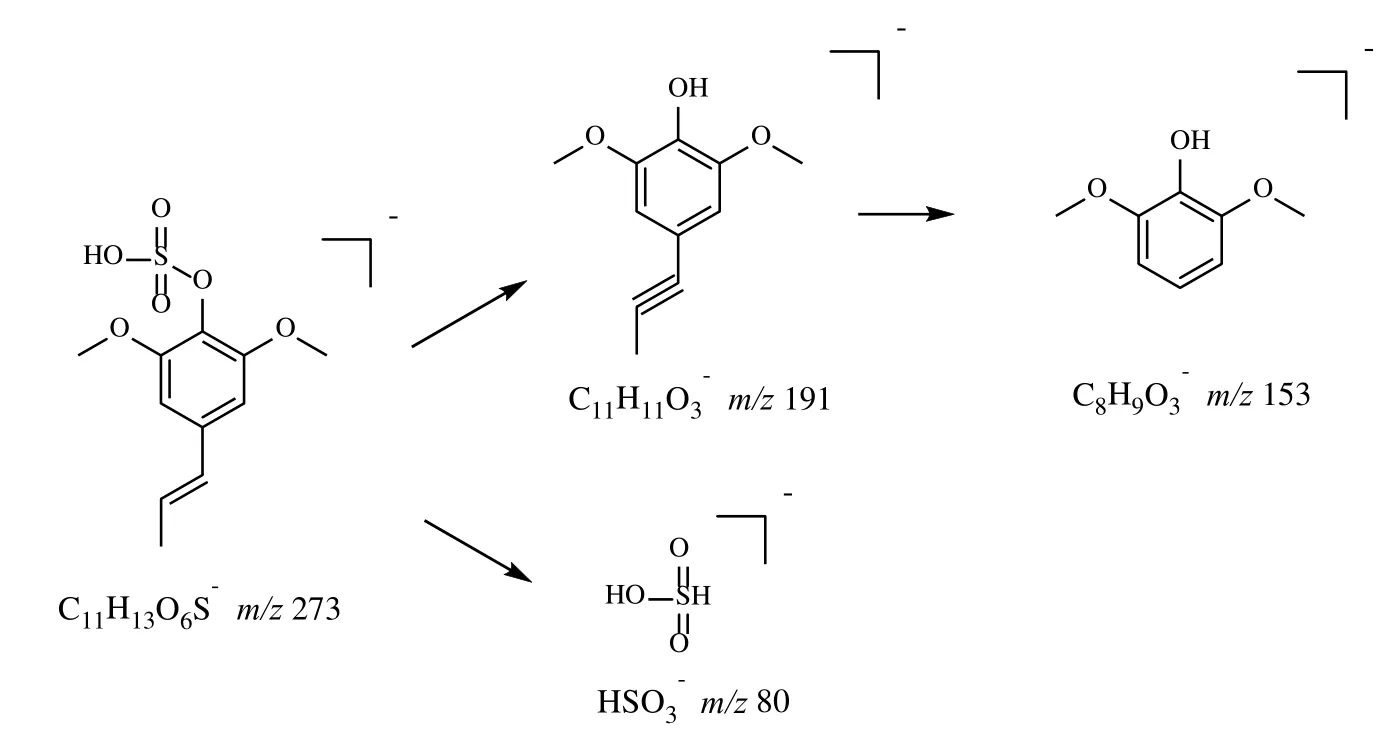
图7 推测的紫丁香苷失去脱氧葡萄糖脱氧后硫酸酯化产物裂解途径Fig.7 Speculative cleavage pathway of sulphate conjugation after lost deoxyglucose and oxygen of syringin
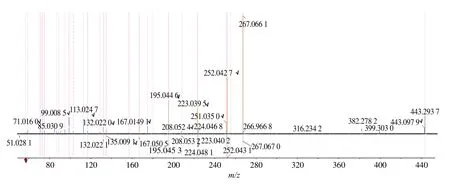
图8 芒柄花素葡萄糖醛酸化产物和芒柄花素在负离子模式下的质谱图Fig.8 Mass spectra of glucuronidation of formononetin in negative mode

图9 推测的芒柄花素葡萄糖醛酸化产物裂解途径Fig.9 Speculative cleavage pathway of glucuronidation of formononetin
4 讨论
本实验在取血方式上,选取腹主动脉取血,腹主动脉取血的取血量较大,更适合用于后续的样品制备。在样品处理方法上,比较了甲醇沉淀法、固定相萃取-甲醇洗脱法2 种血清处理方法,结果显示,甲醇沉淀法检测到的血中移行成分较多,故选择甲醇沉淀法作为血清最佳处理方法。在釆血时间上考察了0、0.5、1、2、4、8、12、24 h 共8 个不同时间点,结果在给药1 h 后采血所检测的色谱峰数目最多、响应值最强,故选择给药1 h 后采血为最佳采血时间点。
在大鼠ig 芪风固表颗粒ig 药液后的含药血清中共鉴定出37 个入血成分,包括17 个原型成分,20 个代谢产物。其中来自黄芪的多为黄酮类成分,黄芪中的芒柄花素及其苷类、毛蕊异黄酮及其苷类等黄酮类成分,能抗病毒[12],改善肺纤维化肺功能[13],还能通过降低模型动物的脾细胞辅助T 细胞1/辅助T 细胞2(T helper 1 cell/T helper 2 cell,Th1/Th2)和高细胞增殖活性等改善其机体免疫功能失调,又能增强机体的耐力[14]。防风的主要成分升麻素等色原酮及其苷类,具有解热抗炎[15]作用。刺五加中的紫丁香苷等刺五加苷类[16]及有机酸类等成分,可能具有抗疲劳[17],调节免疫功能等多重作用。五味子具有免疫调节作用[18]。麦冬中的主要皂苷元鲁斯可皂苷元具有抗炎作用,马丽等[19]通过体外实验发现,鲁斯可皂苷元可显著抑制细胞因子肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)诱导的急髓白血病HL-60 细胞与人脐静脉内皮ECV304 细胞之间的黏附作用,从而发挥抗炎活性。结合各味药传统功效及现代药理学研究,初步可以推断,本次实验分析所得入血的37 种成分可能为其体内发挥作用的药效物质基础。
实验中运用中药血清药物化学方法及UPLC-Q-TOF-MS 技术,简单、快捷分析了中药复方芪风固表颗粒中的入血成分,初步探究了该方的药效物质基础,进一步锁定其质量控制指标性成分,为其质量标准的提升研究提供依据,为传统品种的二次开发提供了良好的参考依据。
利益冲突所有作者均声明不存在利益冲突
