不同温度下恩诺沙星在克氏原螯虾体内的药代动力学
2021-02-02王欢许荔立陈孝煊袁军法田丁蒋飞吴志新
王欢,许荔立,陈孝煊,3,袁军法,田丁,蒋飞,吴志新,3
1.华中农业大学水产学院,武汉 430070; 2.湖北省水生动物病害防控工程技术研究中心,武汉430070;3.水产养殖国家级实验教学示范中心(华中农业大学),武汉 430070
克氏原螯虾(Procambarusclarkii)具有分布广泛、适应力强、繁殖力高等特点,在我国部分湿地形成自然种群[1],是我国重要的淡水养殖品种之一。2018年克氏原螯虾经济总产值已达3 690亿元,养殖密度的提高以及养殖水体污染等原因,导致克氏原螯虾疾病频发。副溶血性弧菌(Vibrioparahaemolyticus)、嗜水气单胞菌(Aeromonashydrophila)、拟态弧菌(Vibriomimicus)等细菌性病原被认为是造成螯虾某养殖业经济损失的原因之一[2-4]。
恩诺沙星enrofloxacin(ENR)作为人工合成的广谱抗菌药,具有对细菌选择性高,口服给药迅速,生物利用度高,半衰期较长,血药浓度、毒副作用小等特点应用于兽医临床,预防和治疗多种细菌和支原体感染,在临床治疗中已成为很多感染性疾病的首选药物,使用频率仅次于青霉素类[5]。
国内外学者采用不同的给药方式,研究了恩诺沙星在水生动物中的药物动力学及残留特征,如银鲫(Carassiusauratusgibelio)(肌肉注射)[6]、大菱鲆(Scophthalmusmaximus)(静脉注射和口灌)[7]、拟穴青蟹(Scyllaparamamosain)(肌肉注射和口灌)[8]、大西洋马蹄蟹(Limuluspolyphemus)(围心窦注射)[9]等。本研究分析了在18 ℃和25 ℃ 2种温度下克氏原螯虾围心窦注射20 μg/kg的恩诺沙星后,恩诺沙星及其代谢物环丙沙星(ciprofloxacin,CIP)在虾体内的组织分布和药代动力学特征,以期为制定合理用药量和休药期提供指导。
1 材料与方法
1.1 仪器与设备
Agilent 1200型高效液相色谱仪,Agilent Chemistation色谱工作站,美国Agilent公司;全自动样品快速研磨仪,上海净信实业发展有限公司;MTN-2800W恒温水浴氮吹装置,天津奥赛恩斯仪器有限公司;WH-2微型漩涡混合仪,上海沪西仪器分析厂。
1.2 药品与试剂
恩诺沙星标准品(纯度99%)、环丙沙星标准品(纯度98%),Dr. Ehrenstorfer GmbH公司;色谱级乙腈和甲醇,美国Tedia公司;正己烷、乙腈、三乙胺等试剂为分析纯,购于国药化学试剂有限公司。恩诺沙星原粉(含量99%),上虞京新药业有限公司。
恩诺沙星与环丙沙星标准储备液的配制:分别准确称取0.01 g恩诺沙星及环丙沙星标准品,分别用0.03 mol/L氢氧化钠溶液助溶,用超纯水定容至100 mL,配置成100 μg/mL的标准储备液。
恩诺沙星注射液的配制:称取4 g的恩诺沙星原药,用少量氢氧化钠溶液助溶,用超纯水定容至100 mL,配置成40 mg/mL的标准储备液。
1.3 试验动物
试验所用克氏原螯虾来自湖北武汉克氏原螯虾某养殖基地,平均体质量(20.0±2.0) g,暂养于消毒后的水族箱中,试验用水为经过曝气的自来水,分别控制水温在(18±1) ℃和(25±1) ℃。试验前停食1 d,选择健康活泼的虾进行试验。
1.4 试验方法
1)色谱条件。色谱柱:Shodex Silica C18(250 mm ×4.6 μm,5 μm),流动相:0.05 mol/L磷酸溶液(用三乙胺调节pH值至2.4)/乙腈=86/14(V/V);流速:1.0 mL/min;紫外线检测波长:278 nm;柱温:40 ℃;进样量:20 μL。
2)给药与取样。正式给药前禁食1 d,给药前采集空白血淋巴及组织样品检测是否有药物残留。用100 μL微量注射器将恩诺沙星药液注射到克氏原螯虾围心窦,剂量为20 μg/kg(约10 μL)。于 0.083、0.25、0.5、0.75、1、2、4、6、8、12、24、36、48、72、120 h时间点采集血淋巴、肌肉、肝胰腺。每个时间点取6只螯虾。使用注射器从围心窦取血淋巴,并取肌肉、肝胰腺,样品保存于-80 ℃冰箱。
3)样品处理。冷冻保存的样品室温下自然解冻。吸取0.5 mL血淋巴于10 mL离心管中,加入7 mL的提取液(1 mol/L盐酸∶乙腈=4∶500,V/V),旋涡混合2 min,8 000 r/min 离心10 min,将上清液置于40 ℃恒温水浴氮气吹干。准确加入1 mL流动相,过0.22 μm滤膜,滤液用高效液相色谱仪检测。取1 g组织(肌肉、肝胰腺)匀浆,加入1 mL氯化钠溶液(1 mol/L)和1 mL PBS缓冲液,涡旋振荡2 min,加入4 mL酸化乙腈(1 mol/L盐酸∶乙腈=4∶500,V/V),涡旋混合2 min,4 ℃条件下8 000 r/min离心10 min。提取上清液移入另一离心管中,残留物加4 mL酸化乙腈充分涡旋震荡2 min,4 ℃下8 000 r/min离心10 min,提取上清液。合并上清液,取上清液于氮吹仪上40 ℃氮吹至干,用1 mL流动相溶解,2 mL正己烷去脂,取下清液用0.22 μm滤膜过滤,滤液用高效液相色谱检测药物含量。因为肝胰腺中脂肪含量较多,增加一次去脂步骤。
4)标准曲线。将标准工作液用超纯水分别稀释为0.01、0.05、0.1、0.5、1、5、10、20 μg/mL标准稀释液,取10 μL进样检测进行分析。以药物峰面积为纵坐标(Y),标准质量浓度C(μg/mL或μg/g)为横坐标(X)做标准曲线,计算回归方程及相关系数。
5)工作曲线。将克氏原螯虾中空白血淋巴或空白组织匀浆,加入已知浓度的标准溶液,制成含恩诺沙星和环丙沙星为0.01、0.05、0.1、0.5、1、5、10、20 μg/mL(μg/g)的血淋巴样品和组织样品。将各样品将按照本文“1.4”样品方法处理后,进行HPLC分析,求出工作曲线方程和相关系数。
6)回收率、精密度和检测限。取空白血淋巴和组织,分别添加100、10、1 μg/mL标准溶液100 μL,使各组织恩诺沙星、环丙沙星药物含量为10、1、0.1 μg,将各样品处理后,每个质量浓度重复测定3次,连续测定3 d,计算回收率和精密度。以引起3倍信噪比(S/N=3)的浓度为检测限。
2 结果与分析
2.1 色谱行为
恩诺沙星和环丙沙星出峰时间分别为9.529、13.351 min,目标药物峰形明显尖锐,基线平稳(图1)。本方法可以有效地分离恩诺沙星和环丙沙星,在样品中与其他色谱峰明显分离,无干扰峰(图2~4)。

图1 恩诺沙星(ENR)和环丙沙星(CIP)标准溶液色谱图
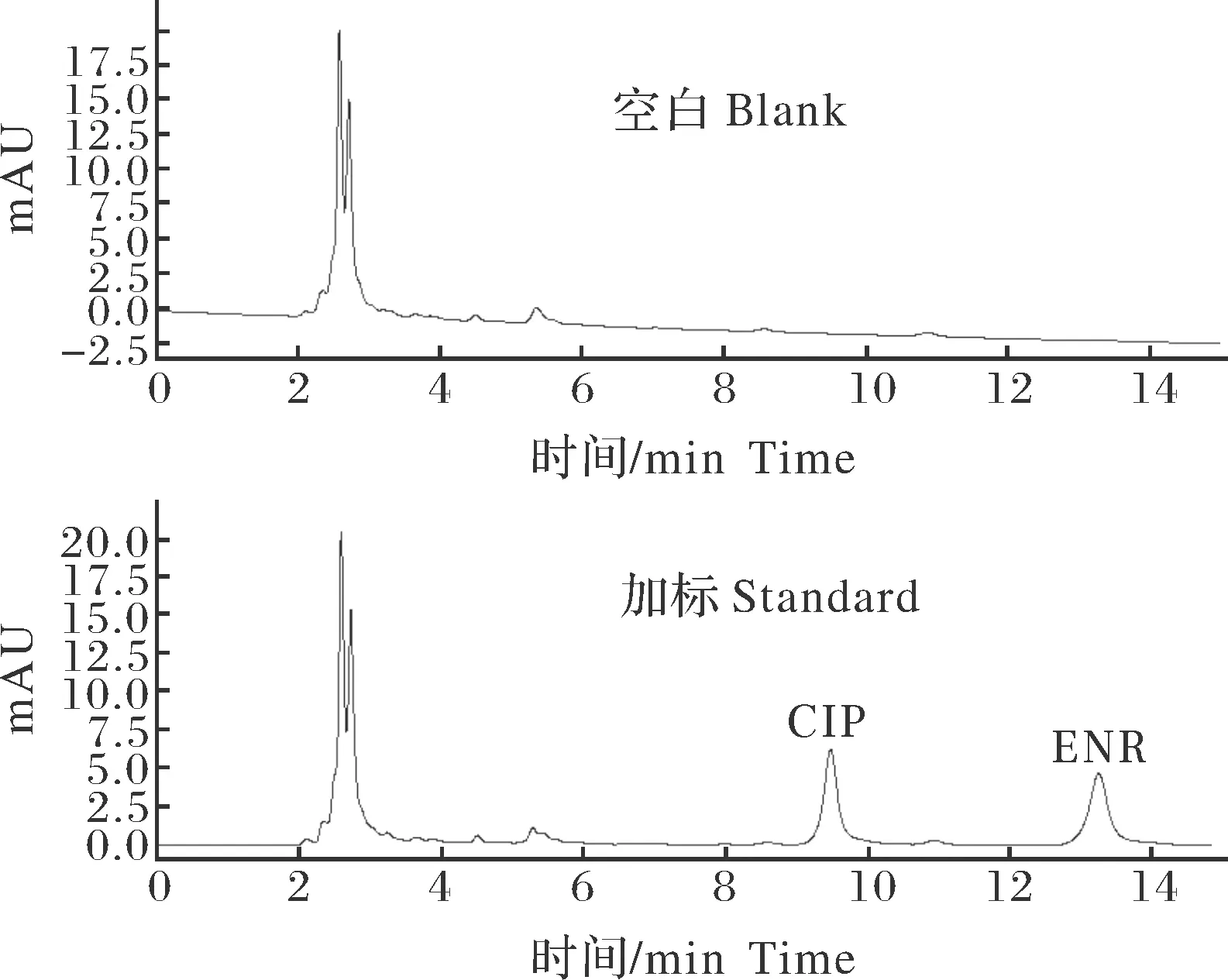
图2 空白血淋巴色谱图与加标血淋巴色谱图
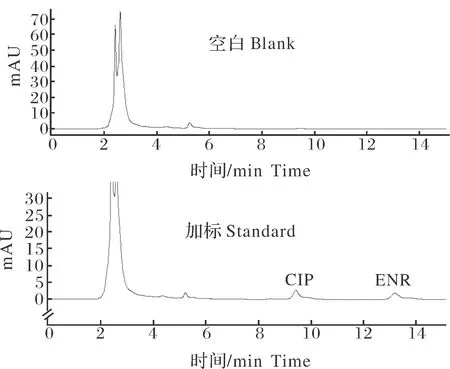
图3 空白肌肉色谱图与加标肌肉色谱图

图4 空白肝胰脏色谱图与加标肝胰腺色谱图
2.2 分析方法验证
恩诺沙星和环丙沙星的标准曲线方程分别为Y=61.618X-2.6977,Y=60.376X+0.1429,相关系数R2均大于0.99。恩诺沙星及环丙沙星在0.01~20 μg/mL质量浓度范围内线性关系良好(表1)。各组织中恩诺沙星和环丙沙星回收率均在80%~110%,说明回收率是在合理范围的(表2)。检测值日内变异系数均小于5%,日间变异系数均小于6%;检测限在0.003~0.008 μg/mL(μg/g),均低于欧盟(0.1 μg/mL 或μg/g)和日本(0.01 μg/mL或μg/g)规定的最高残留限量,表明本试验所用样品前处理和高效液相色谱检测方法具有较高的精确度。

表1 恩诺沙星和环丙沙星的工作曲线方程和相关系数 Table 1 ENR and CIP work composition line sum correlation number

表2 恩诺沙星和环丙沙星的回收率、变异系数、检测限 Table 2 ENR and CIP-like recovery rate,variation number,limit of measurement
2.3 恩诺沙星和环丙沙星在克氏原螯虾体内的药-时变化规律
注射给药后,恩诺沙星在克氏原螯虾血淋巴的药时曲线见图5。由图5可见,恩诺沙星在18 ℃和25 ℃下在0.083 0 h达到峰值,分别为20.185 4 μg/mL和19.248 6 μg/mL,1~8 h恩诺沙星药物质量浓度呈快速下降趋势,8~120 h时药物质量浓度缓慢下降。18 ℃时环丙沙星在2 h达到第1个峰值(18 ℃为0.054 0 μg/mL),24 h时会出现第2个峰值(0.050 0 μg/mL);25 ℃时环丙沙星在2 h有1个峰值(0.072 6 μg/mL)。
注射给药后,恩诺沙星在克氏原螯虾肌肉中的药时曲线见图6。恩诺沙星在25 ℃(0.026 3 h)比18 ℃(0.344 7 h)更快达到峰值,随后出现缓慢下降,18 ℃时在6 h会出现第2个峰(9.848 5 μg/g)。18 ℃时,环丙沙星在0.75 h达到峰值(0.150 3 μg/g),在8 h时出现第2个峰(0.157 9 μg/g)。25 ℃时,环丙沙星在0.25 h达到峰值(0.733 9 μg/g),在4 h达到第2个峰,然后很快下降。

图5 18 ℃(A)和25 ℃(B)下单次注射后ENR和CIP在血淋巴中的药-时曲线(n=6)

图6 18 ℃(A)和25 ℃(B)下单次注射后ENR和CIP在肌肉中的药-时曲线(n=6)
单次注射给药后,恩诺沙星在克氏原螯虾肝胰腺中的药时曲线见图7。18 ℃时,恩诺沙星质量浓度在0~1 h时间段快速上升,4 h达到峰值,4~8 h出现快速下降;25 ℃时,恩诺沙星质量浓度在1 h达到峰值。18 ℃下环丙沙星分别在0.75、4 h达到峰值;25 ℃时,环丙沙星浓度在2 h达到峰值。

图7 18 ℃(A)和25 ℃(B)下单次注射后ENR和CIP在肝胰腺中的药-时曲线(n=6)
2.4 药代动力学特征
恩诺沙星在克氏原螯虾体内的药时数据用PK2.0软件和Graphpad Prism5软件进行拟合分析,结果显示,恩诺沙星在克氏原螯虾血淋巴中的药时数据符合二室开放模型,恩诺沙星在克氏原螯虾肌肉和肝胰腺中的药时数据符合一级吸收二室开放模型,其动力学参数见表3。环丙沙星在克氏原螯虾体内的药时数据为非房室模型,其主要动力学参数见表4。

表3 恩诺沙星在克氏原螯虾体内的药代动力学参数 Table 3 Pharmacokinetic parameters of enrofloxacin in Procambarus clarkii

表4 环丙沙星在克氏原螯虾体内的药代动力学参数 Table 4 Pharmacokinetic parameters of ciprofloxacin in Procambarus clarkii
3 讨 论
3.1 恩诺沙星在克氏原螯虾体内的药代动力学特征
恩诺沙星在克氏原螯虾血淋巴中的药时数据符合二室开放模型,在肌肉和肝胰腺中的药时数据符合一级吸收二室开放模型,这与恩诺沙星在三疣梭子蟹[10]、金鳟[11]、西伯利亚鲟[12]、中华绒螯蟹[13]中的结果相似。
本试验中,在18 ℃水温下,恩诺沙星在克氏原螯虾血淋巴、肌肉、肝胰腺中的Tmax分别为0.083 0、0.344 7、1.933 5 h,Cmax分别为20.185 4、13.221 3、16.555 5 μg/mL,在25 ℃水温下,恩诺沙星在克氏原螯虾血淋巴、肌肉、肝胰腺中的Tmax分别为0.083 0、0.263 4、1.165 8 h,Cmax分别为19.248 6、16.425 0、30.731 3 μg/mL,这说明温度较高时,恩诺沙星在克氏原螯虾体内达峰时间快。与不同温度下恩诺沙星在中华绒螯蟹中的达峰时间快和达峰浓度的规律一致[13]。
18 ℃水温下,恩诺沙星在克氏原螯虾血淋巴、肌肉、肝胰腺中的T1/2α分别为0.896 5、3.559 6、6.641 1 h,AUC(0-t)分别为514.306 2、494.711 3、745.454 9(μg·h)/mL;25 ℃时T1/2α分别为0.297 3、1.681 1、11.174 5 h,AUC(0-t)分别为257.857 3、531.497 0、1 293.194 5(μg·h)/mL。AUC越大,说明恩诺沙星在克氏原螯虾中分布越广泛,可以更好地起到杀菌作用。温度较高时,恩诺沙星在血淋巴、肌肉中的分布半衰期更短。在大菱鲆中,温度同样促进了分布半衰期的减少[7]。
消除半衰期T1/2β和清除率CL是药物在体内消除快慢的主要药动学参数[13]。18 ℃时恩诺沙星在克氏原螯虾血淋巴、肌肉、肝胰腺中的T1/2β分别为68.552 7、58.914 4、74.622 1 h,25 ℃时分别为18.608 7、52.743 7、55.740 3 h。18 ℃恩诺沙星在克氏原螯虾血淋巴、肌肉、肝胰腺中的CL分别为0.021 9、0.027 2、0.011 2 L/(h·kg),25 ℃时分别为0.065 5、0.028 0、0.012 6 L/(h·kg),温度提高,血淋巴、肌肉、肝胰腺中的恩诺沙星消除加快,这与有关的研究结果一致[14]。温度提高可以促进恩诺沙星在克氏原螯虾体内的分布和消除,但由于生物种类、给药剂量、养殖环境的不同,恩诺沙星代谢程度存在差异[15-17],与其他甲壳类动物[18]一样,克氏原螯虾拥有开放性循环系统,肝胰腺是药物吸收的主要器官,因此肝胰腺中药物浓度高、消除半衰期较长。
3.2 环丙沙星在克氏原螯虾体内的药代动力学特征
研究表明,恩诺沙星在水生动物体内大部分以原药形式存在,有一部分去乙基代谢转化为环丙沙星[19],因此研究恩诺沙星的代谢产物环丙沙星在体内的药代动力学同样具有重要意义。在本试验中,18 ℃时环丙沙星在克氏原螯虾血淋巴、肌肉、肝胰腺中的消除斜率常数分别为0.005 0、0.003 1、0.011 5 1/h,在肝胰腺中消除最快,其次是血淋巴、肌肉。25 ℃水温条件下环丙沙星在克氏原螯虾血淋巴、肌肉、肝胰腺中的消除斜率常数分别为0.014 6、0.015 5、0.012 3 1/h,在肌肉中消除最快,其次是血淋巴、肝胰腺。温度较高时,加快了各组织中环丙沙星的消除。除血淋巴外,肌肉和肝胰腺中的达峰时间在25 ℃ 时( 0.25 h、2 h)比18 ℃ (8 h、12 h)快,血淋巴、肌肉、肝胰腺在25 ℃时的清除率也比18 ℃快。试验中发现,环丙沙星的浓度比恩诺沙星的浓度要低得多,水温18 ℃和25 ℃下血淋巴中环丙沙星和恩诺沙星的AUC比值分别为0.8%和0.5%,这与大菱鲆(口灌)[7]和鲫(注射和口灌)[16]中的结果相似。肝胰腺中环丙沙星的比值要比血淋巴、肌肉中高,这种现象也存在于中华绒螯蟹中[13]。药物主要代谢产物所占的比例在一定程度上体现动物对该药的代谢强度[20],且与水温成正比[17]。试验中环丙沙星呈不规则衰减的方式,可能受恩诺沙星代谢的影响[21]。
3.3 休药期
由于恩诺沙星在克氏原螯虾的肝胰腺中代谢较慢,同时要不断转化为环丙沙星,因此把肝胰腺作为药物残留的靶器官。在2019年发布的《食品安全国家标准 食品中兽药最大残留限量》中,规定的最大残留限量为0.2 μg/g(恩诺沙星+环丙沙星)[18];日本则规定恩诺沙星最高残留限量为0.01 μg/g。以0.2 μg/g为残留标准,利用软件WT 1.4计算出本试验中25 ℃水温时恩诺沙星在肝胰腺达到残留标准需要311.470 0 h,18 ℃水温时恩诺沙星在肝胰腺达到残留标准为417.770 0 h。以0.01 μg/g为残留标准,利用软件WT 1.4计算出本试验中25 ℃时恩诺沙星在肝胰腺达到残留标准为490.640 0 h,18 ℃时恩诺沙星在肝胰腺达到残留标准为680.580 0 h。制定休药期不仅要考虑残留量,还要考虑水温等状况[22]。根据本试验结果,按照国家标准0.2 μg/g为残留标准,建议休药期为325 (℃·d)。以日本0.01 μg/g为残留标准,建议休药期为511 (℃·d)。
