环丙沙星在盐碱土中吸附特性的研究
2016-11-11边炜涛马秀兰王富民张力媛任力洁王玉军高迪
边炜涛,马秀兰*,王富民,张力媛,任力洁,王玉军,高迪
(1.吉林农业大学资源与环境学院,长春130118;2.国家供水水质监测网长春监测站,长春130022;3.吉林省商品粮基地土壤资源可持续利用重点实验室,长春130118)
环丙沙星在盐碱土中吸附特性的研究
边炜涛1,3,马秀兰1,3*,王富民1,3,张力媛1,2,任力洁1,3,王玉军1,3,高迪1,3
(1.吉林农业大学资源与环境学院,长春130118;2.国家供水水质监测网长春监测站,长春130022;3.吉林省商品粮基地土壤资源可持续利用重点实验室,长春130118)
采用OECD guideline 106批平衡吸附法研究环丙沙星在碱土中的等温吸附特性、吸附动力学、吸附热力学以及pH值和Ca2+浓度对其吸附的影响。结果表明环丙沙星在盐碱土中的吸附较好地符合Freundlich方程(拟合系数R2=0.981),不同初始浓度的环丙沙星在盐碱土中的吸附过程符合准二级动力学方程,吸附常数为1.17×10-3~5.67×10-3kg·min-1·mL-1。吸附过程可分为快速吸附和慢速平衡两个阶段,初始浓度分别为80、100、120 mg·L-1的环丙沙星吸附平衡时间为24 h,平衡吸附比例分别为89.9%、92.2%、92.7%。吸附热力学参数ΔG<0且ΔH=-3.58 5 kJ·mol-1,表明环丙沙星在盐碱土上的吸附为自发的放热反应。随着溶液pH值的升高,盐碱土对环丙沙星的吸附能力不断减弱,当pH>9后吸附能力快速减少。以不同浓度CaCl2作为背景液,环丙沙星在盐碱土中的等温吸附曲线用Freundlich方程拟合效果较好,lgKf值随着CaCl2背景溶液浓度的增加而减小,且环丙沙星初始浓度较小时其所受离子强度的影响相对较小。
环丙沙星;盐碱土;吸附;pH值;Ca2+强度
近年来我国生产和使用的抗生素数量迅速增长[1]。《2010—2015年中国化学行业投资分析及前景预测报告》指出,喹诺酮类抗生素在临床上的使用已成为除头孢类抗生素外的第二大类抗菌药物。喹诺酮类抗生素具有抗菌活性强、抗菌谱广、半衰期长、体内分布广、不良反应较轻等特点,因此它被广泛应用于畜禽养殖业[2]。由于畜禽饲料中添加的抗生素不能完全被生物吸收转化,大部分抗生素以原形随畜禽粪尿排出体外,并随着粪肥的随意堆放和直接施用进入土壤造成污染[3]。邰义萍等[4]发现在东莞市蔬菜基地土壤中环丙沙星的平均含量为24.93 μg·kg-1。当长时间降水,尤其是弱酸性降水时土壤中的喹诺酮抗生素会变得易于迁移,使污染扩散[5]。暴露在环境中的抗生素会通过食物链富集对生物和人类健康造成伤害。
随着我国耕地面积的减少,盐碱土已成为具有巨大开发潜力的耕地后备资源。盐碱土的修复受到了国内外研究者们的广泛关注,在修复的过程中为了改善盐碱土的通气、透水和养分等状况通常会增施有机肥料[6],如王睿彤等[7]使用牛粪作为盐碱土的改良剂,随之会出现粪便中的抗生素污染土壤的情况。近年来关于环丙沙星在土壤中的吸附行为已有许多报道,但在盐碱土等肥力较低土壤中的吸附行为研究较少,因此本文选取环丙沙星,结合吸附等温试验、吸附动力学试验、吸附热力学试验分析环丙沙星在盐碱土中的吸附特征,同时研究不同背景溶液pH值和Ca2+浓度对其吸附特性的影响,以期为评价环丙沙星在盐碱土中的环境风险提供科学依据。
1 材料与方法
1.1 供试材料与仪器
1.1.1 供试材料
环丙沙星标准品(C17H18FN3O3)购自上海晶纯生化科技股份有限公司,纯度≥98%;甲醇为色谱纯。
供试土壤取自吉林省前郭县套浩太乡碱巴拉村,介于东经124°29′~124°47′,北纬44°46′~45°02′。土壤样品为0~20 cm的混合土样,去除土样中的砂砾、根系植物、秸秆等杂物,自然风干研磨,过100目筛,备用。供试土壤理化性质见表1。
1.1.2 试验仪器
Agilent1100型高效液相色谱仪(美国Agilent公司),TDL-40B型低速台式离心机(上海安亭科学仪器厂),水浴恒温振荡器(金坛市瑞华仪器有限公司),PHS-3C型pH计(上海精密科学仪器有限公司),KQ-250B型超声波清洗器(昆山市超声仪器有限公司)。
1.2 色谱条件
液相色谱仪(HPLC)配置紫外检测器和C18色谱柱(ZORBAX Eclipse XDB-C18 150 mm×4.6 mm),流动相为甲醇∶水=32∶68(V/V)的混合溶液。流动相流速为1 mL·min-1,柱温为30℃,进样量为20 μL,紫外检测波长为277 nm,保留时间8 min。
1.3 数据分析方法
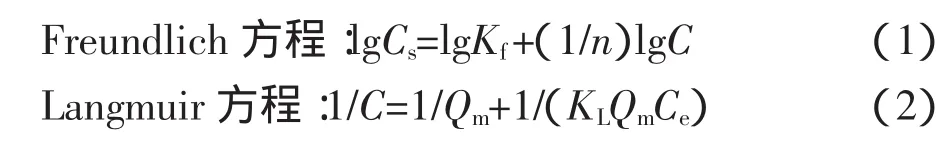
式中:吸附常数Kf代表吸附容量,但不代表最大吸附量,其值越大,只表明环丙沙星吸附容量越大,吸附剂与吸附质之间结合能力越强;1/n反映吸附的非线性程度和吸附机制的差异,也可表征吸附过程的亲和力[8];Cs为单位质量土壤对环丙沙星的吸附量,mg· kg-1;Ce为平衡溶液中环丙沙星的质量浓度,mg·L-1;Qm为当抗生素为单分子层吸附时,理论最大吸附量,mg·kg-1。
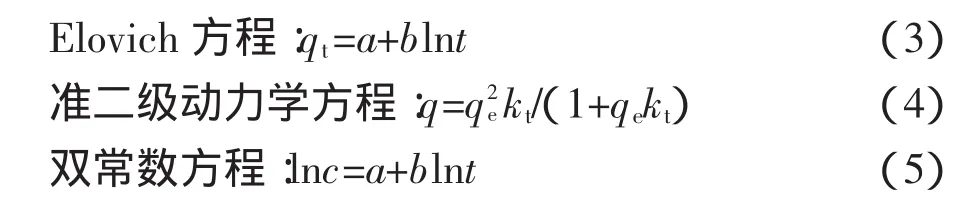
式中:a、b分别为Elovich方程和双常数方程的吸附动力学速率常数;q和qe分别是时间t和吸附达平衡时吸附质在吸附剂表面的吸附量;k是准二级吸附速率常数。
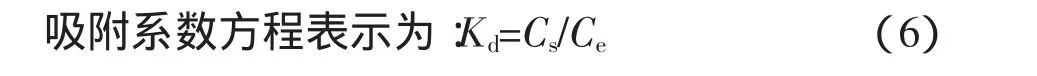
式中:Cs为单位质量土壤对环丙沙星的吸附量,mg· kg-1;Ce为平衡溶液中环丙沙星的质量浓度,mg·L-1;Kd,L·g-1。


表1 供试土壤理化性质Table 1 Physicochemical properties of tested soil
式中:ΔG为吸附标准自由能改变量,kJ·mol-1;ΔH为标准吸附热,kJ·mol-1;ΔS为吸附标准熵变值,kJ·mol-1· K-1;R为气体摩尔常数,J·mol-1·K-1;T为绝对温度,K;K为平衡吸附常数[9]。
根据式(8)以lnK为纵坐标,1/T为横坐标作图,可得到ΔH和ΔS。
1.4 吸附试验方法
1.4.1 等温吸附试验
参照OECD guideline 106批平衡吸附试验方法进行。称取(0.500 0±0.000 5)g样品放于50 mL聚乙烯离心管中,按水土比50∶1加入25 mL含不同浓度环丙沙星的背景溶液(为抑制样品中细菌活动,再加入0.01 mol·L-1的NaN3),使环丙沙星的浓度为40、60、80、100、120、140 mg·L-1。在25℃下,恒温、避光振荡至吸附平衡后,于4000 r·min-1离心10 min,取上清液经0.45 μm滤膜过滤,测定滤液中环丙沙星浓度。
1.4.2 吸附动力学试验
参照1.4.1的试验方法,分别加入80、100、120 mg·L-1环丙沙星的背景溶液。在25℃下,恒温、避光振荡,分别在1、5、15、30 min和1、2、4、6、12、24 h时取样,离心、过滤后,测定滤液中环丙沙星的浓度。
1.4.3 吸附热力学试验
参照1.4.1的试验方法,分别在15、25、35℃下进行重复试验,测定平衡溶液中环丙沙星浓度,研究不同温度对其吸附作用的影响。
1.4.4 背景溶液不同pH值对吸附的影响
用0.1 mol·L-1HCl或NaOH溶液调节背景溶液的pH,使样品pH值达到3、5、7、9、11,参照1.4.1的试验方法进行重复试验,测定平衡溶液中环丙沙星浓度,研究不同背景溶液pH值对其吸附作用的影响。
1.4.5 背景溶液不同Ca2+浓度对吸附的影响
配制不同浓度的Ca2+的背景溶液,使CaCl2浓度为0.01、0.05、0.10、0.15、0.20 mol·L-1。参照1.4.1的试验方法进行重复试验,测定环丙沙星浓度,研究不同Ca2+浓度对环丙沙星吸附作用的影响。
以上所有试验均设置3次重复。
2 结果与讨论
2.1环丙沙星在盐碱土中的等温吸附特性
环丙沙星在盐碱土中的吸附等温试验分别用Langmuir方程、Freundlich方程进行拟合。吸附等温线见图1,吸附常数和相关系数见表2。结果表明,Freundlich方程和Langmuir方程的相关系数R2分别为0.981和0.794,因此Freundlich方程更适用于拟合环丙沙星在盐碱土中的吸附行为,表明盐碱土对环丙沙星的吸附有多种吸附点位同时作用。Freundlich方程中的lgKf为1.716,1/n>1,表明吸附自由能和加入吸附物的量成正比。根据1/n值与等温吸附线的形状关系可知[10],其吸附等温线属“S型”,其产生的原因有两种:一是溶质分子之间的引力可能产生协同吸附作用;二是溶液中存在溶质的竞争性抑制剂[11]。由此推断,在环丙沙星浓度较低时,抑制吸附过程的主要原因可能是溶液中的水分子与其竞争吸附点位,环丙沙星的吸附比例也随其初始浓度的增加而增加[12]。这与本试验中不同水溶液pH值和不同Ca2+强度对盐碱土吸附环丙沙星的影响结果相符合。
2.2 环丙沙星在盐碱土中的吸附动力学
不同初始浓度的环丙沙星在盐碱土中的吸附量随时间的变化如图2所示。结果表明,环丙沙星在盐碱土中的吸附过程分为快速吸附阶段和慢速平衡阶段。在0~30 min时初始浓度为80、100、120 mg·L-1的环丙沙星的吸附量分别占吸附总量的99.2%、98.7%、95.9%,在30 min至24 h时属于慢速平衡阶段,且24 h时盐碱土对环丙沙星的吸附趋于平衡,此时3种初始浓度的环丙沙星的吸附比例分别为89.9%、92.2%、92.7%,其吸附比例均与环丙沙星的初始浓度成正比。
这与崔皓等[13]研究的环丙沙星在潮土中的吸附过程相似。
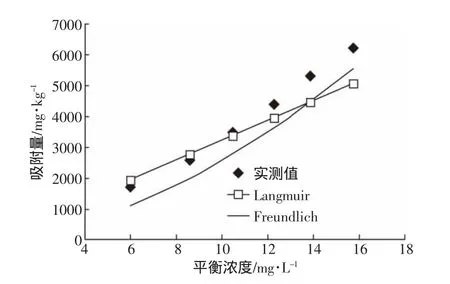
图1 环丙沙星在盐碱土中的吸附等温线Figure 1 Adsorption isotherms of ciprofloxacin on saline-alkali soil

表2 盐碱土对环丙沙星等温吸附线的拟合参数Table 2 Isotherm parameters of ciprofloxacin adsorption on saline-alkali soil
环丙沙星在盐碱土中的吸附动力学分别采用Elovich方程、双常数方程、准二级动力学方程进行拟合,结果见表3。表明准二级动力学方程对环丙沙星的拟合效果最好,R2值分别为0.962、0.983、0.941,其次为Elovich方程,双常数的拟合性相对较差。这说明准二级动力学方程描述盐碱土对环丙沙星的吸附行为比较合适。但由于准二级动力学方程涵盖了表面吸附、外部液膜扩散以及粒子内扩散等吸附过程,不能反映吸附过程的具体动力学机制。由此推断环丙沙星在盐碱土中的吸附动力学机制并不是单一的,而是由多个吸附动力学机制组成。张艳红等[14]的研究表明,蒙脱土和硅藻土对环丙沙星的吸附过程符合准二级动力学方程,其吸附过程受控于物理化学吸附。Li等[15]的研究表明,环丙沙星在高岭土上的二级吸附动力学速率常数显著大于四环素,其原因可能是环丙沙星迅速地被吸附到高岭土的表面而非进入晶层。

图2 盐碱土对环丙沙星的吸附动力学曲线Figure 2 Kinetics of ciprofloxacin adsorption on saline-alkali soil
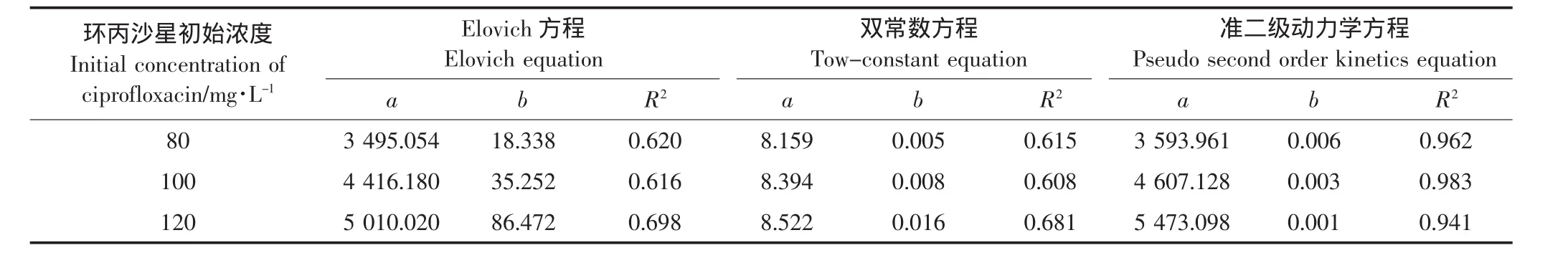
表3 盐碱土对环丙沙星吸附动力学拟合的相关参数Table 3 Kinetic parameters of ciprofloxacin adsorption on saline-alkali soil
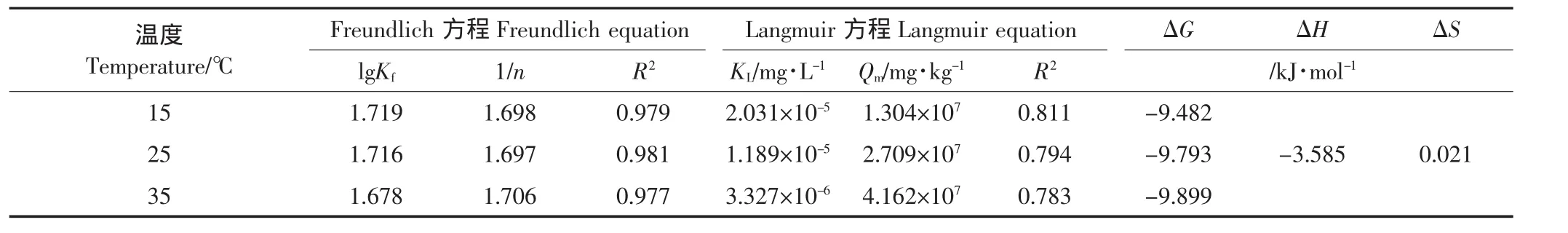
表4 不同温度的吸附模拟方程参数和热力学参数Table 4 Isothermal and thermodynamic parameters of ciprofloxacin adsorption at different temperatures
2.3 环丙沙星在盐碱土中的吸附热力学
不同温度下环丙沙星在盐碱土中吸附等温试验用Langmuir方程、Freundlich方程进行拟合,拟合数据和热力学参数见表4。结果表明,随着温度升高吸附容量Kf和吸附表面强度KL呈减小趋势,说明温度升高不利于环丙沙星的吸附。ΔG<0说明其吸附自发进行,ΔH=-3.585 kJ·mol-1说明其吸附为放热反应。根据Vonopen等[16]对各种吸附作用力引起的吸附焓变化范围的总结,可得出此吸附为物理吸附,吸附机理可能包括范德华力、氢键力和偶极矩力。ΔS=0.021说明熵值小,体系处于比较有序的状态[17]。
2.4 pH值对环丙沙星吸附特性的影响
土壤吸附系数Kd是土壤吸附环丙沙星量与平衡溶液中环丙沙星浓度的比值,以Kd值作为衡量土壤吸附抗生素的标准在近年来被广泛采用。在不同pH的条件下,盐碱土对环丙沙星的平衡吸附量和吸附常数Kd值变化如图3、图4所示。
由图3、图4可知环丙沙星的平衡吸附量和Kd值随背景溶液pH的升高而下降。pH=3时盐碱土对环丙沙星的吸附效果最好,初始浓度从低到高的平衡吸附量分别为3 821.167、4 776.028、5 724.081 mg· kg-1,Kd值分别为1.068、1.066、1.037 L·g-1;而当pH>9后环丙沙星的平衡吸附量快速减少,在pH达到11时,盐碱土对环丙沙星的吸附效果最差,初始浓度由低到高的平衡吸附量分别减少为2763.510、3 532.942、
4 312.043 mg·kg-1,Kd值分别减少为0.112、0.120、0.128 L·g-1。由此推断,在高pH条件下存在大量的OH-可能会降低环丙沙星的吸附效果,阳离子吸附是盐碱土中环丙沙星吸附的主要机制之一。
本试验采用Freundlich方程和Langmuir方程对不同背景溶液pH值下的环丙沙星吸附等温线进行拟合,拟合相关系数见表5。结果表明,Freundlich拟合方程的相关系数R2的平均值为0.985,Langmuir拟合方程的R2平均值为0.916,因此Freundlich方程更适合用来拟合不同背景溶液pH条件下盐碱土对环丙沙星的吸附行为,Freundlich方程的吸附常数lgKf随着pH升高而减少,表明随着背景溶液pH值的增加盐碱土与环丙沙星之间的结合能力减弱。
Vasudevan D等[18]的研究表明,环丙沙星含有-NH3和-COOH(pKa值分别为6.18和8.76)可以分别与溶液中的H+和OH-结合,在溶液中以阳离子、兼性离子或阴离子形态存在。当pH值小于pKa1时,环丙沙星的-NH3与H+结合以形态为主;当pKa1<pH< pKa2时,环丙沙星以CIPH±的形态存在为主;当pH值大于pKa2时,环丙沙星的-COOH与OH-结合而以CIPH±或CIP-形态存在为主[19]。本试验所用的盐碱土本身pH值为9.7,当加入背景溶液pH<7时,环丙沙星在盐碱土中以CIPH+的形态存在为主,当背景溶液7<pH<9时,环丙沙星在背景溶液中以CIPH±形态存在为主,当背景溶液pH>9时环丙沙星在水溶液中以CIPH±或CIP-形态存在为主。这表明阳离子吸附是盐碱土中环丙沙星吸附的主要机制之一。
2.5 Ca2+浓度对环丙沙星吸附特性的影响

图3 不同pH下环丙沙星的平衡吸附量Figure 3 Equilibrium adsorption capacity of ciprofloxacin at different pH
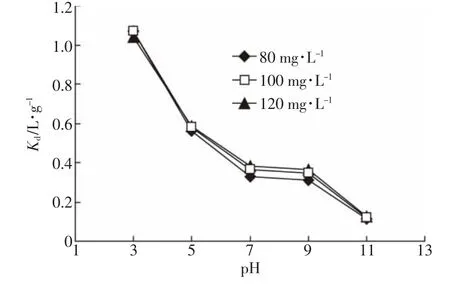
图4 不同pH下环丙沙星的吸附分配系数Figure 4 Distribution coefficients of ciprofloxacin at different pH
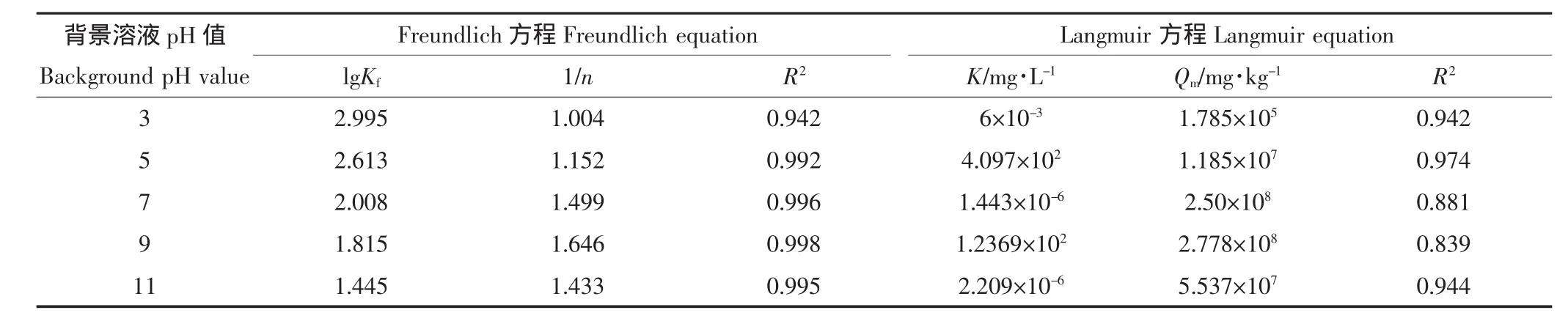
表5 不同pH下环丙沙星的等温吸附参数Table 5 Isothermal parameters of ciprofloxacin at different pH
不同Ca2+浓度对环丙沙星的吸附量如图5所示。随着CaCl2浓度的升高,盐碱土对环丙沙星的吸附量逐渐降低,且不同初始浓度的环丙沙星在盐碱土中的吸附受Ca2+强度的影响不同。当环丙沙星初始浓度为40 mg·L-1时,盐碱土对环丙沙星的吸附比例为69.2%;当环丙沙星浓度为140 mg·L-1时,盐碱土对环丙沙星的吸附比例为52.5%。这可能是由于环丙沙星在低浓度时,盐碱土中有较多的吸附位点,环丙沙星能被盐碱土充分吸附。此外,离子强度的变化对盐碱土吸附的影响较小。
在不同CaCl2浓度的条件下,盐碱土对环丙沙星的吸附常数Kd值变化如图6所示。结果表明,随着CaCl2浓度的增大,其对应Kd值呈减小趋势,在Ca2+浓度从0.10 mol·L-1增加到0.20 mol·L-1的过程中,Kd
值的减少幅度相对变小,说明盐碱土吸附环丙沙星的能力随着土壤中Ca2+浓度的增大而减弱。
本试验采用Freundlich方程和Langmuir方程对不同Ca2+强度下的环丙沙星吸附等温线进行拟合,拟合参数见表6。结果表明,Freundlich方程对环丙沙星的拟合效果较好,R2的平均值为0.992,Langmuir方程拟合R2平均值为0.838。该结果表明Freundlich方程适合用来拟合不同Ca2+强度条件下盐碱土对环丙沙星的吸附行为。Kf代表盐碱土对环丙沙星的吸附容量,而lgKf值随着CaCl2溶液浓度增加而减小,表明随着离子强度的增强,环丙沙星在盐碱土中的吸附量降低。这可能是因为Ca2+浓度的增大,与环丙沙星竞争盐碱土上阳离子吸附位点,使吸附量减少。
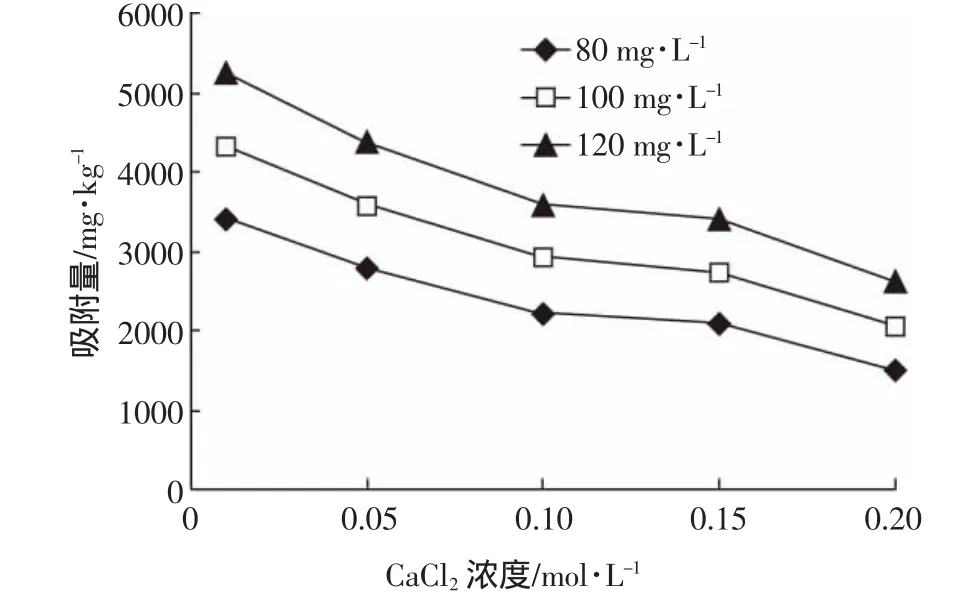
图5 不同CaCl2浓度下环丙沙星的平衡吸附量Figure 5 Equilibrium adsorption capacity of ciprofloxacin at different CaCl2concentrations
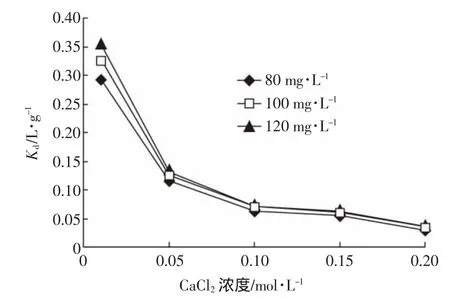
图6 不同CaCl2浓度下环丙沙星的吸附系数Figure 6 Distribution coefficients of ciprofloxacin at different CaCl2concentrations

表6 不同CaCl2浓度下环丙沙星的等温吸附参数Table 6 Isothermal parameters of ciprofloxacin at different CaCl2concentrations
3 结论
(1)环丙沙星在盐碱土上的吸附规律用Freundlich方程拟合较好(R2=0.981),其吸附等温线属于“S”型。当溶液中环丙沙星浓度较低时,溶液中的水分子会与其竞争吸附点位抑制吸附过程。
(2)环丙沙星在盐碱土中的吸附过程分为快速和慢速吸附两个阶段,在24 h达到吸附平衡。准二级动力学能够较好拟合吸附过程,动力学常数为1.17×10-3~5.67×10-3kg·min-1·mL-1。
(3)环丙沙星在盐碱土上的吸附是自发的放热过程。
(4)随着溶液pH的升高,盐碱土对环丙沙星的吸附能力逐渐减弱,当pH>9后,环丙沙星在水溶液中以CIPH±或CIP-形态存在为主,吸附能力快速减弱。
(5)随着Ca2+浓度的增加,环丙沙星在盐碱土中的吸附量降低。
[1]Richardson B J,Lam P K S,Martin M.Emerging chemicals of concern:Pharmaceuticals and personal care products(PPCPs)in Asia,with particular reference to Southern China[J].Marine Pollution Bulletin,2005,50(9):913-920.
[2]Díaz-Cruz M S,Alda M J L D,Barceló D.Environmental behavior and analysis of veterinary and human drugs in soils,sediments and sludge[J]. Trends in Analytical Chemistry,2003,22(6):340-351.
[3]Marc-Oliver A,Frauke G,Travis G R,et al.Distribution of sulfamethazine,chlortetracycline and tylosin in manure and soil of Canadian feedlots after subtherapeutic use in cattle[J].Environmental Pollution,2008,156(3):1243-251.
[4]邰义萍,莫测辉,吴小莲,等.东莞市蔬菜基地土壤中喹诺酮类抗生素的污染特征研究[J].环境科学学报,2011,31(4):839-845.
TAI Yi-ping,MO Ce-hui,WU Xiao-lian,et al.Occurrence of quinolone antibiotics in soils from vegetable fields of Dongguan City[J].Acta Scientiae Circumstantiae,2011,31(4):839-845.
[5]张旭,向垒,莫测辉,等.喹诺酮类抗生素在土壤中的迁移行为及影响因素研究[J].农业环境科学学报,2014,33(7):1345-1350. ZHANG Xu,XIANG Lei,MO Ce-hui,et al.Migration behavior and influence factors of quinolone antibiotics in soil[J].Journal of Agro-Environment Science,2014,33(7):1345-1350.
[6]路浩,王海泽.盐碱土治理利用研究进展[J].现代化农业,2004(8):10-12.
LU Hao,WANG Hai-ze.Advances in the use of saline-alkali soil governance[J].Modernizing Agriculture,2004(8):10-12.
[7]王睿彤,陆兆华,孙景宽,等.土壤改良剂对黄河三角洲滨海盐碱土的改良效应[J].水土保持学报,2012,26(4):240-244.
WANG Rui-tong,LU Zhao-hua,SHUN Jing-kuan,et al.Effect of soil ameliorants on coastal saline-alkali soil in the Yellow River delta[J]. Journal of Soil and Water Conservation,2012,26(4):240-244.
[8]Gundogan R,Acemiolgˇu B,Alma M H.Copper(Ⅱ)adsorption from aqueous solution by herbaceous peat[J].Journal of Colloid and Interface Science,2004,269(2):303-309.
[9]王耀晶,刘鸣达,陈蕾蕾,等.外源硅对不同pH水田土壤铅吸附热力学特征的影响[J].农业环境科学学报,2012,31(9):1729-1733.
WANG Yao-jing,LIU Ming-da,CHEN Lei-lei,et al.Effect of added silicon on the adsorption and the thermodynamics of lead in paddy field soil with different pH[J].Journal of Agro-Environment Science,2012,31(9):1729-1733.
[10]Calvet R.Adsorption of organic chemicals in soils[J].Environmental Health Perspectives,1989,83:145-177.
[11]Hinz C.Description of sorption data with isotherm equations[J].Geoderma,2001,99(3/4):225-243.
[12]Sukul P,Lamshöft M,Zühlke S,et al.Sorption and desorption of sulfadiazine in soil and soil-manure systems[J].Chemosphere,2008,73(8):1344-1350.
[13]崔皓,王淑平.环丙沙星在潮土中的吸附特性[J].环境科学,2012,33(8):2896-2990.
CUI Hao,WANG Shu-ping.Adsorption characteristics of ciprofloxacin in ustic cambosols[J].Environmental Science,2012,33(8):2896-2990.
[14]张艳红,王风贺,纪营雪,等.不同黏土对盐酸环丙沙星和诺氟沙星的吸附特性[J].环境工程学报,2015,7(9):3107-3114.
ZHANG Yan-hong,WANG Feng-he,JI Ying-xue,et al.Adsorption characteristics of ciprofloxacin and norfloxacin onto two kinds of clay minerals[J].ChineseJournalofEnvironmentalEngineering,2015,7(9):3107-3114.
[15]Li Z H,Hong H L,Liao L B,et al.A mechanistic study of ciprofloxacin removal by kaolinite[J].Colloids and Surfaces B:Biointerfaces,2011,88(1):339-344.
[16]Von-open B,Kördel W,Klein W.Sorption of nonpolar and polar compounds to soils:Processes,measurement and experience with the applicability of the modified OECD-guideline[J].Chemosphere,1991,22(3/ 4):285-304.
[17]刘保峰,魏世强.胡敏酸-镍络合稳定性及热力学特征研究[J].农业环境科学学报,2007,26(6):2071-2074.
LIU Bao-feng,WEI Shi-qiang.Stability and thermodynamics characteristics of humic acid-nickel complexes[J].Journal of Agro-Environment Science,2007,26(6):2071-2074.
[18]Vasudevan D,Bruland G L,Torrance B S,et al.pH-dependent ciprofloxacin sorption to soils:Interaction mechanisms and soil factors influencingsorption[J].Geoderma,2009,151(3/4):68-76.
[19]武庭瑄.环丙沙星在3种不同土壤中的吸附特征研究[J].北方环境,2012,25(3):54-57.
WU Ting-xuan.Adsorption of ciprofloxacin on three different soils[J]. Northern Environment,2012,25(3):54-57.
AdsorPtion characteristics of ciProfloxacin on saline-alkali soil
BIAN Wei-tao1,3,MA Xiu-lan1,3*,WAN Fu-min1,3,ZHANG Li-yuan1,2,REN Li-jie1,3,WANG Yu-jun1,3,GAO Di1,3
(1.School of Resource and Environment Science,Jilin Agricultural University,Changchun 130118,China;2.Changchun Monitoring Station of National Water Quality Monitoring Network,Changchun 130041,China;3.Key Laboratory of Soil Resource Sustainable Utilization for Jilin Province Commodity Grain Bases,Changchun 130118,China)
Adsorption isotherms,adsorption kinetics and adsorption thermodynamics of ciprofloxacin on a saline-alkali soil were investigated by batch equilibrium studies according to DECD Guideline 106.The effects of pH and Ca2+concentration on adsorption process were also examined.Results indicated that the adsorption isotherm of ciprofloxacin was well fitted to the Freundlich equation,with correlation constant R2of 0.981.The kinetics of ciprofloxacin adsorption by saline-alkali soil at different initial concentrations was in accordance with the pseudo-second order kinetic equation,with adsorption constant of 1.17×10-3~5.67×10-3kg·min-1·mL-1.The whole process of ciprofloxacin adsorption by soil can be divided into two stages:the fast adsorption and the slow equilibrium.The adsorption equilibrium time of ciprofloxacin at initial concentrations of 80 mg·L-1,100 mg·L-1and 120 mg·L-1was 24 h.The equilibrium adsorption ratios were 89.9%,92.2%and 92.7%,respectively.The ΔH values of-3.585 kJ·mol-1and negative ΔG values revealed that the adsorption of ciprofloxacin on the salinealkali soil was a spontaneous exothermic process.The capacity of ciprofloxacin adsorption decreased constantly with increasing pH,and reduced drastically when pH was above 9.At different concentrations of CaCl2as background solution,the isothermal adsorption curves of ciprofloxacin by saline-alkali soil were well described by the Freundlich equation.The lgKfvalues decreased with the increase of CaCl2concentration.The impact of ionic strength on ciprofloxacin adsorption was less when its initial concentrations were lower.
ciprofloxacin;saline-alkali soil;adsorption;pH value;Ca2+concentration
X53
A
1672-2043(2016)10-1953-07
10.11654/jaes.2016-0196
边炜涛,马秀兰,王富民,等.环丙沙星在盐碱土中吸附特性的研究[J].农业环境科学学报,2016,35(10):1953-1959.
BIAN Wei-tao,MA Xiu-lan,WAN Fu-ming,et al.Adsorption characteristics of ciprofloxacin on saline-alkali soil[J].Journal of Agro-Environment Science,2016,35(10):1953-1959.
2016-02-17
吉林省科技厅重大科技攻关专项(20130204054SF0);吉教科合字[2014]第467号
边炜涛(1991—),男,浙江诸暨人,硕士研究生,从事水处理技术研究。E-mail:bianweitao2011@163.com
*通信作者:马秀兰E-mail:1974malan@163.com
