氟离子选择电极法测定废旧锂电池回收浸出液中氟含量①
2021-01-30谢堂锋陈若葵蔡罗蓉
谢堂锋, 陈若葵, 王 明, 蔡罗蓉
(湖南邦普循环科技有限公司,湖南 长沙410600)
在废旧锂电池回收系统中电解液和黏结剂成分均含大量氟化物,如LiPF6,PVDF 等。 废旧锂电池正负极废料经酸浸处理后,氟直接进入浸出液中,使生产设备及管道遭受严重腐蚀,恶化企业生产环境,危害人体健康。 该浸出液成分复杂,重金属、有机物、无机盐等[1-2]含量高,氟含量的检测一直存在较大困难。
目前,测定氟离子的主要方法有氟离子选择电极法[3]、离子色谱法[4]、分光光度法[5]等,离子选择电极法因其选择性好、灵敏度高、响应速度快、操作简便等优点被广泛采用。 在采用该方法测定废旧锂电池回收浸出液中氟含量时,发现氟离子含量随样品稀释倍数增大而增高的现象。 本文对该浸出体系中可能存在的影响测定的因素进行了探讨并进行精密度和准确度分析,为废旧电池回收行业酸浸体系中氟化物测定方法的选择提供参考依据。
1 实验部分
1.1 主要仪器
实验主要仪器包括ZD-2 型精密自动电位滴定仪、氟离子选择电极、饱和甘汞电极、美国赛默飞iCAP 7200 ICP-OES 光谱仪等。
1.2 主要试剂及配制
乙酸钠溶液(30%):称取150 g 乙酸钠溶解后定容到500 mL 容量瓶中;总离子强度缓冲溶液(TISAB):称取58.8 g 二水合柠檬酸钠和85 g 硝酸钠,加水溶解,用盐酸(50%)调节pH 值至5.5~6.0,加水稀释至1 000 mL,摇匀;氟标准储备溶液(1 000 μg/mL):购自国家有色金属及电子材料分析测试中心;氟标准工作溶液:按配制浓度分别准确移取相应体积氟标准储备溶液至100 mL容量瓶中,分别加入20 mL TISAB,加水稀释至刻度,摇匀。
实验所用试剂除特别说明外,均为分析纯,水均为电阻率18.2 MΩ·cm 的超纯水。
废旧锂电池浸出液由湖南邦普循环科技有限公司提供,采用美国赛默飞iCAP 7200 ICP-OES 光谱仪测定其主要化学元素组成,结果如表1 所示。
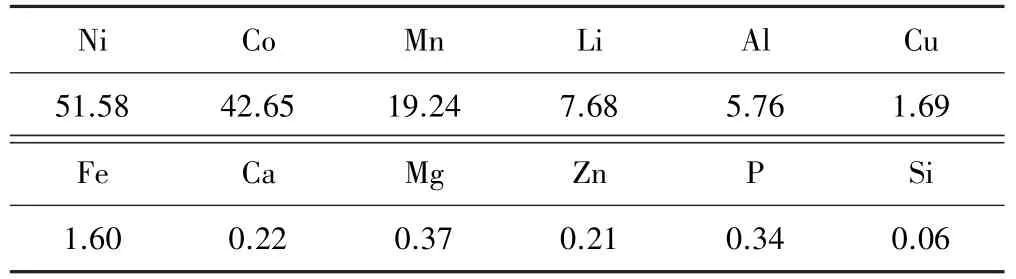
表1 废旧锂电池浸出液主要元素组成/(g·L-1)
1.3 实验原理及方法
1.3.1 工作原理
以氟化镧单晶片制成的氟离子选择电极,对样品溶液中氟离子具有良好的选择性,与饱和甘汞电极插入待测含氟溶液中构成电化学电池。 其电极膜电位变化即电动势(E)与溶液中氟离子活度的对应关系符合能斯特(Nernst)方程,当待测溶液中总离子强度维持一定时,则上述方程可表示为[6]:
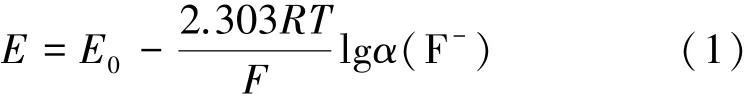
式中E0为标准电极电势,mV; R 为摩尔气体常数,J/(mol·K);F 为法拉第常数,C/mol;T 为绝对温度,K;α(F-)为氟离子活度,在稀电解质溶液中可视为被测离子浓度,mg/L。 通过测量标准溶液电动势绘制氟离子标准曲线,之后利用待测试样的电位值E 即可根据标准曲线计算待测试样中氟离子含量。
1.3.2 氟离子工作曲线的绘制
25 ℃条件下,将配制的不同质量浓度的氟标准溶液分别置于聚乙烯烧杯中,插入经洗净的电极连续搅拌,待读数稳定后读取电位值,按浓度顺序从低至高依次测量,记录测试结果,作电位和浓度对数的标准曲线,如图1 所示。
1.3.3 样品测定
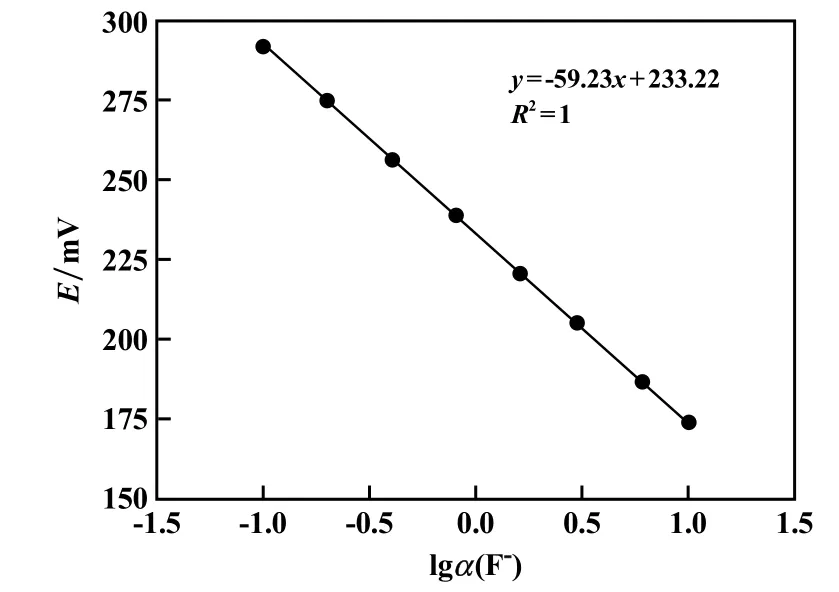
图1 氟离子质量浓度标准曲线
按不同稀释倍数取适量浸出液置于100 mL 聚乙烯烧杯中,用乙酸钠调节pH 值至5.5~6.0,加入20 mL TISAB,转入100 mL 容量瓶中,加水稀释至刻度,摇匀。 倒出部分于50 mL 聚乙烯烧杯中,控制温度为25 ℃,插入清洗干净的电极,连续搅拌溶液,电位稳定后,读取平衡电位值,根据标准曲线计算得出稀释液氟含量,再乘以稀释倍数得出待测浸出液氟含量。
2 结果与讨论
2.1 稀释倍数的影响
按实验方法测定了浸出液样品不同稀释倍数下的氟含量,结果如表2 所示。

表2 不同稀释倍数下浸出液氟含量的测定结果
从表2 可以看出,浸出液氟含量测定值随稀释倍数增高而逐渐增大,当稀释倍数为500~2 000 倍时,氟含量基本趋于稳定;当稀释倍数为5 000 倍时,氟含量有所降低。
2.2 总离子强度缓冲溶液的影响
由于离子选择电极法测定的是游离态的氟离子,由表1 可知浸出液组分中含有大量的Ni、Co、Mn、Al、Fe、Ca、Mg、Zn 等杂质金属元素,易与氟离子形成稳定的络合物而干扰测定。 另外,在使用氟离子选择电极测量待测样品氟含量时,溶液的离子强度变化直接影响氟离子的平均活度系数进而影响测量结果。 加入总离子强度缓冲溶液(TISAB)可以维持溶液离子强度一致,防止待测溶液由于离子活度之间的差异而引起误差,掩蔽干扰离子,同时还能使络合物中的氟游离出来形成能与氟电极响应的氟离子[7-8]。 以溶液中干扰能力强的Al、Fe 为例,柠檬酸钠与Al、Fe 发生配合反应,其化学反应式为[9]:

为探索TISAB 加入量对氟含量测定的影响,根据实验方法将样品分别稀释100 倍和1 000 倍进行氟含量测定,结果如表3 所示。
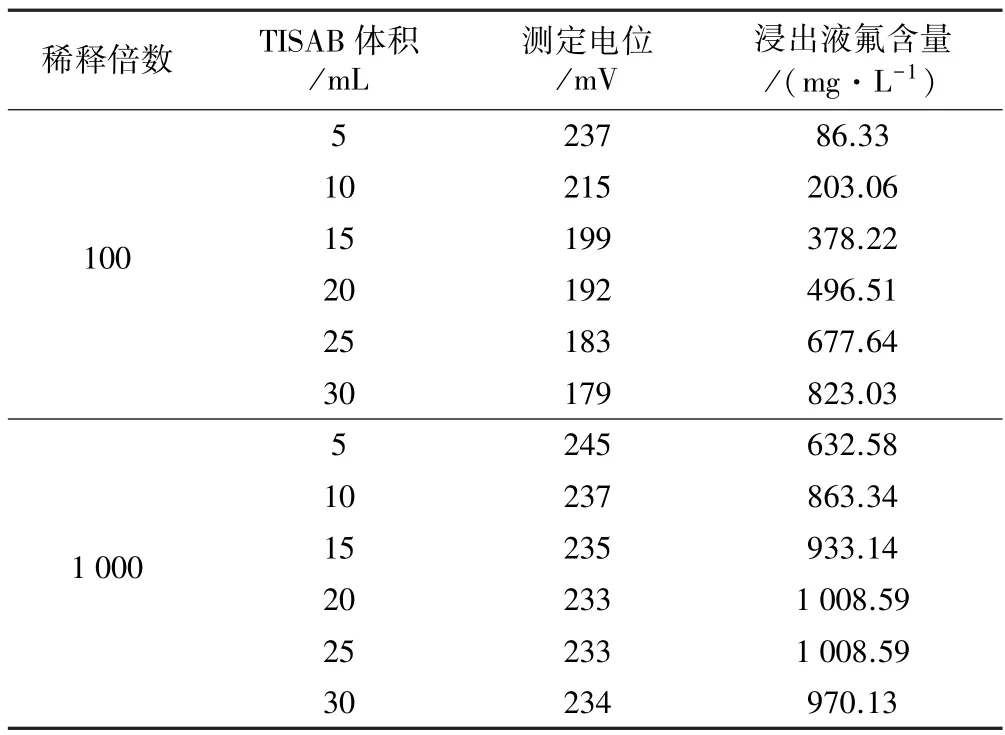
表3 不同TISAB 加入量条件下浸出液氟含量的测定结果
表3 结果表明,浸出液在100 倍低稀释倍数下,氟含量测定值随TISAB 加入量增加而显著增大;在1 000倍高稀释倍数下,当TISAB 用量在20~25 mL 时,电位值保持稳定,且测定时电极灵敏度高,平衡时间短。 这主要是由于低稀释倍数条件下浸出液中杂质金属元素含量还是很高,TISAB 加入量不足以完全释放络合物中的氟离子,随着溶液稀释倍数增大,溶液中金属元素含量大大降低,随着TISAB 加入量增大,TISAB 相对过量,氟的络合物与柠檬酸钠发生反应使得氟离子充分游离出来。 考虑到试剂的消耗,选择TISAB 加入量为20 mL。
2.3 温度的影响
温度对氟含量的测试影响主要体现在对氟离子电极膜电位的影响上[10]。 在不同温度条件下进行氟离子工作曲线建立实验,结果如表4 所示。 由表4 可知,随着温度升高,电极的实际响应斜率逐渐增大。
为进一步验证标准曲线建立和待测溶液氟离子测定温度不一致对测量结果的影响,本实验在25 ℃下建立工作曲线,按照实验方法将待测样品稀释1 000 倍,分别在不同温度下测定浸出液氟含量,结果如表5 所示。

表4 不同温度条件下氟离子工作曲线斜率的测定结果
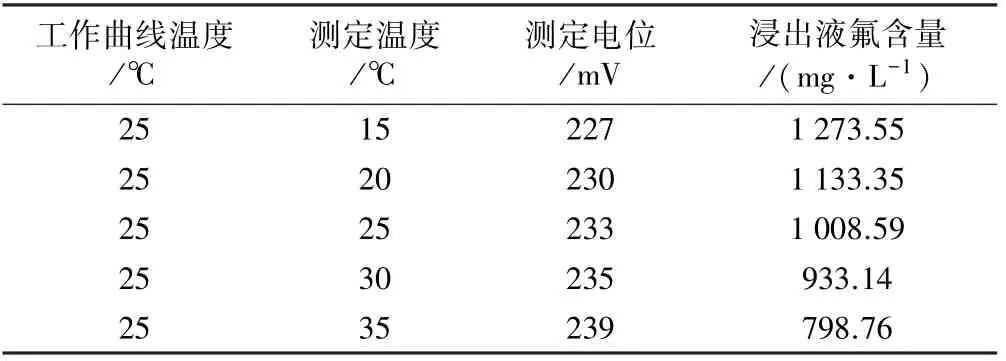
表5 不同温度条件下浸出液氟含量的测定结果
表5 结果表明,温度升高,电位值升高,测量值减小。 这主要是因为氟离子活度随温度升高而增强,电极膜电位也随之增大。 因此,为保证测量数据的准确性,在进行标准曲线建立和待测溶液氟离子检测时温度需保持一致。
2.4 溶液pH 值的影响
待测样品溶液的酸度对氟电极的响应有影响,且这种影响随氟离子活度降低而增大[11]。 为探讨浸出液酸度对测定的影响,分别用盐酸或氢氧化钠将总离子缓冲溶液TISAB 的pH 值调节为4.0~9.0,按实验方法将样品稀释1 000 倍再进行氟含量的测定,结果如表6 所示。
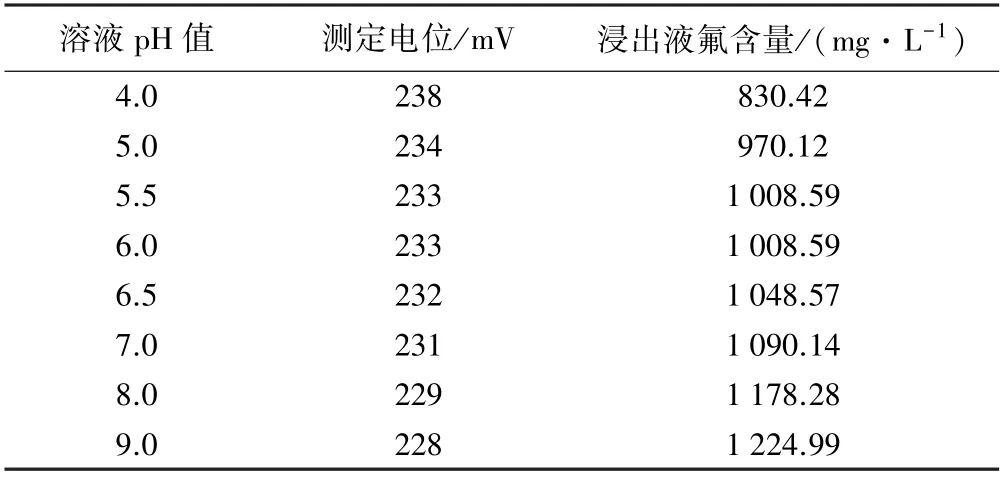
表6 不同pH 值条件下浸出液氟含量的测定结果
由表6 可以看出,随着pH 值升高,电极电位降低,浸出液氟含量测定值随之升高,在pH 值为5.5~6.0时,电位值保持稳定。 这主要是因为当pH 值较低时,F-与H+易形成难离解的HF 和HF2-,使待测溶液中游离氟离子浓度降低,测量结果偏低;当pH 值较高时,由于OH-和F-在溶液中具有相近的有效离子半径,OH-可能穿透氟离子电极的氟化镧单晶膜,占据氟化镧晶格中氟离子所在位置,同时与氟化镧晶体反应形成La(OH)2+、La(OH)2+,使膜中F-外渗,造成氟离子浓度升高的假象[12]。 因此,选择合适的溶液pH 值为5.5~6.0。
2.5 精密度实验
按照实验方法分别对稀释倍数为500~2 000 倍的浸出液样品测定7 次,结果见表7。

表7 方法精密度实验结果
不同稀释倍数下的试样分析结果表明,在该实验条件下试样分析结果相对标准偏差小于3%,方法精密度良好。
2.6 准确度实验
为研究该方法的准确性,分别在稀释500 倍的浸出液样品中加入不同量的氟标准溶液,按照试验方法进行加标回收率重复性试验,测定结果见表8。

表8 方法准确度实验结果
结果表明,在该实验条件下样品加标回收率在97.33%~101.50%之间,方法准确度良好。
3 结 论
1) 过量的TISAB 使氟离子从废旧电池回收液的氟络合物中充分释放,导致采用氟离子选择电极法测定浸出液中氟含量时,其测定值随溶液稀释倍数增加而增高。
2) 控制废旧电池回收液pH 值为5.5 ~6.0、加入体积分数为20%的TISAB、溶液稀释500~2 000 倍、标准曲线建立温度和测定温度保持一致时,采用氟离子选择电极-标准曲线法测定浸出液中氟含量,测定结果精密度和准确度高,操作简便,该方法适用于废旧电池回收行业复杂浸出液体系中氟的测定。
